長基因間非蛋白編碼RNA 472對阿爾茨海默病神經元鐵死亡的作用機制研究
【摘要】目的 探究長基因間非蛋白編碼RNA 472(LINC00472)對阿爾茨海默病(AD)神經元鐵死亡的作用機制,為臨床治療提供參考。方法 選取雄性昆明種小鼠30只,隨機分為空白組、模型組、模型+加藥組,各10只。空白組小鼠腹腔注射等量的生理鹽水和灌胃等量的雙蒸水,模型組小鼠灌胃人β淀粉樣蛋白1-42(Aβ1-42)5 mg/kg(雙蒸水配制)建立AD模型,模型+加藥組小鼠在模型組基礎上腹腔注射環磷酸腺苷(cAMP)篩選出的抑制LINC00472靶向藥物。比較3組小鼠迷宮測試結果,腦組織炎癥因子水平、β淀粉樣蛋白(Aβ)mRNA水平、微管相關蛋白(tau)mRNA水平、谷胱甘肽過氧化物酶4(GPX4)mRNA水平、甲基轉移酶3(METTL3)水平、凋亡信號調節激酶1(ASK1)水平及3組小鼠的Aβ、tau、GPX4免疫組化檢測結果。結果 空白組、模型+加藥組小鼠Y形迷宮覓食時間、莫里斯水迷宮(MWM)逃逸時間均短于模型組,且空白組均短于模型+加藥組;空白組、模型+加藥組小鼠MWM有效區域停留時間均長于模型組,且空白組長于模型+加藥組(均P<0.05)。空白組、模型+加藥組小鼠白細胞介素-6(IL-6)、單核細胞趨化蛋白(MCP-1)、白細胞介素-1β(IL-1β)、Aβ mRNA、tau mRNA、METT3 mRNA、ASK1水平均低于模型組,且空白組均低于模型+加藥組;空白組、模型+加藥組小鼠GPX4 mRNA水平均高于模型組,且空白組高于模型+加藥組(均P<0.05)。模型組小鼠海馬體Aβ1-42沉積增加,模型+加藥組Aβ1-42表達水平低于模型組;模型組小鼠海馬體tau磷酸化增加,模型+加藥組海馬體tau磷酸化程度低于模型組;模型組小鼠海馬體GPX4表達減少,模型+加藥組海馬體GPX4表達高于模型組。結論 LINC00472抑制有助于減輕神經炎癥,減少Aβ沉積、tau磷酸化,并提高GPX4表達,進而通過抑制AD神經元鐵死亡改善神經功能,且AD神經元鐵死亡的作用機制與METT3/ASK1通路有關。
【關鍵詞】長基因間非蛋白編碼 RNA 472;阿爾茨海默病;鐵死亡
【中圖分類號】R322.8 【文獻標識碼】A 【文章編號】2096-2665.2024.21.0001.05
DOI:10.3969/j.issn.2096-2665.2024.21.001
阿爾茨海默病(Alzheimer's disease, AD)是常見的神經退行性疾病,其發病原因和機制目前尚不明確,與遺傳、環境、年齡增長等有關,可出現進行性加重性認知功能障礙與行為損害、記憶和學習能力受損,該病患者腦內的斑塊、小膠質細胞、纏結神經元中可觀察到鐵沉積現象[1-2]。鐵死亡是非凋亡性程序性細胞死亡,其特征為鐵依賴性的脂質氫過氧化物累積到致死水平,是AD病理生理學的主要過程[3]。除鐵死亡外,腦組織還易受到神經炎癥的影響,鐵滯留可觸發AD中的小膠質細胞活化和白細胞介素產生,加劇淀粉樣β蛋白(Aβ)沉積和微管相關蛋白(tau)磷酸化。有研究表明,鐵死亡抑制劑在卒中疾病動物模型中具有保護神經元、恢復認知功能的作用[4]。長基因間非蛋白編碼RNA 472(LINC00472)與鐵死亡密切相關,其在多種腫瘤中的表達研究較多,但關于其在AD中的表達及作用機制相關研究較少。基于此,本研究探究LINC00472對AD神經元鐵死亡的作用機制,現報道如下。
1 材料與方法
1.1 實驗材料 選取雄性昆明種小鼠30只[購于上海杰思捷實驗動物有限公司,動物生產許可證號: SCXK(滬)2020-0004], 3月齡,體質量300~400 g。適應性喂養1周后,隨機分為空白組、模型組、模型+加藥組,各10只。
空白組小鼠腹腔注射等量的生理鹽水和灌胃等量的雙蒸水;模型組小鼠灌胃人β淀粉樣蛋白1-42(Aβ1-42)5 mg/kg(雙蒸水配制)建立AD模型;模型+加藥組小鼠在模型組基礎上腹腔注射環磷酸腺苷(cAMP)篩選出的抑制LINC00472靶向藥物,在造模成功1周后連續灌胃給藥8周。 3組小鼠均于末次給藥后進行迷宮實驗,取腦組織,置于-80 ℃環境保存待測。研究過程遵循國際通行的動物福利和倫理準則。
1.2 研究方法 ⑴迷宮實驗。 Y形迷宮由3個臂組成,包括1個起始臂和2個目標臂(每個臂的尺寸為30 cm×6 cm×30 cm)。訓練小鼠3 d后進行測試。小鼠在正式測試前禁食12 h。第41天,在2個目標臂之一放置食物,將小鼠分別放置在起始臂末端,用攝像機記錄每只小鼠的運動軌跡和尋找食物所用的時間,并使用
ANY-maze動物行為分析軟件進行分析。
第43天使用莫里斯水迷宮(MWM)評估小鼠的空間記憶和導航能力,訓練和正式測試均使用MT-200水迷宮視頻跟蹤分析系統進行。水槽被分成4個象限,向水槽中添加二氧化鈦使水變渾濁。訓練小鼠放入水中后有60 s內到達平臺,并在平臺上停留20 s。若有60 s內未找到平臺,則手動帶小鼠到平臺上并停留20 s。共訓練
3天。第46天和第47天分別在盲測條件下進行導航測試和探索試驗,記錄小鼠找到平臺所用時間和(或)通過有效區域的時間。
⑵酶聯免疫吸附試驗(ELISA)。取小鼠腦組織,裂解、研磨,低速離心后取上清液,使用ELISA檢測白細胞介素-6(IL-6)、單核細胞趨化蛋白1(MCP-1)、白細胞介素-1β(IL-1β)水平。
⑶免疫組化染色。干燥載玻片,并用二甲苯和乙醇脫蠟。用檸檬酸緩沖液在100 ℃下進行載玻片表位檢索,煮沸30 min,用3%過氧化氫孵育。切片用5%的牛血清白蛋白(BSA)阻斷,然后用Aβ、tau、谷胱甘肽過氧化物酶4(GPX4)一抗(均購自和光純藥工業有限公司)孵育過夜。最后,加入山羊抗兔二抗孵育,并用3,3'-二氨基聯苯胺(購自賽默飛世爾科技)染色。在反應結束時,用Harris蘇木精進行反染色。用95%和100%乙醇和二甲苯洗滌脫水后,用永久貼載介質覆蓋組織切片,在共聚焦顯微鏡下觀察免疫組化染色情況。
⑷RNA分離和定量反轉錄PCR(qRT-PCR)。取大鼠腦組織在1 mL 組織裂解緩沖液中裂解,于冰浴狀態下在玻璃研磨機中研磨成勻漿,然后4 ℃裂解30 min,離心20 min。成骨細胞使用1 mL 組織裂解緩沖液裂解后離心,使用TRIzol試劑提取總RNA,并使用Hifair Ⅲ第一鏈cDNA合成Super Mix轉錄成cDNA。使用Hieff qPCR SYBR Green Master Mix(購自賽默飛世爾科技)行定量實時PCR。以甘油醛-3-磷酸脫氫酶(GAPDH)為內參基因,根據2-ΔΔCt方法計算Aβ、tau、GPX4 mRNA表達水平。
⑸蛋白質印跡分析。取大鼠腦組織在1 mL組織裂解
緩沖液中裂解,于冰浴狀態下在玻璃研磨機中研磨成勻漿,然后4 ℃裂解30 min,離心20 min。成骨細胞使用1 mL 組織裂解緩沖液裂解后離心,使用補充了1%苯基甲基磺酰氟的放射免疫沉淀測定(RIPA)緩沖液提取成骨細胞的蛋白質并轉移到聚偏二氟乙烯(PVDF膜)上,用脫脂奶粉(5%)在含有0.05%Tween-20(TBST)的Tris緩沖鹽溶液中封閉。然后,將PVDF膜分別與甲基轉移酶
3(METTL3)、細胞凋亡信號調節激酶1(ASK1)、β-肌動蛋白(β-actin)(購自和光純藥工業有限公司)在室溫下過夜。用TBST洗滌后,將PVDF膜與二抗IgG,在室溫下孵育2 h。將膜浸入增強型化學發光溶液。在無光條件下顯影后,觀察條帶并拍照記錄,以β-actin作為內參,使用2-ΔΔCt方法計算METT3、ASK1蛋白相對表達水平。
1.3 統計學分析 采用SPSS 21.0統計學軟件進行數據分析。計量資料以(x)表示,組間比較采用獨立樣本t檢驗,多組間比較使用單因素方差分析。以P<0.05為差異有統計學意義。
2 結果
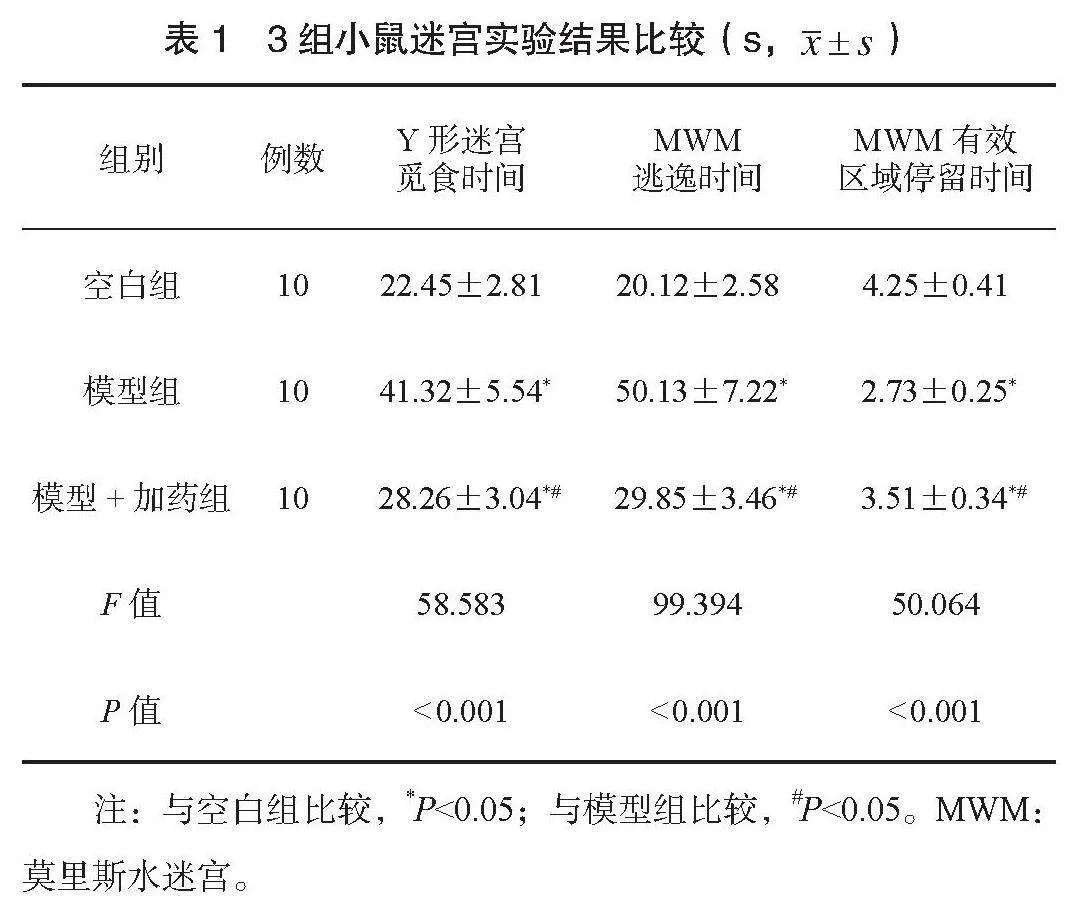
2.1 3組小鼠迷宮實驗結果比較 空白組、模型+加藥組小鼠Y形迷宮覓食時間、 MWM逃逸時間均短于模型組,且空白組短于模型+加藥組;空白組、模型+加藥組小鼠MWM有效區域停留時間均長于模型組,且空白組長于模型+加藥組,差異均有統計學意義(均P<0.05),
見表1。
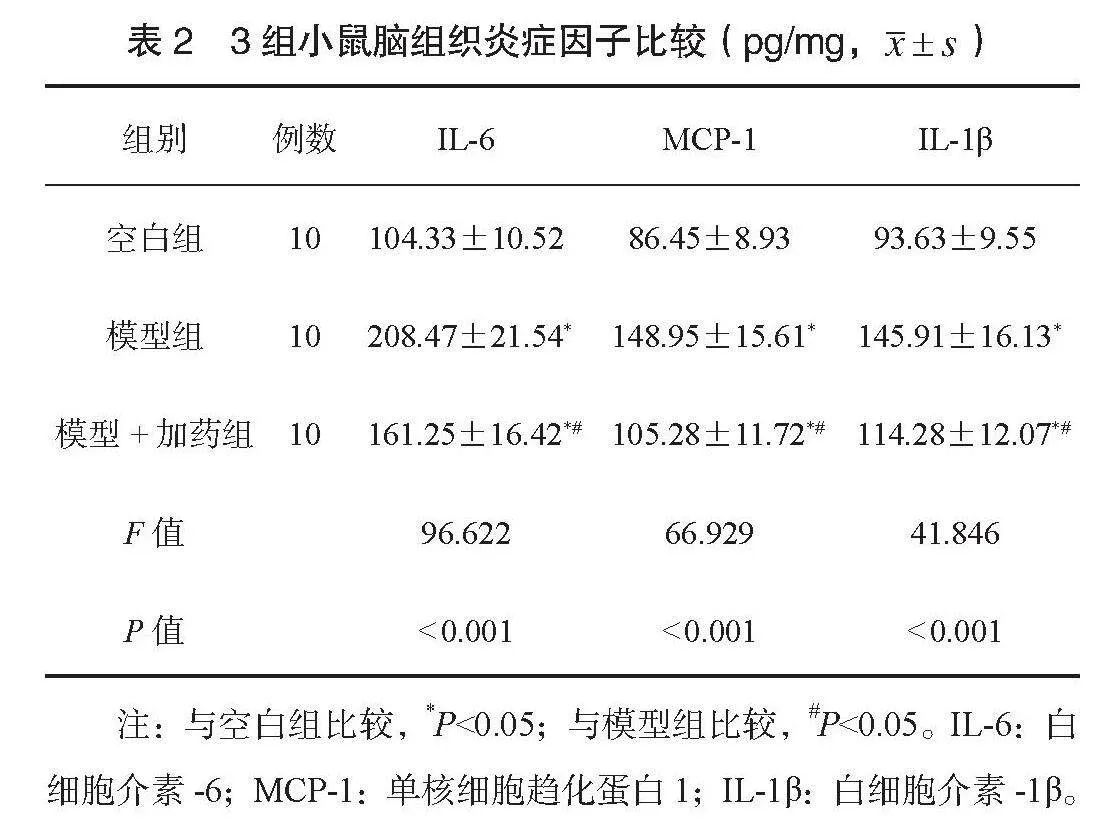
2.2 3組小鼠腦組織炎癥因子水平比較 空白組、模型+加藥組小鼠IL-6、 MCP-1、 IL-1β水平均低于模型組,且空白組均低于模型+加藥組,差異均有統計學意義(P<0.05),見表2。
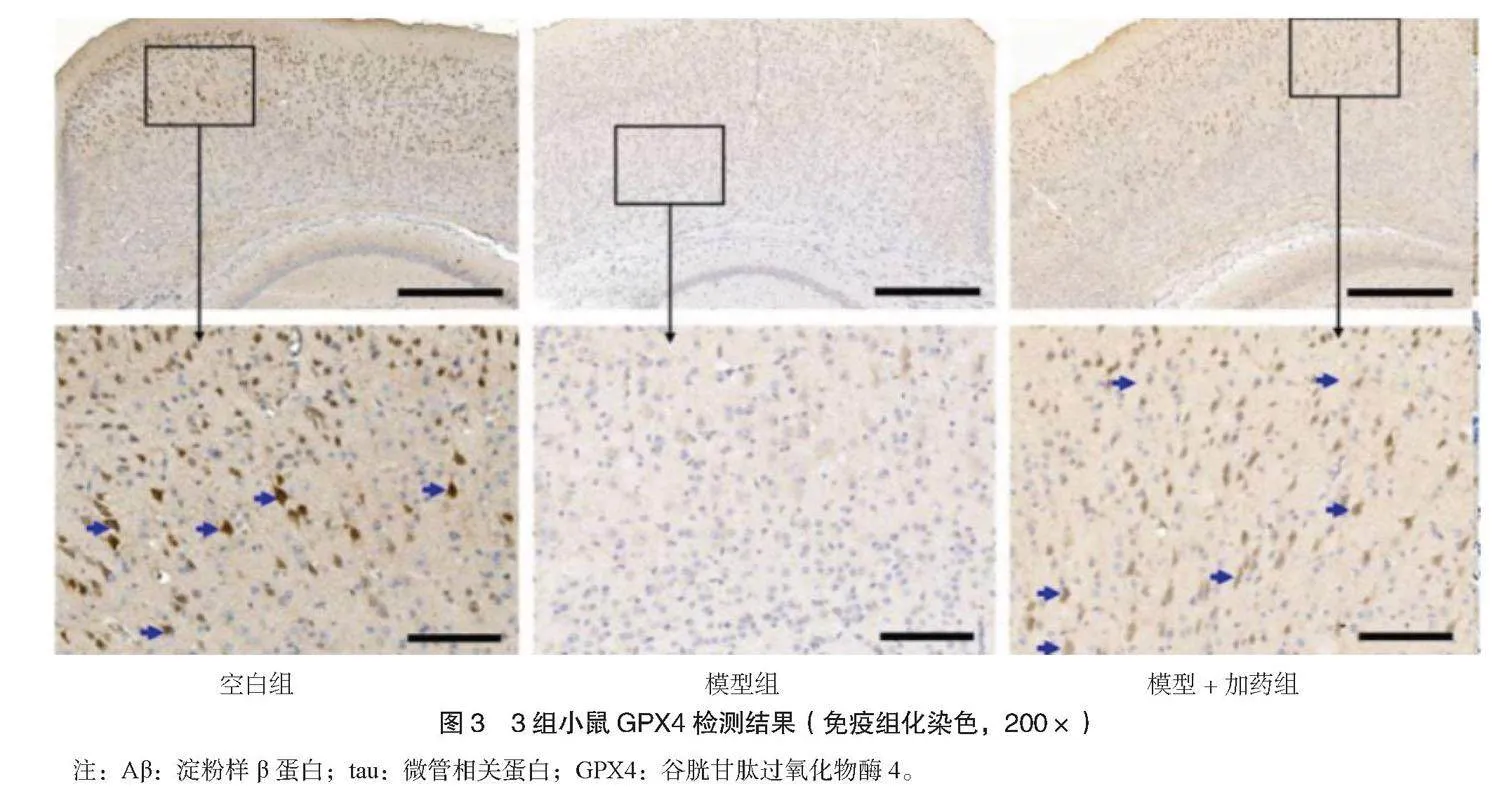
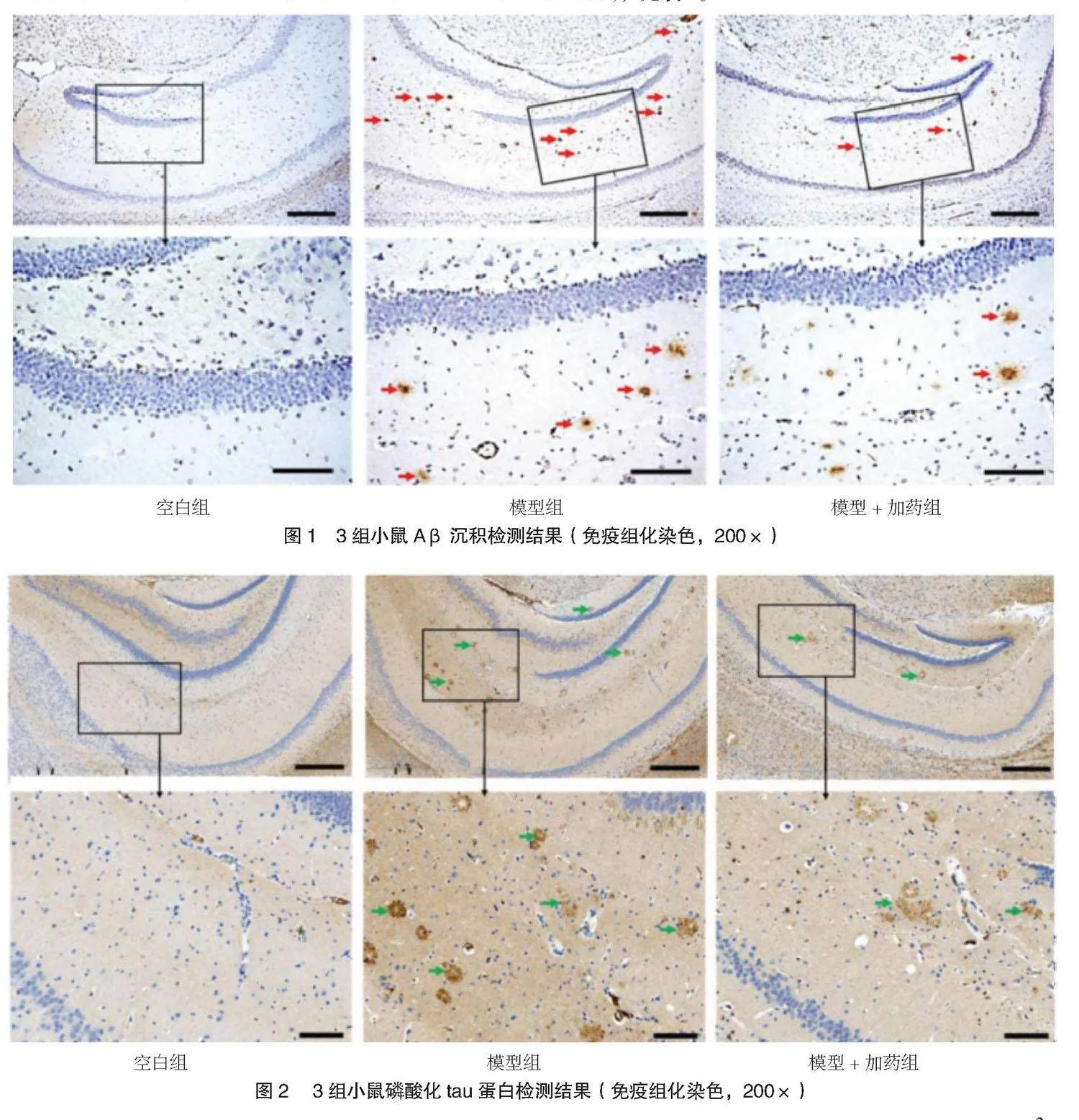
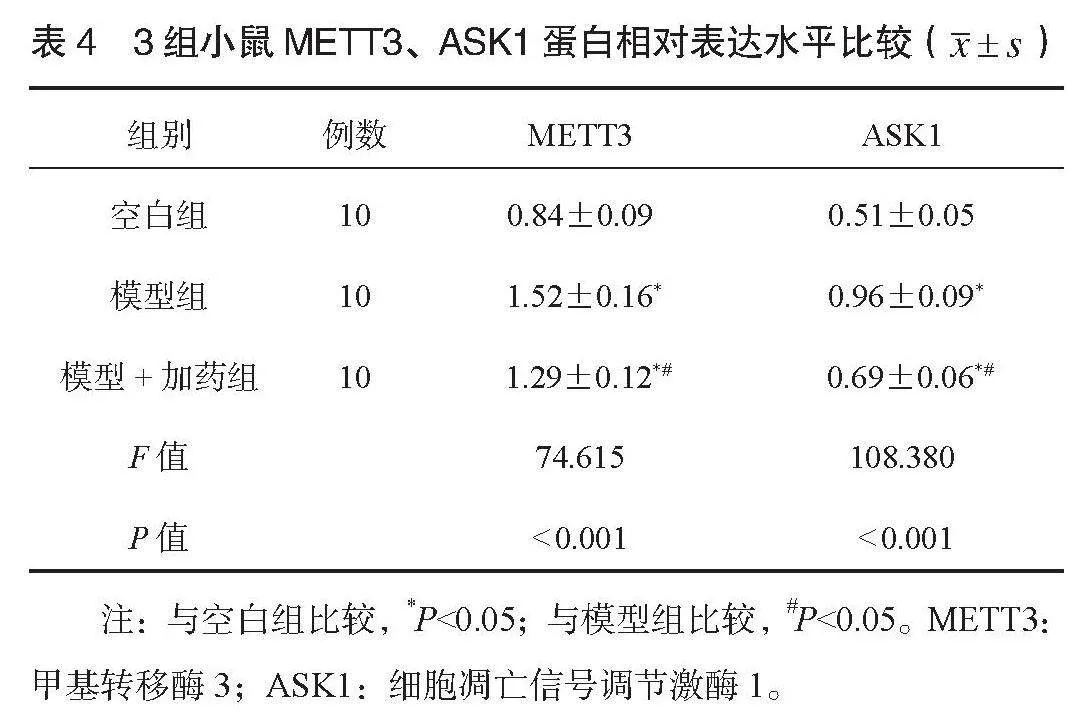
2.3 3組小鼠腦組織Aβ、tau、GPX4免疫組化檢測結果 模型組小鼠海馬體Aβ1-42沉積增加,模型+加藥組Aβ1-42低于模型組,見圖1;模型組小鼠海馬體tau磷酸化增加,模型+加藥組海馬體tau磷酸化低于模型組,見圖2;模型組小鼠海馬體GPX4表達減少,模型+加藥組海馬體GPX4表達高于模型組,見圖3。
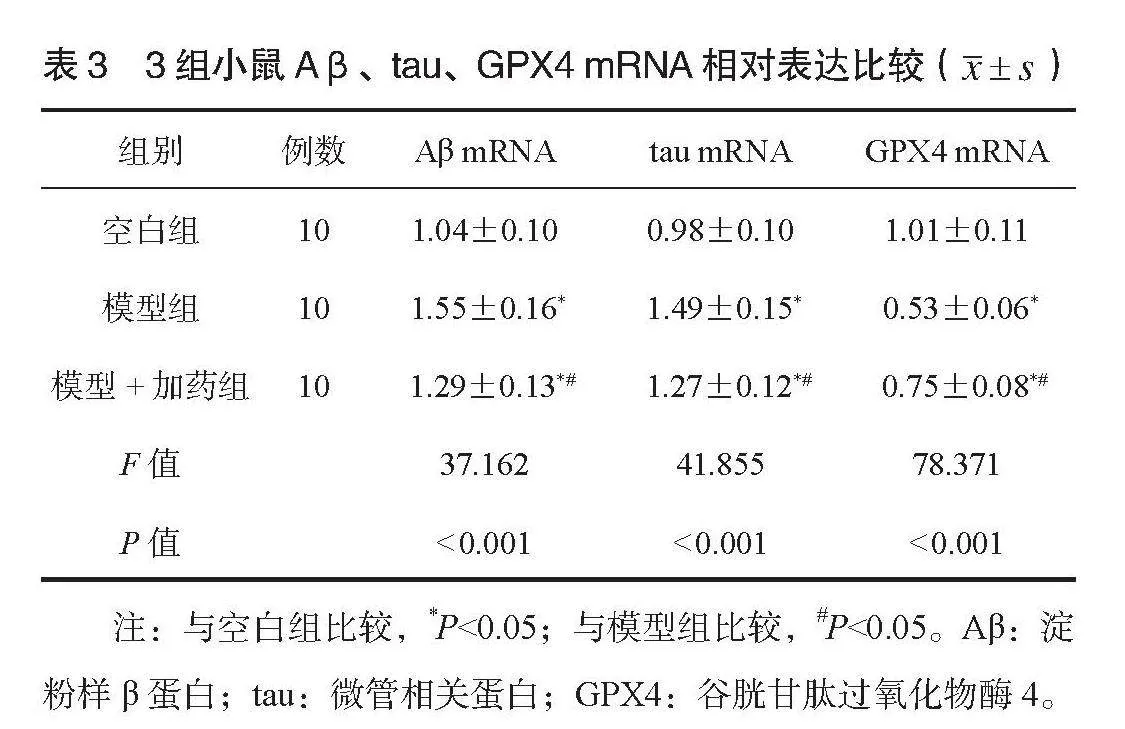
2.4 3組小鼠Aβ、 tau、 GPX4 mRNA相對表達水平比較 空白組、模型+加藥組小鼠Aβ、 tau mRNA水平均低于模型組,且空白組均低于模型+加藥組;空白組、模型+加藥組小鼠GPX4 mRNA水平均高于模型組,且空白組高于模型+加藥組,差異均有統計學意義(均P<0.05),見表3。
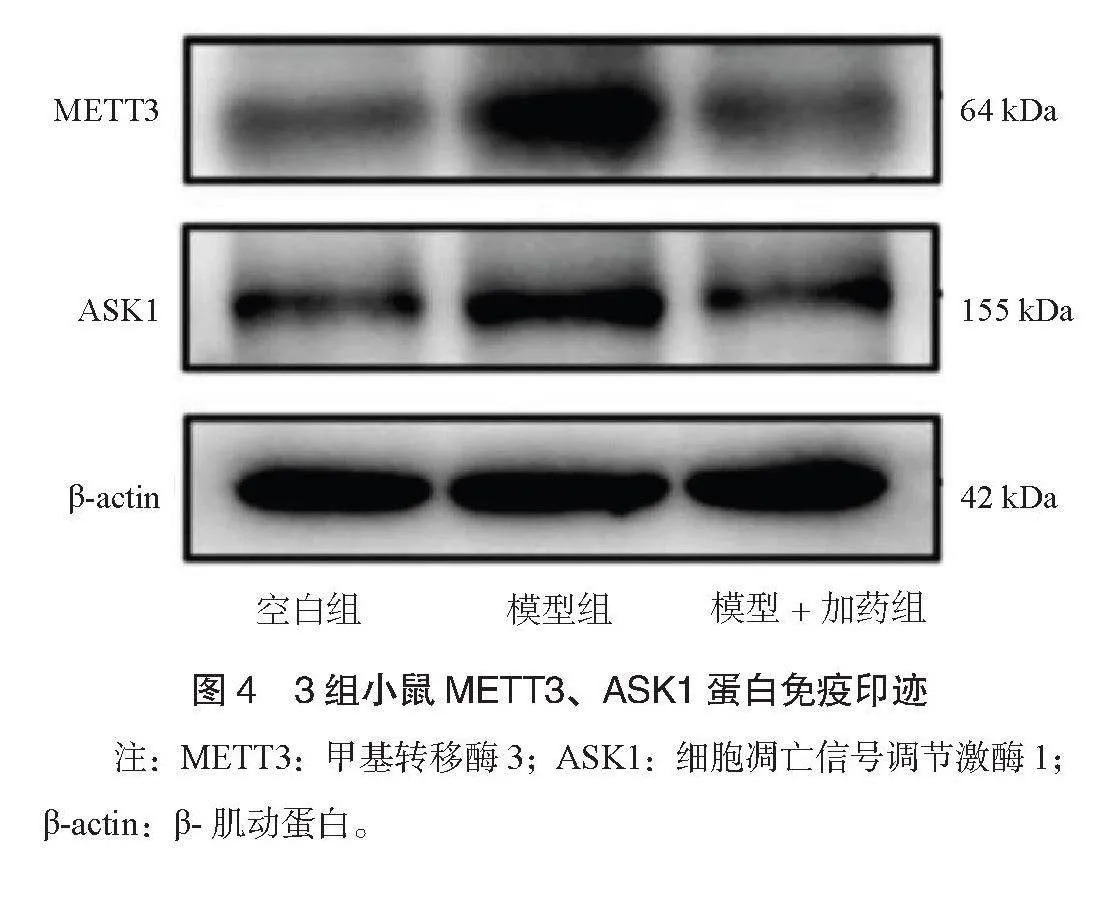
2.5 3組小鼠METT3、 ASK1蛋白相對表達比較 空白組、模型+加藥組小鼠METT3、 ASK1蛋白表達水平均低于模型組,且空白組均低于模型+加藥組,差異均有統計學意義(P<0.05),見表4。 3組小鼠METT3、 ASK1蛋白免疫印跡情況,見圖4。
3 討論
鐵死亡是一種非凋亡性的細胞死亡形式,其在形態學、生化、遺傳學上均不同于其他形式的細胞死亡(如凋亡、壞死、自噬),鐵過載可在體內誘導鐵死亡,而鐵螯合劑可預防鐵死亡[5]。鐵死亡可見于各種神經系統疾病相關的神經元細胞死亡中,如出血性卒中、缺血性卒中、帕金森病、亨廷頓病等,并伴有脂質過氧化、線粒體功能障礙及GPX4減少[6]。
腦鐵過載與AD等神經退行性疾病的病理機制相關,然而其潛在機制尚不明確。此外,鐵死亡抑制劑已在卒中疾病動物模型中被證明可保護神經元、恢復認知功能,且敲除小鼠的 GPX4可直接導致年齡依賴性的神經退行性變化和嚴重的神經元丟失[7]。考慮AD 中過量鐵的積累會導致腦內活性氧(ROS)的產生顯著增加,因此,鐵死亡可能與 AD 的神經元丟失和認知障礙有關。
Aβ、tau、GPX4是鐵死亡及鐵過載的重要反映指標。Aβ前體蛋白(APP)是一種1型跨膜糖蛋白,是Aβ生成的關鍵前體,可先被α-分泌酶或β-分泌酶切割,然后再被γ-分泌酶切割。在健康狀態下,α-分泌酶首先切割APP,即處于非淀粉樣變性途徑。然而,APP首先被β-分泌酶切割,可產生具有神經毒性的40~42個氨基酸的淀粉樣蛋白(淀粉樣變性途徑)。而弗林蛋白酶在介導α-分泌酶或
β-分泌酶的蛋白酶解活化率方面起關鍵作用,其濃度與
α-分泌酶活性呈正相關,與β-分泌酶活性呈負相關。胞內鐵濃度過高可通過減少弗林蛋白酶,增強β分泌酶活性,從而增加淀粉樣變性途徑的Aβ生成。此外,APP mRNA是5'-非翻譯區(5'-UTR)編碼鐵反應元件(IRE),該元件與胞內鐵含量密切相關。當胞內鐵濃度升高時,5'-UTR mRNA中的IRE上調APP的翻譯,從而增加APP蛋白的數量,并促進Aβ的生成。鐵還能直接與Aβ的His6、His13、His14氨基酸殘基結合,從而增強Aβ的神經毒性[8]。
在APP/PS1小鼠AD模型中,亞微米分辨率的X線顯微鏡技術顯示,淀粉樣斑塊形態與鐵直接相關[9]。鐵可通過誘導激酶影響蛋白磷酸酶 2A活性,促進tau過度磷酸化,還可通過tau蛋白中的鐵結合基序引起過度磷酸化的 au聚集[10]。GPX4通過將膜脂質氫過氧化物還原為脂質醇來抑制脂質過氧化,被認為是鐵死亡的中樞調節器。GPX4的敲除可誘導脊髓運動神經元的鐵死亡,從而導致成年小鼠迅速癱瘓和死亡。有研究表明,鐵死亡通過敲除前腦神經元GPX4,引發海馬神經變性中的主要細胞死亡,這與認知障礙的發生發展直接相關。此外,鐵沉積和肽-血紅素復合物的形成與Aβ和tau相互作用,可產生涉及鐵死亡途徑的ROS[11]。
本研究結果顯示,空白組、模型+加藥組小鼠Y形迷宮覓食時間、MWM逃逸時間均短于模型組,且空白組短
于模型+加藥組;空白組、模型+加藥組小鼠MWM有效區域停留時間均長于模型組,且空白組長于模型+加藥組,提示小鼠神經功能改善。且免疫組化及PCR實驗證實,在AD小鼠中Aβ、tau表達增加,GPX4表達減少,LINC00472抑制則逆轉其變化,表明LINC00472抑制有助于通過減少AD小鼠神經細胞鐵死亡改善其神經功能。
ASK1是各種依賴于ros的細胞死亡過程中的關鍵調節因子,不僅參與氧化鋁納米顆粒誘導的海馬神經元鐵凋亡的調控,還能通過ASK1-p38 mapk通路,在冷應激誘導的鐵凋亡中發揮重要作用[12]。有研究表明,ASK1參與多種ros依賴性細胞死亡過程,作為多個信號級聯的樞紐[13]。本研究結果顯示,空白組、模型+加藥組METT3、ASK1蛋白表達低于模型組,空白組低于模型+加藥組,推測LINC00472抑制可能是通過METT3/ASK1通路介導進而抑制AD小鼠神經細胞鐵死亡。
綜上所述,LINC00472抑制有助于抑制神經炎癥,減少Aβ沉積、tau磷酸化,并提高GPX4表達,通過抑制鐵死亡改善神經功能,且對阿爾茨海默病神經元鐵死亡的作用機制與METT3/ASK1通路有關。
參考文獻
張平,季暉,胡慶華.阿爾茨海默癥的臨床治療和天然來源潛在藥物的研究進展[J].藥學學報, 2022, 57(7): 1954-1961.
林小玲,柯維強,唐文軍,等.大黃酚對Aβ1-42致阿爾茨海默癥大鼠學習記憶及海馬CA1區組織JNK通路的影響[J].中成藥, 2022, 44(6): 1977-1981.
張朋飛,章立華,華東. Triapine通過ROS/GSH/GPX4軸誘導A549細胞鐵死亡[J].中國藥理學通報, 2023, 39(5): 833-838.
廖鐘玲,林秀苗,王潔瓊,等.中藥治療缺血性腦卒中鐵死亡機制的研究進展[J].中西醫結合心腦血管病雜志, 2023, 21(12): 2230-2233.
ZHANG G, ZHANG Y, SHEN Y, et al. The potential role of ferroptosis in Alzheimer’s disease[J]. Journal of Alzheimers Disease, 2021, 80(3): 907-925.
冷蕭如,葉宇航,胡霞敏.鐵死亡在缺血性腦卒中的作用[J].生命的化學, 2023, 43(9): 1337-1345.
李賽菲,馮衛生,袁培培,等.熟地黃通過抑制自噬和鐵死亡改善缺血性腦卒中大鼠神經功能損傷[J].中國實驗方劑學雜志, kk29Kyi4pgBzMebjbaeVFQ==2024(8): 6-33.
黃健,安紅偉,曹詩杰.鐵死亡與阿爾茨海默病的研究進展[J].中國病理生理雜志, 2021(11): 2088-2093.
郭少博,朱文慧,白宇,等.冰菖散通過Nrf2/HO-1信號通路改善APP/PS1阿爾茨海默病小鼠鐵死亡及認知功能障礙的研究[J].南京中醫藥大學學報, 2024, 40(6): 598-607.
于放,馬晶瑩,馬旺然,等.脂氧合酶在鐵死亡驅動阿爾茨海默病中作用的研究進展[J].實用心腦肺血管病雜志, 2022, 30(12): 128-132.
蔡雅文,柴玉慧,繆明星,等.細胞焦亡介導的阿爾茲海默癥發病機制研究進展[J].中國藥學雜志, 2021, 56(21): 1701-1705.
袁美玲,張云,汪光云,等.通竅活血湯含藥腦脊液調控ASK1/MKK4/JNK信號通路對OGD/R損傷HT22細胞的保護作用[J].中國中藥雜志, 2022, 47(19): 10.
OGIER J M, GAO Y, DUNNE E M ,et al. ASK1 is a novel molecular target for preventing aminoglycoside-induced hair cell death[J].Journal of Molecular Medicine, 2022, 100(5): 797-813.
1基金項目:2022年度黑龍江省省屬本科高校基本科研業務費科學技術研究項目(編號:2022-KYYWF-0815)
作者簡介:林萍,碩士研究生,副主任醫師,研究方向:神經內科疾病的診療。

