外源褪黑素調控母牛繁殖性能的研究進展




摘" 要: 母牛繁殖性能是養牛業發展的基礎,褪黑素作為一種多功能激素,具有結合MT1和MT2受體,降低促炎細胞因子(IL-1β、TNF-α、IL-6)和升高抗炎細胞因子(IL-10、IL-1Ra)的水平,促進抗氧化酶基因(Sod、Cat、Gpx、Gpx4)的表達,以及調節細胞自噬和線粒體自噬相關基因的水平,改變瘤胃和陰道微生物組成等多種作用,從而調控母牛卵泡細胞、顆粒細胞、胚胎發育以及發情、排卵、妊娠等繁殖性能。因此,本文綜述了外源褪黑素在體內(外)調控母牛生殖的應用現狀及其作用機制,為合理應用褪黑素提高母牛繁殖性能提供理論參考。
關鍵詞: 褪黑素;牛;繁殖性能;機制
中圖分類號:S823.3
"文獻標志碼:A
文章編號:0366-6964(2024)12-5379-12
doi: 10.11843/j.issn.0366-6964.2024.12.005
開放科學(資源服務)標識碼(OSID):
收稿日期:2024-05-31
基金項目:中國博士后面上科學基金 (2020M672233);河南省農業良種聯合攻關項目(2022020104)
作者簡介:劉彩鳳(2003-),女,河南上蔡人,本科生,主要從事動物遺傳育種與繁殖研究,E-mail:liucf2916389782@qq.com
*通信作者:劉深賀,主要從事動物遺傳育種與繁殖研究,E-mail: liush2016@qq.com;姬普雨,主要從事動物遺傳育種與繁殖研究,E-mail:jipuyu0576@163.com
Research Progress on Regulation of Reproductive Performance by Exogenous Melatonin in Cows
LIU" Caifeng1, WANG" Jingzhuo1, WANG" Xi1, LIU" Zirui1, JI" Puyu2*, LIU" Shenhe1*
(1.College of Animal Science and Technology, Henan Agricultural University, Zhengzhou 450046," China;
2.Shangqiu Rural Industry Development Center, Shangqiu 476000, China)
Abstract: The reproductive performance of cows is the basis for the development of cattle industry. As a multifunctional hormone, melatonin interacts with MT1 and MT2 receptors, reduces the levels of pro-inflammatory cytokines (IL-1β, TNF-α, IL-6), enhances the levels of anti-inflammatory cytokines (IL-10, IL-1Ra), and promotes the expression of antioxidant enzyme genes (Sod, Cat, Gpx, Gpx4). Additionally, it modulates autophagy and mitochondrial autophagy-related genes expression, alters the composition of rumen and vaginal microbiota, thereby influencing reproductive performance in bovine follicular cells, granulosa cells as well as embryonic development alongside estrus cycles, ovulation processes, and pregnancy outcomes. Consequently, this article reviews the current status and mechanisms underlying exogenous melatonin's role in regulating cow reproduction both in vivo and in vitro while providing a theoretical framework for its rational application to enhance reproductive efficiency in cattle.
Key words: melatonin; cattle; reproductive performance; mechanism
*Corresponding authors: LIU Shenhe,E-mail: liush2016@qq.com; JI Puyu, E-mail:jipuyu0576@163.com
母牛的繁殖性能是影響養牛業經濟效益的關鍵因素。繁殖性能主要受環境、管理和遺傳因素的相互作用影響。此外,與發情、排卵、妊娠等相關的疾病也會造成母牛繁殖效率降低、預期生產壽命縮短和產奶量下降[1,2]。因此,維持或提高母牛的繁殖效率,預防繁殖疾病的發生十分必要。褪黑素是一種多功能細胞保護分子,具有清除活性氧(reactive oxygen species, ROS)、抗氧化、抗細胞凋亡、抗炎等多種作用,其不僅在松果體中分泌,也在胃腸道、腎臟、性腺、胎盤和子宮等器官和組織中產生[3-5] 。因此,褪黑素既可以在體內調控母牛發情、排卵、妊娠等繁殖性能,也可在體外調控母牛生殖細胞功能,以及預防和緩解繁殖疾病。本文綜述了外源褪黑素在體(內)外調控母牛繁殖性能的應用效果及其通過MT1和MT2受體通路、抗炎、抗氧化等5個方面調控母牛繁殖性能的作用機制,以期為合理應用褪黑素提高母牛繁殖性能提供新的思路與見解。
1" 外源褪黑素在母牛生殖中的應用效果
1.1" 外源褪黑素在體內調控母牛繁殖
褪黑素具有高脂溶性和弱水溶性,可以通過包括血腦屏障在內的大多數細胞膜[6]。因此,外源褪黑素可以自由通過細胞膜進入母牛體內的循環系統,影響其繁殖狀態[7]。大量研究證明,皮下埋植、注射或口服褪黑素能夠影響母牛發情、排卵、妊娠等繁殖性能(表1)。
例如,Brockus等[8]在妊娠第190~262天的荷斯坦小母牛日糧中補充20 mg褪黑素能夠使母牛子宮動脈血流量增加25%,血清總抗氧化能力提高43%,但妊娠期長度和犢牛出生體重保持不變。趙增元等[9]證實,皮下埋植160 mg褪黑素能夠提高荷斯坦奶牛超數排卵效果,主要表現在可用胚胎數、胚胎質量和胚胎移植妊娠率的提升。Ratchamak等[10]對熱應激下進行超數排卵處理的泰國-荷斯坦雜交奶牛肌肉注射18 mg/50 kg體重的褪黑素,可以增加其大卵泡和黃體數量,恢復熱應激導致的卵子/胚胎、受精卵和可移植胚胎的數量下降。因此,通過不同方式補充外源褪黑素可以提高奶牛的繁殖性能,并可恢復熱應激造成的繁殖損失。水牛季節性發情較強,外源添加褪黑素也能夠緩解該現象。例如,Ghuman等[11]研究表明,在不發情摩拉水牛皮下埋植18 mg/50 kg體重的褪黑素,能夠顯著提高其總妊娠率、黃體活性、優勢卵泡直徑和血漿黃體酮(P4)水平。同樣,Ghuman等[12]對夏季不發情的小母水牛體內也植入相同劑量的褪黑素,可以成功地實現排卵大小的非排卵期卵泡排卵,啟動卵巢周期。Lochan等[13]指出,在產后早期水牛皮下埋植18 mg/50 kg體重的褪黑素,可以有效降低產后水牛氧化應激,使卵巢活動提前恢復,提高產后水牛的發情表現和排卵率。
褪黑素對肉牛繁殖性能的影響卻不盡相同。McCarty等[14]在肉牛的妊娠中期至晚期每30 d植入48 mg褪黑素,能夠增加妊娠中晚期肉牛的子宮動脈血流量,但對犢牛出生體重無顯著影響。Guo等[15]通過對雜交肉牛間隔14 d兩次皮下注射0.24 mg·kg-1體重的褪黑素,能夠增加血清抗氧化酶活性,提高肉牛受孕率,但對P4濃度無顯著影響。Reid等[16]對妊娠第190天至分娩后60天的安格斯牛每30 d補充48 mg褪黑素,可以提高血漿褪黑素水平,但乳脂率和總產奶量趨于下降,對犢牛出生體重也無顯著影響。Swanson等[17]在妊娠第160~240天的肉牛日糧中每天補充20 mg褪黑素,發現其乳脂率和產奶量有降低趨勢,出生犢牛體重無明顯差異。褪黑素可以增加子宮動脈血流量和抗氧化酶的活性,提高肉牛的受孕率,但卻會導致產奶量和乳脂率呈下降趨勢。已知褪黑素對白色脂肪組織和脂肪源性干細胞具有脂溶特性,這可能是導致母牛產奶量和乳脂率下降的原因之一[18,19]。
綜上,外源褪黑素可以調控母牛繁殖性能,但褪黑素在不同品種(屬)母牛的最適添加劑量、添加方式和添加階段等仍有待進一步明確。
1.2" 褪黑素調控體外母牛生殖細胞
1.2.1" 褪黑素調控體外母牛卵母細胞的發育
卵母細胞體外成熟(IVM)是體外胚胎生產(IVEP)過程中的關鍵階段,此階段的卵母細胞獲得了持續維持胚胎發育的潛能[20]。卵母細胞質量影響早期胚胎存活、妊娠建立和維持胎兒發育[21]。因此,通過優化卵母細胞體外培養條件能夠提高其體外發育的能力。大量研究表明,在卵母細胞培養基中添加褪黑素能夠促進體外卵母細胞發育(表2)。例如,Zhao等[22]在牛卵母細胞IVM培養基中添加不同濃度(10-7、10-9、10-11" mol·L-1)褪黑素,發現褪黑素能夠改善細胞器的正態分布,增加細胞內谷胱甘肽(GSH)和腺嘌呤核苷三磷酸(ATP)水平,增強內源性抗氧化基因的表達,從而顯著促進牛卵母細胞細胞質成熟,其中以10-9 mol·L-1效果最顯著。Pang等[23]也證明,10-9 mol·L-1褪黑素促進牛卵母細胞細胞質和細胞核成熟的效果最佳,表現為第一極體擠壓、皮質顆粒和線粒體正態分布以及線粒體膜電位升高。Cavalcante等[24]在牛卵巢皮質組織體外培養過程中,添加10-9 mol·L-1和2×10-9 mol·L-1褪黑素可促進牛原始卵泡激活,并維持基質細胞密度。El-Raey等[25]在牛卵母細胞IVM培養基中分別添加10和50 ng·mL-1褪黑素,均能夠顯著促進牛卵母細胞核成熟,積云細胞擴張和改變線粒體分布模式。以上研究表明,外源褪黑素可以促進牛卵母細胞成熟,主要表現在細胞質和細胞核的成熟。此外,已知不適合牛胚胎發育的劣質卵母細胞約占收集到的未成熟卵母細胞的三分之一以上,Yang等[26]用10-9 mol·L-1褪黑素培養牛劣質卵母細胞,發現褪黑素可以上調卵母細胞成熟相關基因生長分化因子-9(GDF-9)、骨形態生成蛋白-15(BMP-15)、ATP合酶Fo亞基6(ATPase6)和ATP合酶Fo亞基8(ATPase8)的mRNA表達,促進卵母細胞成熟,提高劣質卵母細胞的質量。該研究結果為應用褪黑素提高牛卵母細胞的合格率提供了方向,但培養后牛卵母細胞的質量是否達到體外胚胎生產的水平仍有待進一步研究。
過量添加褪黑素也會抑制牛卵母細胞的成熟。例如,Tian等[27]研究發現在牛卵母細胞培養基中添加10-9 mol·L-1褪黑素可使牛卵母細胞卵裂率、囊胚率、平均細胞數/囊胚達到最大值,隨著褪黑素濃度從10-9 mol·L-1增加到10-3 mol·L-1,卵裂率和囊胚率均顯著下降,說明高濃度褪黑素可能會延遲卵母細胞胞質成熟,從而影響胚胎發育,這與高超等[28]在牛卵母細胞上的研究結果相一致。另外,褪黑素也可以促進豬[29]、綿羊[30]、小鼠[31]等其他物種的體外卵母細胞成熟,表明褪黑素對卵母細胞IVM的促進作用不具有物種特異性,為褪黑素應用于一些稀有物種卵母細胞的IVM提供了理論基礎。
1.2.2" 褪黑素調控體外母牛顆粒細胞的發育
顆粒細胞是卵泡中的主要功能細胞,以自分泌和旁分泌的方式影響卵泡的生長、發育和成熟[32]。顆粒細胞的不同狀態,包括凋亡、氧化應激、自噬或細胞周期阻滯,都可能引發卵泡閉鎖。此外,類固醇激素合成的變化也會影響顆粒細胞狀態[3]。大量研究發現,褪黑素對不同狀態下母牛顆粒細胞的發育具有調控作用(表3)。例如,Wang等[33]將牛顆粒細胞暴露于不同濃度(400、800、1 200、1 600、2 000 pg·mL-1)褪黑素中24、48或72 h,發現不同濃度褪黑素對細胞早期凋亡率影響不大,但隨著培養時間變長,細胞的凋亡率降低,表明外源褪黑素以一種時間依賴性的方式調節牛顆粒細胞的凋亡。Wang等[34]在牛顆粒細胞培養基中添加1 200 pg·mL-1褪黑素,發現褪黑素可以通過上調B細胞淋巴瘤-2 (Bcl-2)、B細胞淋巴瘤/白血病-xl(BCL-XL)、谷胱甘肽過氧化物酶4(GPX4)和超氧化物歧化酶1(Sod1)基因的表達,下調Bcl-2相關X蛋白(Bax)、胱天蛋白酶3(CASP3)和腫瘤蛋白P53(TP53)基因的表達來抑制顆粒細胞凋亡。Riaz等[35]用10-9 mol·L-1和10-7 mol·L-1的褪黑素培養水牛顆粒細胞24 h,可以提高顆粒細胞有絲分裂過程中G2期的細胞數量,這與細胞周期抑制劑蛋白p21、p27水平的顯著下降相一致。Wang等[33]添加1 200 pg·mL-1褪黑素培養奶牛顆粒細胞,可以呈時間依賴性刺激P4的產生,抑制雌二醇的生物合成,其中72 h時P4濃度最高,雌二醇濃度最低。Xu等[32]使用10-8 mol·L-1褪黑素預處理氧化應激下的牛卵巢顆粒細胞,發現褪黑素可以通過沉默信息調節因子1(SIRT1)/肝臟叉頭框蛋白O1(FoxO1)信號通路促進線粒體自噬,減輕氧化應激誘導的牛卵巢顆粒細胞凋亡和線粒體損傷。楊方曉等[36]證實,使用10-4 mol·L-1褪黑素預處理奶牛卵巢顆粒細胞,能夠顯著降低HT-2毒素誘導的細胞內自噬相關基因微管相關蛋白輕鏈3-Ⅱ(LC3-Ⅱ)的水平,減輕顆粒細胞的自噬作用。以上研究表明,適量褪黑素對正常狀態和應激狀態下體外培養的母牛顆粒細胞發育都有積極的促進作用。
1.2.3" 外源褪黑素調控母牛體外胚胎發育
IVP作為一種世界范圍內使用的輔助生殖技術,是畜牧業中較多生殖問題的替代方案[37]。褪黑素能夠顯著促進牛體外胚胎的發育,提高體外胚胎質量(表4)。例如,Manjunatha等[38]在水牛卵母細胞培養基中添加10-5 mol·L-1和5×10-5 mol·L-1的褪黑素,發現褪黑素可以提高細胞減數分裂成熟率(分別為90.3%和88.8%)和可移植胚胎(TE)產量(分別為28.4%和27.2%)。Sampaio等[39]研究表明,在牛卵母細胞IVM培養基中添加10-12 mol·L-1的褪黑素可提高IVM質量以及受精后胚胎卵裂率和囊胚率。Gutirrez-Aez等[40]在奶牛卵丘卵母細胞復合物培養基中添加10-11 mol·L-1的褪黑素,可以提高體外受精后胚胎囊胚的百分比、內細胞團數(ICM)、胚胎總細胞數。Wang等[41]將10-7 mol·L-1褪黑素添加到牛受精卵的體外培養基中,發現牛胚胎的卵裂率、8細胞胚產量和培養后第7天的囊胚數量顯著升高。
然而,當褪黑素濃度過高或過低時,則對牛胚胎發育無促進作用。Wang等[42]用不同濃度(10-3、10-5、10-7、10-9、10-11 mol·L-1)褪黑素培養牛胚胎,發現10-3 mol·L-1組牛胚胎的囊胚率、孵化囊胚率和平均細胞數/囊胚數與不含褪黑素的效果相當。Tsantarliotou等[43]在牛卵丘-卵母細胞復合物成熟培養基中添加不同濃度(10-5、10-4、10-3 mol·L-1)的褪黑素,與不添加褪黑素(71.0%和41.3%)相比,添加褪黑素對牛胚胎的卵裂率(72.8%、72.5%、72.7%)和囊胚率(33.8%、39.4%、38.3%)無顯著影響。以上研究表明,在牛IVEP過程中添加適量的褪黑素可以有效促進胚胎的發育以及提高體外胚胎的數量和質量,但若添加的濃度過低或過高,都不會發揮有益作用。
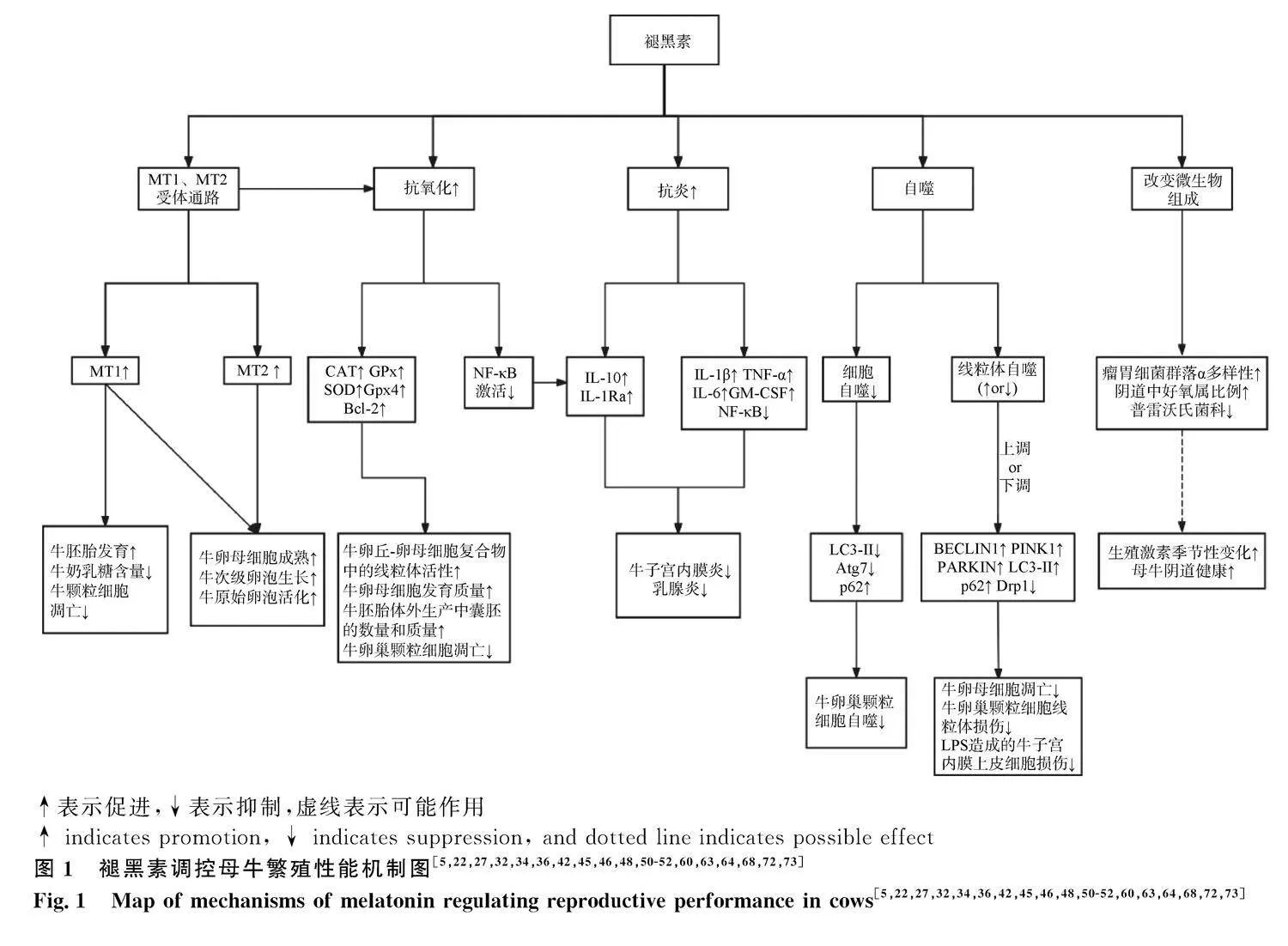
2" 褪黑素調控母牛生殖的作用機理(圖1)
2.1" MT1和MT2受體通路
褪黑素主要通過與G蛋白偶聯受體(MT1和MT2)結合在母牛生殖中發揮有益作用[44]。Tian等[27]使用褪黑素受體激動劑IIK7和拮抗劑luzindole研究褪黑素對牛卵母細胞的作用,發現褪黑素通過受體MT1和MT2介導牛卵母細胞IVM。同樣,在牛次級卵泡的發育過程中,Paulino等[45]也證實了相同的觀點,即褪黑素通過MT1和MT2受體促進牛次級卵泡生長,而luzindole阻斷了褪黑素對卵泡生長的作用。Silva等[46]發現,褪黑素可以通過MT1和MT2受體調節磷脂酰肌醇-3激酶(PI3K)/蛋白激酶B(AKT)/ 哺乳動物雷帕霉素靶蛋白(mTOR)通路,增加牛卵巢組織細胞外基質(ECM)中的膠原纖維,促進ECM中的原始卵泡活化。可見,褪黑素能夠結合MT1和MT2受體調控母牛生殖細胞功能。
MT1受體在母牛繁殖性能調控中占據主導作用。在牛卵巢中,El-Raey等[25]證實在牛卵母細胞和卵丘細胞中,MT1基因在卵丘卵母細胞復合物中表達,而MT2基因僅在卵母細胞中表達。Liu等[47]研究證明,敲低牛顆粒細胞中MT2水平并不會破壞褪黑素抑制顆粒細胞凋亡或阻斷細胞周期的作用,即MT2敲低后,MT1的表達上調,而褪黑素在MT2敲低或不敲低的情況下均促進了MT1的表達。Wang等[34]研究發現,MT1可能通過下調促凋亡基因TP53、Bax和CASP3的表達,上調抗凋亡基因Bcl-2的表達來抑制牛顆粒細胞的凋亡。在牛胚胎中,Wang等[42]發現作為非選擇性MT1和MT2拮抗劑的luzindole阻斷了褪黑素誘導的胚胎發育,而選擇性MT2拮抗劑4-D-PDOT對褪黑素誘導的胚胎發育影響很小,說明褪黑素對牛胚胎發育的有益作用是通過MT1介導的。在牛泌乳中,Liu等[48]研究發現褪黑素通過受體MT1減少牛奶中乳糖含量,即激活MT1下調了催乳素受體基因(PRLR)的mRNA表達,進而抑制了半乳糖轉運蛋白 (SLC35B1)的基因表達。以上研究表明,褪黑素主要通過結合MT1受體調控母牛生殖,但褪黑素通過 MT1受體調控牛卵巢和胚胎發育的具體機制需要更深入地研究。
2.2" 抗炎作用
褪黑素可以下調生殖細胞中抗炎因子的表達,調控母牛的生殖。褪黑素通過在不同的病理或生理條件下調節促炎和抗炎細胞因子發揮其抗炎作用,緩解母牛的生殖炎癥[49]。Gao等[50]證實,褪黑素可以顯著降低牛子宮內膜上皮細胞(BEND)中白細胞介素-1β(IL-1β)、腫瘤壞死因子α(TNF-α)和白細胞介素-6(IL-6)的mRNA表達和釋放,抑制LPS誘導的BEND細胞中核苷酸結合寡聚化結構域樣受體蛋白(NLRP)3炎癥小體的激活,在牛子宮內膜炎中發揮保護作用。Yao等[51]通過荷斯坦奶牛瘤胃旁路進行褪黑素喂養(RBMF),發現褪黑素可以顯著降低奶牛血清中促炎細胞因子IL-6和TNF-α的水平,升高抗炎細胞因子白細胞介素-10(IL-10)的水平,增強奶牛自身的抗炎能力。Yu等[52]發現,在培養基中添加4.3×10-5 mol·L-1褪黑素培養荷斯坦奶牛乳腺上皮細胞,可以顯著降低LPS誘導的促炎細胞因子IL-1β、TNF-α、IL-6和粒細胞-巨噬細胞集落刺激因子(GM-CSF)mRNA水平,增加抗炎細胞因子白介素-1受體拮抗劑(IL-1Ra)mRNA水平,保護細胞免受LPS誘導的炎癥和氧化應激損傷。
此外,褪黑素可以通過抑制轉錄因子核因子κB (NF-κB)的激活發揮抗炎作用,減少活性氧(ROS)導致的母牛生殖炎癥[53]。NF-κB的激活會誘導炎癥介質的表達,對母牛的繁殖性能產生不利影響[54]。NF-κB通過p50和p65蛋白與抑制亞基I-κB連接,以同源或異源二聚體的形式存在[55]。當I-κB存在時,NF-κB以無活性形式存在于細胞質中,而ROS可以激活NF-κB[56]。當細胞受到氧化應激誘導劑的刺激,I-κB激酶激活p65的磷酸化,NF-κB被轉運到細胞核中,進而上調炎癥細胞因子白細胞介素-1(IL-1)、IL-6和TNF-α的轉錄和翻譯,誘發母牛的炎癥反應[55,57,58]。褪黑素可以通過其抗氧化作用,抑制NF-κB的激活,使炎癥介質的表達減少[54,59]。Zheng等[60]添加2.5×10-6 mol·L-1的褪黑素培養牛子宮內膜上皮細胞,發現褪黑素可以降低氨誘導的Toll樣受體4(TLR-4)、NF-κB和IL-6的蛋白表達水平,通過抑制NF-κB信號通路降低IL-6表達,最終改善奶牛VEGF(子宮接受性相關基因)表達和子宮接受性,抑制細胞的炎癥反應。
綜上所述,褪黑素可以抑制促炎因子的表達,增加抗炎因子的表達,進而緩解母牛的乳腺炎和子宮內膜炎。褪黑素具有抗炎作用,但褪黑素調節奶牛子宮炎的具體作用機理還不清楚,有待進一步研究。
2.3" 抗氧化作用
氧化應激會導致母牛生殖細胞內核酸、蛋白質、脂質和碳水化合物的氧化損傷,給細胞造成不可逆的傷害[61]。褪黑素可以通過酶系統清除自由基,直接消除ROS,增加編碼超氧化物歧化酶(SOD)、過氧化氫酶(CAT)等抗氧化酶基因表達,減少母牛的氧化應激[62]。例如,Zhao等[22]用10-7 mol·L-1褪黑素培養牛卵母細胞,可以顯著降低細胞中的ROS水平,增加內源性抗氧化基因Cat、Sod1和谷胱甘肽過氧化物酶(GPx)mRNA的表達水平,改善牛卵母細胞發育質量。Silva等[63]在含有10-8 mol·L-1褪黑素的培養基中進行牛卵丘-卵母細胞復合物(COCs)IVM,發現褪黑素提高了成熟COCs中的SOD和CAT mRNA表達,增加了線粒體活性。Yang等[64]研究證實,10-4 mol·L-1褪黑素可以顯著增加SOD和CAT蛋白的表達,減弱β-玉米烯醇介導的牛卵巢顆粒細胞氧化應激和凋亡。Peng等[65]研究證實,添加10-4 mol·L-1褪黑素可以使H2O2誘導的牦牛著床前胚胎中GPx和CAT活性增加,ROS水平降低,顯著改善牦牛胚胎體外生產中囊胚的數量和質量。Wang等[42]發現,10-7 mol·L-1褪黑素在牛胚胎發育過程中顯著上調了抗氧化基因Gpx4和Sod1的表達,從而清除ROS,減少氧化損傷,促進牛胚胎健康發育。
褪黑素通過清除自由基減少氧化應激的能力與其濃度直接相關。在更高的濃度下有更多的抗氧化劑分子可以淬滅自由基,從而降低氧化損傷和相關疾病[66]。Zhao等[22]將牛卵母細胞用不同濃度(10-7、10-9、10-11 mol·L-1)的褪黑素進行培養,發現10-7 mol·L-1褪黑素組ROS水平最低,高濃度的褪黑素顯著降低了牛卵母細胞中的ROS水平。Marques等[62]用不同濃度(10-7、10-9、10-11 mol·L-1)的褪黑素培養牛卵丘-卵母細胞復合物,發現10-7 mol·L-1褪黑素處理的卵母細胞內ROS量最低。綜上所述,褪黑素可以通過其抗氧化作用,增加母牛卵泡細胞、顆粒細胞以及胚胎中抗氧化酶基因的表達,直接清除ROS,減輕細胞氧化應激。
2.4" 自噬作用
褪黑素可以通過調節生殖細胞內自噬反應調控母牛生殖。褪黑素能夠減少對母牛生殖細胞內關鍵成分的損害,包括線粒體基因組和電子傳遞鏈的蛋白質等,調節細胞自噬[67]。Gao等[50]用褪黑素(10-3 mol·L-1)預處理牛BEND細胞1 h,隨后與LPS(1 μg·mL-1)共孵育24 h,發現褪黑素增加了BEND細胞中線粒體自噬相關蛋白芐氯素1(BECLIN1)、LC3-II、帕金森蛋白(PARKIN)和磷酸酶張力蛋白誘導激酶1 (PINK1)的表達水平,降低了p62的表達,表明褪黑素可以調節線粒體自噬,促進LPS誘導的BEND細胞自噬能力,緩解LPS造成的損傷。Xu等[32]研究證實,用10-8 mol·L-1褪黑素預處理牛卵巢顆粒細胞可以增加PINK1、PARKIN、BECLIN1和LC3-II/微管相關蛋白輕鏈3I(LC3-I)的表達,促進氧化應激誘導的牛卵巢顆粒細胞線粒體自噬以及有絲分裂體和溶酶體的融合,改善牛卵巢顆粒細胞線粒體損傷和線粒體自噬不足,緩解牛卵巢顆粒細胞凋亡。褪黑素也可以通過抑制細胞自噬和線粒體自噬緩解霉菌毒素對母牛生殖的毒害作用。Yang等[36]使用褪黑素培養牛卵巢顆粒細胞,可以顯著抑制HT-2毒素誘導的細胞自噬相關因子7(Atg7)mRNA表達的上調,減輕HT-2毒素引起的p62 mRNA和蛋白表達下調,降低HT-2毒素誘導的LC3-Ⅱ蛋白表達上調,有效緩解HT-2毒素誘導的牛卵巢顆粒細胞自噬作用。El-Sheikh等[68]在胡茹酮暴露的牛卵母細胞培養基中添加2×10-5 mol·L-1褪黑素治療,發現褪黑素可以顯著降低胡茹酮誘導的卵母細胞動力蛋白相關蛋白1(Drp1)的表達水平,抑制線粒體自噬,緩解卵母細胞凋亡。綜上,褪黑素可以通過調節細胞自噬和線粒體自噬相關基因和蛋白質的表達緩解不利因素對母牛生殖細胞的損傷。
近年來,有研究發現褪黑素可以緩解鐵過載誘導的鐵死亡,減輕線粒體功能障礙,減少生殖細胞自噬[69]。鐵穩態的調節對于維持細胞內氧化還原反應的動態平衡十分必要。鐵穩態失衡會觸發鐵過載,鐵過載可作為氧化還原反應的催化劑,導致脂質過氧化物的積累,從而誘導細胞毒性[70]。Fu等[71]研究證實,補充10-3 mol·L-1褪黑素可以抵消玉米赤霉烯酮(ZEN)誘導的人顆粒細胞系(KGN)和小鼠子宮內膜基質細胞(mEC)鐵死亡,降低鐵死亡相關標志物(P53和酰基輔酶A合成酶長鏈家族成員(ACSL4)的蛋白表達,減少ZEN誘導的病理性線粒體和自噬體的產生。因此,褪黑素可以用于緩解鐵過載誘導的鐵死亡,從而緩解生殖細胞自噬,但目前尚未發現褪黑素調控鐵死亡誘導母牛生殖細胞自噬的相關研究。
2.5" 改變微生物組成
褪黑素可以改變瘤胃微生物組成,進而影響母牛繁殖和生殖道健康狀態。Fu等[5]通過建立奶牛體外瘤胃發酵模型,發現褪黑素可以提高瘤胃細菌群落的α多樣性,顯著降低產生丙酸的主要瘤胃細菌普雷沃氏菌科,增加有益細菌的豐度,降低致病細菌的豐度。郭燕[72]通過分析褪黑素與水牛瘤胃微生物和其他生殖激素季節性變化的關系,發現不同季節水牛瘤胃液和血清中的褪黑素濃度以及其他生殖激素均與瘤胃微生物相關,其中Latescibacterota 與水牛瘤胃內褪黑素水平負相關。Acidobacteriota與瘤胃液中的孕酮(P)濃度負相關,與瘤胃液中的促卵泡素(FSH)濃度正相關;Gemmatimonadota、Actinobacteriota與FSH、促黃體素(LH)濃度正相關,與P濃度負相關;Caldatribacteriota與LH、P濃度負相關;Dependentiae與P、雌激素(E2)濃度正相關;Methylomirabilota與LH、E2濃度負相關。褪黑素能夠改變瘤胃微生物的組成,后者又影響其他生殖激素的分泌。因此,外源褪黑素可能通過調節瘤胃微生物組成,從而調控母牛生殖。
此外,褪黑素也可能通過調節母牛陰道微生物群的變化來調控母牛生殖。Messman等[73]證實,從母牛妊娠第160天開始,每天在其日糧中添加20 mg褪黑素,可以改變牛陰道細菌群落的β多樣性,導致好氧屬比例增加。表明褪黑素可以改變陰道微生物群的組成,而陰道微生物群又與生殖道的健康有關。Otero等[74]研究了健康奶牛從斷奶到配種年齡的陰道細菌菌群改變,發現鏈球菌和葡萄球菌在整個研究期間水平相似,而乳酸桿菌水平在奶牛生長過程中增加,定植在奶牛陰道黏膜上的本地微生物群通過動態的細菌群落促進了生殖道的健康。Wang等[75]通過評估肉牛卵泡期和黃體期之間的陰道微生物群落結構,發現肉牛卵泡期和黃體期陰道細菌總數無顯著差異,但黃體期陰道鏈球菌數量顯著高于卵泡期,卵泡期陰道乳酸菌屬數量顯著高于黃體期。Bicalho等[76]研究發現,患有胎盤滯留(RP)、子宮炎、子宮內膜炎(CE)的奶牛在產后第7天時總細菌載量(TBL)均顯著高于健康奶牛,表明陰道微生物群對母牛的繁殖性能十分重要。
因此,褪黑素可能通過調節陰道微生物的變化進而影響母牛的繁殖性能。但關于褪黑素對母牛陰道微生物的調節機制研究較少,褪黑素如何通過陰道微生物調控母牛的繁殖性能目前還尚未有定論。
3" 小結和展望
適量外源褪黑素可以通過與受體(MT1或MT2)結合,促進抗炎因子、抑制促炎因子表達,增強抗氧化功能,調節細胞自噬或線粒體自噬以及改變微生物組成等通路促進正常或應激狀態下母牛體內(外)卵母細胞、顆粒細胞和胚胎發育。下一步應深入研究褪黑素對不同品種(屬)母牛個體或生殖細胞的最適添加劑量、添加方式和添加階段,以及褪黑素在不同生殖器官和生殖細胞中發揮作用的具體機制。
參考文獻(References):
[1]" ARERO G B.Major Reproductive health disorders in dairy cows[J].J Anim Biol Vet Sci,2022,1:1-11.
[2]" ENDO N.Possible causes and treatment strategies for the estrus and ovulation disorders in dairy cows[J].J Reprod Dev,2022, 68(2):85-89.
[3]" LI Z Q,ZHANG K Y,ZHOU Y M,et al.Role of melatonin in bovine reproductive biotechnology[J].Molecules,2023,28(13): 4940.
[4]" DIRANDEH E,ANSARI-PIRSARAEI Z,THATCHER W.Melatonin as a smart protector of pregnancy in dairy cows[J].Antioxidants,2022,11(2):292.
[5]" FU Y,YAO S Y,WANG T K,et al.Effects of melatonin on rumen microorganisms and methane production in dairy cow:results from in vitro and in vivo studies[J].Microbiome,2023,11(1):196.
↑表示促進,↓表示抑制,虛線表示可能作用
↑ indicates promotion, ↓ indicates suppression, and dotted line indicates possible effect
[6]" AHMAD S B,ALI A,BILAL M,et al.Melatonin and health:Insights of melatonin action,biological functions,and associated disorders[J].Cell Mol Neurobiol,2023,43(6):2437-2458.
[7]" ROMANINI E B,VOLPATO A M,DOS SANTOS J S,et al.Melatonin concentration in cow’s milk and sources of its variation[J].J Appl Anim Res,2019,47(1):140-145.
[8]" BROCKUS K E,HART C G,GILFEATHER C L,et al.Dietary melatonin alters uterine artery hemodynamics in pregnant Holstein heifers[J].Domest Anim Endocrinol,2016,55:1-10.
[9]" 趙增元,吳" 昊,姚松陽,等.皮下埋植褪黑素對奶牛超數排卵效果的影響[J].中國奶牛,2022(11):17-22.
ZHAO Z Y,WU H,YAO S Y,et al.Effects of implantation melatonin on superovulation results in dairy cows[J].China Dairy Cattle,2022(11):17-22.(in Chinese)
[10]" RATCHAMAK R,THANANURAK P,BOONKUM W,et al.The melatonin treatment improves the ovarian responses after superstimulation in Thai-Holstein crossbreeds under heat stress conditions[J].Front Vet Sci,2022,9:888039.
[11]" GHUMAN S S,HONPARKHE M,SINGH B.Effect of melatonin implantation prior to ovsynch plus cidr protocol on subsequent ovarian activity and pregnancy rate in summer anestrous Murrah buffaloes[J].Buffalo Bull,2023,42(2):263-269.
[12]" GHUMAN S P S,SINGH J,HONPARKHE M,et al.Induction of ovulation of ovulatory size non-ovulatory follicles and initiation of ovarian cyclicity in summer anoestrous buffalo heifers (bubalus bubalis) using melatonin implants[J].Reprod Domest Anim,2010,45(4):600-607.
[13]" LOCHAN S,HONPARKHE M,CHEEMA R S,et al.Ameliorating postpartum reproductive cyclicity using exogenous melatonin implant in water buffalo (Bubalus bubalis)[J].Indian J Anim Sci,2020,90(2):181-184.
[14]" MCCARTY K J,OWEN M P T,HART C G,et al.Effect of chronic melatonin supplementation during mid to late gestation on maternal uterine artery blood flow and subsequent development of male offspring in beef cattle[J].J Anim Sci,2018,96(12): 5100-5111.
[15]" GUO L,LI M,GAO X,et al.Two melatonin treatments improve the conception rate after fixed-time artificial insemination in beef heifers following synchronisation of oestrous cycles using the CoSynch-56 protocol[J].Aust Vet J,2021,99(10):449-455.
[16]" REID D S,GEARY T W,ZEZESKI A L,et al.Effects of prenatal and postnatal melatonin supplementation on overall performance,male reproductive performance,and testicular hemodynamics in beef cattle[J].J Anim Sci,2023,101:skad111.
[17]" SWANSON R M,CONTRERAS-CORREA Z E,DINH T,et al.Effects of melatonin supplementation during mid-to late-gestation nutrient restriction on maternal and fetal amino acid concentrations[J].J Anim Sci,2021,99(S2):17.
[18]" BRYDON L,PETIT L,DELAGRANGE P,et al.Functional expression of MT2 (Mel1b) melatonin receptors in human PAZ6 adipocytes[J].Endocrinology,2001,142(10):4264-4271.
[19]" HEO J S,PYO S,LIM J Y,et al.Biological effects of melatonin on human adipose-derived mesenchymal stem cells[J].Int J Mol Med,2019,44(6):2234-2244.
[20]" RAKHA S I,ELMETWALLY M A,EL-SHEIKH ALI H,et al.Importance of antioxidant supplementation during in vitro maturation of mammalian oocytes[J].Vet Sci,2022,9(8):439.
[21]" KRISHER R L.The effect of oocyte quality on development[J].J Anim Sci,2004,82(S13):E14-E23.
[22]" ZHAO X M,WANG N,HAO H S,et al.Melatonin improves the fertilization capacity and developmental ability of bovine oocytes by regulating cytoplasmic maturation events[J].J Pineal Res,2018,64(1):e12445.
[23]" PANG Y W,ZHAO S J,SUN Y Q,et al.Protective effects of melatonin on the in vitro developmental competence of bovine oocytes[J].Anim Sci J,2018,89(4):648-660.
[24]" CAVALCANTE B N,MATOS-BRITO B G,PAULINO L R F M,et al.Effects of melatonin on morphology and development of primordial follicles during in vitro culture of bovine ovarian tissue[J].Reprod Domest Anim,2019,54(12):1567-1573.
[25]" EL-RAEY M,GESHI M,SOMFAI T,et al.Evidence of melatonin synthesis in the cumulus oocyte complexes and its role in enhancing oocyte maturation in vitro in cattle[J].Mol Reprod Dev,2011,78(4):250-262.
[26]" YANG M H,TAO J L,CHAI M L,et al.Melatonin improves the quality of inferior bovine oocytes and promoted their subsequent IVF embryo development:mechanisms and results[J].Molecules,2017,22(12):2059.
[27]" TIAN X Z,WANG F,HE C J,et al.Beneficial effects of melatonin on bovine oocytes maturation:a mechanistic approach[J].J Pineal Res,2014,57(3):239-247.
[28]" 高" 超,田秀芝,張" 璐,等.外源褪黑素對牛卵母細胞體外成熟的影響[J].中國農業科學,2011,44(17):3634-3640.
GAO C,TIAN X Z,ZHANG L,et al.Effect of exogenous melatonin (MT) in bovine oocyte in vitro maturation[J].Scientia Agricultura Sinica,2011,44(17):3634-3640.(in Chinese)
[29]" YANG L,WANG Q K,CUI M S,et al.Effect of melatonin on the in vitro maturation of porcine oocytes,development of parthenogenetically activated embryos,and expression of genes related to the oocyte developmental capability[J].Animals (Basel),2020,10(2):209.
[30]" BARROS V R P,MONTE A P O,SANTOS J M S,et al.Effects of melatonin on the in vitro growth of early antral follicles and maturation of ovine oocytes[J].Domest Anim Endocrinol,2020,71:106386.
[31]" NIKMARD F,HOSSEINI E,BAKHTIYARI M,et al.Effects of melatonin on oocyte maturation in PCOS mouse model[J].Anim Sci J,2017,88(4):586-592.
[32]" XU G Q,DONG Y Y Y,WANG Z,et al.Melatonin attenuates oxidative stress-induced apoptosis of bovine ovarian granulosa cells by promoting mitophagy via SIRT1/FoxO1 signaling pathway[J].Int J Mol Sci,2023,24(16):12854.
[33]" WANG S J,LIU W J,WU C J,et al.Melatonin suppresses apoptosis and stimulates progesterone production by bovine granulosa cells via its receptors (MT1 and MT2)[J].Theriogenology,2012,78(7):1517-1526.
[34]" WANG S J,LIU W J,WANG L K,et al.The role of Melatonin receptor MTNR1A in the action of Melatonin on bovine granulosa cells[J].Mol Reprod Dev,2017,84(11):1140-1154.
[35]" RIAZ H,YOUSUF M R,LIANG A X,et al.Effect of melatonin on regulation of apoptosis and steroidogenesis in cultured buffalo granulosa cells[J].Anim Sci J,2019,90(4):473-480.
[36]" 楊方曉,李" 蓮,趙若含,等.褪黑素對HT-2毒素誘導的牛卵巢顆粒細胞內質網應激與自噬的影響[J].南京農業大學學報,2020,43(1):143-150.
YANG F X,LI L,ZHAO R H,et al.Effects of melatonin on endoplasmic reticulum stress and autophagy in bovine ovarian granulosa cells induced by HT-2 toxin[J].Journal of Nanjing Agricultural University,2020,43(1):143-150.(in Chinese)
[37]" DE AVILA FERRONATO G,DOS SANTOS C M,DA S ROSA P M,et al.Bovine in vitro oocyte maturation and embryo culture in liquid marbles 3D culture system[J].PLoS One,2023,18(4):e0284809.
[38]" MANJUNATHA B M,DEVARAJ M,GUPTA P S P,et al.Effect of taurine and melatonin in the culture medium on buffalo in vitro embryo development[J].Reprod Domest Anim,2009,44(1):12-16.
[39]" SAMPAIO R V,CONCEIO D S B,MIRANDA M S,et al.MT3 melatonin binding site,MT1 and MT2 melatonin receptors are present in oocyte,but only MT1 is present in bovine blastocyst produced in vitro[J].Reprod Biol Endocrinol,2012,10:103.
[40]" GUTIRREZ-AEZ J C,LUCAS-HAHN A,HADELER K G,et al.Melatonin enhances in vitro developmental competence of cumulus-oocyte complexes collected by ovum pick-up in prepubertal and adult dairy cattle[J].Theriogenology, 2021,161: 285-293.
[41]" WANG F,TIAN X Z,ZHOU Y H,et al.Melatonin improves the quality of in vitro produced (IVP) bovine embryos:implications for blastocyst development,cryotolerance,and modifications of relevant gene expression[J].PLoS One,2014,9(4):e93641.
[42]" WANG F,TIAN X Z,ZHANG L,et al.Beneficial effects of melatonin on in vitro bovine embryonic development are mediated by melatonin receptor 1[J].J Pineal Res,2014,56(3):333-342.
[43]" TSANTARLIOTOU M P,ATTANASIO L,DE ROSA A,et al.The effect of melatonin on bovine in vitro embryo development[J]. Ital J Anim Sci,2007,6(S1):488-489.
[44]" GAO Y,ZHAO S Q,ZHANG Y,et al.Melatonin receptors:a key mediator in animal reproduction[J].Vet Sci,2022,9(7):309.
[45]" PAULINO L R F M,BARROSO P A A,SILVA B R,et al.Immunolocalization of melatonin receptors in bovine ovarian follicles and in vitro effects of melatonin on growth,viability and gene expression in secondary follicles[J].Domest Anim Endocrinol, 2022, 81:106750.
[46]" SILVA B R,COSTA F C,DE LIMA NETO M F,et al.Melatonin acts through different mechanisms to control oxidative stress and primordial follicle activation and survival during in vitro culture of bovine ovarian tissue[J].Domest Anim Endocrinol, 2024,86:106824.
[47]" LIU W J,WANG S J,ZHOU J X,et al.RNAi-mediated knockdown of MTNR1B without disrupting the effects of melatonin on apoptosis and cell cycle in bovine granulose cells[J].PeerJ,2018,6:e4463.
[48]" LIU Y J,YAO S Y,MENG Q G,et al.A novel signaling transduction pathway of melatonin on lactose synthesis in cows via melatonin receptor 1 (MT1) and prolactin receptor (PRLR)[J].Peer J,2023,11:e15932.
[49]" FAVERO G,FRANCESCHETTI L,BONOMINI F,et al.Melatonin as an anti-inflammatory agent modulating inflammasome activation[J].Int J Endocrinol,2017,2017:1835195.
[50]" GAO Y J,LI Y N,WANG J M,et al.Melatonin alleviates lipopolysaccharide-induced endometritis by inhibiting the activation of NLRP3 inflammasome through autophagy[J].Animals (Basel),2023,13(15):2449.
[51]" YAO S Y,WU H,MA H,et al.Effects of rumen bypass melatonin feeding (RBMF) on milk quality and mastitis of Holstein cows[J].PeerJ,2020,8:e9147.
[52]" YU G M,KUBOTA H,OKITA M,et al.The anti-inflammatory and antioxidant effects of melatonin on LPS-stimulated bovine mammary epithelial cells[J].PLoS One,2017,12(5):e0178525.
[53]" FERLAZZO N,ANDOLINA G,CANNATA A,et al.Is melatonin the cornucopia of the 21st century?[J].Antioxidants (Basel),2020,9(11):1088.
[54]" BANTOUNOU M,PLASCEVIC J,GALLEY H F.Melatonin and related compounds:Antioxidant and anti-inflammatory actions[J].Antioxidants(Basel),2022,11(3):532.
[55]" LI H Y,SUN P.Insight of melatonin:the potential of melatonin to treat bacteria-induced mastitis[J].Antioxidants (Basel),2022, 11(6):1107.
[56]" MUOZ-JURADO A,ESCRIBANO B M,CABALLERO-VILLARRASO J,et al.Melatonin and multiple sclerosis: Antioxidant,anti-inflammatory and immunomodulator mechanism of action[J]. Inflammopharmacology, 2022,30(5): 1569-1596.
[57]" CHO J H,BHUTANI S,KIM C H,et al.Anti-inflammatory effects of melatonin:A systematic review and meta-analysis of clinical trials[J].Brain Behav Immun,2021,93:245-253.
[58]nbsp; TOMS-ZAPICO C,COTO-MONTES A.A proposed mechanism to explain the stimulatory effect of melatonin on antioxidative enzymes[J]. J Pineal Res,2005,39(2):99-104.
[59]" MA J Y,WANG J E,HU S M,et al.Effects of melatonin on development and hormone secretion of sheep theca cells in vitro[J].Theriogenology,2023,198:172-182.
[60]" ZHENG P,QIN X,FENG R,et al.Alleviative effect of melatonin on the decrease of uterine receptivity caused by blood ammonia through ROS/NF-κB pathway in dairy cow[J].Ecotoxicol Environ Saf,2022,231:113166.
[61]" ARANDA-RIVERA A K,CRUZ-GREGORIO A,ARANCIBIA-HERNNDEZ Y L,et al.RONS and oxidative stress:an overview of basic concepts[J].Oxygen,2022,2(4):437-478.
[62]" MARQUES T C,DA SILVA SANTOS E C,DIESEL T O,et al.Melatonin reduces apoptotic cells,SOD2 and HSPB1 and improves the in vitro production and quality of bovine blastocysts[J].Reprod Domest Anim,2018,53(1):226-236.
[63]" SILVA B R,BARROZO L G,NASCIMENTO D R,et al.Effects of cyclic adenosine monophosphate modulating agents during oocyte pre-maturation and the role of melatonin on in vitro maturation of bovine cumulus-oocyte complexes[J].Anim Reprod Sci,2023,257:107327.
[64]" YANG F X,LI L,CHEN K L,et al.Melatonin alleviates β-zearalenol and HT-2 toxin-induced apoptosis and oxidative stress in bovine ovarian granulosa cells[J].Environ Toxicol Pharmacol,2019,68:52-60.
[65]" PENG W,LEI M T,ZHANG J,et al.The protective effect of melatonin on the in vitro development of yak embryos against hydrogen peroxide-induced oxidative injury[J].Zygote,2019,27(3):118-125.
[66]" REITER R J,MAYO J C,TAN D X,et al.Melatonin as an antioxidant:under promises but over delivers[J].J Pineal Res,2016,61(3):253-278.
[67]" TARGHAZEH N,REITER R J,RAHIMI M,et al.Oncostatic activities of melatonin:Roles in cell cycle,apoptosis,and autophagy[J].Biochimie,2022,202:34-48.
[68]" EL-SHEIKH M,MESALAM A A,KANG S M,et al.Modulation of apoptosis and autophagy by melatonin in juglone-exposed bovine oocytes[J].Animals (Basel),2023,13(9):1475.
[69]" HU W Y,ZHANG Y,WANG D L,et al.Iron overload-induced ferroptosis impairs porcine oocyte maturation and subsequent embryonic developmental competence in vitro[J].Front Cell Dev Biol,2021,9:673291.
[70]" XIA L J,SHEN Y P,LIU S Y,et al.Iron overload triggering ECM-mediated Hippo/YAP pathway in follicle development:a hypothetical model endowed with therapeutic implications[J].Front Endocrinol (Lausanne),2023,14:1174817.
[71]" FU W,DAI C,MA Z F,et al.Enhanced glutathione production protects against zearalenone-induced oxidative stress and ferroptosis in female reproductive system[J].Food Chem Toxicol,2024,185:114462.
[72]" 郭" 燕.褪黑素與水牛瘤胃菌群和生殖激素季節性波動的關系[D].武漢:華中農業大學,2023.
GUO Y.Relationship between melatonin and rumenflora and seasonal fluctuation of reproductive hormones in buffalo[D]. Wuhan:Huazhong Agricultural University,2023.(in Chinese)
[73]" MESSMAN R D,CONTRERAS-CORREA Z E,PAZ H A,et al.Melatonin-induced changes in the bovine vaginal microbiota during maternal nutrient restriction[J].J Anim Sci,2021,99(5):skab098.
[74]" OTERO C,SAAVEDRA L,DE RUIZ C S,et al.Vaginal bacterial microflora modifications during the growth of healthy cows[J].Lett Appl Microbiol,2000,31(3):251-254.
[75]" WANG J,LIU C,NESENGANI L T,et al.Comparison of vaginal microbial community structure of beef cattle between luteal phase and follicular phase[J].Indian J Anim Res,2019,53(10):1298-1303.
[76]" BICALHO M L S,SANTIN T,RODRIGUES M X,et al.Dynamics of the microbiota found in the vaginas of dairy cows during the transition period:Associations with uterine diseases and reproductive outcome[J].J Dairy Sci,2017,100(4):3043-3058.
(編輯" 郭云雁)

