西尼羅熱診斷技術
摘" 要: 西尼羅熱(West Nile fever,WNF)是由西尼羅病毒(West Nile virus,WNV)感染引起的一種人獸共患病,主要通過蚊子叮咬傳播,臨床表現以發熱、皮疹和淋巴結腫大等為主,可侵犯中樞神經系統產生腦炎癥狀,人類對其高度易感且致死率較高。對于WNF的防控目前尚無可用疫苗和特效治療藥物。及時、準確的診斷,對治療和防止疫情的快速傳播具有極重要的意義。本文對當前WNV檢測技術的最新成果、診斷方法發展方向進行了概述,其中病原學診斷技術主要包括病毒分離、RT-PCR、等溫擴增技術等,血清學診斷包括ELISA、免疫熒光法和免疫組織化學技術等,近年來基于高通量測序的宏基因組技術也成功應用于WNF的診斷與研究,新技術的創新及其在疫病檢測上的應用將極大地促進WNF的檢測和防控技術的發展。
關鍵詞: 西尼羅熱;西尼羅病毒;診斷技術
中圖分類號:S852.659.6
文獻標志碼:A
文章編號:0366-6964(2024)12-5423-08
doi: 10.11843/j.issn.0366-6964.2024.12.009
開放科學(資源服務)標識碼(OSID):
收稿日期:2023-11-07
基金項目:重大外來動物疫病阻斷與防控技術研發項目(2022YFD1800500)
作者簡介:周師眾(1999-),男,湖南人,碩士生,主要從事布魯氏菌耐藥性及其生物信息學研究,E-mail: aa1245846152@163.com
*通信作者:沈青春,主要從事動物支原體、布魯氏菌病防控及其生物信息學研究,E-mail: shenqingchun@caas.cn
Diagnostic Technology of West Nile Fever
ZHOU" Shizhong, QIAN" Jiahao, ZHANG" Boyuan, LIU" Dan, GAO" Jianshuai, DING" Jiabo, QIN" Tong, SHEN" Qingchun*
(Key Laboratory of Animal Biosafety Risk Prevention and Control (North) of Ministry of Agriculture and Rural Affairs, Institute of Animal Sciences of CAAS, Beijing 100193," China)
Abstract: West Nile fever (WNF) is an infectious zoonotic ailment engendered by the West Nile virus(WNV), predominantly disseminated via mosquito bites. The clinical presentation of this malady includes symptoms like fever, rash, and lymphadenopathy, with a potential to affect the central nervous system, leading to encephalitic manifestations. Humans demonstrate considerable vulnerability and a relatively elevated mortality rate associated with this disease. Presently, the absence of efficacious vaccines or specific therapeutic agents for WNF necessitates the importance of prompt, accurate, and timely diagnostic procedures for effective patient management and curtailing the swift spread of epidemics. This review delineates the recent advancements WNV detection technologies and the evolving landscape of diagnostic methodologies. Principal etiological diagnostic approaches comprise virus isolation, RT-PCR, and isothermal amplification, whereas serological diagnostics include techniques like ELISA, immunofluorescence, and immunohistochemistry. Additionally, the advent of metagenomics, underpinned by high-throughput sequencing, has been effectively utilized in the diagnosis and exploration of WNF in recent years. The ongoing innovation in novel technologies and their integration into disease detection are pivotal in augmenting the progression of WNF detection and preventive strategies.
Key words: West Nile fever; West Nile virus; diagnostic technology
*Corresponding author: SHEN Qingchun,E-mail: shenqingchun@caas.cn
西尼羅熱(West Nile fever,WNF)是一種由西尼羅病毒(West Nile virus,WNV)引起的人畜共患病。WNV最初于1937年在烏干達西尼羅地區一名發熱女性患者的血液中被分離獲得,因而得名。該病毒主要通過蚊子傳播,尤其是伊蚊和庫蚊,主要感染鳥類、人類及馬、牛等哺乳動物,鳥類是其主要儲存宿主。在宿主體內,WNV能復制并產生病毒血癥,可能導致人類和馬出現致命的腦炎,以及雞和野生鳥類的死亡[1]。人類通常通過被攜帶病毒的蚊蟲叮咬而感染,臨床癥狀主要包括高熱、頭痛、肌肉疼痛、皮疹和淋巴結腫大等。該病毒可侵襲中樞神經系統,引發腦膜炎癥狀。一旦出現并發的神經性癥狀,其致死率和致殘率較高。研究表明,免疫系統的過度激活可能導致炎癥反應和組織損傷,進而加重WNV感染的嚴重程度[2]。
1" 西尼羅病毒概況
WNV為黃病毒科黃病毒屬的成員,根據遺傳學特性,可分為至少5個不同的譜系,即譜系1~譜系5,其中譜系1和譜系2與人類西尼羅熱相關。1937年首次被發現的WNV以及其后在全球部分地區傳播的毒株(如NY99、Israel 1998、Morocco 2003等)屬于譜系1;譜系2最早在非洲發現,21世紀初出現在中歐和東歐地區的毒株(如Kunjin、Hungary 2004、Greece 2010等)也屬于譜系2。
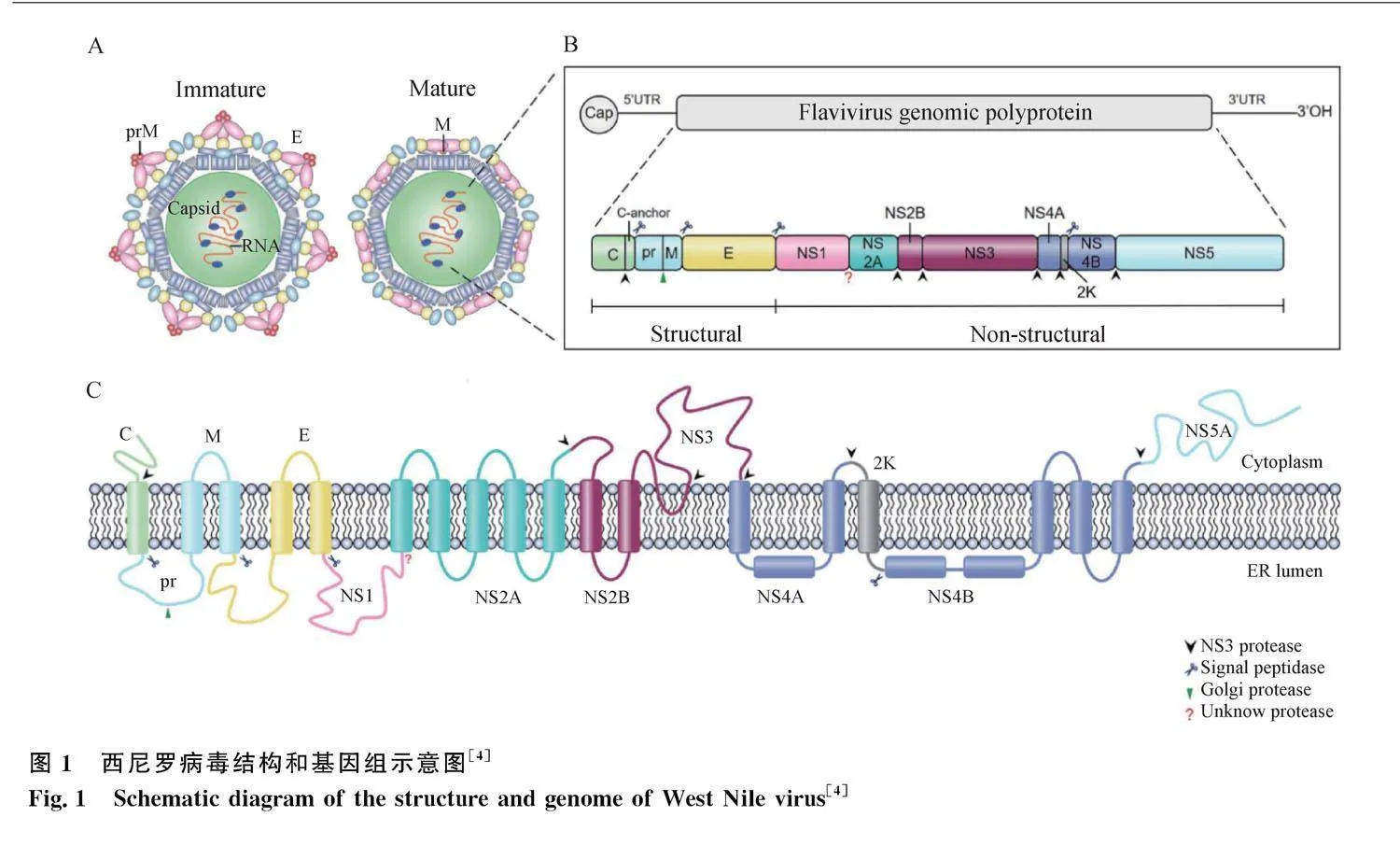
WNV直徑約50 nm,外殼為被脂質包膜包圍的二十面體核衣殼[3],其結構示意圖和基因組結構圖見圖1[4]。該病毒基因組為長度11 kb左右的單鏈RNA,5′端為I型帽結構(m7GpppAmp),3′端沒有ployA尾巴[5]。病毒RNA可以被翻譯成多個蛋白,被細胞和病毒蛋白酶切割成3種結構蛋白(C蛋白、E蛋白和prM蛋白)和7種非結構蛋白(NS1、NS2a、NS2b、NS3、NS4a、NS4b和NS5蛋白)[6],C蛋白是構成病毒衣殼的主要成分[7];E蛋白是與宿主細胞受體結合的主要表面蛋白;prM蛋白促進病毒顆粒形成和從宿主細胞釋放,保護E蛋白不被宿主細胞識別[8];NS1蛋白參與病毒復制與免疫逃逸[9];在同為黃病毒屬的登革熱病毒中,NS2A蛋白和NS2B蛋白被證明通過形成膜通道來滲透不同的膜模型,以及通過自寡聚參與一系列病毒功能[10];NS3蛋白是病毒復制和組裝的關鍵酶,具有蛋白酶和核酸酶活性[11];NS4A、NS4B蛋白功能尚不完全明確;NS5是黃病毒非結構蛋白中最保守的蛋白,負責病毒基因組的蓋帽、甲基化和復制[12-14]。其中,E蛋白[15]和NS1蛋白[16]具有良好的免疫原性,是血清學檢測方法的重要靶點,這兩個蛋白基因的保守序列及WNV基因組的非翻譯區保守基因序列也常被用于核酸檢測的靶標序列。
WNV在全球范圍內廣泛分布,近年來在歐洲、非洲、東地中海、北美和西亞地區的傳播尤為活躍,且在歐洲顯示出頻發趨勢。據統計,自2019年起,希臘共診斷出35例西尼羅病毒感染病例,患者年齡在52至91歲之間。2022年,歐盟共報告了1 133個西尼羅河感染病例(其中92例死亡),涉及11個歐洲國家。意大利報告的病例最多(感染723例,死亡51例),其次為希臘(感染286例)。2023年7月,歐洲4個國家再次報告了41例感染病例,死亡3例,其中包括意大利(26例,死亡1例)、希臘(11例,死亡2例)、法國(3例)和匈牙利(1例)[17-19]。同時,西班牙和德國也報告了動物(馬和鳥類)的疫情,盡管未發現人類感染病例。
目前,尚無特定的抗病毒藥物可用于治療WNV感染,針對人類的疫苗也尚未上市。一種基于植物提取物的候選疫苗正在研發中[2]。
2" 診斷技術
國際上對西尼羅河熱的防控是以大規模監測和預防為主,主要防控措施包括防蚊措施推廣、風險區域的人員與動物的監測以及對疑似或確診病例進行隔離治療等。西尼羅河熱的檢測技術可分為病原學診斷技術、血清學診斷技術及其他新型診斷技術。
2.1" 病原分離鑒定
病毒分離是病毒學研究的基礎,主要目的是從臨床樣本中分離出病原體,并通過對病原體的鑒定和分析,了解其基本特征和生物學特性。常用細胞培養法分離西尼羅病毒,即取腦組織(尤其是后腦和髓質)、脊髓或感染早期血清接種于RK-13細胞、Vero細胞或BHK21細胞,每天觀察細胞病變情況。病毒的鑒定和定型通常采取中和試驗(neutralization test)進行,主要包括蝕斑減少中和試驗
(plaque reduction neutralization test,PRNT)、微量中和試驗(micro-neutralization test,MNT)、病毒中和試驗(virus neutralization test,VNT),其中PRNT被認為是定量和定性檢測抗黃病毒中和抗體或黃病毒科的病毒鑒定與定性的金標準[20-21]。
西尼羅病毒分離培養鑒定所需的時間長(約6 d),操作復雜,對樣品質量要求高,并且必須在生物安全Ⅲ級及以上的實驗室內操作。
2.2" 核酸檢測技術
2.2.1" RT-PCR技術
RT-PCR技術可通過特異性地擴增西尼羅病毒特征序列實現對微量的病毒RNA監測,具有良好的特異性和敏感性,也可方便檢測出早期感染者。當前廣泛應用于臨床的檢測方法主要包括兩種,即巢式RT-PCR和熒光定量RT-PCR。
巢式RT-PCR,又稱為嵌套式RT-PCR,比常規RT-PCR的敏感度高十倍以上,可以靈敏地檢測出組織病料中的微量RNA。Zaayman等[22]開發的巢式RT-PCR可以檢測出WNV譜系1a、1b和2,同時在特異性和敏感性方面表現俱佳。
熒光定量RT-PCR,相較于巢式RT-PCR,具有更快的檢測速度和較低的污染風險。在保證了靈敏度的同時,還具備更適合定量檢測且適用于高通量分析等優點,因而也得到了廣泛的應用。邱璐等[23]針對E蛋白基因的保守序列設計引物,建立了WNV核酸的熒光定量RT-PCR方法,發現不與同屬的日本腦炎病毒和登革病毒發生交叉反應,靈敏度可達0.01 pg,相較于常規PCR靈敏度提高了100倍。Linke等[24]針對WNV譜系1和2建立了一種熒光定量RT-PCR方法,基于譜系1和2的保守區域進行擴增,可靈敏、快速檢測譜系1和2,并且與其他黃病毒如黃熱病病毒、登革病毒、日本腦炎病毒和圣路易斯腦炎病毒無反應,適用于西尼羅河病毒的診斷和監測研究。但除了西尼羅病毒譜系1和2之外還有其他變異株。Vzquez等[25]則為填補這一空白,建立了更為全面的熒光定量RT-PCR方法,可以檢測到其他WNV譜系和變異株。它將引物和探針設計在病毒基因組的3′端非翻譯區,結果與所有測序的西尼羅病毒株完美匹配,靈敏度可以達到1.5到15個copies·μL-1。
近些年,數字PCR(digital PCR,dPCR)也被應用于WNV的檢測。dPCR可將單個核酸分子制成微反應單元,通過檢測微反應單元的熒光濃度達到絕對定量。張俊鋒等[26]建立的WNV上沖微滴式數字PCR敏感性和特異性俱佳,并且在高病毒濃度和低病毒濃度下的變異系數較小,體現了dPCR在病毒定量檢測方面的高可靠性。
2.2.2" 等溫擴增技術
等溫擴增技術(isothermal amplification)是一種在恒定溫度下進行的DNA或RNA的快速擴增方法,省略了復雜的溫度循環,快速簡便,對于抑制物質(如血液、組織提取物等)的耐受性較好,所需的設備相對簡單,降低了成本,因此適用現場檢測或者大批量的快速檢測。
環介導等溫擴增技術(loop-mediated isothermal amplification,LAMP)是一種基于等溫擴增技術的核酸檢測方法。2004年,Parida等[27]開發了一種快速檢測WNV的實時RT-LAMP方法,具有極高的靈敏度,可以檢測到0.1 PFU病毒,且不與相關的黃病毒屬成員發生交叉反應,但實時濁度分析可能會受到背景干擾。Cao等[28]開發了一種新的診斷西尼羅病毒的LAMP方法,結合VF顯示條帶判斷結果,這些條帶被封閉在塑料防漏設備中,從而減少受污染或干擾的風險。
逆轉錄重組酶聚合酶擴增技術(RT-RPA)、逆轉錄酶促重組等溫擴增技術(RT-ERA)與逆轉錄重組酶介導擴增檢測(RT-RAA)三者的原理相似,不同之處在于重組酶的來源,這導致了它們的專利和命名的差異。呂沁風等[29]建立了一種西尼羅病毒逆轉錄重組酶介導擴增檢測方法(RT-RAA),反應溫度為39 ℃,在20 min內出結果,敏感度可達10 copies·μL-1,并且其他黃病毒屬的黃熱病毒、登革病毒、日本腦炎病毒及甲病毒屬的基孔肯雅病毒無擴增曲線,具有良好的特異性。而在張逸龍等[30]建立的RT-ERA方法中,敏感度可以提高至1 copies·μL-1。
2.2.3" 宏基因組學
宏基因組學是基于高通量測序的研究樣品中所有微生物群體的物種和豐度信息的技術,可以被用于對蚊子或其他宿主中的病毒群體進行監測,從而提前預測可能的疫情爆發。除此之外,通過對不同時間、地點或宿主來源的樣本進行宏基因組測序,可以跟蹤西尼羅病毒的遺傳變異和進化。Wollants等[31]對一名比利時的老年患者進行了一系列常規診斷測試,所有結果均為陰性,但通過對培養的呼吸道樣本進行高通量測序和宏基因組分析,檢測人員得到了一個完整的西尼羅病毒基因組。
2.3" 血清學檢測技術
血清學檢測技術包括抗原檢測和抗體檢測兩大類。抗體檢測通過檢測體液中的特定抗體來確認病原體接觸史,適用于免疫監測和疫苗效果評估。抗原檢測直接檢測病原體存在,適用于早期診斷和疫情控制。抗體檢測相對穩定,但可能錯過早期感染,而抗原檢測速度快但穩定性較差。WNV感染機體后,會刺激機體產生抗體,有利于WNV顆粒從活體動物的機體中清除[32-34],因此WNV抗體的檢測更為常用。
血清學檢測技術已廣泛應用于西尼羅病毒診斷和傳染病監測,常用的技術包括中和試驗(neutralization test,NT)、酶聯免疫吸附測定法(enzyme-linked immunosorbent assay,ELISA)、免疫熒光法(immuno-fluorescence assay,IFA)等。中和試驗為早期的檢測方法,當前主要用于病毒鑒定或中和抗體的定性與定量。ELISA和IFA可以檢測體液中的抗原或抗體,還有血凝抑制試驗(hemagglutination inhibition,HI)和補體結合試驗(complement fixation test,CFT)主要用于檢測體液中的抗體,免疫組化法(immunohistochemistry,IHC)主要用于檢測組織樣本中的抗原。
2.3.1" ELISA
酶聯免疫吸附試驗(enzyme-linked immunosorbent assay,ELISA)在WNV檢測中扮演著重要角色,不僅為臨床診斷提供了工具,也為疫情監控和病毒學研究提供了支持,是目前應用得最為廣泛的血清學檢測方法,在臨床實踐中,以檢測WNV抗體為目的的ELISA方法更為常用。
由于IgM抗體不能穿過血腦屏障,其在腦脊液中的存在證明宿主的中樞神經系統已受到感染和損害。腦脊液中檢測西尼羅河病毒IgM抗體是一種非常敏感的檢測方法,幾乎所有腦炎或腦膜炎患者在癥狀出現后8 d內腦脊液中均可檢測到高水平的IgM抗體[35]。Martin等[36]在建立一種基于西尼羅病毒E蛋白的IgM捕獲ELISA檢測方法過程中,發現IgM捕獲ELISA比IgG捕獲ELISA有著更低的交叉反應。Ludolfs等[37]建立了一種獨特的反向ELISA方法(reverse-ELISA)來檢測基于西尼羅病毒E蛋白Ⅲ結構域的IgG抗體,用過氧化物酶標記原核表達的WNV E蛋白結構域III抗原,再通過將血清樣品與酶標記抗原混合,形成免疫復合物,同時可以被類風濕因子包被的微量滴度板識別。經檢驗,符合率為77.6%(206份WNV感染者血清檢出160份陽性),在檢測急性確診的WNV感染血清樣本中,檢測符合率為100%,特異性為98.5%。由于部分黃病毒科成員(如寨卡病毒、日本腦炎病毒)的E蛋白Ⅲ結構域與WNV的相似性較高,檢測結果還需進一步評估。
2015年巴西爆發寨卡病毒疫情,暴露了黃病毒診斷的一大難點,即基于E蛋白建立的ELISA方法不能有效區分同屬不同種類的黃病毒。E蛋白抗原的交叉反應表位主要位于融合環內或附近,在70到115位氨基酸之間,參與病毒與細胞膜的融合,在黃病毒屬內高度保守[38-39]。基于寨卡病毒NS1蛋白的ELISA檢測方法顯示出更好的特異性[40]。Ding等[41]開發了基于WNV的NS1蛋白抗原捕獲ELISA方法表現出良好的特異性,對黃病毒屬的其他成員無交叉反應等。也有人更加深入地去開發基于WNV E蛋白的ELISA方法,曹增國[42]成功建立了一種針對WNV抗體的間接ELISA方法,與含日本乙型腦炎、委內瑞拉馬腦炎、東部馬腦炎、西部馬腦炎抗體的陽性血清均不發生交叉反應,批內和批間重復試驗變異系數均小于7%。
當前對WNF的血清學檢測方法主要包括IgM捕獲ELISA(MAC-ELISA)和IgG捕獲ELISA(IgG-ELISA),IgM捕獲ELISA常應用于感染前期的檢測,一般在感染后1~2周間檢測更為敏感,而IgG捕獲ELISA的檢測窗口期較長,一般在病程2周后檢測更為敏感。2012年,美國WNV流行病爆發時,各州衛生與環境部門采用IgM捕獲ELISA技術進行大規模的WNV感染監測。
2.3.2" 免疫熒光法(IFA)
IFA是一種常用的定性檢測和定量方法,它利用熒光標記的二抗或其他探針來檢測待測樣本中是否存在特定的抗原或抗體。Malan等[43]利用IFA檢測了82份血清樣本和16份腦脊液樣本中針對WNV的IgM和IgG,并將結果分別與MAC-ELISA和IgG-ELISA檢測結果進行比對,發現IgG-IFA的一致性、臨床敏感性和臨床特異性分別為92%、100%和90%,而IgM-IFA的一致性、臨床敏感性和臨床特異性分別為98%、96%和100%。這表明IFA與ELISA檢測結果相近,但對于急性感染的檢測,ELISA敏感性略高于IFA,且IFA對設備和實驗人員的技術要求更高。
2.3.3" 免疫組織化學法(IHC)
IHC是一種結合顯微解剖學和免疫生物學成分的方法,最常用于檢測死亡病例組織樣本中的WNV抗原,但其對操作人員技術要求高、時間長等特點都限制了這項技術的廣泛應用。Pennick等[44]使用基于E蛋白Ⅲ結構域的一個表位抗體對馬進行IHC檢測,并用RT-PCR進行驗證。結果表明,陽性馬腦組織的IHC陽性率為零。在Godhardt等[45]的研究中,對19個陽性鴉類的腦、腎、皮膚組織進行IHC檢查,腎組織中有17份被檢測到WNV,皮膚樣本中有15份陽性,而在腦組織中只有9份陽性。因此,腦組織不推薦使用免疫組織化學法進行檢測。
血凝抑制試驗(HI)和補體結合試驗(CFT)可作為一種輔助檢測WNV抗體的手段,沒有實驗室生物安全等級限制,具有檢測快速、成本低廉的優點。
2.4" 其他診斷技術
近些年發展起來的微流控技術,以其在微米尺度上對流體的精密操控而聞名,通過與其他診斷方法的結合應用,已成為生物醫學研究和臨床診斷的重要工具。這項技術通過在芯片上集成微型管道、閥門和其他功能單元,實現了對流體流動和化學反應的高度控制,特別是在處理極小量的生物樣本(皮升到納升級別)時。針對WNV的檢測,微流控技術不僅提高了檢測WNV的靈敏度和特異性,還支持實時監測,加快了對病毒暴發的響應速度。微流控設備的便攜性非常適合于田間檢測監測。該技術能夠集成多種分析方法,如聚合酶鏈式反應(PCR)和酶聯免疫吸附測定(ELISA),為WNV的綜合診斷提供了有效的平臺。在羅馬就已有文獻利用高通量微流控結合熒光定量PCR技術成功檢測到蚊子排泄物中的2譜系西尼羅病毒[46]。
在我國,為了確保公共衛生安全和預防疾病的傳播,研究人員采用了多種方法來對各種病毒進行檢測。針對西尼羅病毒的檢測,我國現行的國家標準GB/T 27518—2011已經明確規定了幾種檢測技術,包括蝕斑減少中和試驗PRNT、IgM捕獲ELISA、RT-PCR(熒光定量RT-PCR、套式RT-PCR)。通過這幾種技術手段,人們可以更加準確地診斷西尼羅病毒,從而更好地進行預防和控制。在國際上,WOAH對西尼羅熱的推薦診斷方法與我國類似,除了以上方法外,還包括了免疫組化法。
3" 展" 望
西尼羅熱(WNF)當前仍然是一個全球性的公共衛生挑戰。過去幾十年已經在其診斷與監測上取得了顯著進步,但該病的感染特性和流行的復雜性仍然要求人類不斷探索更先進、更有效的科學手段。診斷技術的不斷改進和創新為人們提供了新的希望,以高通量測序技術為主的宏基因組學分析手段,能夠更加迅速和準確地識別病毒序列,在疫情早期進行預警和風險提示;微流控技術的發展提供了一種高效和低成本的檢測手段;人工智能和機器學習技術的引入,使得數據分析的速度、準確性和系統性都將得到顯著提升,使人類能夠更好地理解病毒傳播的模式和動態,如Farooq等[47]采用人工智能技術分析了生態氣候在歐洲西尼羅熱爆發中的影響。科技的進步正不斷提升人們的應對和處置各類疫病風險的能力,為預防、預警、監測和治療疾病的感染提供更有效的手段,以保障人類和動物的健康與安全。
參考文獻(References):
[1]" MAEZONO K,KOBAYASHI S,TABATA K,et al.Development of a highly specific serodiagnostic ELISA for West Nile virus infection using subviral particles[J].Sci Rep,2021,11(1):9213.
[2]" CHAN K R,ISMAIL A A,THERGARAJAN G,et al.Serological cross-reactivity among common flaviviruses[J].Front Cell Infect Microbiol,2022,12:975398.
[3]" MUKHOPADHYAY S,KIM B S,CHIPMAN P R,et al.Structure of West Nile virus[J].Science,2003,302(5643):248.
[4]" ZHANG S Z,HE Y,WU Z,et al.Secretory pathways and multiple functions of nonstructural protein 1 in flavivirus infection[J].Front Immunol,2023,14:1205002.
[5]" KHROMYKH A A,MEKA H,GUYATT K J,et al.Essential role of cyclization sequences in flavivirus RNA replication[J].J Virol,2001,75(14):6719-6728.
[6]" MARKOFF L.5′- and 3′-noncoding regions in flavivirus RNA[J].Adv Virus Res,2003,59:177-228.
[7]" TAN T Y,FIBRIANSAH G,LOK S M.Capsid protein is central to the birth of flavivirus particles[J].PLoS Pathog,2020,16(5):e1008542.
[8]" LI L,LOK S M,YU I M,et al.The flavivirus precursor membrane-envelope protein complex:structure and maturation[J].Science,2008,319(5871):1830-1834.
[9]" REYES-SANDOVAL A,LUDERT J E.The dual role of the antibody response against the flavivirus non-structural protein 1 (NS1) in protection and immuno-pathogenesis[J].Front Immunol,2019,10:1651.
[10]" SHRIVASTAVA G,VISOSO-CARVAJAL G,GARCIA-CORDERO J,et al.Dengue virus serotype 2 and its non-structural proteins 2A and 2B activate NLRP3 inflammasome[J].Front Immunol,2020,11:352.
[11]" ZEIDLER J D,FERNANDES-SIQUEIRA L O,BARBOSA G M,et al.Non-canonical roles of dengue virus non-structural proteins[J].Viruses,2017,9(3):42.
[12]" EGLOFF M P,DECROLY E,MALET H,et al.Structural and functional analysis of methylation and 5'-RNA sequence requirements of short capped RNAs by the methyltransferase domain of dengue virus NS5[J].J Mol Biol,2007,372(3):723-736.
[13]" DONG H P,CHANG D C,HUA M H C,et al.2′-O methylation of internal adenosine by flavivirus NS5 methyltransferase[J].PLoS Pathog,2012,8(4):e1002642.
[14]" EGLOFF M P,BENARROCH D,SELISKO B,et al.An RNA cap (nucleoside-2'-O-)-methyltransferase in the flavivirus RNA polymerase NS5:crystal structure and functional characterization[J].EMBO J,2002,21(11):2757-2768.
[15]" WANG T,ANDERSON J F,MAGNARELLI L A,et al.West Nile virus envelope protein[J].Ann N Y Acad Sci,2001,951(1):325-327.
[16]" KNENKAMP L,ZIEGLER U,NAUCKE T,et al.Antibody ratios against NS1 antigens of tick-borne encephalitis and West Nile viruses support differential flavivirus serology in dogs[J].Transbound Emerg Dis,2022,69(5):e2789-e2799.
[17]" 王淑娟,王" 瑩,徐天剛,等.西尼羅熱國內外疫情形勢與防控[J].中國動物檢疫,2023,40(9):82-90.
WANG S J,WANG Y,XU T G,et al.Global outbreak status and control of West Nile fever[J].China Animal Health Inspection,2023,40(9):82-90.(in Chinese)
[18]" 曹振軒.科學防控西尼羅熱[J].中國海關,2023(8):63.
CAO Z X.The scientific prevention and control of West Nile fever[J].China Customs,2023(8):63.(in Chinese)
[19]" 龔震宇.2019年美國亞利桑那州一起西尼羅熱暴發疫情簡況[J].疾病監測,2021,36(6):634.
GONG Z Y.An outbreak of west Nile virus—Arizona,2019[J].Disease Surveillance,2021,36(6):634.(in Chinese)
[20]" GUY B,GUIRAKHOO F,BARBAN V,et al.Preclinical and clinical development of YFV 17D-based chimeric vaccines against dengue,West Nile and Japanese encephalitis viruses[J].Vaccine,2010,28(3):632-649.
[21]" 鄭小龍,朱來華,王" 群,等.西尼羅病毒病診斷技術研究進展[J].動物醫學進展,2014,35(3):92-97.
ZHENG X L,ZHU L H,WANG Q,et al.Progress on diagnostic techniques of West Nile virus disease[J].Progress in Veterinary Medicine,2014,35(3):92-97.(in Chinese)
[22]" ZAAYMAN D,HUMAN S,VENTER M.A highly sensitive method for the detection and genotyping of West Nile virus by real-time PCR[J].J Virol Methods,2009,157(2):155-160.
[23]nbsp; 邱" 璐,李小林,蔣" 靜,等.實時熒光PCR檢測西尼羅病毒方法的建立[J].畜牧與獸醫,2012,44(9):4-7.
QIU L,LI X L,JIANG J,et al.Detection of West Nile virus by real-time RT-PCR[J].Animal Husbandry amp; Veterinary Medicine,2012,44(9):4-7.(in Chinese)
[24]" LINKE S,ELLERBROK H,NIEDRIG M,et al.Detection of West Nile virus lineages 1 and 2 by real-time PCR[J].J Virol Methods,2007,146(1-2):355-358.
[25]" VZQUEZ A,HERRERO L,NEGREDO A,et al.Real time PCR assay for detection of all known lineages of West Nile virus[J].J Virol Methods,2016,236:266-270.
[26]" 張俊鋒,張雅麗,王瑞晨,等.流行性乙型腦炎和西尼羅病毒雙重微滴數字PCR檢測方法的建立[J].中國媒介生物學及控制雜志,2023,34(3):285-290.
ZHANG J F,ZHANG Y L,WANG R C,et al.Establishment of a duplex droplet digital PCR assay for Japanese encephalitis and West Nile viruses[J].Chinese Journal of Vector Biology and Control,2023,34(3):285-290.(in Chinese)
[27]" PARIDA M,POSADAS G,INOUE S,et al.Real-time reverse transcription loop-mediated isothermal amplification for rapid detection of West Nile virus[J].J Clin Microbiol,2004,42(1):257-263.
[28]" CAO Z G,WANG H L,WANG L N,et al.Visual detection of West Nile virus using reverse transcription loop-mediated isothermal amplification combined with a vertical flow visualization strip[J].Front Microbiol,2016,7:554.
[29]" 呂沁風,廖" 靜,羅" 鵬,等.西尼羅病毒的逆轉錄重組酶介導擴增檢測方法[J].微生物學通報,2020,47(2):659-664.
L Q F,LIAO J,LUO P,et al.Development of a reverse transcription recombinase aided amplification assay for detection of West Nile virus[J].Microbiology China,2020,47(2):659-664.(in Chinese)
[30]" 張逸龍,葉" 潤,勒" 斌,等.基于逆轉錄-酶促重組等溫擴增原理的西尼羅病毒基因檢測方法的建立[J].中國寄生蟲學與寄生蟲病雜志,2022,40(3):344-348,354.
ZHANG Y L,YE R,LE B,et al.A reverse transcriptase aid-enzymatic recombinase isothermal amplification-based method for detection of West Nile virus[J].Chinese Journal of Parasitology and Parasitic Diseases,2022,40(3):344-348,354.(in Chinese)
[31]" WOLLANTS E,SMOLDERS D,NAESENS R,et al.Use of next-generation sequencing for diagnosis of West Nile virus infection in patient returning to Belgium from Hungary[J].Emerg Infect Dis,2018,24(12):2380-2382.
[32]" JOHNSON D J,OSTLUND E N,PEDERSEN D D,et al.Detection of North American West Nile virus in animal tissue by a reverse transcription-nested polymerase chain reaction assay[J].Emerg Infect Dis,2001,7(4):739-741.
[33]" XIAO S Y,GUZMAN H,ZHANG H,et al.West Nile virus infection in the golden hamster (Mesocricetus auratus):a model for West Nile encephalitis[J].Emerg Infect Dis,2001,7(4):714-721.
[34]" CASTILLO-OLIVARES J,WOOD J.West Nile virus infection of horses[J].Vet Res,2004,35(4):467-483.
[35]" PRINCE H E,CALMA J,PHAM T,et al.Frequency of missed cases of probable acute West Nile virus (WNV) infection when testing for WNV RNA alone or WNV immunoglobulin M alone[J].Clin Vaccine Immunol,2009,16(4):587-588.
[36]" MARTIN D A,MUTH D A,BROWN T,et al.Standardization of immunoglobulin M capture enzyme-linked immunosorbent assays for routine diagnosis of arboviral infections[J].J Clin Microbiol,2000,38(5):1823-1826.
[37]" LUDOLFS D,NIEDRIG M,PAWESKA J T,et al.Reverse ELISA for the detection of anti West Nile virus IgG antibodies in humans[J].Eur J Clin Microbiol Infect Dis,2007,26(7):467-473.
[38]" THROSBY M,GEUIJEN C,GOUDSMIT J,et al.Isolation and characterization of human monoclonal antibodies from individuals infected with West Nile Virus[J].J Virol,2006,80(14):6982-6992.
[39]" OLIPHANT T,NYBAKKEN G E,AUSTIN S K,et al.Induction of epitope-specific neutralizing antibodies against West Nile virus[J].J Virol,2007,81(21):11828-11839.
[40]" BALMASEDA A,STETTLER K,MEDIALDEA-CARRERA R,et al.Antibody-based assay discriminates Zika virus infection from other flaviviruses[J].Proc Natl Acad Sci U S A,2017,114(31):8384-8389.
[41]" DING X X,LI X F,DENG Y Q,et al.Development of a double antibody sandwich ELISA for West Nile virus detection using monoclonal antibodies against non-structural protein 1[J].PLoS One,2014,9(10):e108623.
[42]" 曹增國.西尼羅病毒快速檢測方法的建立與應用[D].北京:中國人民解放軍軍事醫學科學院,2016.
CAO Z G.Developments and applications of west Nile Virus rapid diagnosis methods[D].Beijing:Academy of Military Medical Sciences,2016.(in Chinese)
[43]" MALAN A K,STIPANOVICH P J,MARTINS T B,et al.Detection of IgG and IgM to West Nile virus:development of an immunofluorescence assay[J].Am J Clin Pathol,2003,119(4):508-515.
[44]" PENNICK K E,MCKNIGHT C A,PATTERSON J S,et al.Diagnostic sensitivity and specificity of in situ hybridization and immunohistochemistry for Eastern equine encephalitis virus and West Nile virus in formalin-fixed,paraffin-embedded brain tissue of horses[J].J Vet Diagn Invest,2012,24(2):333-338.
[45]" GODHARDT J A,BEHELER K,O'CONNOR M J,et al.Evaluation of antigen-capture ELISA and immunohistochemical methods for avian surveillance of West Nile virus[J].J Vet Diagn Invest,2006,18(1):85-89.
[46]" CRIVEI L A,MOUTAILLER S,GONZALEZ G,et al.Detection of West Nile virus lineage 2 in eastern Romania and first identification of sindbis virus RNA in mosquitoes analyzed using high-throughput microfluidic real-time PCR[J].Viruses,2023,15(1):186.
[47]" FAROOQ Z,ROCKLV J,WALLIN J,et al.Artificial intelligence to predict West Nile virus outbreaks with eco-climatic drivers[J].Lancet Reg Health Eur,2022,17:100370.
(編輯" 范子娟)

