唾液乳桿菌對奶山羊隱性乳房炎的治療效果分析



摘" 要: 旨在探究唾液乳桿菌對奶山羊隱性乳腺炎的治療效果。本試驗隨機選用患有乳腺炎的奶山羊12只,其中6只作為益生菌治療組,6只作為乳腺炎模型對照組;隨機選用健康奶山羊12只,其中6只作為益生菌對照組,6只作為空白對照組。益生菌治療組與益生菌對照組每天飼喂唾液乳桿菌,其余不作處理。在飼喂第0、28天采集奶山羊血液、糞便和乳汁,通過熒光定量PCR和16S rRNA菌群測序的方法,分別檢測血清炎癥因子、腸道和乳汁菌群變化。結果發現,奶山羊飼喂唾液乳桿菌后隱性乳腺炎的發病率從36.36%下降至13.64%;血液中IL-17、IL-1β和IL-6等炎性因子的相對表達量顯著降低,而抗炎因子IL-10的相對表達量顯著升高;腸道和乳汁中的微生物Alpha多樣性升高,菌群多樣性增加,在腸道微生物門水平上顯著提高了厚壁菌門的相對豐度,降低了擬桿菌門的相對豐度,在乳汁微生物門水平上提高了厚壁菌門和藍藻菌門的相對豐度,降低了變形菌門的相對豐度。綜上表明,唾液乳桿菌對隱性乳腺炎具有較好的治療效果,具有應用于隱性乳腺炎治療的臨床前景。
關鍵詞: 奶山羊;隱性乳腺炎;唾液乳桿菌;腸道菌群;乳汁微生物
中圖分類號:S857.26
文獻標志碼:A
文章編號:0366-6964(2024)12-5706-10
doi: 10.11843/j.issn.0366-6964.2024.12.033
開放科學(資源服務)標識碼(OSID):
收稿日期:2023-10-31
基金項目:陜西省2023年大學生創新創業訓練項目(S202310712366);中央高校基本科研業務費專項資金(2452023072)
作者簡介:朱" 芳(1998-),女,河南商丘人,碩士,主要從事奶山羊乳房炎研究,E-mail: zhufang@nwsuaf.edu.cn;李璐璐(2001-),女,河北邯鄲人,碩士,主要從事動物益生菌研究,E-mail:lilulu778@nwsuaf.edu.cn。朱芳和李璐璐為同等貢獻作者
*通信作者:趙慧英,主要從事動物神經內分泌研究,E-mail: zhaohuiying@nwsuaf.edu.cn;陳德坤,主要從事山羊重大疫病的免疫防治研究,E-mail:cdk@nwsuaf.edu.cn;馬文濤,主要從事山羊重大疫病的免疫防治研究,E-mail:mawentao@nwsuaf.edu.cn#同等貢獻作者
Treatment Effects of Lactobacillus salivarius on Subclinical Mastitis in Dairy Goats
ZHU Fang1, LI" Lulu1, ZHAO" Hongyi1, DONG" Yarong1, JIANG" Yuecai1, LI" Dengliang1, ZHANG" Tianliang2, XIONG" Nannan1, CHEN" Dekun1*, MA" Wentao1*, ZHAO" Huiying1*
(1.College of Veterinary Medicine, Northwest Aamp;F University, Yangling 712100," China;
2.Shaanxi Qianyang Shaneng Milk Goat Development Company, Baoji 721100," China)
Abstract:" The aim of this study was to explore the therapeutic effect of Lactobacillus salivarius on latent mastitis of dairy goats, in this study, 12 dairy goats with mastitis were randomly selected, of which 6 were used as probiotic treatment group and 6 were used as mastitis model control group. Another twelve healthy dairy goats were selected, of which 6 were used as probiotics prevention group and 6 were used as blank control group. Probiotic treatment group and probiotic control group were fed Lactobacillus salivary every day, and the rest groups were not treated. The milk, anticoagulant and rectal contents of dairy goats were collected after feeding on day 0 and 28. The changes of blood inflammatory factors, intestinal flora and milk flora were detected by fluorescence quantitative PCR and 16S rRNA microflora sequencing, respectively. The results showed that the incidence of subclinical mastitis of dairy goats fed Lactobacillus salivary decreased from 36.36% to 13.64%, The relative expression levels of inflammatory factors such as IL-17, IL-1β and IL-6 were significantly decreased, while the relative expression levels of anti-inflammatory factor IL-10 were significantly increased. The microbial Alpha diversity increased in the gut and milk, and the diversity of flora increased, which significantly increased the relative abundance of Firmicutes and decreased the relative abundance of Bacteroidetes at the phylum level of intestinal microbiome, and increased the relative abundance of Firmicutes and Cyanobacteria at the phylum level of milk microbiome, and decreased the relative abundance of Proteobacteria.In conclusion, Lactobacillus salivarius has a good therapeutic effect on occult mastitis, and has a clinical prospect for the treatment of occult mastitis.
Key words: dairy goats; subclinical mastitis; Lactobacillus salivarius; intestinal flora; milk microorganisms
*Corresponding authors:" ZHAO Huiying, E-mail: zhaohuiying@nwsuaf.edu.cn; CHEN Dekun, E-mail:cdk@nwsuaf.edu.cn; MA Wentao, E-mail:mawentao@nwsuaf.edu.cn
隱性乳腺炎是泌乳期奶山羊較常發生的一種乳腺炎類型,會導致產奶量下降和奶品質降低,給奶山羊養殖戶帶來不小的經濟損失且對奶山羊養殖業造成不利影響[1-2]。調查顯示,我國奶山羊乳腺炎的發病率在40%左右,其中隱性乳腺炎的檢出率較高[3],但因其癥狀不明顯,臨床上很難及時采取相應的防治措施,在特定條件下會轉變成亞臨床型乳腺炎,進一步發展為臨床乳腺炎,對奶山羊造成難以挽回的損傷。由此可見,隱性乳腺炎是奶山羊養殖過程中最大的潛在威脅之一,因此做好預防措施、及早發現及早治療對奶山羊養殖業有十分重要的意義。病原微生物是引起奶山羊乳腺炎的主要因素,故長期以來多以抗生素治療為主[4],但抗生素的長期使用不但存在細菌耐藥風險,殘留在乳中的抗生素也會嚴重影響乳汁品質,降低其經濟效益的同時帶來一系列的食品安全問題,因此尋求安全有效的乳腺炎治療方法具有重要意義[5-6]。近年來,中藥[7]、抗菌肽[8]、乳酸菌[9]和細菌素[10]等逐漸應用于乳腺炎的治療并取得良好的效果。乳酸菌作為乳腺組織中的一種有益菌,可以有效抑制入侵乳腺組織的病原菌生長[11]。研究發現,乳酸菌中的唾液乳桿菌具有免疫調節功能[12]、抗氧化作用[13]和抑菌功能[14]等,且對引起隱性乳腺炎的金黃色葡萄球菌和大腸桿菌等主要致病菌具有較好的抑制作用[15]。本研究通過飼喂奶山羊唾液乳桿菌,并利用加利福尼亞乳腺炎試驗(California mastitis test, CMT)、熒光定量PCR和16S rRNA菌群測序等方法,研究唾液乳桿菌對奶山羊隱性乳腺炎的治療效果,以期為唾液乳桿菌在乳腺炎上的應用提供理論指導和技術支撐。
1" 材料與方法
1.1" 材料
1.1.1" 試驗動物
從陜西省千陽縣某規模化養殖場選擇1~3歲泌乳期奶山羊24只。
1.1.2" 菌種
唾液乳桿菌由西北農林科技大學免疫學實驗室提供,分離自健康奶山羊糞便。
1.1.3" 主要儀器和試劑
熒光定量PCR儀,美國Life Technologies公司;4℃高速離心機,美國Sigma公司;核酸蛋白測定儀,賽默飛世技科技有限公司;漩渦振蕩器,江蘇天翎儀器有限公司;不同量程移液器,德國Eppendorf公司。
RNA-iso Plus,日本TaKaRa公司;Fast Kingc DNA試劑盒和SYBR Premix Ex Taq試劑,天根生化科技有限公司。
1.2" 方法
1.2.1" 加利福尼亞乳腺炎試驗方法
無菌采集2~3 mL乳汁樣本,進行加利福尼亞乳腺炎試驗(CMT)。加利福尼亞乳腺炎快速診斷試劑的配置方法與判定標準依據本實驗室前期創建的方法[16],奶山羊患有隱性乳腺炎時,乳汁CMT檢測會有絮狀沉淀物。在測試盤用2 mL CMT診斷試劑與乳汁混合、緩慢搖動,觀察液體顏色變化和凝膠沉聚變化,20 s內判定結果,判定標準如表1所示。
1.2.2" 試驗動物分組
將泌乳期奶山羊的乳汁樣本進行CMT檢測后,隨機選用患有乳腺炎的奶山羊12只,其中6只作為益生菌治療組,6只作為乳腺炎模型對照組;選用未患有乳腺炎的健康奶山羊12只,其中6只作為益生菌對照組,6只作為空白對照組。空白對照組與乳腺炎模型對照組不進行飼喂唾液乳桿菌;益生菌治療組與益生菌對照組:每天飼喂唾液乳桿菌100 mL,唾液乳桿菌的濃度為1.0×108 CFU·mL-1。
1.2.3" 樣品采集
飼喂前為第0天,分別在飼喂的第0、28天使用乳房基底部按摩擠壓的方法采集各組奶山羊乳汁,4℃保存,用于后續CMT檢測和菌群測序分析;在飼喂的第0、28天收集益生菌治療組奶山羊直腸糞便樣本,并將采集的糞便樣本立即放置于液氮中儲存并轉運至實驗室-80℃低溫冰箱保存,用于后續菌群測序分析;在飼喂的第28天采集奶山羊血液于抗凝管中,4℃保存,用于PBMCs的分離提取以及相關細胞因子的檢測。
1.2.4" 唾液乳桿菌的濃度測定
活化培養唾液乳桿菌菌株,菌液按2%接種量分別接種于MRS液體培養基中,37 ℃靜置培養24 h后取出,將菌液濃度稀釋至1.0×108 CFU·mL-1。
1.2.5" 熒光定量PCR檢測血液樣品中炎性因子表達
1.2.5.1" 外周血單個核細胞(PBMCs)的分離:
采集試驗羊頸靜脈外周血1 mL于抗凝血管中,置于水平離心機800×g離心5 min。吸棄上清液并在超凈工作臺中加入5 mL的紅細胞裂解液,充分混勻后置于4 ℃冰箱靜置10 min,期間每隔5 min顛倒混勻1次。裂解后加入5 mL的無菌PBS緩沖液終止,800×g離心5 min。吸棄上清液,底部沉淀即為PBMCs。取1 mL的RNAiso plus溶液加到上述分離的PBMCs中,混勻后置于-80 ℃冰箱保存。
1.2.5.2" 樣品RNA提取:
將上述樣品從-80 ℃冰箱取出后,室溫溶解,然后顛倒混勻,在冰上放置5 min;加入1/5體積的預冷三氯甲烷,在漩渦振蕩器上振蕩15 s,使其充分乳化后,室溫放置5 min,4℃下12 000×g離心15 min;將上層水相吸出,加入到一個新的 RNase-free EP管里;加入相同體積的預冷異丙醇,顛倒混勻,室溫放置10 min,4℃下12 000×g離心10 min;棄掉上清,沿管壁緩緩加入1 mL試驗前預冷的75% DEPC乙醇,輕輕上下顛倒洗滌,4℃下12 000×g離心5 min;棄掉上清,室溫干燥沉淀2~5 min,沿管壁緩緩加入10~100 μL的無RNA酶的水溶解RNA,輕輕吹打使其混勻,測定其濃度,將RNA立即進行反轉錄或-80 ℃保存備用。
1.2.5.3" RNA反轉錄:
按照試劑盒說明書的方法,配制基因組DNA的去除體系和反轉錄反應體系;將反轉錄反應中的Mix,加到gDNA去除步驟的反應液中,充分混勻;42℃,孵育15 min;95 ℃,孵育3 min之后放于冰上,得到的cDNA可用于后續試驗,或低溫保存。
1.2.5.4" Real-time PCR檢測相關因子變化:
引物序列如表2所示;按照試劑盒說明書要求配制反應體系和設置熒光定量PCR擴增儀器反應程序。2-△△CT法分析擴增結果。
1.2.6" 糞便和乳汁16S rRNA菌群測序
測序區域為細菌16S rRNA基因V3~V4區。使用Illumina Mi Seq平臺進行結果分析。F.BF代表益生菌治療組飼喂唾液乳桿菌前采集的糞便,即第0天的糞便;F.AF代表飼喂唾液乳桿菌后采集的糞便,即第28天的糞便。M.BF代表益生菌治療組飼喂唾液乳桿菌前采集的乳汁,即第0天的乳汁;M.AF代表益生菌治療組飼喂唾液乳桿菌后采集的乳汁,即第28天的乳汁。此部分試驗由北京諾禾致源科技股份有限公司完成。
1.2.7" 統計分析
數據采用SPSS20.0 統計軟件進行分析,對數據進行單因素方差分析,用t檢驗進行組件差異顯著性檢驗。“*”表示差異顯著Plt;0.05,“**”表示差異極顯著Plt;0.01。
2" 結" 果
2.1" 唾液乳桿菌對奶山羊隱性乳腺炎的治療效果
對采取的乳汁樣本進行 CMT 試驗檢測結果如" 表3所示,飼喂唾液乳桿菌28 d后,隱性乳腺炎檢出率從36.36%下降至13.64%(Plt;0.05);未飼喂唾液乳桿菌組隱性乳腺炎檢出率從36.11%上升至38.89%。(檢出率/%=奶山羊隱性乳腺炎陽性樣品數/總樣品數×100)
2.2" 唾液乳桿菌對奶山羊隱性乳腺炎血液中炎癥因子的影響
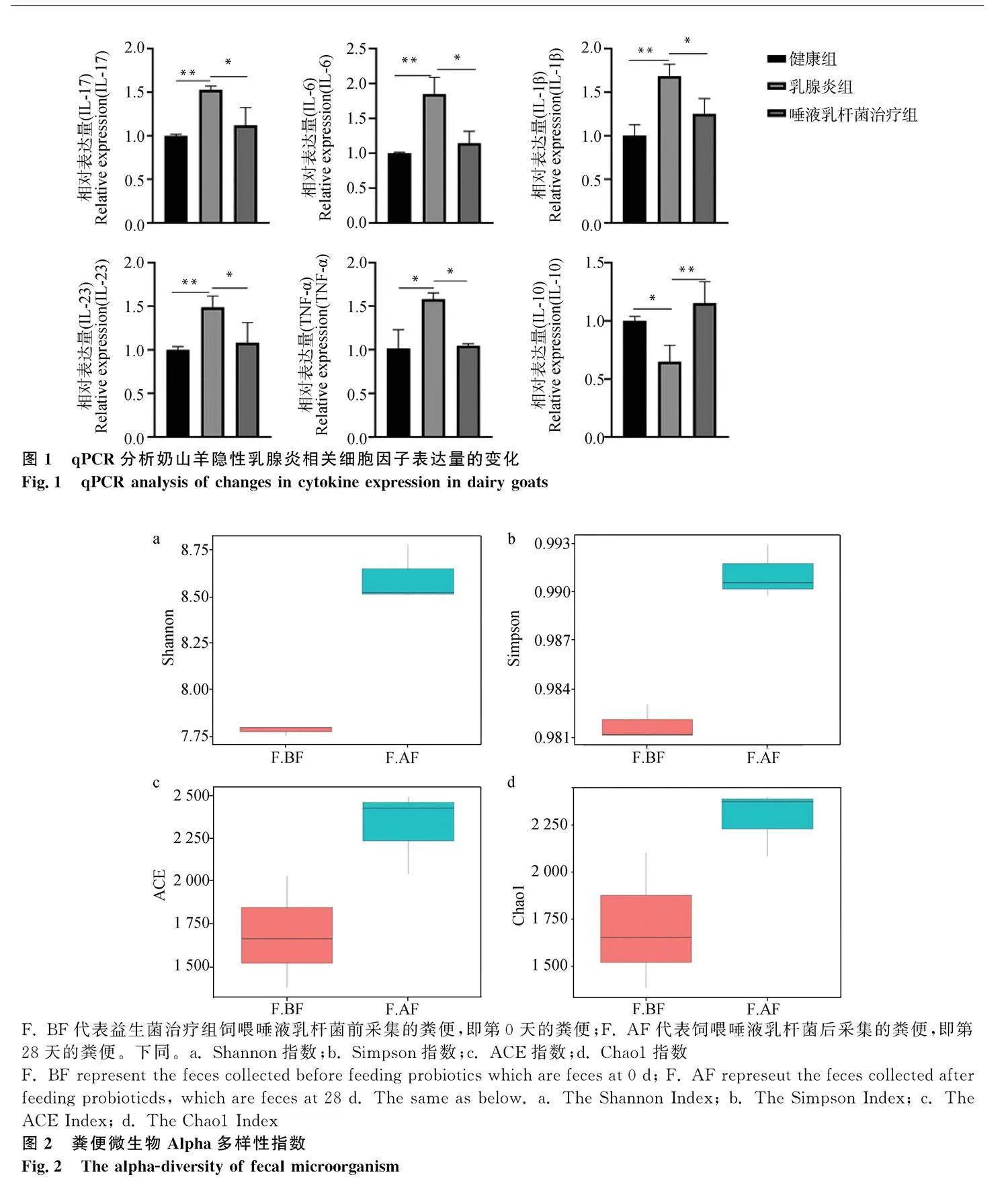
將采取的奶山羊血液樣本分離外周血細胞,使用qPCR的方法檢測奶山羊血液中相關細胞因子相對表達量的變化,檢測結果如圖1。與空白對照組相比,乳腺炎組IL-17、IL-6、IL-1β、IL-23和TNF-α的相對表達量均顯著升高,而IL-10的相對表達量降低;益生菌治療組飼喂唾液乳桿菌后,與乳腺炎組相比,細胞因子IL-17、IL-6、IL-1β、IL-23和TNF-α的相對表達量均顯著降低,IL-10的相對表達量顯著升高。
2.3" 唾液乳桿菌對隱性乳腺炎奶山羊腸道菌群的影響
2.3.1" 糞便微生物Alpha多樣性指數
Alpha多樣性指數適用于評估樣品自身菌群的豐度與多樣性之間的差異,其中Shannon指數與群落多樣性和物種分布有關,Simpson指數用來表征群落內物種分布的多樣性和均勻度,ACE指數是用來估計群落中OTU數目的指數,Chao1指數用于估計群落樣品中包含的物種總數。Shannon及Simpson指數值越大,表明群落的多樣性越高,Chao1或ACE指數越大,表明群落的豐富度越高[17]。圖2結果可知,F.AF的Shannon和Simpson指數均顯著高于F.BF;Chao1和ACE指數有上升趨勢但無明顯差異。
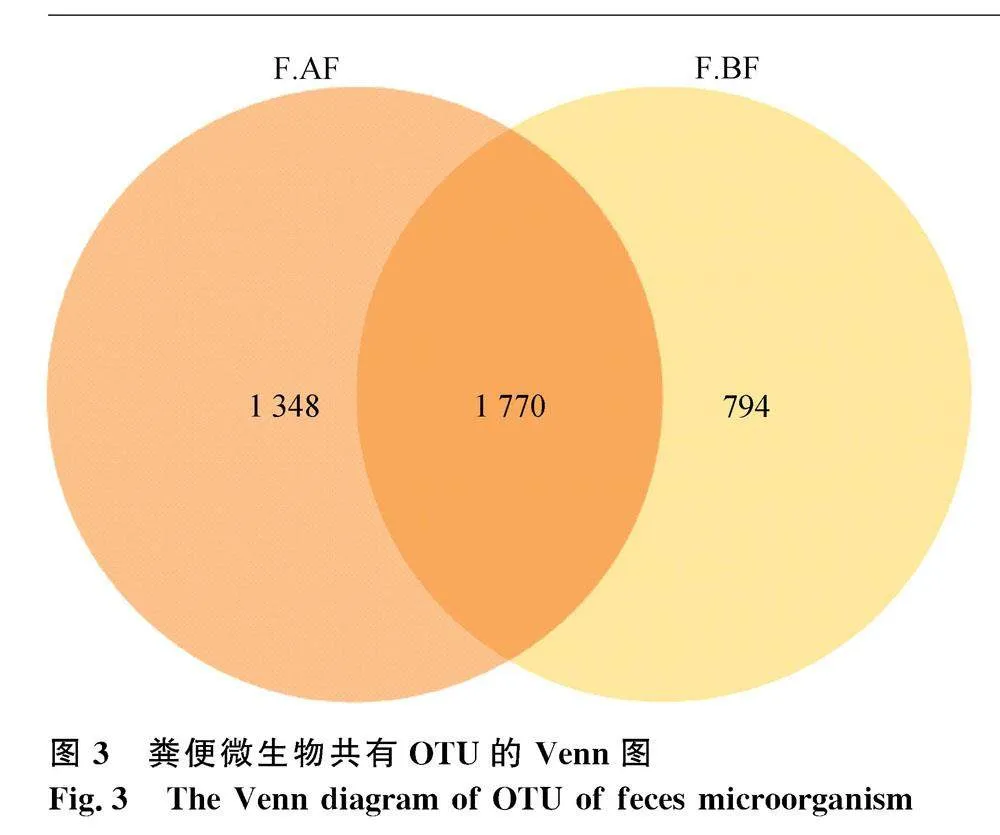
2.3.2" 糞便微生物共有OTU分析結果
依據糞便菌群測序結果計算糞便微生物共有的OTU數量,樣本間共有的OTU和獨有的OTU之間的關系通過Venn圖展示。結果見圖3,圖中每個圓代表一組樣本,重疊區域為各組所共有的OTU,每個區域的數字表示該區域所對應的OTU數量。結果表明,經飼喂唾液乳桿菌,糞便微生物所獨有的OTU數量大于飼喂前。
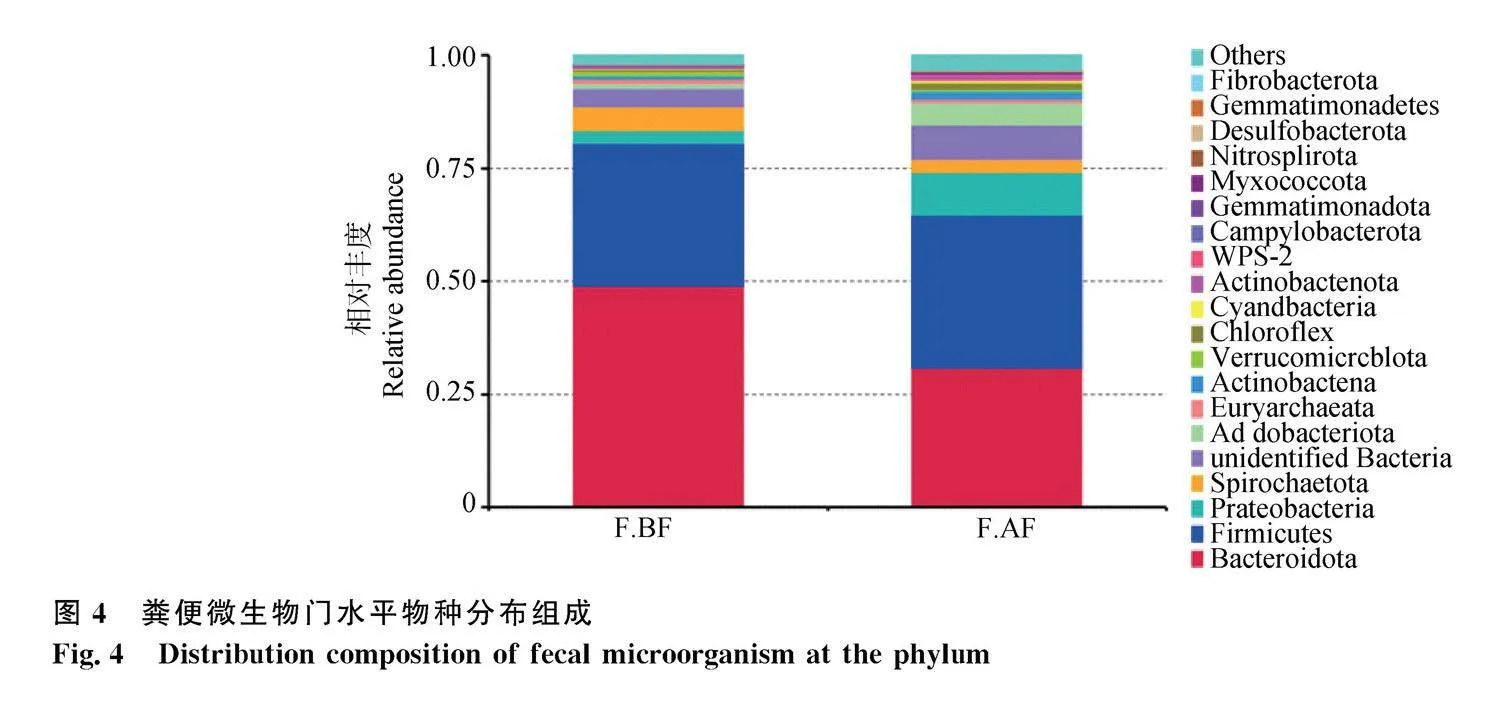
2.3.3" 糞便微生物門水平菌群結構分析結果
飼喂唾液乳桿菌后奶山羊腸道菌群門水平上的變化
結果如圖4。可見奶山羊糞便中主要優勢菌門為擬桿菌門(Bacteroidetes)、厚壁菌門(Firmicutes)和變形菌門(Proteobacteria)。經飼喂唾液乳桿菌,奶山羊腸道中微生物類群在門水平上顯著升高,厚壁菌門的相對含量有所增加,擬桿菌門的相對含量顯著降低。
2.4" 唾液乳桿菌對奶山羊乳汁菌群的影響
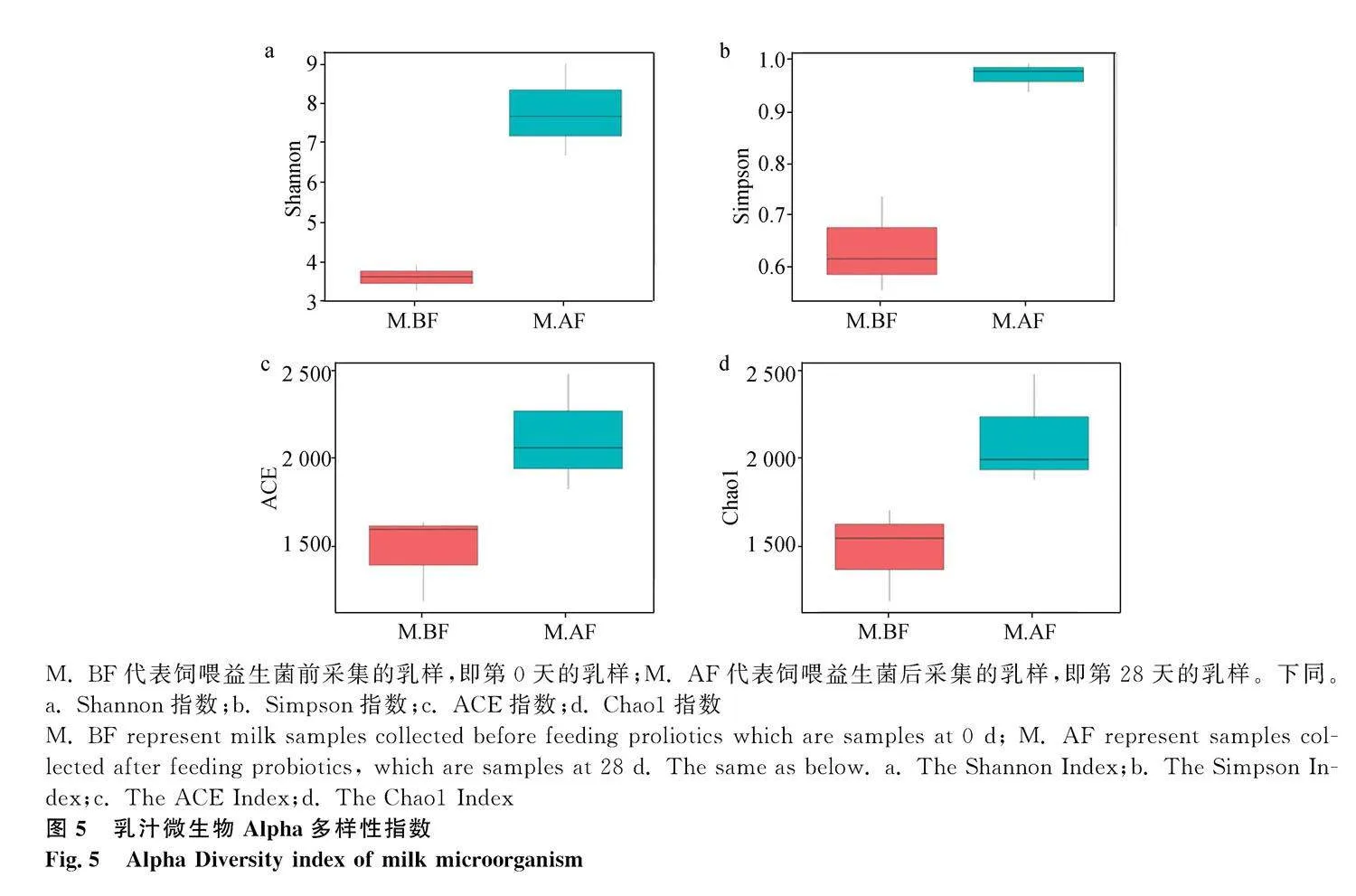
2.4.1" 乳汁微生物Alpha多樣性指數
對飼喂唾液乳桿菌前、后的乳汁樣本進行微生物菌群測序,結果如圖5,M.AF的Shannon指數和Simpson指數明顯高于M.BF,表明飼喂唾液乳桿菌可使乳汁菌群多樣性升高。
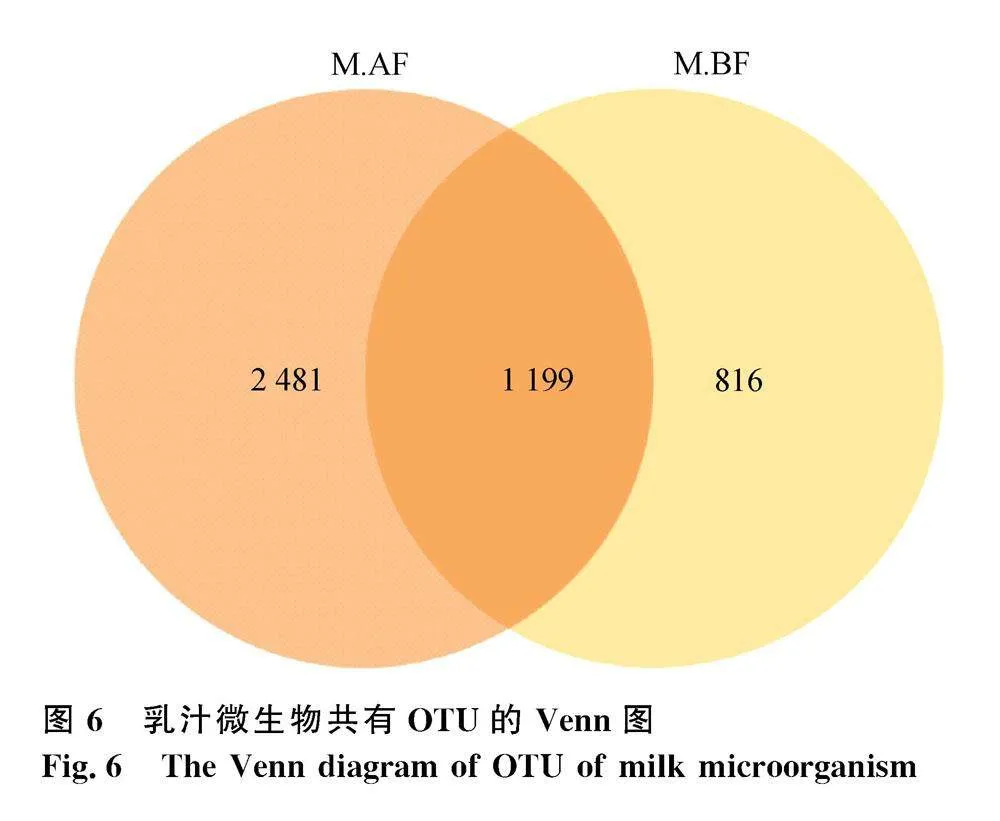
2.4.2" 乳汁微生物共有OTU分析結果
依據乳汁菌群測序結果計算乳汁微生物的OTU數量,將各組樣本共有的OTU和獨有的OTU之間的關系通過Venn圖展示。結果見圖6,圖中每個圓代表一組樣本,重疊區域表示各組所共有的OTU,每個區域的數字表示該區域所對應的OTU數量。由圖可見,飼喂唾液乳桿菌后乳汁微生物所獨有的OTU數量大于飼喂前。
2.4.3" 乳汁微生物門水平菌群結構分析結果
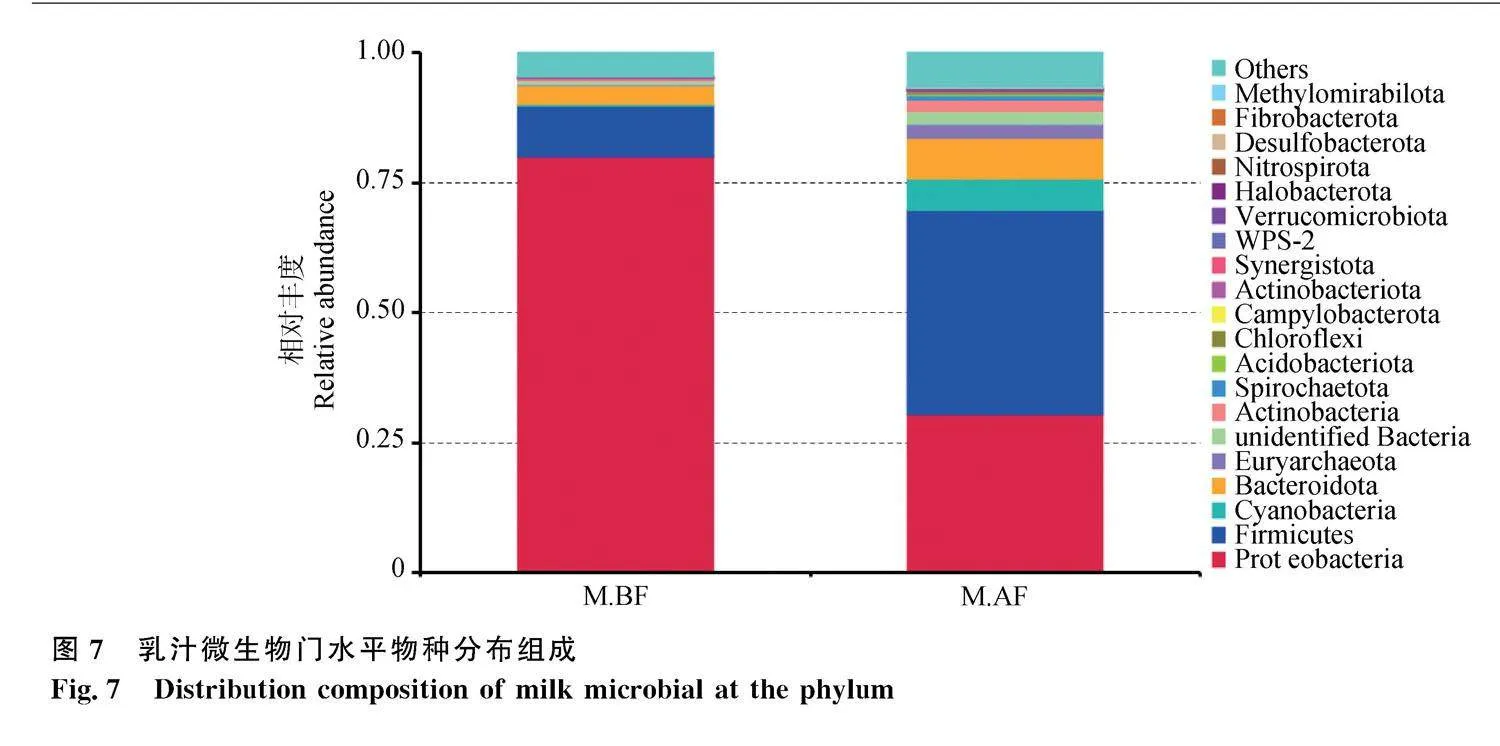
對乳汁微生物在門水平的組成及分布進行分析,結果如圖7。奶山羊乳汁中主要優勢菌門為變形菌門(Proteobacteria)、厚壁菌門(Firmicutes)、藍藻菌門(Cyanobacteria)和擬桿菌門(Bacteroidetes)。飼喂唾液乳桿菌后乳汁微生物菌群在門水平上的微生物類群數顯著升高,變形菌門的相對豐度顯著降低,厚壁菌門和藍藻菌門的相對豐度顯著升高。
3" 討" 論
細胞因子在動物機體內發揮著重要的作用,Th1細胞釋放引起炎癥和抗病毒作用的細胞因子,如IL-1、IL-2、TNF-α、TNF-β和IFN-γ等,這些細胞因子可促進T細胞介導的免疫反應;Th2細胞可產生促進體液免疫反應的細胞因子,如IL-4,IL-5,IL-6,IL-10和IL-13等[18]。正常情況下,Th1和Th2兩類細胞有一定的比例,兩者協調,使人體免疫保持平衡。但機體發生功能異常時,常表現出平衡偏向其中一方,一旦Th1/Th2之間的平衡狀態被打破,會導致相關疾病的發生。菌株對炎癥的益處是通過調節細胞因子的產生和平衡來介導的,而這種調節可以通過細胞因子血清水平的測量結果來顯示[19]。研究發現,唾液乳桿菌對TNF-α、IL-1β等促炎細胞因子具有抑制作用,并使抑炎細胞因子IL-10和TGF-β的表達增加[20]。本研究結果顯示,當奶山羊發生隱性乳腺炎時,血液中TNF-α、IL-1β、IL-17、IL-6等炎癥相關細胞因子的相對表達量顯著升高,而IL-10的相對表達量顯著降低。飼喂唾液乳桿菌后,血液中IL-17、IL-6和IL-1β等的相對表達量降低,IL-10的相對表達量升高。以上研究表明,唾液乳桿菌對機體具有免疫調節作用。
越來越多的證據表明,在乳腺疾病期間可能存在腸道-乳腺軸[21],腸道微生物群在宿主防御乳腺炎過程中發揮重要作用。Zhao等[22]研究顯示,腸道菌群的失調促進了志賀桿菌在腸-乳腺軸上的易位,正常情況下,腸道處于嚴格的厭氧環境,有利于厚壁菌門(Firmicutes)和擬桿菌門(Bacteroidetes)等專性厭氧細菌的生存。然而,腸道炎癥或微生物生態失調引起的腸道通透性增加增加了腸道內的氧含量,使兼性厭氧菌如變形桿菌茁壯成長。代謝產物如硝酸鹽和亞硝酸鹽等也可以為腸桿菌科提供生長優勢[23]。因此,腸道炎癥或生態失調可能有利于腸桿菌科等在腸道中的生長,并隨后轉移到乳腺。Hu等[24]也研究了瘤胃微生物群對牛乳腺炎的影響,結果表明外源性致病微生物和內源性致病因素共同引起乳腺炎,瘤胃菌群失調所導致的瘤胃脂多糖的含量升高,脂多糖通過血液循環進入乳腺,破壞血乳屏障,進而誘發奶牛的乳腺炎癥。研究腸道菌群在宿主防御金黃色葡萄球菌感染引起的乳腺炎中的功能和調節機制的過程中發現,腸道微生物群失調小鼠的血乳屏障通透性增加,致病菌的豐度顯著增加,而產生短鏈脂肪酸的細菌門(如厚壁菌門)的相對豐度顯著降低,加快了金黃色葡萄球菌誘導乳腺炎的進程,進行菌群移植后可減輕致病菌對乳腺組織的損傷[25]。本研究經飼喂唾液乳桿菌,發現奶山羊腸道中微生物類群在門水平上顯著升高,厚壁菌門(Firmicutes)的相對含量有所增加,擬桿菌門(Bacteroidetes)的相對含量顯著降低,說明唾液乳桿菌能夠幫助恢復腸道微生物的平衡。同時,改變的乳腺微環境有利于致病菌的生存[26]。因此本研究也對乳汁菌群進行了檢測,發現飼喂唾液乳桿菌后乳汁微生物菌群在門水平上的微生物類群數顯著升高,變形菌門的相對豐度顯著降低,厚壁菌門和藍藻菌門的相對豐度顯著升高,顯現出唾液乳桿菌飼喂對乳汁菌群的調節能力。
本研究將唾液乳桿菌分別飼喂患有隱性乳腺炎的奶山羊和未患隱性乳腺炎的奶山羊,探究唾液乳桿菌對奶山羊隱性乳腺炎的防治效果。通過CMT試驗對奶山羊乳汁進行隱性乳腺炎發病率的檢測,結果顯示,飼喂唾液乳桿菌28 d后,奶山羊隱性乳腺炎的檢測率顯著降低,空白對照組隱性乳腺炎的檢測率有微弱上升趨勢。隨后為了探究唾液乳桿菌對隱形乳腺炎產生影響的方式,又檢測了山羊血液中炎癥因子的表達變化,發現患有隱性乳腺炎的奶山羊經飼喂唾液乳桿菌,血液中促炎因子的相對表達量顯著降低、抑炎因子的相對表達量顯著升高。之后將奶山羊隱性乳腺炎治療組的糞便與乳汁樣本進行菌群檢測發現,飼喂唾液乳桿菌前、后奶山羊的糞便和乳汁菌群均發生了顯著差異。與飼喂前相比,飼喂唾液乳桿菌后的奶山羊腸道和乳汁菌群Alpha多樣性升高,這說明唾液乳桿菌可以改變腸道和乳汁菌群的物種分布,從而使菌落多樣性顯著提高。與飼喂前相比,腸道和乳汁微生物在門水平上的類群數量均顯著升高。表明唾液乳桿菌具有調節腸道和乳汁的菌群組成的功能,對奶山羊隱性乳腺炎具有較好的治療效果。
4" 結" 論
奶山羊飼喂唾液乳桿菌后,隱性乳腺炎的檢測率顯著下降,隱性乳腺炎奶山羊血液中促炎因子的相對表達量顯著降低,表明唾液乳桿菌對隱性乳腺炎有較好的防治效果。患有隱性乳腺炎的奶山羊飼喂唾液乳桿菌后,糞便和乳汁微生物菌群多樣性顯著增加,糞便中厚壁菌門(Firmicutes)的相對含量有所增加,擬桿菌門(Bacteroidetes)的相對含量顯著降低,乳汁中厚壁菌門(Firmicutes)相對豐度增加,擬桿菌門(Bacteroidetes)和變形菌門(Proteobacteria)的相對豐度降低,表明唾液乳桿菌能夠調節腸道和乳汁的菌群組成。
參考文獻(References):
[1]" 趙興緒.獸醫產科學[M].第3版.北京:農業出版社,2002.
ZHAO X X.Veterinary obstetrics[M].3rd ed.Beijing:China Agriculture Press,2002.(in Chinese)
[2]" PUGGIONI G M G,TEDDE V,UZZAU S,et al.Relationship of late Lactation milk Somatic cell count and cathelicidin with intramammary infection in small ruminants[J].Pathogens,2020,9(1):37.
[3]" 彭" 群.奶山羊隱性乳房炎病原菌分離鑒定及滅活疫苗免疫效果評估[D].楊凌:西北農林科技大學,2021.
PENG Q.Isolation and identification of pathogenic bacteria of recessive mastitis in dairy goats and evaluation of immune effect of inactivated vaccine[D].Yangling:Northwest Aamp;F University,2021.(in Chinese)
[4]" 顏余同.山羊乳汁體細胞中抗菌肽S100A7與乳房炎的關系研究[D].楊凌:西北農林科技大學,2021.
YAN Y T.Study on the relationship between antibacterial peptide S100A7 in goat milk somatic cells and mastitis[D].Yangling:Northwest Aamp;F University,2021.(in Chinese)
[5]" RAINARD P,RIOLLET C.Innate immunity of the bovine mammary gland[J].Vet Res,2006,37(3):369-400.
[6]" RUEGG P L.Making antibiotic treatment decisions for clinical mastitis[J].Vet Clin North Am:Food Anim Pract,2018,34(3):413-425.
[7]" ALEKISH M O,ISMAIL Z B,AWAWDEH M S,et al.Effects of intramammary infusion of sage (Salvia officinalis) essential oil on milk somatic cell count,milk composition parameters and selected hematology and serum biochemical parameters in Awassi sheep with subclinical mastitis[J].Vet World,2017,10(8):895-900.
[8]" 田" 琛.黃芪中藥組合方劑對奶牛乳房炎的治療效果[J].中獸醫學雜志,2021(7):8-9.
TIAN C.Therapeutic effect of astragalus combined with traditional Chinese medicine on mastitis in dairy cows[J].Chinese Journal of Traditional Veterinary Science,2021(7):8-9.(in Chinese)
[9]" 郭子記,趙湖北,王" 平,等.復合納米抗菌肽防治奶山羊乳房炎效果的研究[J].動物醫學進展,2022,43(11):114-117.
GUO Z J,ZHAO H B,WANG P,et al.Preventing and treating effects of composite Nano antibacterial peptides on dairy goat mastitis[J].Progress in Veterinary Medicin,2022,43(11):114-117.(in Chinese)
[10]" LI K,YANG M,JIA L,et al.The prevention effect of Lactobacillus plantarum 17-5 on Escherichia coli-induced mastitis in mice[J].Probiotics Antimicrob Proteins,2023,15(6):1644-1652.
[11]" PADUCH J H,LCKING J,MANSION-DE VRIES E,et al.Prevention of intramammary infections by prepartum external application of a teat dip containing Lactic acid bacteria with antimicrobial properties in dairy heifers[J].Pathogens,2020,9(4):288.
[12]" KOZAKOVA H,SCHWARZER M,TUCKOVA L,et al.Colonization of germ-free mice with a mixture of three lactobacillus strains enhances the integrity of gut mucosa and ameliorates allergic sensitization[J].Cell Mol Immunol,2016,13(2):251-262.
[13]" BERGSTROM K S B,XIA L J.Mucin-type O-glycans and their roles in intestinal homeostasis[J].Glycobiology,2013,23(9):1026-1037.
[14]" GRANADO-SERRANO A B,MARTN-GAR M,SNCHEZ V,et al.Faecal bacterial and short-chain fatty acids signature in hypercholesterolemia[J].Sci Rep,2019,9(1):1772.
[15]" 蔡賽波.唾液乳桿菌微膠囊制備工藝的研究[D].昆明:昆明理工大學,2021.
CAI S B.Study on preparation technology of Lactobacillus salivarius microcapsule[D].Kunming:Kunming University of Science and Technology,2021.(in Chinese)
[16]" 趙燕清.奶山羊隱性乳腺炎的流行病學調查及S.aureus感染小鼠乳腺后Th細胞免疫應答機制研究[D].楊凌:西北農林科技大學,2015.
ZHAO Y Q.Epidemiological Investigation of subclinical mastitis in dairy goats and research on immune response mechanisms of t helper cells to infection with Staphylococcus aureus in murine mammary gland[D].Yangling:Northwest Aamp;F University,2015.(in Chinese)
[17]" 同娟珍.山羊羊口瘡及乳房炎病程中腸道菌群改變及其對免疫功能影響的研究[D].楊凌:西北農林科技大學,2021.
TONG J Z.Study on the changes of intestinal flora and its effects on immune function during ORF and mastitis in goats[D].Yangling:Northwest Aamp;F University,2021.(in Chinese)
[18]" 朱彤波.醫學免疫學[M].四川:四川大學出版社,2017.
ZHU T B.Medical immunology[M].Sichuan:Sichuan University Press,2017.(in Chinese)
[19]" HOLOWACZ S,BLONDEAU C,GUINOBERT I,et al.Lactobacillus salivarius LA307 and Lactobacillus rhamnosus LA305 attenuate skin inflammation in mice[J].Benefic Microbes,2018,9(2):299-309.
[20]" WANG C H,YEN H R,LU W L,et al.Adjuvant Probiotics of Lactobacillus salivarius subsp.salicinius AP-32,L.johnsonii MH-68,and Bifidobacterium animalis subsp.lactis CP-9 attenuate glycemic levels and inflammatory cytokines in patients with type 1 diabetes mellitus[J].Front Endocrinol,2022,13:754401.
[21]" PARIDA S,WU S G,SIDDHARTH S,et al.A procarcinogenic colon microbe promotes breast tumorigenesis and metastatic progression and concomitantly activates Notch and β-catenin axes[J].Cancer Discov,2021,11(5):1138-1157.
[22]" ZHAO C J,BAO L J,QIU M,et al.Commensal cow Roseburia reduces gut-dysbiosis-induced mastitis through inhibiting bacterial translocation by producing butyrate in mice[J].Cell Rep,2022,41(8):111681.
[23]" CHANIN R B,WINTER M G,SPIGA L,et al.Epithelial-derived reactive oxygen species enable AppBCX-mediated aerobic respiration of Escherichia coli during intestinal inflammation[J].Cell Host Microbe,2020,28(6):780-788.e5.
[24]" HU X Y,GUO J,ZHAO C J,et al.The gut microbiota contributes to the development of Staphylococcus aureus-induced mastitis in mice[J].ISME J,2020,14(7):1897-1910.
[25]" HU X Y,LI S,MU R Y,et al.The rumen microbiota contributes to the development of mastitis in dairy cows[J].Microbiol Spectr,2022,10(1):e0251221.
[26]" SOTO-PANTOJA D R,GABER M,ARNONE A A,et al.Diet alters entero-mammary signaling to regulate the breast microbiome and tumorigenesis[J].Cancer Res,2021,81(14):3890-3904.
(編輯" 范子娟)

