豬Lck蛋白在豬圓環病毒2型體外復制過程中的作用
摘" 要: 為了鑒定豬圓環病毒2型(PCV2)侵染細胞建立感染的重要宿主因子,本文分析在PK-15細胞中豬淋巴細胞特異性酪氨酸激酶Lck表達及活性對PCV2感染復制的影響,確定Lck是調控PCV2感染復制的新靶點。首先,本研究基于豬Lck結構特性和序列保守性分析,選取Lck SH3結構域為免疫原基因序列,利用原核表達目的蛋白制備小鼠抗豬Lck的多克隆抗體。然后,通過Western blot檢測PCV2感染PK-15和3D4/21細胞后對Lck表達及活性的影響。最后,在PK-15細胞中利用瞬時轉染過表達或Lck特異性抑制劑(A770041),通過Western blot和熒光定量PCR(RT-qPCR)檢測豬Lck表達和磷酸化對PCV2復制的影響。結果顯示,成功制備了鼠源性抗豬Lck的多克隆抗體。在PCV2感染PK-15和3D4/21細胞早期階段,Lck表達水平未見明顯變化,但Lck磷酸化水平顯著上調。過表達Lck可顯著上調PCV2 Cap蛋白表達及病毒拷貝數,而采用A770041抑制Lck磷酸化水平后,可顯著下調PCV2 Cap蛋白表達、病毒拷貝數和病毒滴度,這些結果表明Lck正調控PCV2的感染復制,為發現PCV2感染的新分子機制奠定重要基礎。
關鍵詞: PCV2;Capsid;Lck;SH3結構域;病毒復制
中圖分類號: S852.659.2
文獻標志碼:A
文章編號:0366-6964(2024)12-5751-11
doi: 10.11843/j.issn.0366-6964.2024.12.037
開放科學(資源服務)標識碼(OSID):
收稿日期:2024-01-16
基金項目:湖南省自然科學基金面上項目(2022JJ30298);湖南省技術攻關“揭榜掛帥”項目(2021NK1030);湖南省大學生創新創業訓練計劃一般項目(S202310537036)
作者簡介:劉偉姣(1998-),女,湖南長沙人,碩士生,主要從事動物重要病毒性疫病病原學研究,E-mail:1149283137@stu.hunau.edu.cn
*通信作者:王乃東,主要從事動物重要病毒性疫病病原學研究,E-mail:naidongwang@hunau.edu.cn
The Role of Porcine Lck Protein in PCV2 Replication in vitro
LIU" Weijiao1, HE" Qing1, JIANG" Yifan1, CAO" Siyu1, ZHANG" Shirui2, L Jialu2, LONG" Ping2, YANG" Lingchen1, ZHOU" Chuan2, WANG" Naidong1*
(1.College of Veterinary Medicine, Hunan Agricultural University, Hunan Provincial Key Laboratory of Protein Engineering in Animal Vaccines, R amp; D Center for Animal Reverse Vaccinology of Hunan Province, Changsha 410128," China;
2.College of Veterinary Medicine, Hunan Agricultural University, Changsha
410128," China)
Abstract:" In order to identify important host factors in cell entry and establishment of infection of porcine circovirus type 2 (PCV2), the effects of porcine lymphocyte specific tyrosine kinase Lck expression and activity on PCV2 infection replication were analyzed, and Lck was identified as a new target for the regulation of PCV2 replication. In this study, based on analysis of the structural characteristics and sequence conservation of porcine Lck, the Lck SH3 domain was selected as the immunogen gene sequence, and the polyclonal antibody against porcine Lck was prepared in mice using the protein expressed the E. coli expression system. Then, the effect of PCV2 infection on the expression and activity of Lck in PK-15 and 3D4/21 cells was detected using Western blot. Finally, the effects of porcine Lck expression and phosphorylation on PCV2 replication in PK-15 cells transiently transfected with overexpressed vector or treated with Lck specific inhibitor (A770041) were detected by Western blot and RT-qPCR, respectively. The results showed that mouse derived polyclonal antibodies against pig Lck were successfully prepared. There was no significant change in the expression level of Lck, but the phosphorylation level of Lck was significantly up-regulated in the early stage of PCV2 infection in PK-15 and 3D4/21 cells. Overexpression of Lck significantly increased PCV2 Cap protein expression and viral copy number, while inhibition of Lck phosphorylation level with A770041 could significantly downregulate the expression of PCV2 Cap protein, viral copy number and virus titer. These results indicated that Lck positively regulated PCV2 replication, which lays an important foundation for exploring the new molecular mechanism of PCV2 infection.
Key words: PCV2; capsid; Lck; SH3 domain; virus replication
*Corresponding author:" WANG Naidong, E-mail: naidongwang@hunau.edu.cn
豬圓環病毒2型(porcine circovirus type 2, PCV2)是目前哺乳動物中發現的最小的無囊膜、單鏈環狀DNA病毒[1]。是引起斷奶仔豬多系統衰竭綜合征等PCV2相關性系統疾病的主要病原體。臨床上,PCV2與其他病原體混合感染常常發生,給養豬業造成重大經濟損失[2-4]。PCV2基因組僅1 767~1 768 nt,其開放閱讀框(ORFs)分別編碼兩個主要蛋白(Rep/Rep’和Cap)[5],其中,核衣殼蛋白(Cap)是PCV2唯一的結構蛋白[6],在病毒的感染與誘導宿主免疫應答反應等方面發揮重要功能。對PCV2 Cap蛋白結構進行分析,發現其羧基端9個氨基酸序列(CT序列)末端具有保守的PXXP基序,而非致病性PCV1缺少該基序[6]。研究報道病毒結構蛋白的PXXP基序可與Src激酶家族(Src-family kinases,SFKs)SH3結構域互作,并通過多種機制對病毒感染和復制過程有重要影響[7-11],因此該基序可能會與含有SH3結構域的蛋白質相互作用,輔助病毒感染宿主細胞,進而在PCV2致病性中發揮作用[6]。
SFKs是具有酪氨酸蛋白激酶活性的重要信號傳導分子,廣泛存在于各種細胞中,在維持細胞穩態和功能中發揮著至關重要的作用。SFKs包含9個具有相似結構和功能的成員(c-Src、Lck、Hck、Fyn、Blk、Lyn、Fgr、Yes和Yrk),其中,淋巴細胞特異性蛋白酪氨酸激酶(lymphocyte specific protein tyrosine kinase,Lck)是SFKs重要成員(分子量56 ku),主要由1個UD結構域(unique domain)、2個" 調節結構域(SH3和SH2 domains)和1個激酶結構域(kinase domain)組成。Lck可游離于細胞質中,也可通過其N末端的脂肪酸化修飾(肉豆蔻酰化和/或棕櫚酰化)將Lck與細胞膜內側相連。其中,SH3結構域是Lck活性功能發揮的重要結構域,它可通過介導Lck分子內和分子間相互作用,調節Lck的活性并影響其信號傳遞[12]。有研究報道Lck可參與多種病毒的入侵及增殖,如單純皰疹病毒1型(HSV-1)[13]、人類免疫缺陷病毒1型(HIV-1)[9-10,14-16]和丙型肝炎病毒(HCV)[7-8]等,其中HIV-1 Nef蛋白、HCV NS5A蛋白均可通過多聚脯氨酸基序(PXXP)與Lck相互作用進而促進病毒復制。充分了解Lck表達及激活對PCV2感染復制的調節作用,有利于發現PCV2感染的新分子機制和提供干預PCV2疾病新靶點。
前期研究發現,以PXXP突變毒株作為對照,PCV2侵染PK-15細胞早期過程中(lt;1 hpi),顯著上調SFKs關鍵成員Lck基因mRNA水平[17],為了揭示豬Lck蛋白在PCV2體外復制過程中的作用,本研究基于豬Lck結構分析,分別構建包含Lck全長及其SH3結構域的表達載體,并制備豬Lck-SH3多克隆抗體,利用該抗體檢測發現Lck在PCV2感染的靶細胞中均有表達,進一步研究發現Lck及其SH3結構域過表達均促進PCV2復制,而且Lck特異性抑制劑A770041可有效抑制PCV2的細胞復制,本研究將有助于揭示Lck激酶應答介導PCV2感染復制的新機制。
1" 材料與方法
1.1" 主要試驗材料及實驗動物
原核表達載體pET-28a(+)、真核表達質粒pCI-neo、HEK 293 T細胞和PK-15細胞由筆者所在實驗室保存;PCV2病毒由本實驗室保存的PCV2毒株(GenBank登錄號:KJ867555)。E. coli DH5α和E. coli BL21(DE3)感受態細胞購自金沙生物有限公司,T4 DNA連接酶、Taq DNA聚合酶、蛋白Marker、限制性內切酶購自美國Thermo Fisher公司。質粒小提試劑盒購于Omega公司。DMEM培養基、胎牛血清購自Gibco公司。弗氏完全佐劑(FCA)和弗氏不完全佐劑(FIA)購自Sigma公司。兔源HA標簽單克隆抗體(MAb)購自Zen Bioscience公司。鼠源His標簽單克隆抗體(MAb)購自Solarbio公司。Alexa Fluor-488山羊抗兔IgG、Alexa Fluor-594山羊抗鼠IgG購自Life Technologies公司。Lck(phosphorylation Tyr394)抗體(GTX133876)購自GeneTex公司;Lck抑制劑A770041(HY-11011)購自MCE公司。SPF級6周齡雌性BALB/c小鼠購自湖南斯萊克景達實驗動物技術有限公司。
1.2" 豬Lck結構特征分析
利用ExPASy在線軟件的ProtParam程序(https://web.expasy.org/protparam/)預測豬Lck蛋白理化性質;利用在線軟件MultAlin(http://multalin.toulouse.inra.fr/multalin/)進行多序列比對;利用在線軟件Genomenet(https://www.genome.jp/tools-bin/clustalw)進行保守性分析;利用Pymol軟件預測Lck蛋白三級結構。
1.3" 目的基因擴增
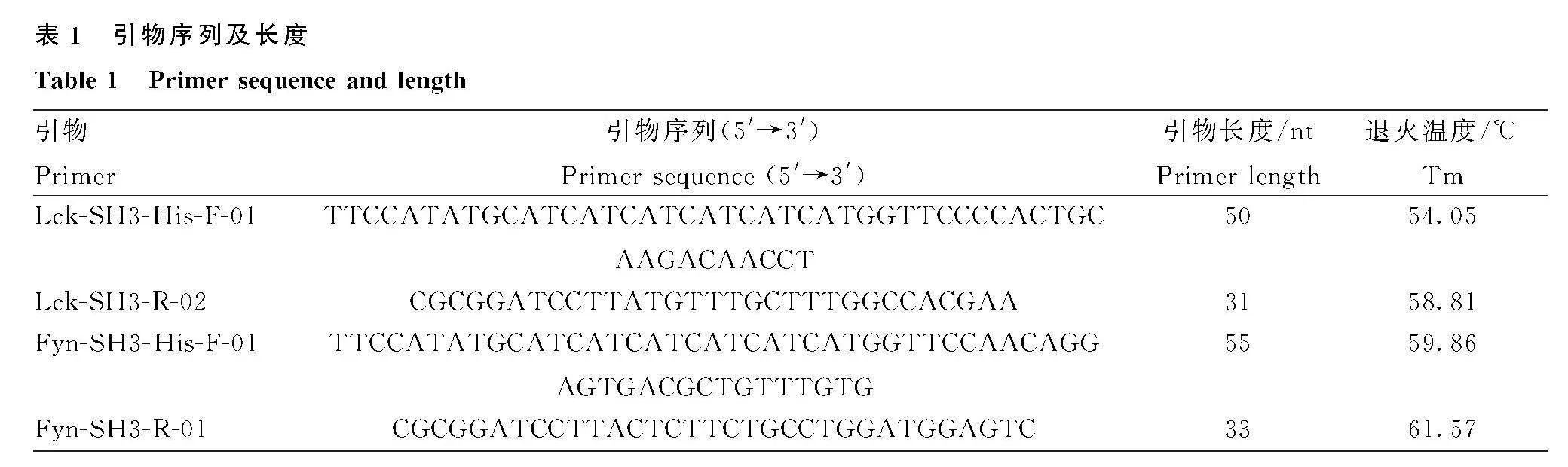
根據GenBank中的豬Lck序列(登錄號:NM_001143713.1)及Fyn序列(登錄號:NM_001080 206.2),利用Primer Premier 5軟件設計克隆引物(表1),以豬脾cDNA為模板,通過PCR擴增Lck基因片段,膠回收PCR產物,擴增Lck SH3結構域序列。引物由擎科生物工程股份有限公司合成。
1.4" 重組質粒構建
膠回收PCR產物與載體分別限制性內切酶進行雙酶切。回收目的片段后,按照T4 DNA連接酶說明書4℃連接過夜。隨后將連接產物轉化到E. coli DH5α感受態細胞中,涂平板后挑選陽性單克隆菌落進行菌液擴增和質粒提取,酶切鑒定正確后送至擎科生物工程股份有限公司進行測序。
1.5" 豬Lck-SH3蛋白原核表達與純化
將重組質粒pET-28a(+)-Lck-SH3、pET-28a(+)-Fyn-SH3轉化E. coli BL21(DE3)感受態細胞,挑取單個克隆進行自誘導培養。收集菌液,超聲破碎后,利用鎳親和層析柱進行純化。將所獲得的樣品(Total、Sup、FT、W、E1、E2、E4、E6)加入5×SDS Buffer,進行SDS-PAGE電泳。
1.6" 豬Lck多克隆抗體制備及鑒定
使用純化后的Lck-SH3分別對BALB/c小鼠進行免疫,皮下注射20 μg·只-1,共免疫3次,每次間隔2周,首次免疫使用弗氏完全佐劑,之后2次免疫使用弗氏不完全佐劑,佐劑與蛋白等體積混合并充分乳化。3次免疫后采集血液,收集血清進行后續驗證。
1.7" 豬Lck多克隆抗體特異性檢測
1.7.1" Western blot檢測
將純化的豬蛋白Lck-SH3、Fyn-SH3加入5×Loading Buffer煮沸后,經15%SDS-PAGE分離蛋白質,將其轉移到PVDF膜上,用5%脫脂奶粉封閉1 h;將鼠源多克隆抗體(1∶3 000)4 ℃孵育過夜,PBST洗滌3次,5 min·次-1;在37℃條件下與HRP標記山羊抗兔IgG孵育1 h,PBST洗滌3次,5 min·次-1;用超敏ECL化學發光試劑盒顯色觀察。
1.7.2" 間接免疫熒光試驗(IFA)檢測
將pCI-neo-Lck或pCI-neo-Lck-SH3重組質粒轉染HEK 293 T細胞48 h后,將細胞樣品進行固定、透膜和封閉處理。分別以Lck鼠多抗(1∶200)作為一抗,然后以Alexa Fluor-594山羊抗鼠IgG(1∶2000)作為二抗進行IFA試驗,用熒光顯微鏡觀察顯示的紅色熒光。
1.8" PCV2感染PK-15細胞
將無PCV1/PCV2污染的PK-15細胞接種于6孔細胞培養板中,用含5%胎牛血清(FBS)的DMEM培養基培養細胞,細胞長至60%。用PCV2(MOI=1)感染PK-15或3D4/21細胞1 h后收集細胞蛋白,作為試驗組;未感染的細胞作為對照組(NC)。
1.9" 過表達Lck對PCV2復制的影響
通過擎科生物工程股份有限公司合成豬Lck編碼區序列,構建Lck過表達載體pCI-neo-Lck。轉染前將PK-15細胞鋪于24孔板中,待第2天細胞長至80%后依據Lipofectamine 2000說明書進行轉染。轉染24 h后,PCV2以MOI=1感染PK-15細胞。病毒感染48 h后,收集細胞樣品至離心管中,分別通過Western blot、IFA或RT-qPCR[18]進行檢測。
1.10" CCK8細胞毒性測定
A770041抑制劑稀釋為不同的濃度(0、0.5、1、1.5、2、2.5和3 μmol·L-1),每個濃度設定5個重復,分別加至已長成單層PK-15細胞的96孔培養板(1×104·孔-1)中,同時設定含0.5%DMSO的細胞對照組和空白細胞對照組。置37℃培養箱中培養24 h后,每孔加入10 μL CCK8溶液,繼續培養2 h,酶標儀于450 nm波長處檢測OD值。以對照組細胞的存活率為100%,試驗組細胞活性=[(對照-空白)-(試驗-空白)]/(對照-空白)×100%。
1.11" Lck特異性抑制劑A770041對PCV2復制的影響
培養板中的細胞達到60%左右時,使用不同濃度A770041(1、2 μmol·L-1)預處理PK-15細胞2 h(以DMSO作對照),然后加入MOI=1的PCV2病毒液感染細胞,48 h后收取細胞及其上清,檢測PCV2 Cap蛋白表達、PCV2的病毒拷貝數及子代病毒滴度。
1.12" 子代病毒滴度測定
采用半數細胞培養物感染量(TCID50)來進行測定病毒滴度,將PK-15細胞以1.3×104·孔-1鋪于96孔板,待每個孔的單層細胞長至60%時,棄去上清,用PBS潤洗3次;然后加入用DMEM細胞維持液(含2%FBS)10倍倍比稀釋的病毒樣品,獲得稀釋度依次為10-1~10-7的待測病毒稀釋液;96孔板的第一列對應10-1稀釋度的病毒液,第二列對應10-2稀釋度的病毒液,依次類推,最后兩列作為空白組,每個稀釋度設8個重復。置于細胞培養箱,培養72 h。通過間接免疫熒光法進行檢測。用倒置熒光顯微鏡進行觀察,并按照Karber方法計算TCID50。
1.13" 數據分析
研究中Western blot得蛋白條帶使用Image J軟件對灰度值進行掃描,進行統計分析。使用GraphPad prism80軟件(One-way ANOVA test)進行統計學分析并繪圖,所有數據都被表示為平均值±標準差(x-±s),Plt;0.05(*)表示差異顯著,Plt;0.01(**)表示差異極顯著。
2" 結" 果
2.1" 豬Lck SH3 結構域的表達純化
2.1.1" 豬Lck蛋白的生物信息學分析
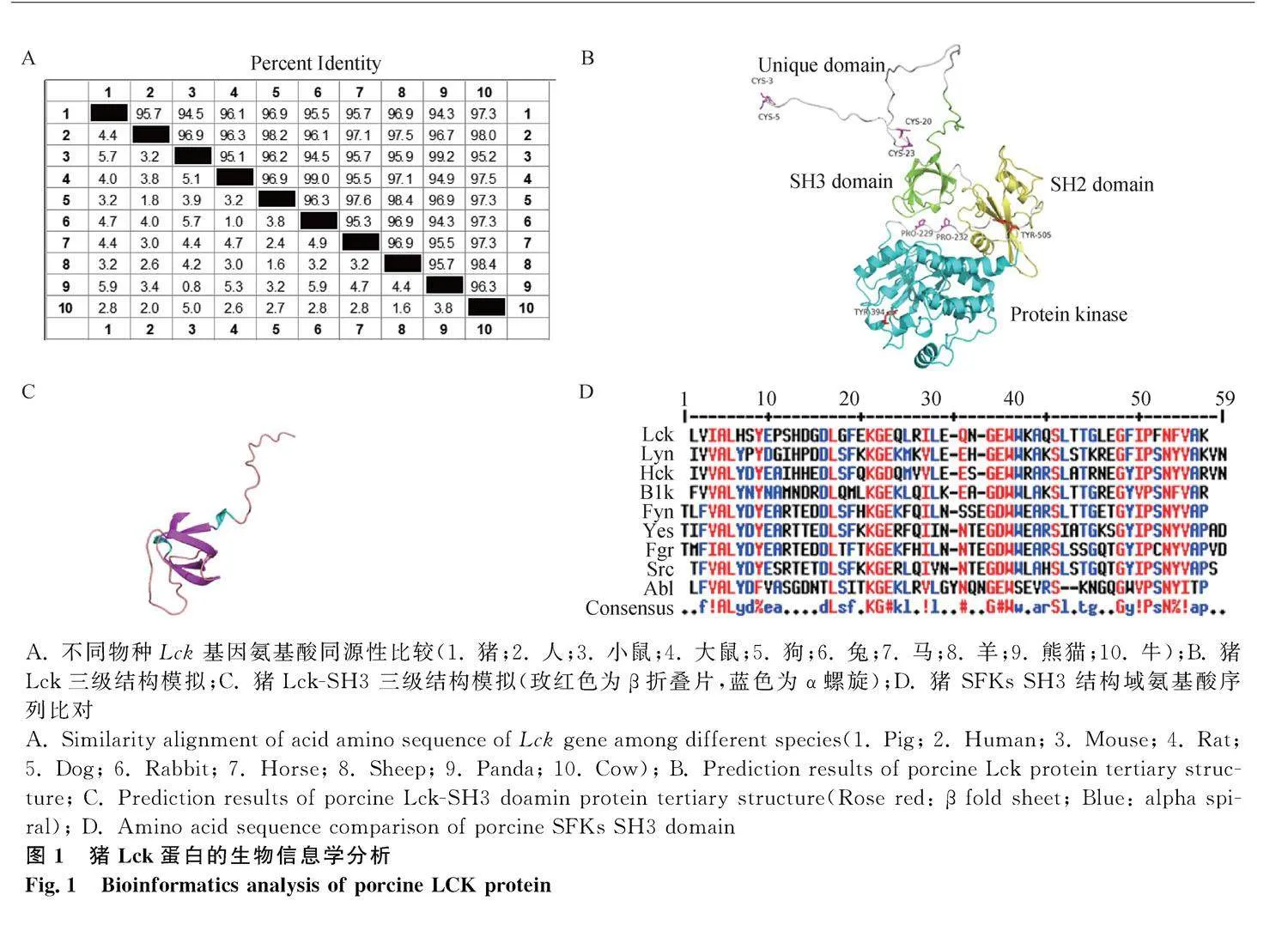
不同物種Lck氨基酸序列比對結果顯示,豬、馬、大熊貓、狗、牛、人、兔、羊、小鼠和大鼠間的Lck相似性均高達94%以上,表明Lck在不同物種間具有較高的保守性。其中,豬Lck與人Lck的氨基酸相似性為95.7%(圖1A),這與前期報道一致[19]。利用Pymol軟件基于AlphaFold Protein Structure Database中人Lck蛋白的結構“AF-P06239-F1”對豬Lck基因編碼蛋白三級結構進行預測(圖1B),其中豬Lck SH3結構域的三級結構包括5個β-折疊和2個小的α-螺旋(圖1 C)。另外,比對分析豬SFKs成員SH3結構域氨基酸序列,結果顯示SFKs各成員的SH3結構域保守性較低(圖1 D),提示以豬源性SFKs SH3基因序列作為免疫原制備抗體可降低不同成員間的交叉反應。因此,本文將通過大腸桿菌原核表達系統表達豬Lck-SH3蛋白,以制備特異性豬Lck多克隆抗體,同時以Fyn-SH3作為對照,為后續研究提供實驗材料。
2.1.2" Lck-SH3、Fyn-SH3 的原核表達及純化
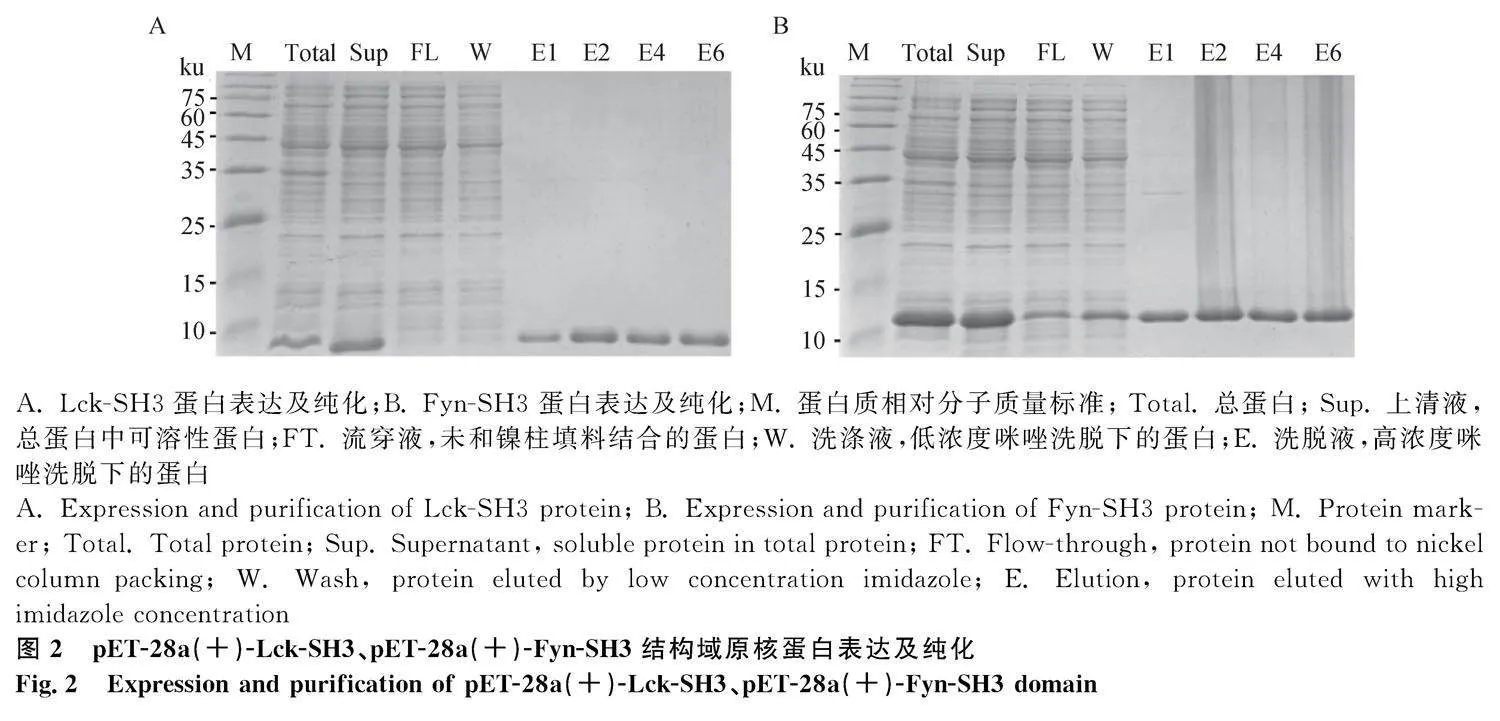
以豬肺組織的cDNA為模板進行PCR擴增,獲得Fyn-SH3-His和Lck-SH3-His基因片段,成功構建得到重組表達質粒pET-28a(+)-Lck-SH3、pET-28a(+)-Fyn-SH3。將重組質粒分別轉化E. coli BL21(DE3)感受態細胞,挑選單克隆菌落進行自誘導表達,并通過鎳柱親和層析法純化蛋白樣品。SDS-PAGE結果顯示,Lck-SH3(圖2A)、Fyn-SH3(圖2B)蛋白均為可溶性蛋白,蛋白大小均在10 ku左右,與預期一致。
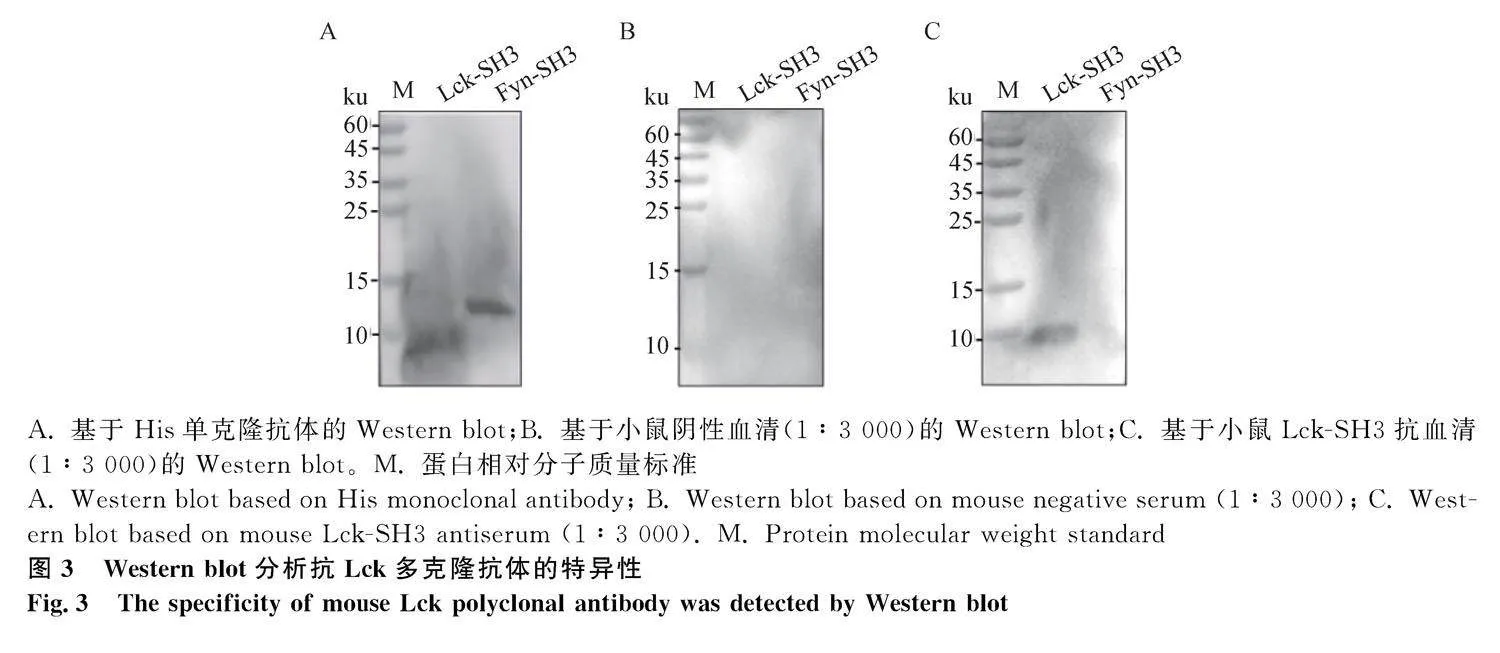
2.1.3" 豬 Lck 多克隆抗體的制備與鑒定
通過His單克隆抗體對重組蛋白進行Western blot鑒定,結果顯示標簽抗體可特異性識別Lck-SH3、Fyn-SH3目的蛋白(圖3 A)。然后利用Lck-SH3鼠抗血清對誘導表達的重組蛋白進行Western blot分析,Fyn-SH3蛋白作為對照,進一步表明制備的多克隆抗體能夠識別Lck-SH3蛋白,且與Fyn-SH3蛋白無交叉識別(圖3C);而選取陰性小鼠血清作為一抗孵育后,兩個泳道均未見特異性條帶(圖3 B),結果表明制備的Lck-SH3多克隆抗體具有良好的特異性和反應性。
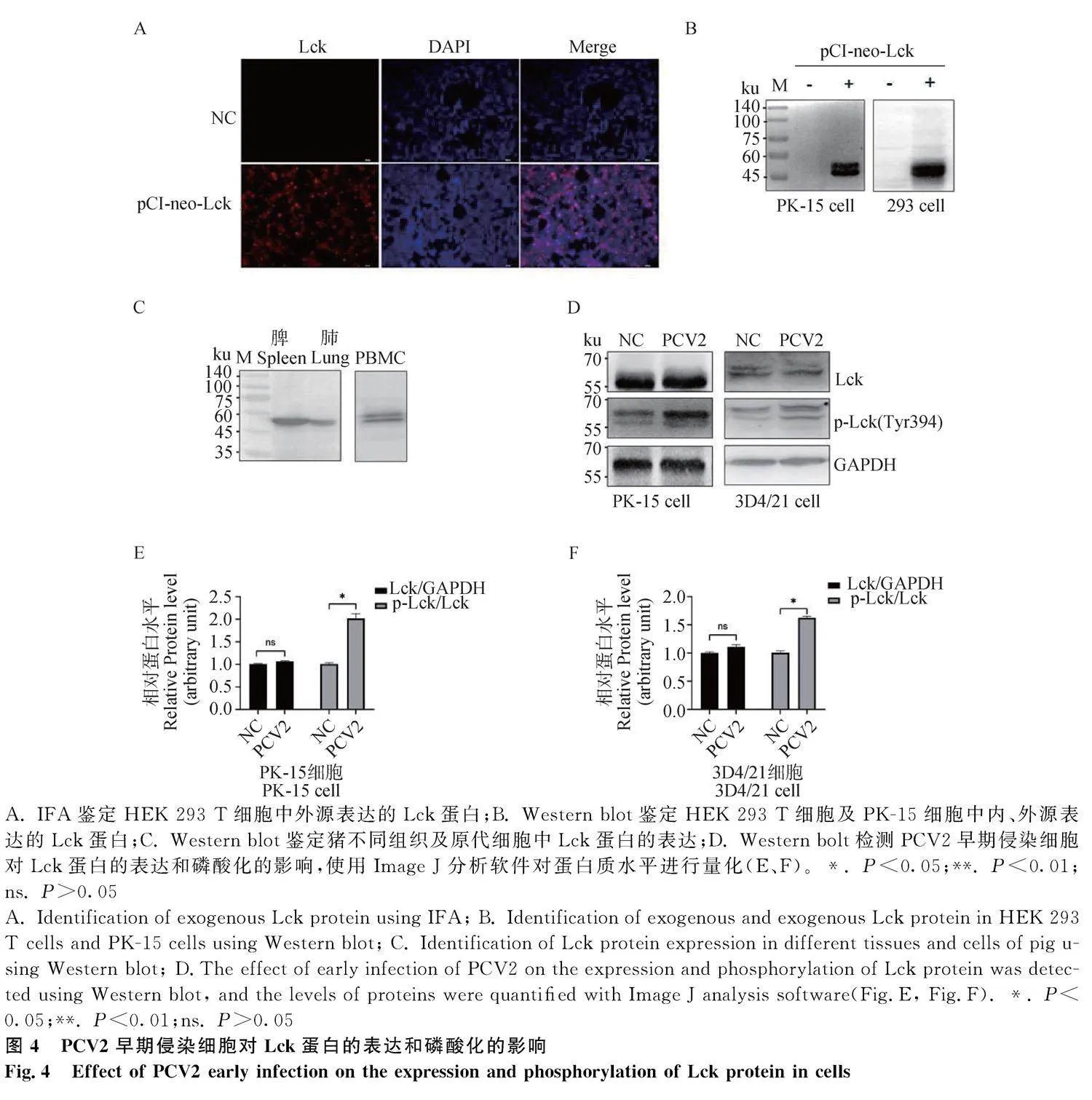
2.2" PCV2早期侵染細胞對Lck蛋白表達和磷酸化的影響
將真核表達質粒pCI-neo-Lck轉染HEK 293 T或PK-15細胞,Lck多抗的IFA鑒定結果顯示,HEK 293 T細胞轉染組可見特異性熒光(圖4 A);Western blot檢測結果顯示,HEK 293 T和PK-15細胞轉染組均可見符合預期大小的條帶(圖4B),說明制備的Lck多抗可用于IFA和Western blot檢測外源表達的Lck蛋白。然后利用該Lck多抗進一步檢測發現,Lck在豬肺、脾組織及PBMC細胞中均有較高水平的表達(圖4C),而且在PCV2感染PK-15和3D4/21細胞的早期階段(1 h),Lck表達水平未見明顯變化,但 Lck磷酸化的水平顯著上調(圖4D~F,P<0.05)。
2.3" 過表達Lck對PCV2在PK-15細胞中復制的影響
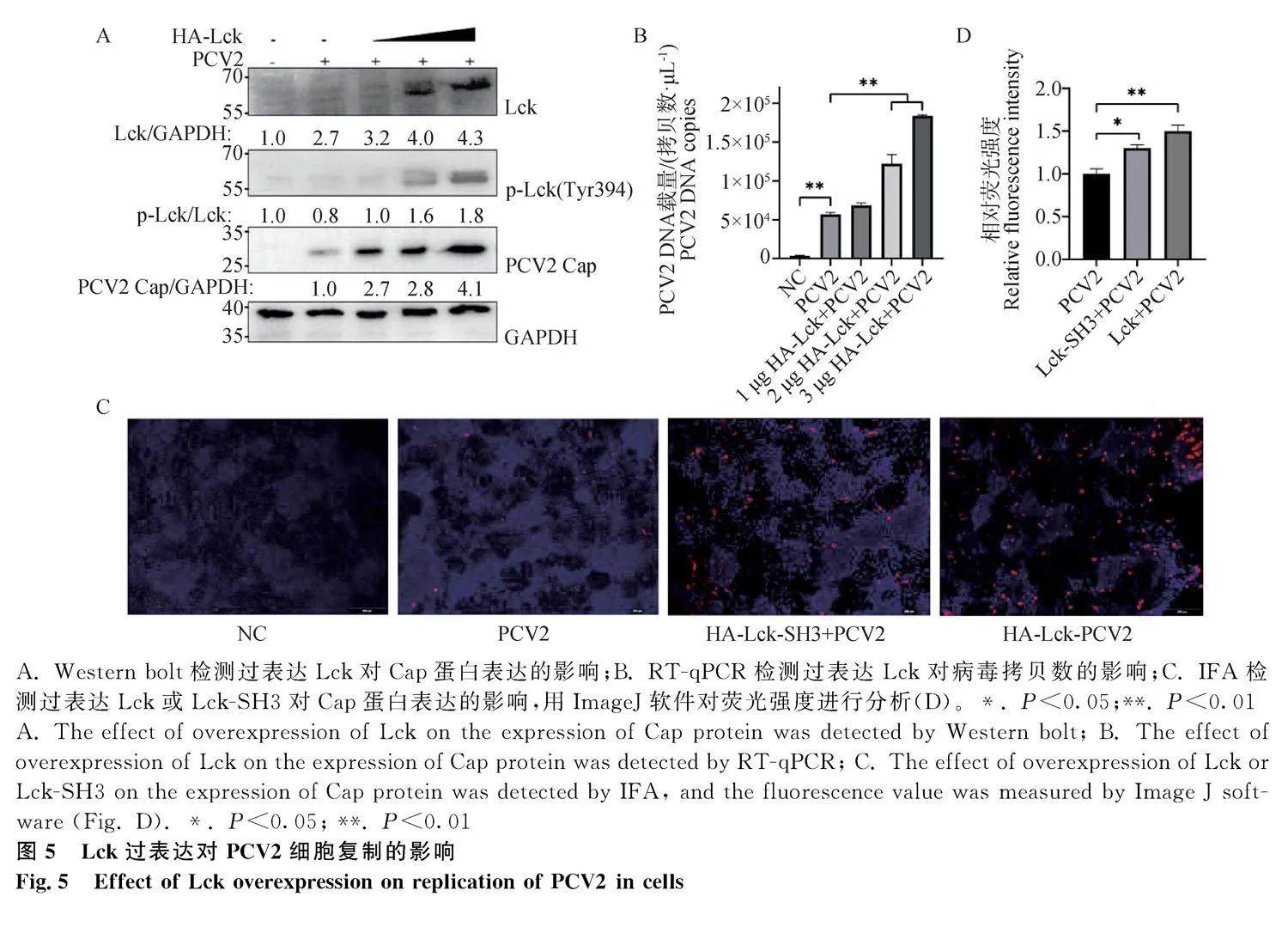
為了探究Lck是否介導PCV2在宿主細胞中的復制,將pCI-neo-Lck瞬時轉染至PK-15細胞后,用PCV2進行感染(MOI=1)。Western blot結果顯示,與正常PK-15細胞相比,Lck過表達誘導Cap蛋白表達水平升高,且存在劑量依賴性(圖5 A)。RT-qPCR結果顯示Lck過表達導致PCV2在PK-15細胞中的拷貝數顯著升高(圖5 B,P<0.05)。IFA顯示與前面結果一致,上調Lck表達或Lck-SH3表達均可促進病毒在PK-15細胞內的復制(圖5 C)。通過Image J軟件對熒光強度進行分析,與PCV2單獨感染組相比,過表達Lck組的紅色熒光強度極顯著增加(圖5 D,P<0.01),過表達Lck-SH3組的紅色熒光強度顯著增加(圖5D,P<0.05)。
2.4" Lck特異性抑制劑A770041對PCV2在PK-15細胞中復制的影響
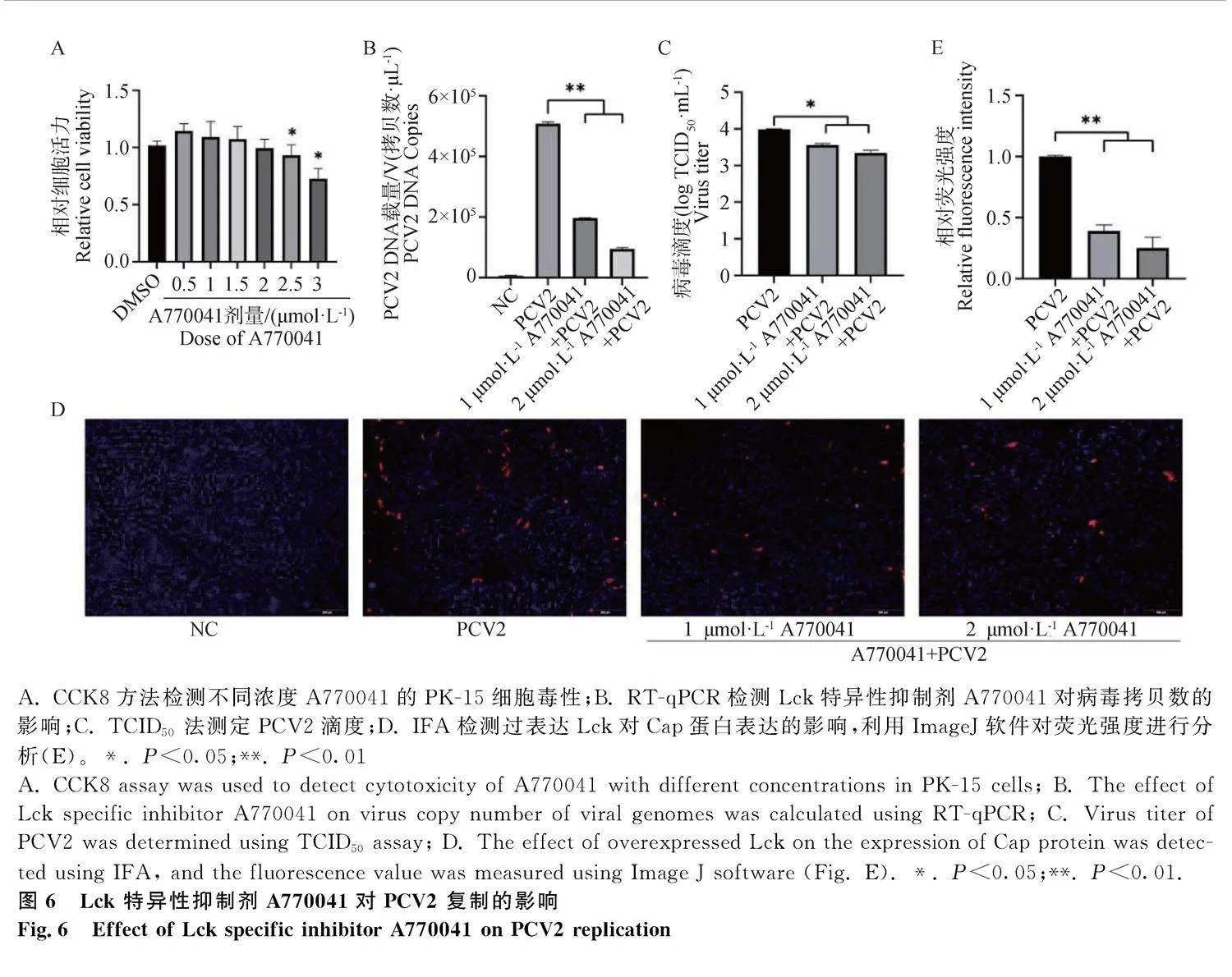
使用不同濃度的Lck磷酸化特異性抑制劑A770041處理PK-15細胞,通過CCK8試劑盒檢測細胞活性,結果顯示,當A770041濃度超過2 μmol·L-1時,出現了明顯的細胞毒性(圖6A)。因此,作者分別使用1和2 μmol·L-1 A770041對PK-15細胞進行預處理2 h后,用PCV2侵染細胞,48 hpi后分別通過RT-qPCR和TCID50檢測病毒的復制水平。結果顯示,與DMSO組相比,不同濃度A770041處理PK-15細胞后,均可顯著抑制細胞內PCV2復制(圖6 B,P<0.01)和細胞上清液中的病毒滴度(圖6 C,P<0.05),并且具有劑量依賴性;同時IFA結果顯示,隨著抑制劑濃度的提高,Cap蛋白表達逐漸降低(圖6 D、E,P<0.01)。上述結果表明Lck正調控PCV2病毒復制。
3" 討" 論
前期研究報道,羅非魚Lck重組蛋白可在大腸桿菌中表達,但主要以不可溶性包涵體形式存在[20]。我們嘗試通過pET-28a(+)原核表達載體轉化至大腸桿菌,用IPTG進行誘導表達豬Lck蛋白,結果顯示豬Lck重組蛋白大部分表達在包涵體,未能獲得蛋白正確折疊形式(結果未顯示)。Lck激酶的SH3結構域可與配體結合[21],啟動Lck關鍵酪氨酸殘基(Tyr394、Tyr505等)的磷酸化/去磷酸化,進而誘導蛋白構象變化來嚴格調控Lck激酶活性(功能)[22]。鑒于SH3結構域是調控Lck激酶活性的關鍵結構,并且SFKs各成員的SH3結構域保守性較低,因此我們選取SH3結構域序列用于Lck抗體制備,并且基于Lck-SH3與Fyn-SH3氨基酸相似性較高(46.3%,圖1),選取Fyn-SH3為對照來驗證Lck抗體的反應特異性。Western blot顯示,鼠抗豬Lck多克隆抗體識別瞬時表達的細胞Lck蛋白和PCV2感染PK-15細胞表達的Lck蛋白(圖4),不識別Fyn-SH3(圖3),該多克隆抗體特異性良好,無交叉反應。Liu和Xia[19]通過RT-qPCR分析發現,豬Lck基因在不同組織中的mRNA水平存在差異,在脾臟及肺臟中高水平表達,作者將Lck多克隆抗體應用于豬組織器官的Lck蛋白檢測,Western blot顯示Lck蛋白在豬脾、肺及PBMC細胞中較高水平表達(圖4 C),與報道一致。豬Lck蛋白多克隆抗體的制備,為進一步探究豬Lck蛋白功能和其表達對PCV2復制的調節作用提供了良好的工具。
宿主細胞的酶和蛋白對PCV2的感染具有一定調控作用,如胞外信號調節激酶(ERK)、蛋白激酶C(PKC)和3-羥基-3-甲基戊二酰輔酶A 還原酶(HMGCR)等[23-26]。研究表明Lck激酶通過與多種病毒的蛋白相互作用,誘導細胞信號轉導,從而參與病毒入侵、復制、病毒釋放及組裝和細胞擴散、轉化[7-10,13-16],但目前豬Lck介導病毒感染的研究報道較少。Islam等[27]在仔豬接種PRRSV后1 d,收集PBMC細胞經qPCR分析發現,其Lck基因表達水平顯著上調;Fernandes等[28]對PCV2感染斷乳仔豬(亞臨床感染)的腸系膜淋巴結和肺轉錄組譜進行分析,發現PCV2感染組中大多數顯著上調基因與免疫應答密切相關,如T細胞活化相關基因Lck等,提示豬Lck與病毒感染復制相關,探索病毒利用宿主細胞Lck激酶完成其生命周期的作用,有望成為研究PCV2致病機理的新切入點。
本團隊前期研究發現,SFKs抑制劑PP2能顯著抑制PCV2病毒復制、DNA和Cap蛋白合成及釋放等細胞感染過程,說明PCV2感染PK-15細胞需要SFKs成員[17]。為了進一步探究SFKs關鍵成員Lck是否影響PCV2感染,本研究在過表達Lck的PK-15細胞中,發現PCV2 Cap蛋白表達水平和病毒基因組拷貝數顯著升高(圖5),而且Lck特異性抑制劑A770041對宿主細胞預處理后,PCV2病毒拷貝數、子代病毒滴度及Cap蛋白的表達水平顯著降低(圖6),說明Lck激酶正調控PCV2的細胞復制,將有助于進一步開展PCV2細胞感染和復制機制研究。前期研究表明PXXP基序與Src家族激酶的SH3結構域互作有助于調節免疫細胞信號轉導、膜運輸和細胞骨架重排等[29],例如HVS-1 Tip蛋白SH3B結構域可與Lck SH3結構域結合,進而影響病毒在T淋巴細胞中的轉化[30-31];HIV-1 Nef蛋白PXXP基序可與SFKs(尤其是Hck和Lyn激酶)的SH3結構域相互作用,促進HIV-1體外復制[9]等。基于此,Lck蛋白SH3結構域與PCV2 Cap蛋白PXXP基序之間是否存在相互作用,以及Lck如何影響PCV2感染復制的作用機制需后續深入探究。
4" 結" 論
本研究通過大腸桿菌原核表達系統成功表達并純化Lck-SH3蛋白,制備了可識別豬Lck蛋白SH3結構域特異性抗體。進一步通過過表達和抑制劑試驗研究發現,上調Lck表達能顯著促進PCV2在PK-15細胞的復制,而抑制Lck活性能顯著抑制PCV2在PK-15細胞的復制。綜上所述,Lck能夠促進PCV2的體外復制,為發現PCV2感染的新分子機制奠定重要基礎。
參考文獻(References):
[1]" GAMAGE L N A, ELLIS J, HAYES S. Immunogenicity of bacteriophage lambda particles displaying porcine Circovirus 2 (PCV2) capsid protein epitopes[J]. Vaccine, 2009, 27(47):6595-6604.
[2]" SEGALS J, KEKARAINEN T, CORTEY M. The natural history of porcine circovirus type 2:from an inoffensive virus to a devastating swine disease?[J]. Vet Microbiol, 2013, 165(1-2):13-20.
[3]" SEGALS J. Best practice and future challenges for vaccination against porcine circovirus type 2[J]. Expert Rev Vac, 2015, 14(3):473-487.
[4]" ALARCON P, RUSHTON J, WIELAND B. Cost of post-weaning multi-systemic wasting syndrome and porcine circovirus type-2 subclinical infection in England - an economic disease model[J]. Prev Vet Med, 2013, 110(2):88-102.
[5]" 蘇" 芮, 王東亮, 陳指龍, 等. PCV2 ORF1~ORF4基因所編碼蛋白功能的研究進展[J]. 經濟動物學報, 2020, 24(1):46-51.
su b, wang d l, chen z l, et al. research progress on major function proteins encoded by PCV2 ORF1-ORF4 Gene[J]. Journal of Economic Animal, 2020, 24(1):46-51. (in Chinese)
[6]" WANG N D, ZHAN Y, WANG A B, et al. In silico analysis of surface structure variation of PCV2 capsid resulting from loop mutations of its capsid protein (Cap)[J]. J Gen Virol, 2016, 97(12):3331-3344.
[7]" MACDONALD A, CROWDER K, STREET A, et al. The hepatitis C virus NS5A protein binds to members of the Src family of tyrosine kinases and regulates kinase activity[J]. J Gen Virol, 2004, 85(3):721-729.
[8]" TRAN T, HOFFMANN S, WIESEHAN K, et al. Insights into human Lck SH3 domain binding specificity:different binding modes of artificial and native ligands[J]. Biochemistry, 2005, 44(45):15042-15052.
[9]" SAKSELA K, CHENG G, BALTIMORE D. Proline-rich (PxxP) motifs in HIV-1 Nef bind to SH3 domains of a subset of Src kinases and are required for the enhanced growth of Nef+ viruses but not for down-regulation of CD4[J]. EMBO J, 1995, 14(3):484-491.
[10]" TRIBLE R P, EMERT-SEDLAK L, SMITHGALL T E. HIV-1 Nef selectively activates Src family kinases Hck, Lyn, and c-Src through direct SH3 domain interaction[J]. J Biol Chem, 2006, 281(37):27029-27038.
[11]" KENNEY S P, MENG X J. An SH3 binding motif within the nucleocapsid protein of porcine reproductive and respiratory syndrome virus interacts with the host cellular signaling proteins STAMI, TXK, Fyn, Hck, and cortactin[J]. Virus Res, 2015, 204:31-39.
[12]" BOMMHARDT U, SCHRAVEN B, SIMEONI L. Beyond TCR signaling:emerging functions of Lck in cancer and immunotherapy[J]. Int J Mol Sci, 2019, 20(14):3500.
[13]" WAGNER M J, SMILEY J R. Herpes simplex virus requires VP11/12 to induce phosphorylation of the activation loop tyrosine (Y394) of the Src family kinase Lck in T lymphocytes[J]. J Virol, 2009, 83(23):12452-12461.
[14]" CHASE A J, WOMBACHER R, FACKLER O T. Intrinsic properties and plasma membrane trafficking route of Src family kinase SH4 domains sensitive to retargeting by HIV-1 Nef[J]. J Biol Chem, 2018, 293(20):7824-7840.
[15]" MELLORS J W, GUO S, NAQVI A, et al. Insertional activation of STAT3 and LCK by HIV-1 proviruses in T cell lymphomas[J]. Sci Adv, 2021, 7(42):eabi8795.
[16]" STRASNER A B, NATARAJAN M, DOMAN T, et al. The Src kinase Lck facilitates assembly of HIV-1 at the plasma membrane[J]. J Immunol, 2008, 181(5):3706-3713.
[17]" ZHANG J X, LEI X N, WANG D L, et al. Inhibition of Abl or Src tyrosine kinase decreased porcine circovirus type 2 production in PK15 cells[J]. Res Vet Sci, 2019, 124:1-9.
[18]" ZHAN Y, YU W T, CAI X, et al. The carboxyl terminus of the porcine circovirus type 2 capsid protein is critical to virus-like particle assembly, cell entry, and propagation[J]. J Virol, 2020, 94(9):e00042-20.
[19]" LIU Y G, XIA X S. Molecular characterization, tissue expression, polymorphism and association of porcine LCK gene[J]. Mol Biol Rep, 2012, 39(4):4023-4028.
[20]" 張永德, 林" 勇, 馮鵬霏, 等. 尼羅羅非魚Lck多克隆抗體的制備及鑒定[J]. 南方農業學報, 2018, 49(11):2304-2310.
ZHANG D Y, LIN Y, FENG P F, et al. Preparation and identification of Lck polyclonal antibody in Nile tilapia[J]. Journal of Southern Agriculture, 2018, 49(11):2304-2310. (in Chinese)
[21]" 張佳鑫. Src和Abl酪氨酸激酶家族介導的豬圓環病毒2型感染機制的初步研究[D]. 長沙:湖南農業大學, 2018.
ZHNAG J X. Study on porcine circovirus 2 infection mechanism mediated by Src and Abl tyrosine kinase family[D]. Changsha:Hunan Agricultural University, 2018. (in Chinese)
[22]" SALMOND R J, FILBY A, QURESHI I, et al. T-cell receptor proximal signaling via the Src-family kinases, Lck and Fyn, influences T-cell activation, differentiation, and tolerance[J]. Immunol Rev, 2009, 228(1):9-22.
[23]" MA T, CHEN X R, OUYANG H S, et al. HMGCR inhibits the early stage of PCV2 infection, while PKC enhances the infection at the late stage[J]. Virus Res, 2017, 229:41-47.
[24]" OUYANG T, NIU G Y, ZHANG Y F, et al. Porcine HMGCR inhibits porcine circovirus type 2 infection by directly interacting with the viral proteins[J]. Viruses, 2019, 11(6):544.
[25]" LIU X W, WANG Y, HAN C, et al. TGF-β from the porcine intestinal cell line IPEC-J2 induced by porcine circovirus 2 increases the frequency of treg cells via the activation of ERK (in CD4+ T cells) and NF-κB (in IPEC-J2)[J]. Viruses, 2022, 14(11):2466.
[26]" WANG T T, DU Q, NIU Y Y, et al. Cellular p32 is a critical regulator of porcine circovirus type 2 nuclear egress[J]. J Virol, 2019, 93(23):e00979-19.
[27]" ISLAM M A, GROE-BRINKHAUS C, PRLL M J, et al. PBMC transcriptome profiles identifies potential candidate genes and functional networks controlling the innate and the adaptive immune response to PRRSV vaccine in Pietrain pig[J]. PLoS One, 2017, 12(3):e0171828.
[28]" FERNANDES L T, TOMS A, BENSAID A, et al. Exploratory study on the transcriptional profile of pigs subclinically infected with porcine circovirus type 2[J]. Anim Biotechnol, 2009, 20(3):96-109.
[29]" PAGANO M A, TIBALDI E, PAL G, et al. Viral proteins and Src family kinases:Mechanisms of pathogenicity from a \"liaison dangereuse\"[J]. World J Virol, 2013, 2(2):71-78.
[30]" WEIS D D, KJELLEN P, SEFTON B M, et al. Altered dynamics in Lck SH3 upon binding to the LBD1 domain of Herpesvirus saimiri tip[J]. Protein Sci, 2006, 15(10):2402-2410.
[31]" ISAKOV N, BIESINGER B. Lck protein tyrosine kinase is a key regulator of T-cell activation and a target for signal intervention by Herpesvirus saimiri and other viral gene products[J]. Eur J Biochem, 2000, 267(12):3413-3421.
(編輯" 白永平)

