加味枳術散對斷奶仔兔腸黏膜屏障和抗氧化能力的影響



摘" 要: 旨在探討加味枳術散對斷奶仔兔回腸腸黏膜屏障的影響,為仔兔腹瀉疾病的防治提供新思路。試驗選取90只35日齡,體重相近的新西蘭白兔,按照雌雄各半的原則隨機分為5組。其中空白組仔兔飼喂基礎日糧,恩諾沙星組、低劑量組、中劑量組和高劑量組分別在基礎日糧中添加0.2%的恩諾沙星粉劑以及0.1%、0.3%、0.5%的加味枳術散粉劑,預飼期7 d,正式試驗14 d。試驗結束后檢測仔兔的腸道屏障完整情況及其抗氧化能力。結果顯示,添加加味枳術散中、高劑量組可以顯著降低腸道的病理組織評分(Plt;0.01)。與空白組相比,其他處理組均顯著升高回腸ZO2(zonula occludens proteins 2)的mRNA表達量(Plt;0.001);高劑量組顯著增加了Occludin、Claudin、ZO1(zonula occludens proteins-1)、ZO2以及JAM2 mRNA的水平(Plt;0.05);加味枳術散顯著增加回腸MUC2蛋白的表達水平(Plt;0.05),且高劑量組顯著降低MPO活性(Plt;0.01);加味枳術散高劑量組可顯著增強回腸sIgA的分泌,降低促炎細胞因子IL-1β、IL-2、IL-6與 TNF-α的水平,提高抗炎細胞因子IL-10與TGF-β的水平;加味枳術散可提高回腸SOD、GSH、CAT的活性和T-AOC。綜上,加味枳術散能夠有效改善斷奶仔兔回腸形態結構、加強腸道細胞間的緊密連接,維持腸黏膜通透性,降低腸道的炎癥反應,增強腸黏膜屏障功能并發揮抗氧化能力,可在替抗使用方面發揮積極作用。
關鍵詞: 仔兔斷奶腹瀉;加味枳術散;腸黏膜屏障;炎癥反應;抗氧化
中圖分類號:S853.74
文獻標志碼:A
文章編號:0366-6964(2024)12-5825-14
doi: 10.11843/j.issn.0366-6964.2024.12.044
開放科學(資源服務)標識碼(OSID):
收稿日期:2023-03-02
作者簡介:
靳茹文(1987-),男,四川達州人,碩士,主要從事獸用中藥對畜禽疾病防治研究和腸靶向制劑開發,E-mail:jingruwen123@163.com;
王英杰(1997-),女,河南淮陽人,碩士生,主要從事獸醫藥理學和毒理學研究,E-mail:1764720963@qq.com;蔣全興(1998-),男,四川德陽人,碩士生,主要從事天然藥物活性研究,E-mail:jiangquanxing27@163.com。靳茹文、王英杰和蔣全興為同等貢獻作者
*通信作者:唐華僑,主要從事獸醫藥理學與毒理學研究,E-mail: turtletang@163.com
Effects of Modified Zhizhu Powder on Intestinal Mucosal Barrier and Antioxidant Capacity
of Weaned Rabbits
JIN" Ruwen1,2, WANG" Yingjie1, JIANG" Quanxing1, LIU" Tianqiang3, DENG Yang4, LUO" Jie5, ZHAO" Ling1, YE" Gang1, SHI" Fei1, LI" Yinglun1, TANG" Huaqiao1*
(1.College of Veterinary Medicine, Sichuan Agricultural University, Chengdu 611130," China;
2. Sichuan Chuanlong Dongke Pharmaceutical Co., Ltd., Chengdu 611230," China;
3.Tongwei Agricultural Development Co., Ltd., Chengdu 610041," China;
4.Chengdu Animal Genetic
Resources Protection Center, Chengdu 610081," China;
5.Tongren Polytechnic College, Tongren
554300," China)
Abstract: The study aimed to investigate the effects of Modified Zhizhu Powder on the ileal intestinal mucosal barrier of weaned rabbits, with the goal of providing new ideas for the prevention and treatment of diarrhea diseases in weaned rabbits. Ninety 35-day-old New Zealand white rabbits, with similar body weights, were randomly divided into 5 groups, based on the principle of 50/50 male and female. Rabbits in control group were fed a basal diet, Enrofloxacin group, low-dose group, medium-dose group and high-dose group were fed the basal diet supplemented with 0.2% Enrofloxacin powder and 0.1%, 0.3% and 0.5% Modified Zhizhu Powder, respectively. The pre-test lasted for 7 days, and the formal test lasted for 14 days. The integrity of the intestinal barrier and its antioxidant capacity were measured after the experiment. The results showed that adding Modified Zhizhu Powder could significantly reduce the intestinal pathological tissue score (Plt;0.05). Compared with the blank group, the other treatment groups all significantly increased the relative expression level of ZO2 (zonula occludens protein 2) mRNA in the ileum (Plt;0.001). The high-dose group significantly increased the mRNA levels of Occludin, claudin, ZO1 (zonula occludens protein 1), ZO2, and JAM2 (junctional adhesion molecule 2) (Plt;0.001). Modified Zhizhu Powder significantly increased the expression of MUC2 (Mucin 2) protein in the ileum (Plt;0.05) and the high-dose group significantly reduced MPO (myeloperoxidase) activity (Plt;0.01). Modified Zhizhu Powder high-doce group could significantly enhance the secretion of sIgA, reduce the levels of pro-inflammatory cytokines IL-1β, IL-2, IL-6, and TNF-α, and increase the levels of anti-inflammatory cytokines IL-10 and TGF-β. Modified Zhizhu Powder could also improve the activity of antioxidant enzymes (SOD, GSH, T-AOC, CAT). In conclusion, the Modified Zhizhu Powder could effectively improve the morphology and structure of the ileum of weaned rabbits, strengthen the tight connection between intestinal cells, maintain the permeability of intestinal mucosa, reduce the inflammatory response of the intestinal tract, enhance the function of the intestinal mucosal barrier, and play an antioxidant role, which can have a positive effect on the use of substitute antibodies.
Key words: weaning diarrhea of young rabbits; Modified Zhizhu Powder; intestinal mucosal barrier; inflammatory response; antioxidation
*Corresponding author: TANG Huaqiao,E-mail: turtletang@163.com
仔兔的繁育被視為養兔生產的基礎以及養兔過程中最為關鍵的飼養管理階段。因此,斷奶初期仔兔的飼養管理和疾病防治尤為重要。消化系統的傳染病目前占所有兔疾病的70%[1]。其中,斷奶腹瀉是早期斷奶仔兔中最常見的一類問題,輕者會導致仔兔生長發育緩慢,體質和免疫力降低;嚴重者將直接造成仔兔的死亡。因此,仔兔斷奶腹瀉的預防成為飼養管理中的重中之重。控制斷奶腹瀉的發生發展被認為是養殖的成功關鍵,其關系到養兔業的持續、健康和穩定發展。
仔兔的腸道器官及其免疫系統要到4~7周齡才能基本發育成熟[2]。在仔兔斷奶初期,由于免疫功能低下、消化道發育不全、飲食變化和環境等因素,仔兔易發生腹瀉等消化道疾病[3]。腹瀉仔兔的腸道屏障受損,腸道上皮細胞遭受細菌的黏附與侵襲[4]。部分細菌和毒素穿過破損的屏障進入體內,影響腸道健康及機體的正常發育[5]。腸黏膜屏障的作用始于腸腔,通過黏膜保護上皮免受機械、化學和酶損傷以及細菌黏附[6]。一旦失去這種保護,免疫系統開始工作,維持腸黏膜的結構和功能,確保消化道消化、吸收等功能的正常發揮[7]。所以,在飼養斷奶仔兔期間,要維護腸黏膜屏障的完整性,提高仔兔的免疫力。由此,保護腸道健康已成為防治仔兔斷奶腹瀉的新策略,這已在一些研究中得到驗證[8-10]。
隨著養殖行業飼料全面禁抗政策的推進,各種中藥替抗產品的開發與應用已成為目前的研究熱點。中獸醫將腹瀉稱為泄瀉[11]。仔兔斷奶腹瀉依據其發生的病因不同共分為三類,即脾虛濕盛型、胃熱積滯型、腸寒濕滯型[12]。此外,仔兔斷奶后與母兔分離,導致情緒不暢,產生焦慮、憤怒等情緒,最終造成肝氣郁結,從而影響仔兔脾胃的消化功能。枳術散,出自龔信的《古今醫鑒》卷六[13]。由枳實、白術二味藥組成。此方健脾消滯,消補并重。早有文獻證明,枳術散具有健胃補脾的作用[14]。臨床常用來治療消化系統疾病和緩解某些疾病出現的胃腸道癥狀[15]。中獸醫將仔兔斷奶腹瀉歸為肝郁脾虛,虛實寒熱錯雜。因此,本研究在枳術散的基礎之上,加上柔肝養陰的白芍和理氣健脾的陳皮,得到“加味枳術散”,共使諸藥可達到疏肝健脾、化濕消食的功效,從而緩解斷奶仔兔消化不良、胃腸不適等問題,進一步保護仔兔腸黏膜屏障的正常發育和完整性,減少腸道疾病的發生。本研究將通過試驗評估加味枳術散對斷奶仔兔腸道功能的改善作用,并通過檢測腸道屏障功能探討其作用機制。
1" 材料與方法
1.1" 試驗動物
試驗選用35日齡,體重 850~900 g的新西蘭""" 白兔90只,雌雄各半,由四川省金堂縣兔場提供。
1.2" 中藥來源及飼料組成
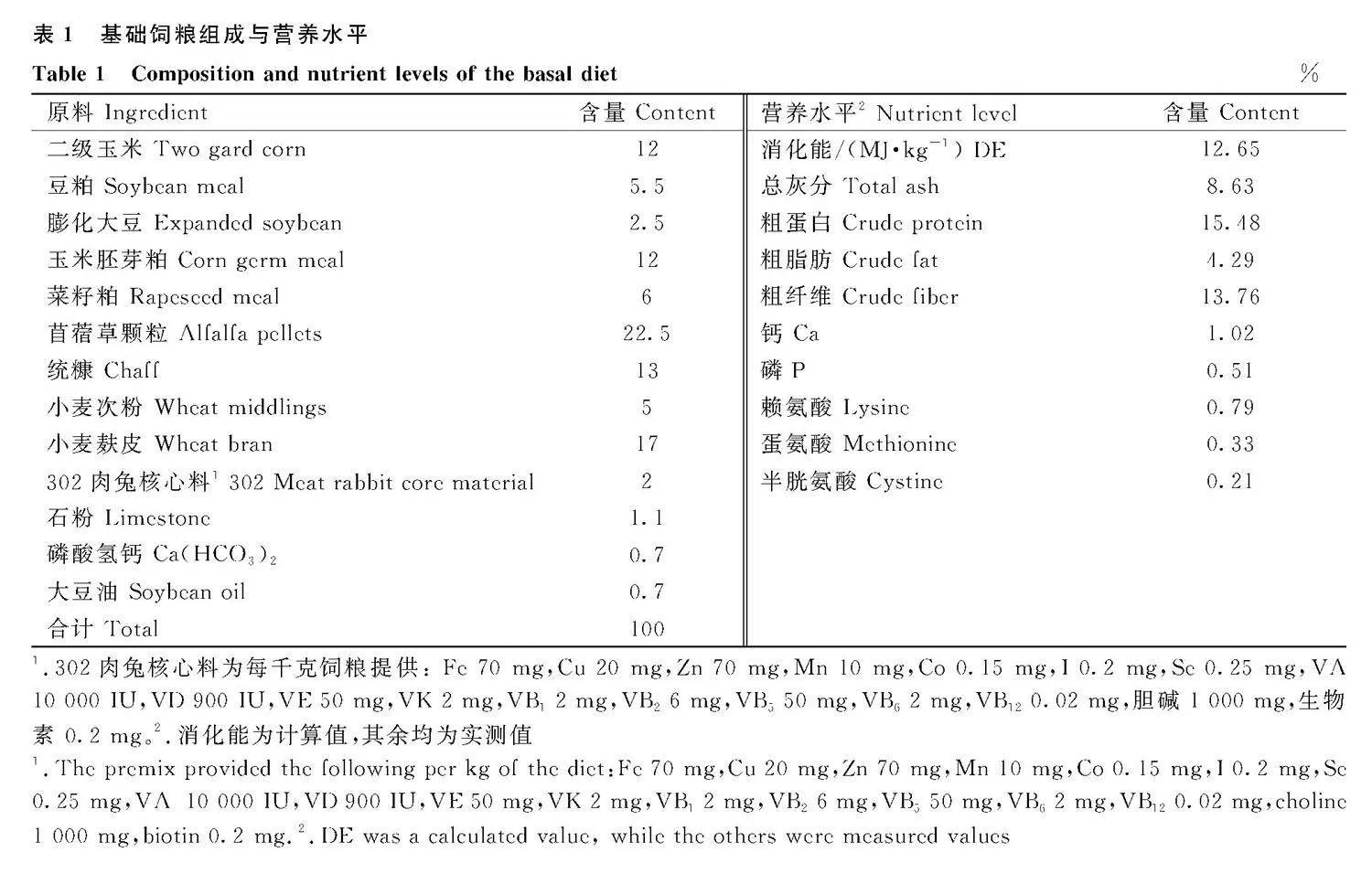
加味枳術散由枳實、白術、白芍、陳皮按照1∶2∶2∶2的比例組成,藥材購自于成都荷花池中藥材市場,經四川農業大學動物醫學院中獸醫教研室鑒定為正品,藥材樣品保存于四川農業大學中獸醫實驗室中。按比例打磨成粗粉后加入基礎飼料中制成顆粒,添加量分別為0.1%、0.3%和0.5%。飼喂斷奶仔兔的基礎飼糧參考兔飼養標準配制[16] ,組成及各組添加成分見表1。
1.3" 主要儀器與設備
主要儀器與設備有:病理切片機(上海徠卡儀器1.302肉兔核心料為每千克飼糧提供The premix provided the following per kg of the diet: Fe 70 mg,Cu 20 mg,Zn 70 mg,Mn 10 mg,Co 0.15 mg,I 0.2 mg,Se 0.25 mg,VA 10 000 IU,VD 900 IU,VE 50 mg,VK 2 mg,VB1 2 mg,VB2 6 mg,VB5 50 mg,VB6 2 mg,VB12 0.02 mg,膽堿 choline 1 000 mg,生物素 biotin 0.2 mg。2.消化能為計算值,其余均為實測值
1.The premix provided the following per kg of the diet:Fe 70 mg,Cu 20 mg,Zn 70 mg,Mn 10 mg,Co 0.15 mg,I 0.2 mg,Se 0.25 mg,VA 10 000 IU,VD 900 IU,VE 50 mg,VK 2 mg,VB1 2 mg,VB2 6 mg,VB5 50 mg,VB6 2 mg,VB12 0.02 mg,choline 1 000 mg,
biotin 0.2 mg.2.DE was a calculated value, while the others were measured values
有限公司,RM2016);正置光學顯微鏡(日本尼康,NIKON Eclipse si);成像系統(日本尼康,NIKON DS-U3);多功能熒光化學發光免疫儀(美國Thermo Scientific公司,Varioskan Flash);伯樂T100 PCR儀(美國Bio-Rad公司,T100);超微量核酸測定蛋白儀(美國Thermo Scientific公司,Nanodrop One);正置熒光顯微鏡(日本尼康,NIKON ECLIPSE TI-SR);高通量熒光PCR儀(上海羅氏診斷產品有限公司,LightCycle 480II)。
1.4" 主要試劑
主要試驗試劑有:一抗ZO1蛋白(江蘇親科生物研究中心有限公司,AF5145);一抗Occludin蛋白(江蘇親科生物研究中心有限公司,DF7504);蘇木素染液套裝(武漢谷歌生物科技有限公司,G1005);熒光二抗(CY3山羊抗兔)(Jackson,111-165-003);DAPI(碧云天,C1002);二抗(HRP標記山羊抗兔鼠通用二抗)(DAKO,K5007);組化試劑盒DAB顯色劑(DAKO,K5007);抗熒光淬滅封片劑(southbiotech,0100-1)。
1.5" 試驗動物分組
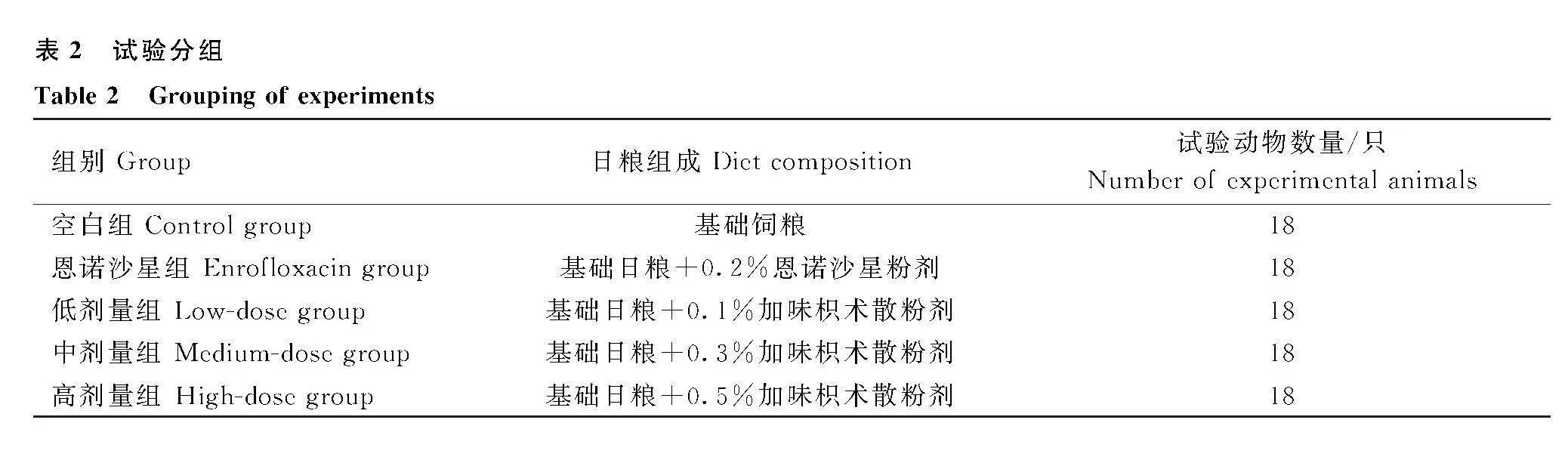
預飼期為斷奶前7 d,飼喂仔兔不含藥物的基礎飼料。正式試驗為斷奶后14 d,將斷奶仔兔按表2分為5個組,分別飼喂不同處理的飼料。
1.6" 樣品的采集與處理
試驗結束時,每個組隨機選取 6 只仔兔,進行采樣。完整分離出回腸,并在兩端結扎,在固定位置的腸段采樣,分離出相應腸段后,剪刀剔除腸段表面的系膜,從同一端將其剪碎后裝入凍存管,標記好組別和腸段名稱。選取一部分腸段泡入4% 多聚甲醛并放室溫保存。最后,將其余樣品放入-80℃保存備用。
1.7" 回腸形態學分析
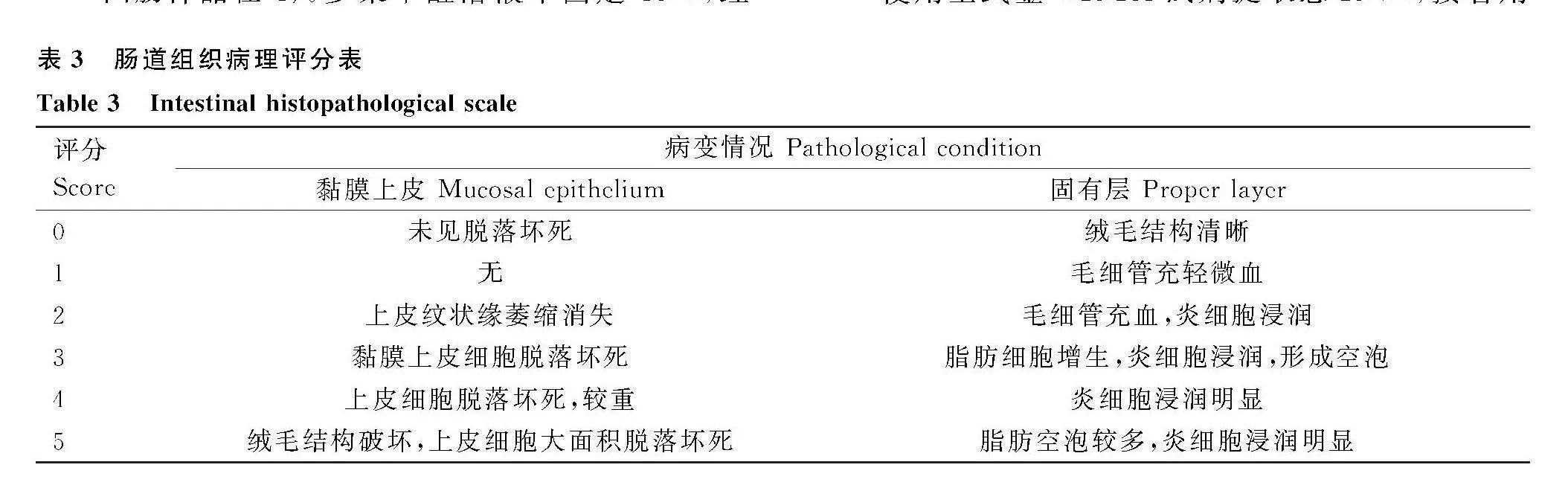
回腸樣品在4%多聚甲醛溶液中固定48 h,經""" 過修塊、脫水、透明和石蠟包埋后,將包埋有樣品的石蠟塊切成5 μm厚的切片,經蘇木精-伊紅染色后晾干,使用倒置顯微鏡對切片進行觀察和分析,擬定病理評分(表3);對腸道組織切片進行拍照,利用ImageJ軟件測量小腸絨毛長度及隱窩深度。垂直測量從隱窩開口到絨毛頂端的距離記為絨毛高度;從隱窩開口至隱窩基部的距離記為隱窩深度,并做好記錄。
1.8" RT-PCR 測定緊密連接蛋白的轉錄水平
使用全式金TRIzol試劑提取總RNA,接著用反轉錄試劑盒將提取的 RNA 迅速反轉錄合成 cDNA,反轉錄的 cDNA 作為模板加入無酶ddH2O稀釋10倍待用,將合成好的10 μmol·L-1的引物(有康生物合成),1∶1取上游引物原液和下游引物原液各50 μL,混勻,熒光定量反應按照如下所示順序在384 孔PCR板中加好樣品,封板膜密封后混勻瞬時離心。
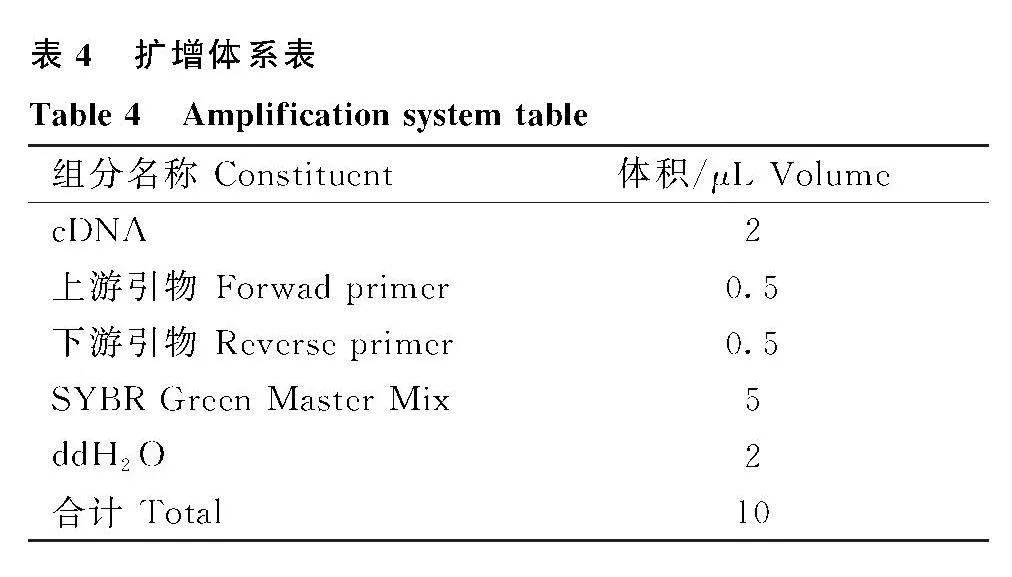
反應條件:95 ℃ 預變性 30 s;95 ℃,5 s,60 ℃,30 s,進行 40次循環;95 ℃,15 s;60 ℃,1 min;95 ℃,15 s。所有樣品做 3 個平行,反應結束后以獲取熔解曲線,觀察數據并分析,擴增體系和RT-PCR引物信息分別見表4、5。
1.9" 免疫熒光檢測ZO1、Occludin蛋白的水平
石蠟切片脫蠟至水,組織切片置于盛滿檸檬酸抗原修復緩沖液(pH6.0)的修復盒中于微波爐內進行抗原修復。用PBS(pH7.4)洗滌3次,每次5 min。在切片上滴加PBS按一定比例配好的一抗,切片平放于濕盒內4℃孵育過夜。用PBS(pH7.4)洗滌3次,每次5 min。切片稍甩干后在圈內滴加與一抗相應種屬的二抗覆蓋組織,避光室溫孵育50min。用PBS(pH7.4)洗滌3次,每次5 min。DAPI復染細胞核,避光室溫孵育10 min。用PBS(pH7.4)洗滌3次,每次5 min。切片稍甩干后用抗熒光淬滅封片劑封片。切片于尼康正置熒光顯微鏡下觀察并采集圖像。
1.10" MPO活性的測定
采用南京建成試劑盒檢測仔兔腸組織中髓過氧化物酶(MPO)的含量,嚴格按照試劑盒說明書進行操作。
1.11" 免疫組織化學法檢測黏蛋白的表達
石蠟切片脫蠟至水,切片用EDTA抗原修復緩沖液(pH8.0)進行抗原修復。與PBS(pH7.4)中洗滌3次,每次5 min。切片放入3%過氧化氫溶液,室溫避光孵育25 min,將玻片置于PBS(pH7.4)中洗滌3次,每次5 min,阻斷內源性過氧化物酶。用3%BSA均勻覆蓋組織,室溫封閉30 min。在切片上滴加PBS按一定比例配好的一抗,4℃孵育過夜。用PBS(pH7.4)洗滌3次,每次5 min。滴加組化試劑盒內與一抗相應種屬的二抗(HRP標記)覆蓋組織,室溫孵育50 min。用PBS(PH7.4)洗滌3次,每次5 min。滴加新鮮配制的DAB顯色液,顯微鏡下控制顯色時間,陽性為棕黃色,自來水沖洗切片終止顯色。Harris蘇木素復染細胞核3 min左右,自來水洗,1%的鹽酸酒精分化數秒,自來水沖洗,氨水返藍,流水沖洗。將切片依次放入75%酒精6 min-85%酒精6 min -無水乙醇Ⅰ6 min -無水乙醇Ⅱ6 min -二甲苯Ⅰ5 min 中脫水透明,將切片從二甲苯拿出來稍晾干,中性樹膠封片。顯微鏡鏡檢,圖像采集分析。
1.12" 腸組織分泌型免疫球蛋白A水平
根據酶聯免疫吸咐試驗 (ELISA) 檢測試劑盒說明書檢測腸黏膜中分泌型免疫球蛋白A (Secreted immunoglobulin A, sIgA)的水平;用石蠟切片免疫組化法檢測回腸組織中sIgA蛋白的相對表達。
1.13" 腸道中氧化應激相關指標水平
取各組仔兔回腸組織,制備成10%組織勻漿,采用博邁德BCA 蛋白濃度檢測試劑盒測定各組仔兔腸組織勻漿蛋白濃度,按南京建成總抗氧化能力(T-AOC)、過氧化氫酶(CAT)、丙二醛(MDA)、還原型谷胱甘肽(GSH)、超氧化物歧化酶(SOD)檢測試劑盒說明書步驟進行各組腸組織氧化應激指標水平的檢測。
1.14" 數據處理與分析
所有數據均用Excel 2013進行初步整理,再用 SPSS25.0 軟件對數據進行 One-way-ANOVA 分析,再用LSD法進行多重比較,并繪圖。試驗結果以“平均數±標準誤(x-±SEM)” 表示,Plt;0.05表示顯著差異,Plt;0.01表示極顯著差異。
2" 結" 果
2.1" 回腸形態學分析結果
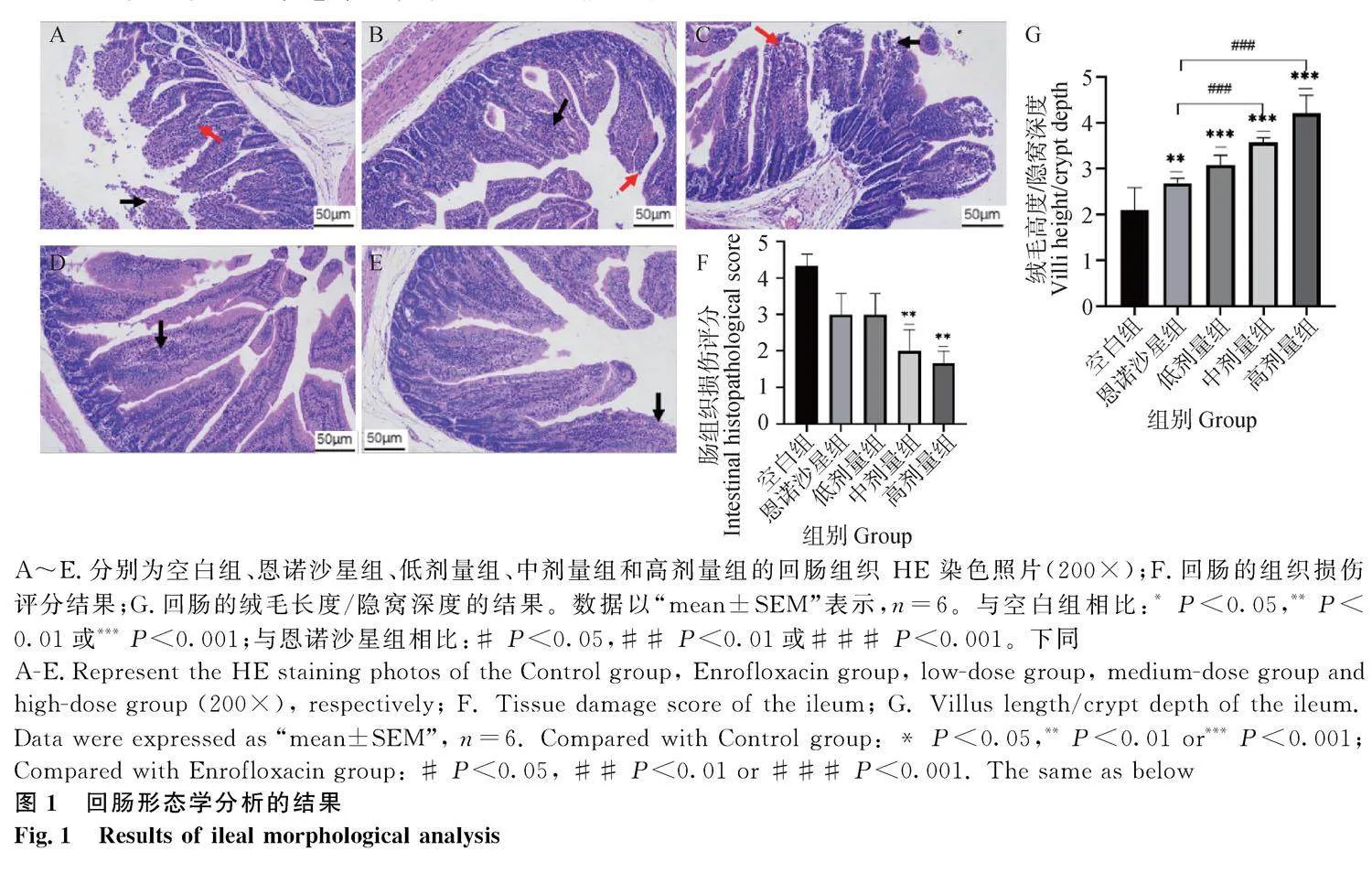
回腸形態學HE染色結果如圖1A~1E所示。""" 圖1A顯示,仔兔腸絨毛結構破壞,上皮細胞大量脫落壞死,碎屑聚集腸腔(黑色箭頭所示);固有層炎細胞浸潤(紅色箭頭所示)。圖1B顯示,固有層毛細管擴張充血,伴有炎細胞浸潤(黑色箭頭所示);上皮紋狀緣消失,部分上皮細胞脫落(紅色箭頭所示)。圖1C可見腸絨毛上皮脫落壞死(黑色箭頭所示);固有層毛細管擴張充血伴有炎細胞浸潤(紅色箭頭所示)。圖1D可觀察到,腸絨毛結構完整,固有層炎細胞浸潤,輕微(黑色箭頭所示)。圖1E則可見上皮紋狀緣萎縮消失,輕微(黑色箭頭所示);其他未見明顯病變。
回腸的組織損傷評分結果如圖1F所示。結果表明,加味枳術散可顯著改善回腸的損傷,減輕腸道損傷程度。與空白組相比,中、高劑量組的仔兔回腸病理學評分呈極顯著降低(Plt;0.01)。
回腸的絨毛長度/隱窩深度的結果如圖1G所示,與空白組相比,低、中、高劑量組的小腸絨毛長度/隱窩深度的比值都極顯著增加(Plt;0.001),恩諾沙星組小腸的絨毛長度/隱窩深度的比值極顯著的大于空白組(Plt;0.01)。與恩諾沙星組相比,中、高劑量組的小腸絨毛長度/隱窩深度的比值均極顯著的增加(Plt;0.001)。
2.2" 回腸緊密連接蛋白的表達水平
回腸緊密連接蛋白的基因表達水平結果如圖2A~2E所示。由圖2A、2D、2E可知,與空白組相比,中、高劑量組處理組空腸ZO1、Occludin和 JAM2 mRNA的相對表達量均高于空白組顯著升高(Plt;0.05),其中,中、高劑量組空腸Occludin mRNA 和JAM2 mRNA的相對表達量極顯著的上升(Plt;0.05);由圖2B可知,處理組的ZO2 mRNA的相對表達量都極顯著的高于空白組(Plt;0.001);由圖2C可知,與空白組相比,各處理組空腸Claudin mRNA的相對表達量均高于空白組,其中,除了且高劑量組和空白組相比顯著上調(Plt;0.05),其他組均無顯著性(Pgt;0.05)。與恩諾沙星組相比,各水平加味枳術散處理可顯著上調ZO2 mRNA的相對表達量(Plt;0.001)。
回腸緊密連接蛋白的蛋白表達水平結果如圖2F~2G所示。由圖2F可知,與空白組相比,各處理組仔兔的回腸中ZO1的蛋白表達量均顯著升高(Plt;0.01),與恩諾沙星組相比,中、高劑量加味枳術散處理組的回腸中ZO1的蛋白表達量顯著升高(Plt;0.01);由圖2G可知,與空白組相比,加味枳術散處理組仔兔的回腸中Occludin的蛋白表達量均極顯著升高(Plt;0.001),且均極顯著高于恩諾沙星組,加味枳術散處理組仔兔的回腸中Occludin的蛋白表達量也均顯著升高(Plt;0.001)。
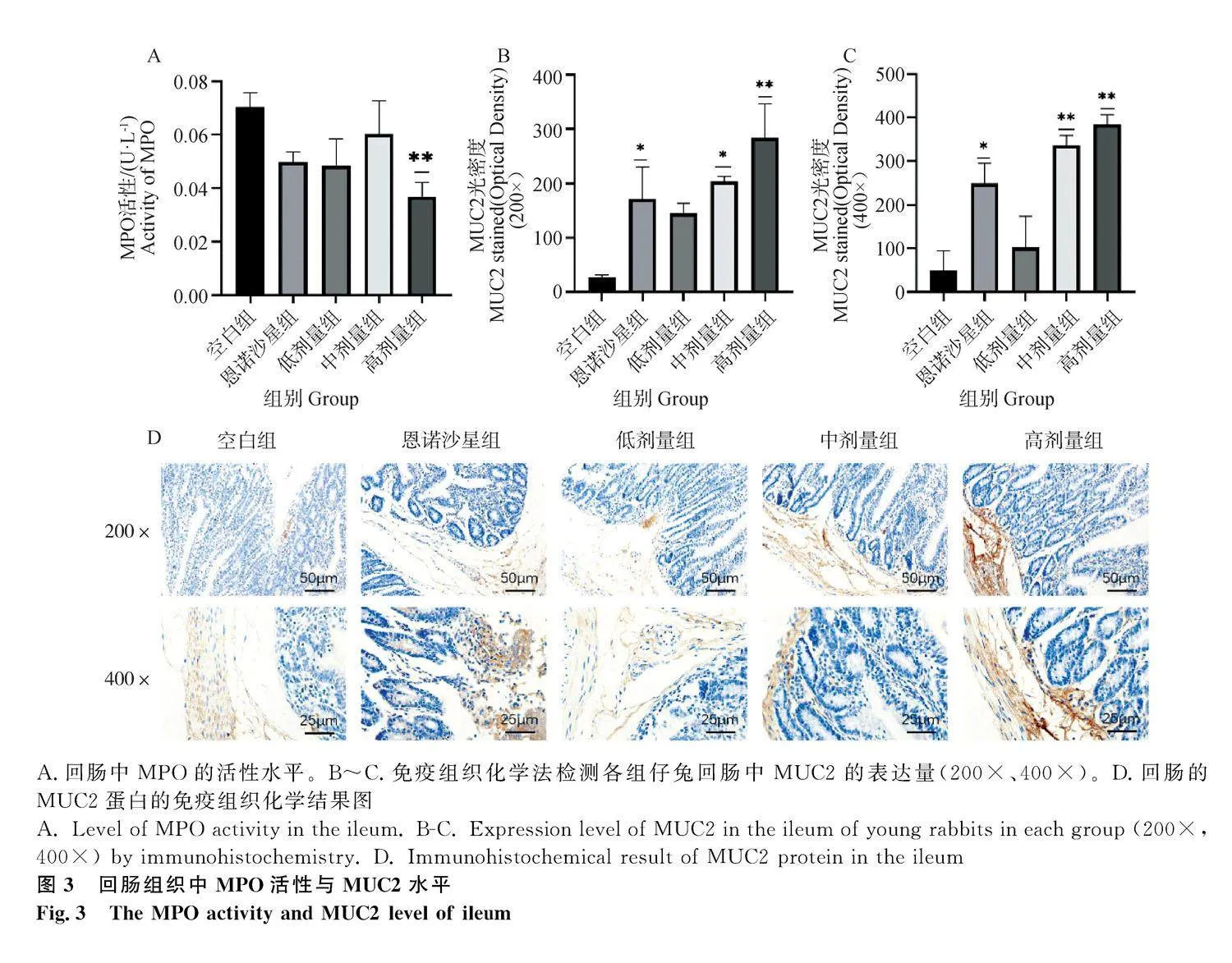
2.3" 回腸組織中MPO與MUC2的水平
回腸中MPO的活性水平結果如圖3A所示,與空白組相比,不同處理組的回腸中 MPO 的活性均降低,其中,高劑量組的MPO活性與空白組相比呈現極顯著降低(Plt;0.01)。回腸中MUC2蛋白的表達量結果如圖3B、3C所示,空白組和各處理組回腸黏膜表面均有MUC2蛋白的表達,與空白組相比,中、高劑量組腸道黏膜表面MUC2的表達量顯著增高(Plt;0.05)。
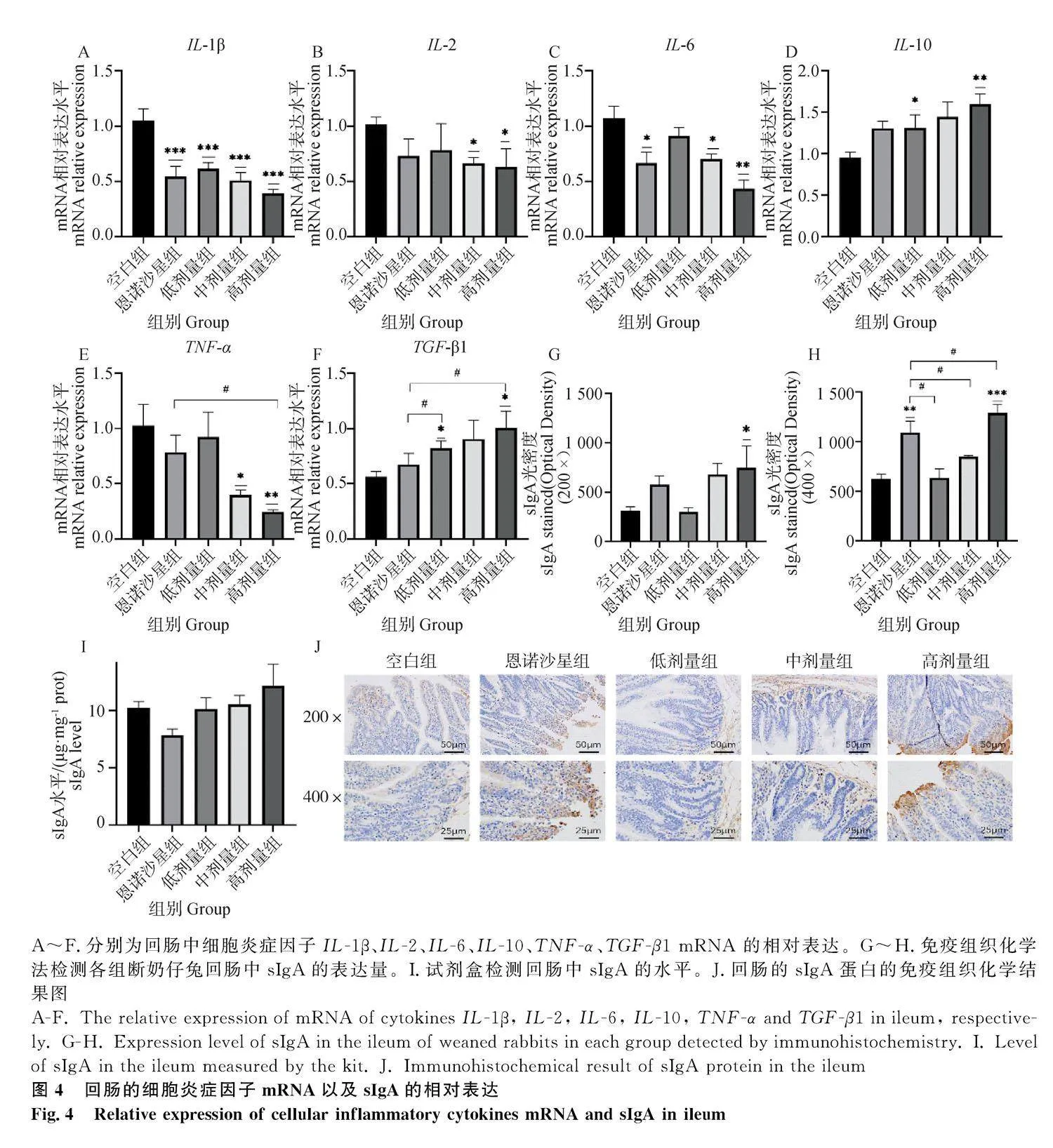
2.4" 回腸中細胞炎癥因子與sIgA的水平
回腸中細胞炎癥因子的mRNA水平如圖4A~4F所示。由圖4A可知,加味枳術散處理組和恩諾沙星組均極顯著的抑制IL-1β mRNA的表達量(Plt;0.001);由圖4B可知,處理組均可以抑制IL-2 mRNA的表達量,其中,中、高劑量組呈現顯著性顯著抑制IL-2 mRNA的表達(Plt;0.05,Plt;0.01);由圖 4C、4E可知,加味枳術散處理組以劑量依賴的方式抑制IL-6和TNF-α mRNA的表達,其中,與空白組相比,中、高劑量組呈現顯著性差異(Plt;0.05,Plt;0.01);由圖4D可知,加味枳術散處理組以劑量依賴的方式促進IL-10 mRNA的表達,其中,低、高劑量組呈現顯著性差異(Plt;0.05,Plt;0.01);由圖4F可知,加味枳術散處理組以劑量依賴的方式促進TGF-β1 mRNA的表達,其中,與空白組相比,低、高劑量組均呈現差異顯著(Plt;0.05),且與恩諾沙星組相比,低、高劑量組均呈現顯著高于恩諾沙星組(Plt;0.05)。回腸中sIgA的表達量如圖4G~4I所示。高劑量組顯著促進回腸sIgA蛋白表達(Plt;0.05)。
2.5" 腸道中氧化應激相關指標的水平
由圖5A、5B可知,飼料中糧添加加味枳術散可以提高SOD 的活性,降低MDA 的水平,除高劑量組SOD 的水平呈現顯著差異外(Plt;0.05),其他均無顯著性(Pgt;0.05);由圖5C可知,與空白組相比,加味枳術散處理組可提高GSH 的水平,中、高劑量組極顯著提高GSH 的水平活性(Plt;0.001),與恩諾沙星組相比,加味枳術散處理組均極顯著提高GSH 的活性(Plt;0.001);由圖5D、E可知,飼料中添加加味枳術散高劑量組還可以顯著提高了T-AOC 和 CAT 的活性(Plt;0.05)。
3" 討" 論
本研究旨在評估加味枳術散對飼喂無抗生素日糧的斷奶仔兔的腸道形態、腸屏障功能以及抗氧化能力的影響。本研究的初衷和重點是為斷奶仔兔尋找抗生素替代品。飼料中添加抗生素能夠保護仔兔的腸道形態及功能的正常發育,本研究選擇恩諾沙星粉劑作為陽性藥,與各加味枳術散處理組的效果作對比,在符合廣泛認可的標準對照的添加效應前提下,為斷奶仔兔尋找抗生素替代品提供參考。
3.1" 加味枳術散對斷奶仔兔腸道機械屏障的影響
眾所周知,保持腸道屏障的完整性和功能對人類和動物的健康至關重要[17]。未成熟的腸道黏膜容易產生結構性的損害,病原體和毒素就可以穿過腸道壁進入機體,引起腹瀉等癥狀。腸絨毛形態及變化可以評估腸道黏膜結構的變化。黃鵬彭婧等[18]研究發現,一定劑量的板藍根多糖可以保護仔鼠小腸黏膜結構的完整性,進而促進營養物質的吸收。本研究應用常規石蠟切片,進行HE染色,觀察仔兔回腸組織黏膜結構,測量其絨毛高度、隱窩深度、絨毛高度/隱窩深度值來研究添加不同水平的加味枳術散對斷奶仔兔回腸黏膜結構的影響。從石蠟切片結果可看出,加味枳術散可以保護仔兔回腸黏膜的結構,抑制炎癥的發生,顯著降低腸道的病理組織評分。與恩諾沙星組相比,日糧添加0.3%、0.5%加味枳術散均能顯著減輕腸道的病變,其保護效果顯著。
緊密連接是維持腸道機械屏障完整性的重要組成部分。緊密連接復合體位于上皮細胞周圍頂端,由跨膜蛋白咬合蛋白(Occludin),閉合蛋白(Claudins),連接黏附分子(JAM)以及胞漿蛋白帶狀閉合蛋白家族(ZO1、ZO2、ZO3)等組成[19-20] 。維持完整的腸上皮細胞緊密連接對保護腸屏障功能、防止細菌移位及毒性大分子進入機體有重要意義。已有的研究顯示,白術可通過上調Occludin、Claudin-1緊密連接蛋白的表達起到對大鼠腸道機械屏障的保護作用[21];白術還可通過顯著上調小腸Claudin-l,Occludin和ZO1的緊密連接蛋白的表達水平,從而修復仔鼠受損的腸黏膜[22]。
本研究通過使用RT-PCR方法和免疫熒光法,評估了加味枳術散對回腸的腸上皮細胞完整性和通透性的保護效果。結果顯示,加味枳術散可顯著提高ZO1的蛋白表達水平。其中,高劑量的加味枳術散可顯著上調回腸Occludin、Claudin、ZO1、ZO2以及JAM2 mRNA的水平,加強腸道細胞間的緊密連接,阻止毒素進入體內,抑制腸炎的發展。
3.2" 加味枳術散對斷奶仔兔腸道化學屏障的影響
腸道化學屏障由腸道分泌物和腸道有益菌群等共同形成。腸道分泌的消化液可以清潔腸腔[23],部分化學物質可以破壞細菌的細胞膜、細胞壁或酶等,從而抵御病原菌的入侵[24]。
合成腸道黏液的主要黏蛋白基因是MUC2和MUC3基因,MUC2主要由腸道杯狀細胞分泌[25]。黏蛋白的組成和降解的變化可以改變細菌對黏膜的黏附[26]。Heczko等[27]研究證實,黏蛋白可以抑制病原體對腸細胞的附著,從而保護胃腸道免受病原體的侵害。嚴重的仔兔斷奶腹瀉會繼發腸炎。既往研究表明,耶爾森氏菌引發的兔的結腸炎會顯著增加回腸末端和結腸近端黏蛋白的產生[28]。本研究通過免疫組織化學法檢測了回腸的MUC2蛋白的水平。結果顯示,加味枳術散可通過顯著增加MUC2蛋白的表達來減少有害菌對回腸黏膜的黏附,從而保護腸道化學屏障。這與朱春洋等[29]的研究結果相似,杯狀細胞數量的增多和MUC2的表達的升高能夠改善十二指腸的化學屏障,治療功能性消化不良。
另外,MPO活性的調節對腸道化學屏障具有兩面性。一方面,MPO通過氧化膽堿和亞硝酸鹽等方式破壞腸道化學屏障,使得腸道內的細菌和毒素等物質穿過腸道壁進入血液,引發炎癥和疾病[30]。另一方面,腸道內的某些益生菌可以調節MPO的活性和分泌,減輕腸道炎癥,恢復腸道化學屏障的功能,從而維持腸道的健康[31]。因此,MPO與腸道化學屏障之間存在著密切的關系,其作用機制還需進一步的研究。本研究結果顯示,高劑量的加味枳術散可顯著降低MPO的活性。綜合分析,在疾病和病理狀態下,抑制MPO的活性成為一個可行的手段[32]。
3.3" 加味枳術散對斷奶仔兔腸道免疫屏障的影響
體內的非特異性免疫與特異性免疫相互協同[33]。斷奶前,仔兔主要通過母兔的Ig傳遞產生被動免疫[34]。這種保護推遲了其自身主動反應的建立。
在特異性免疫中,免疫球蛋白A(IgA)是腸道分泌的主要免疫球蛋白類型[35]。IgA進入腸腔后不會激活補體或炎癥反應,這使它們成為保護黏膜表面的理想選擇[36]。血清型IgA與分泌型IgA(sIgA)的免疫功能不同,sIgA對管腔內的蛋白分解具有抵抗力[37]。sIgA能夠保護上皮細胞免受腸道毒素和病原微生物的侵害[38]。有研究指出,腸道內高水平的sIgA有助于修復損傷的黏膜免疫組織[39]。此外,sIgA還能通過選擇性黏附在腸道細胞上,從而在免疫屏障中發揮作用[40]。腸道微生物群,腸道細胞因子和營養素都參與腸道中sIgA的產生[41-42]。
在腸道中,炎癥反應作為一種免疫應答能夠抵御有害的微生物和其他外部刺激物質[43]。但是,當炎癥反應過度或長期存在時,它可以促進腸道上皮細胞的凋亡與脫落,破壞腸道黏膜屏障和免疫屏障的完整性[44]。此外,炎癥反應過程中,過度激活的免疫細胞和炎性細胞因子會進一步加劇腸道免疫屏障的損傷[45]。腸道的屏障損傷與腸道炎癥發生關系密切,各種原因誘發的動物腸道屏障損傷都有可能使腸道發生炎癥。為評估斷奶仔兔的腸道免疫水平以及腸道炎癥水平,本研究檢測了回腸的sIgA的蛋白水平,并利用 RT-PCR方法檢測回腸中IL-1β、IL-2、IL-6、IL-10、TNF-α、TGF-β1 mRNA 的相對表達,結果顯示,加味枳術散可顯著促進腸道內sIgA的分泌;通過RT-PCR檢測方法,發現3個劑量的加味枳術散均可顯著降低IL-1β的水平,中、高劑量組可顯著降低促炎細胞因子IL-1β、IL-2、IL-6與 TNF-α的水平,降低腸道的炎癥水平。
3.4" 加味枳術散對斷奶仔兔回腸抗氧化能力的影響
氧化應激是與炎癥緊密相關的伴隨反應,抗氧化能力能夠反映機體的健康狀況,機體內的氧化-抗氧化系統共同參與調節自由基的生長與消除,抗氧化酶具有較強清除體內自由基的活性作用[46]。在炎癥過程中,機體易出現氧化-抗氧化系統的失衡[47]。抗氧化酶GSH、SOD和CAT是抗氧化系統中的重要的組成部分[48]。為了抑制氧自由基的積聚,SOD將超氧陰離子催化為過氧化氫,進一步抑制超氧陰離子對細胞造成損傷[49]。大量過氧化氫會破壞組織細胞,CAT能將過氧化氫催化為水和氧氣[50],減輕機體損傷。T-AOC 表示機體總抗氧化能力,MDA 含量直接決定機體脂質過氧化程度,是機體評價脂質氧化損傷的重要指標,同時也可間接反映腸黏膜細胞的損傷程度[51]。因此,本研究通過檢測腸道的氧化應激水平來評估仔兔腸道的抗氧化能力,結果發現,加味枳術散主要通過提高抗氧化酶的活性(SOD、GSH、CAT),維持腸道的正常機能。
4" 結" 論
本研究發現,加味枳術散能夠有效改善斷奶仔兔回腸的形態結構、加強腸道細胞間的緊密連接,維持腸黏膜的通透性,降低腸道的炎癥水平和氧化水平,保護斷奶仔兔的腸道健康。0.3%和0.5%的加味枳術散均對腸道有不同程度的腸道保護功效,但在使用傳統中藥進行治療時,還需要綜合考慮仔兔的身體狀況、病情嚴重程度等。本研究結果有助于在生產上權衡中藥的使用量和療效時作參考。
參考文獻(References):
[1]" CARABAO R,BADIOLA I,CHAMORRO S,et al.New trends in rabbit feeding:Influence of nutrition on intestinal health[J].Span J Agric Res,2008,6(S1):15-25.
[2]" 李亞力.乳酸菌對幼齡獺兔生產性能與免疫性能的影響[D].楊凌:西北農林科技大學,2013.
LI Y L.Effects of lactic acid bacteria on growth performance and immune capability of juvenile rabbits[D].Yangling:Northwest Aamp;F University,2013.(in Chinese)
[3]" CAMPBELL J M,CRENSHAW J D,POLO J.The biological stress of early weaned piglets[J].J Anim Sci Biotechnol,2013,4(1):19.
[4]" CHEN H,HU H Y,CHEN D W,et al.Dietary pectic oligosaccharide administration improves growth performance and immunity in weaned pigs infected by rotavirus[J].J Agric Food Chem,2017,65(14):2923-2929.
[5]" WU Y, TANG L, WANG B,et al.The role of autophagy in maintaining intestinal mucosal barrier[J]. J Cell Physiol. 2019;234(11):19406-19419.
[6]" MARTENS E C,NEUMANN M,DESAI M S.Interactions of commensal and pathogenic microorganisms with the intestinal mucosal barrier[J].Nat Rev Microbiol,2018,16(8):457-470.
[7]" GUSTAFSSON J K,JOHANSSON M E V.The role of goblet cells and mucus in intestinal homeostasis[J].Nat Rev Gastroenterol Hepatol,2022,19(12):785-803.
[8]" XU Q Q,JIAN H F,ZHAO W Y,et al.Early weaning stress induces intestinal microbiota disturbance,mucosal barrier dysfunction and inflammation response activation in pigeon squabs[J].Front Microbiol,2022,13:877866.
[9]" WEN Z S,DU M,TANG Z,et al.Low molecular seleno-aminopolysaccharides protect the intestinal mucosal barrier of rats under weaning stress[J].Int J Mol Sci,2019,20(22):5727.
[10]" WESTRM B,ARVALO SUREDA E,PIERZYNOWSKA K,et al.The immature gut barrier and its importance in establishing immunity in newborn mammals[J].Front Immunol,2020,11:1153.
[11]" 中華中醫藥學會脾胃病分會.泄瀉中醫診療專家共識意見(2017)[J].中醫雜志,2017,58(14):1256-1260.
Spleen and Stomach Disease Branch of the Chinese Association of Traditional Chinese Medicine.Consensus opinion of experts on diagnosis and treatment of diarrhea in traditional Chinese medicine (2017)[J].Journal of Traditional Chinese Medicine,2017,58(14):1256-1260.(in Chinese)
[12]" 薛" 輝,王慶其.結合運氣學說辨治泄瀉證及醫案剖析[J].中國中醫基礎醫學雜志,2010,16(2):103-104.
XUE H,WANG Q Q.Diagnosis and treatment combined with Yun-Qi theory and analysis of medical records of diarrhea[J].Chinese Journal of Basic Medicine in Traditional Chinese Medicine,2010,16(2):103-104.(in Chinese)
[13]" 史" 焱,李" 君,傅海燕.《醫學匯函》引用《古今醫鑒》版本考[J].中國中醫基礎醫學雜志,2016,22(5):602-606.
SHI Y,LI J,FU H Y.Edition reference of Yi Xue Han Hui quoting Gu Jin Yi Jian[J].Chinese Journal of Basic Medicine in Traditional Chinese Medicine,2016,22(5):602-606.(in Chinese)
[14]" 楊東亮,趙翠苗.枳術散熱敷腹部治療結腸癌術后胃腸功能紊亂臨床觀察[J].中醫臨床研究,2016,8(5):73-74.
YANG D L,ZHAO C M.Clinical observation on treating cladding gastrointestinal dysfunction after abdominal surgery colon cancer[J].Clinical Journal of Chinese Medicine,2016,8(5):73-74.(in Chinese)
[15]" 張均華.橘皮枳術散加減預防犢泄瀉[J].中獸醫學雜志,1986(4):49.
ZHANG J H.Modified orange peel Zhizhu powder to prevent calf diarrhea[J].Chinese Journal of Traditional Veterinary Science,1986(4):49.(in Chinese)
[16]" 李桂甫.肉兔飼料及飼養規范探討[J].中國養兔,2019(2):43-44.
LI G F.Discussion on meat rabbit feed and feeding norms[J].Chinese Journal of Rabbit Farming,2019(2):43-44.(in Chinese)
[17]" ZENG Y D,WANG Z R,ZOU T D,et al.Bacteriophage as an alternative to antibiotics promotes growth performance by regulating intestinal inflammation,intestinal barrier function and gut microbiota in weaned piglets[J].Front Vet Sci,2021,8:623899.
[18]" 彭" 婧,肖傳斌,王春秀.板藍根多糖對少乳仔鼠空腸形態的影響[J].養殖與飼料,2021,20(9):47-50.
PENG J,XIAO C B,WANG C X.Effects of Isatis indigotica polysaccharide on the morphology of jejunum in young mice[J].Animals Breeding and Feed,2021,20(9):47-50.(in Chinese)
[19]" BEUTEL O,MARASPINI R,POMBO-GARCA K,et al.Phase separation of zonula Occludens proteins drives formation of tight junctions[J].Cell,2019,179(4):923-936.e11.
[20]" JIN Y H,ZHAI Z A,JIA H,et al.Kaempferol attenuates diquat-induced oxidative damage and apoptosis in intestinal porcine epithelial cells[J].Food Funct,2021,12(15):6889-6899.
[21]" 許" 露,張" 曼,錢" 凱,等.白術/防風藥對對Caco-2細胞屏障功能的協同保護作用及機制研究[J].河南醫學研究,2018,27(5):769-772.
XU L,ZHANG M,QIAN K,et al.Study of the synergistic effects of Atractylodes macrocephala and Saposhnikovia divaricate on Caco-2 cell and it′s mechanism[J].Henan Medical Research,2018,27(5):769-772.(in Chinese)
[22]" 孫必強,周" 英,劉衛東,等.不同劑型七味白術散對腹瀉小鼠腸道菌群失調和腸粘膜緊密連接蛋白的影響[J].時珍國醫國藥,2015,26(12):2835-2837.
SUN B Q,ZHOU Y,LIU W D,et al.Effects of different formulated Qiwei Baizhu powder on intestinal flora and tight junction protein in diarrhea mice[J].Lishizhen Medicine and Materia Medica Research,2015,26(12):2835-2837.(in Chinese)
[23]" 胡紅蓮,高" 民.腸道屏障功能及其評價指標的研究進展[J].中國畜牧雜志,2012,48(17):78-82.
HU H L,GAO M.Research advance in intestinal barrier function and evaluation index[J].Chinese Journal of Animal Science,2012,48(17):78-82.(in Chinese)
[24]" CHELAKKOT C,GHIM J,RYU S H.Mechanisms regulating intestinal barrier integrity and its pathological implications[J].Exp Mol Med,2018,50(8):1-9.
[25]" 汪榮泉,房殿春,羅元輝,等.消化道癌患者胃腸道粘膜中MUC2和MUC3基因的表達[J].基礎醫學與臨床,2000,20(5):421-424.
WANG R Q,FANG D C,LUO Y H,et al.Expression of MUC2 and UUC3 genes in the gastrointestinal mucosas of patients suffered from gastrointestinal neoplasms[J].Basic and Clinical Medicine,2000,20(5):421-424.(in Chinese)
[26]" MANTLE M,HUSAR S D.Binding of Yersinia enterocolitica to purified,native small intestinal mucins from rabbits and humans involves interactions with the mucin carbohydrate moiety[J].Infect Immun,1994,62(4):1219-1227.
[27]" HECZKO U,ABE A,FINLAY B B.In vivo interactions of rabbit enteropathogenic Escherichia coli O103 with its host:an electron microscopic and histopathologic study[J].Microbes Infect,2000,2(1):5-16.
[28] "MANTLE M,BASARABA L,PEACOCK S C,et al.Binding of Yersinia enterocolitica to rabbit intestinal brush border membranes,mucus,and mucin[J].Infect Immun,1989,57(11):3292-3299.
[29]" 朱春洋,趙魯卿,趙靜怡,等.四逆散對FD大鼠十二指腸杯狀細胞及MUC2的影響[J].世界中醫藥,2020,15(11):1575-1578,1584.
ZHU C Y,ZHAO L Q,ZHAO J Y,et al.Effects of Sini powder on duodenum goblet cells and MUC2[J].World Chinese Medicine,2020,15(11):1575-1578,1584.(in Chinese)
[30]" NDREPEPA G.Myeloperoxidase-A bridge linking inflammation and oxidative stress with cardiovascular disease[J].Clin Chim Acta,2019,493:36-51.
[31]" CAO Z H,CHENG G J.Recombinant myeloperoxidase as a new class of antimicrobial agents[J].Microbiol Spectr,2022,10(1):e0052221.
[32]" SIRAKI A G.The many roles of myeloperoxidase:from inflammation and immunity to biomarkers,drug metabolism and drug discovery[J].Redox Biol,2021,46:102109.
[33]" AGRAWAL B.Heterologous immunity:role in natural and vaccine-induced resistance to infections[J].Front Immunol,2019,10:2631.
[34]" WISE R D,LICHTER E A,DRAY S.Presence in rabbit colostrum of IgA autoantibodies to a gastric antigen[J].J Immunol,1971,107(1):47-55.
[35]" LAMM M E.Interaction of antigens and antibodies at mucosal surfaces[J].Annu Rev Microbiol,1997,51:311-340.
[36]" YANG Y,PALM" N W.Immunoglobulin A and the microbiome[J].Curr Opin Microbiol,2020,56:89-96.
[37]" DE FAYS C,CARLIER F M,GOHY S,et al.Secretory immunoglobulin a immunity in chronic obstructive respiratory diseases[J].Cells,2022,11(8):1324.
[38]" CORTHESY B.Multi-faceted functions of secretory IgA at mucosal surfaces[J].Front Immunol,2013,4:185.
[39]" 孫必強,伍參榮,周" 英,等.不同劑型七味白術散對腸道菌群失調小鼠小腸黏膜超微結構和sIgA的影響[J].中國微生態學雜志,2016,28(2):125-1288,137.
SUN B Q,WU C R,ZHOU Y,et al.Effects of different formulations of Qiwei Baizhu powder on the ultrastructure of small intestinal mucosa and sIgA in mice with intestinal dysbacteriosis[J].Chinese Journal of Microecology,2016,28(2):125-128,137.(in Chinese)
[40]" BRANCA J J V,GULISANO M,NICOLETTI C.Intestinal epithelial barrier functions in ageing[J].Ageing Res Rev,2019,54:100938.
[41]" 韓" 渤,劉玥宏,仇志強,等.SIgA表達功能及其在腸道疾病的作用[J].世界華人消化雜志,2017,25(19):1757-1763.
HAN B,LIU Y H,QIU Z Q,et al.Secretory immunoglobulin A and intestinal diseases[J].World""" Chinese Journal of Digestology,2017,25(19):1757-1763.(in Chinese)
[42]" 羅治彬.腸道粘膜SIgA免疫系統的研究進展[J].細胞與分子免疫學雜志,1997,13(S2):38-41.
LUO Z B.Research progress of intestinal mucosal SIgA immune system[J].Journal of Cellular and Molecular Immunology,1997,13(S2):38-41.(in Chinese)
[43]" FIORANELLI M,ROCCIA M G,FLAVIN D,et al.Regulation of inflammatory reaction in health and disease[J].Int J Mol Sci,2021,22(10):5277.
[44]" MALOY K J,POWRIE F.Intestinal homeostasis and its breakdown in inflammatory bowel disease[J].Nature,2011,474(7351):298-306.
[45]" BURGE K,GUNASEKARAN A,ECKERT J,et al.Curcumin and intestinal inflammatory diseases:molecular mechanisms of protection[J].Int J Mol Sci,2019,20(8):1912.
[46]" NIKI E.Assessment of antioxidant capacity in vitro and in vivo[J].Free Radical Biol Med,2010,49(4):503-515.
[47]" 王柏森.綠原酸通過抑制TLR4/MAPK/NFκB通路激活自噬抑制炎癥和氧化應激[D].長春:吉林大學,2021.
WANG B S.Chlorogenic acid inhibits inflammation and oxidative stress by inhibiting TLR4/MAPK/NFκB pathway and activating autophagy[D].Changchun:Jilin University,2021.(in Chinese)
[48]" OLSVIK P A,KRISTENSEN T,WAAGBR,et al.mRNA expression of antioxidant enzymes (SOD,CAT and GSH-Px) and lipid peroxidative stress in liver of Atlantic salmon (Salmo salar) exposed to hyperoxic water during smoltification[J].Comp Biochem Physiol C Toxicol Pharmacol,2005,141(3):314-323.
[49]" SAKAMOTO T,IMAI H.Hydrogen peroxide produced by superoxide dismutase SOD-2 activates sperm in Caenorhabditis elegans[J].J Biol Chem,2017,292(36):14804-14813.
[50]" GOYAL M M,BASAK A.Human catalase:looking for complete identity[J].Protein Cell,2010,1(10):888-897.
[51]" TANG Q,SU Y W,XIAN C J.Determining oxidative damage by lipid peroxidation assay in rat serum[J].Bio Protoc,2019,9(12):e3263.
(編輯" 范子娟)

