SMAD2、SMAD3 和SMAD4 基因在小尾寒羊卵巢活動中的功能分析


摘要:為探究SMAD 基因家族重要成員SMAD2、SMAD3 和SMAD4 基因在小尾寒羊繁殖活動中的生物學功能,利用生物信息學技術對SMAD2、SMAD3 和SMAD4 基因的蛋白理化性質、親疏水性和亞細胞定位進行分析,并對其二級結構、蛋白互作進行預測及GO(gene ontology)和KEGG(kyoto encyclopedia of genes and genomes)的富集分析;然后以小尾寒羊為研究對象,通過免疫組織化學染色(immunohistochemistry,IHC)確定SMAD2、SMAD3和SMAD4蛋白在卵巢組織中的表達,利用實時熒光定量PCR(real-time quantitative PCR,RT-qPCR)和蛋白免疫印跡(western blot,WB)方法測定SMAD2、SMAD3 和SMAD4 基因mRNA及其編碼蛋白在不同生理階段卵巢組織和不同直徑卵泡中表達水平。結果顯示,SMAD2、SMAD3和SMAD4蛋白為親水性蛋白,理論等電點分別為6.67、6.73和6.50,在不同生理階段卵巢組織中的陽性表達主要位于卵母細胞、卵泡膜細胞和顆粒細胞,且二級結構中α螺旋和無規則卷曲的占比較高,其蛋白與FOXH1、ACVR1B、SMAD1、TGFβR1、TGFβR2、ZFYVE9、SKI、SKIL、TGIF1 和ENSOARP0000001869 蛋白存在互作關系。SMAD2、SMAD3 和SMAD4 基因在TGF-β受體信號通路、TGF-β受體結合、TGF-β激活受體活性中發揮生物學功能,且在TGF-β信號通路富集。SMAD2和SMAD4蛋白在撤栓后42 h卵巢組織中的表達量顯著高于撤栓后18 h,其mRNA表達趨勢及其編碼蛋白表達趨勢總體一致;而SMAD3 基因mRNA及其編碼蛋白的表達量在不同生理階段卵巢組織中差異不顯著。SMAD3 基因mRNA及其編碼蛋白在中卵泡中的表達量顯著高于大卵泡;SMAD2 和SMAD4 基因表達量在不同直徑卵泡中差異不顯著。綜上所述,SMAD2、SMAD3 和SMAD4 基因在小尾寒羊卵巢周期性活動中的生物學功能存在差異,SMAD2 和SMAD4 基因參與小尾寒羊發情初期至排卵前的卵巢生理變化,但不參與卵泡發育;而SMAD3 參與卵泡發育。以上研究結果為進一步探索SMAD 基因家族在小尾寒羊卵巢活動中的分子機理提供理論參考。
關鍵詞:小尾寒羊;卵巢;卵泡;SMAD2;SMAD3;SMAD4
doi:10.13304/j.nykjdb.2022.1118
中圖分類號:S826;Q786 文獻標志碼:A 文章編號:1008?0864(2024)07?0069?11
小尾寒羊是中國乃至世界聞名的肉裘兼用型綿羊品種,具有早熟、多羔、生長快、體格大、產肉多、裘皮好、遺傳性穩定及適應性強等優點,被國家認定為名畜良種,從而引起了國內外養羊業的廣泛關注,其最早分布于河北、河南、山東、安徽和江蘇,現已推廣至全國近20 個省(自治區、直轄市),在養羊業生產中呈現出迅猛發展勢頭[1]。綿羊繁殖力受遺傳背景、飼養條件、營養水平等多種因素的調控,其中排卵數對母羊的產羔數具有直接影響,同時排卵數和產羔數也是衡量母羊繁殖力最重要的2個指標[2]。卵巢作為雌性哺乳動物性腺,具有產生卵子、分泌雌激素和孕酮的功能,決定著雌性的第二性征。卵泡是卵巢基本功能單位,分布于卵巢皮質部,由卵母細胞(oocyte)、顆粒細胞(granular cells,GCs)和卵泡膜細胞(thecalcells,TCs)組成,為卵母細胞的發育和成熟提供微環境,不同大小代表不同發育階段。因此,研究小尾寒羊卵巢中卵泡的生長發育過程有助于挖掘小尾寒羊高繁殖力性狀的遺傳機制,為其他綿羊品種提供理論參考。
1995 年,Sekelsky 等[3]在果蠅中首次鑒定出SMAD蛋白家族。SMAD蛋白可以分為3類,受體調節的SMAD 蛋白(R-SMAD)、公共SMAD 蛋白(CoSMAD、SMAD4) 和抑制性SMAD 蛋白(SMAD6/7)。R-SMAD 蛋白中包含SMAD2/3,其作為TGF-β/SMAD 信號途徑中的核轉錄調控因子,磷酸化能夠促進TGF- β 信號傳遞[4?5];公共SMAD 蛋白中的SMAD4 作為TGF-β 信號傳導中的中心介質,不僅可以與SMAD3發揮協同作用,還可以與SMAD2發揮協同作用以介導TGF-β信號傳導[6?7]。有關SMAD2、SMAD3 和SMAD4 基因在不同品種、不同組織及不同細胞類型中的生物學功能報道較多。廖火城等[8]發現,敲低SMAD2基因表達與過表達SMAD7 基因能降低大鼠心肌纖維化。Liu等[9]發現,過表達SMAD3 基因可調控肌生長抑制素(myostatin,MSTN),從而抑制綿羊成肌細胞肌源性分化。張秉芬等[10]發現,抑制TGF-β/SMAD3信號通路激活會對大鼠肺纖維化產生保護作用。范李靜等[11]發現,下調SMAD4 基因表達會抑制TGF-β1誘導的人子宮內膜間質細胞(human endometrial stromal cell,hESC)增殖和纖維化。此外,關于SMAD2、SMAD3 和SMAD4 基因與生殖活動相關的研究報道也越來越多。在TGF-β/SMAD 信號通路中,SMAD 作為下游信號分子通過自分泌/旁分泌途徑發出信號,調控顆粒細胞增殖和卵母細胞生長,影響著卵巢發育[12];SMAD 信號分子還可以調節雄激素和雌激素的形成,從而介導 BMP4 的作用[13]。2000 年,在人卵母細胞中也檢測到SMAD2 和SMAD3 基因的表達[14]。在牛早期胚胎發生過程中SMAD3 基因是關鍵影響基因,并且卵泡抑素(follistatin,FS)要依賴于SMAD2/3信號共同轉導,才能夠發揮出特異性促胚胎發育的作用[15]。Gueripel等[16]研究顯示,促卵泡素(follicle-stimulating hormone,FSH)和促黃體素(luteinizing hormone,LH)能夠增加TGF-BMP 通路相關基因表達量,其中SMAD4 基因起橋梁作用。Pangas 等[17]在小鼠卵巢中發現,干擾SMAD4 基因會破壞卵巢顆粒細胞中的信號傳導,導致顆粒細胞過早黃體化,最終導致卵巢過早衰竭,繁殖力降低,從而出現產仔數顯著減少和超排后卵子數量減少的現象;被活化的SMAD2蛋白也可作為底物,與SMAD4形成聚合體,進而轉入細胞核,啟動基因轉錄,調節目的基因表達,促進小型有腔卵泡的早熟,促進卵泡的釋放[18]。綜上所述,SMAD 基因家族參與哺乳動物繁殖活動,特別是在雌性動物繁殖活動中的生物學功能仍然是目前研究的熱點;然而有關SMAD 基因在小尾寒羊卵巢周期性活動中的研究報道還較少。
基于以上研究背景,本研究欲利用生物信息學分析SMAD2、SMAD3和SMAD4蛋白,然后采集同期發情后的雌性小尾寒羊不同生理階段的卵巢組織,通過免疫組織化學確定SMAD2/3/4蛋白在卵巢組織中的陽性表達,并利用RT-qPCR 和Western blot 方法測定SMAD2、SMAD3 和SMAD4基因及其編碼蛋白在小尾寒羊卵巢組織中的表達水平;同時在屠宰場隨機采集小尾寒羊卵巢,分離出不同直徑的卵泡,利用相同方法測定SMAD2、SMAD3 和SMAD4 基因在不同發育階段卵泡中的表達水平,初探SMAD2、SMAD3和SMAD4 基因在小尾寒羊卵巢周期性活動中的生物學功能,挖掘小尾寒羊高繁殖力潛在的遺傳機理,為深入研究SMAD 基因家族在小尾寒羊繁殖活動中的調控機理提供理論參考。
1 材料與方法
1.1 試驗羊只處理及樣品采集
1.1.1 試驗羊只的處理及卵巢樣品的采集
試驗羊只來自甘肅省臨夏市興華牧業養殖場,選取飼養和管理條件一致,2~3歲健康純種雌性小尾寒羊8只,在其陰道放置孕酮陰道栓(300 mg孕酮,新西蘭Bioniche Animal Health Pty 公司)處理12 d,實施同期發情。在孕酮栓塞撤除后的18和42 h各屠宰4只母羊,解剖分離出兩側卵巢,然后用磷酸鹽緩沖鹽水(phosphate buffer saline,PBS)沖洗。將分離出的左側卵巢放置于凍存管投于液氮中冷凍保存,右側卵巢放置于4%多聚甲醛溶液中,用于后續試驗。
1.1.2 卵泡樣品的采集
在臨夏市康泰屠宰場采集小尾寒羊母羊卵巢,使用剪刀、鑷子等器械分離出卵泡,用游標卡尺測量卵泡直徑。參考Jing等[19] 方法,將獲得的卵泡分為小卵泡(直徑≤2 mm)、中卵泡(3.5 mm≤直徑≤4.5 mm)和大卵泡(直徑≥6 mm)。將測量后的卵泡置于凍存管于液氮中冷凍保存,用于后續試驗。
1.2 試驗方法
1.2.1 生物信息學分析
從NCBI 網站GenBank數據庫獲取SMAD2(XP_027816688.1)、SMAD3(XP_042108005.1)和SMAD4(XP_027816484)的蛋白序列。利用ExPASy-ProtParam tool在線工具對編碼的蛋白質進行理化性質分析;利用ProtScale在線工具分析SMAD 蛋白的親疏水性;參考Chou等[20]的方法進行亞細胞定位分析;通過在線網站SOPMA預測SMAD蛋白的二級結構;最后,利用在線網站STRING預測SMAD蛋白的互作及GO(gene ontology)和KEGG(kyoto encyclopediaof genes and genomes)富集分析。
1.2.2 免疫印跡(western blot)分析
用RIPA 組織裂解液(G2002,Servicebio)提取卵巢組織和卵泡的蛋白,根據BCA蛋白定量試劑盒(PC0020,索萊寶)進行蛋白定量。用30 μL 5×上樣緩沖液(G2013,Servicebio)與120 μL 蛋白樣本混合于200 μL的離心管中,于PCR儀上98 ℃煮沸5 min后,迅速插入冰上,冰浴5 min;重復3 次,置于?80 ℃備用。于?80 ℃中取出變性蛋白樣品,于PCR 儀上95 ℃變性3 min,每孔上樣30 μg,以GAPDH(YM3215,ImmunoWay)為內參,12%的十二烷基硫酸鈉-聚丙烯酰胺凝膠(sodium dodecylsulfate polyacryl-amide gelelectrophoresis,SDS-PAG)進行電泳,轉膜。轉膜后,取PVDF膜(RVH00010,Millipore)置于用脫脂奶粉(D8340,索萊寶公司)配置的5% 脫脂奶封閉液中,室溫搖1.5 h;將PVDF膜按照目的蛋白所處位置裁成長條,分別將其置于用5%脫脂奶封閉液配置的一抗稀釋液中,4 ℃慢搖,孵育過夜。用1×TBS和0.1% Tween-20(T8220,索萊寶公司)配置TBST洗膜,室溫5×6 min 搖洗。加入山羊抗IgG(1∶6000)(RS0002,ImmunoWay),室溫1 h;TBST 洗膜,室溫5×6 min搖洗。用 ECL 發光液(G2020-2,Servicebio)顯影曝光,并觀察試驗結果。
1.2.3 總RNA提取及cDNA合成
將卵巢組織和卵泡在RNA isolater里勻漿或在液氮里研碎,按照RNA isolater Total RNA Extraction Reagent 試劑盒(R401-01,諾唯贊)使用說明提取卵巢組織和卵泡的總RNA。
使用Evo M-MLV RT Mix Kit with gDNAClean for qPCR試劑盒(AG11728,艾科瑞)去除卵巢組織和卵泡總RNA 中的DNA 后,反轉錄合成cDNA,具體操作步驟參照試劑盒使用說明書。獲得的cDNA產物于?80 ℃保存備用。
1.2.4 引物設計與合成
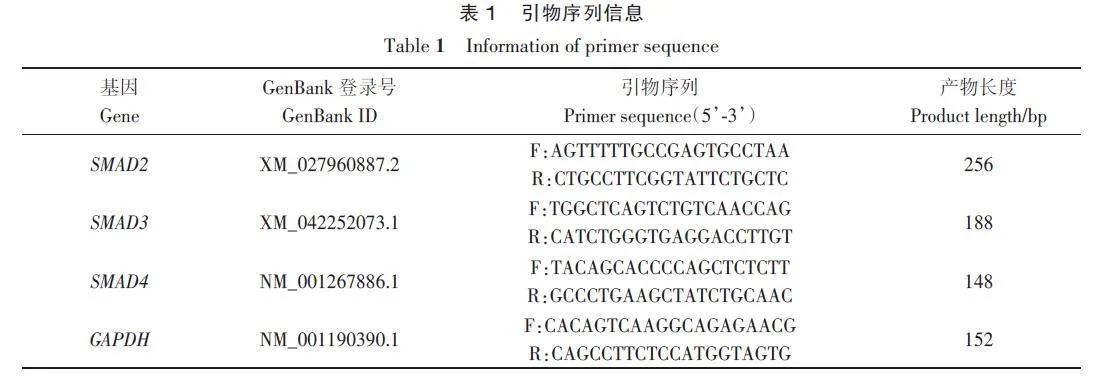
從GenBank數據庫中檢索綿羊SMAD2(XM_027960887.2)、SMAD3(XM_042252073.1)、SMAD4 基因(NM_001267886.1)和內參GAPDH 基因(NM_001190390.1)的mRNA序列,利用Primer Premier 3.0 軟件設計引物(表1),并進行BLAST檢測后,將引物序列信息發送至楊凌天潤奧科生物科技有限公司進行引物合成。
1.2.5 實時熒光定量 PCR(RT-qPCR)技術
采用實時熒光定量PCR 儀(Thermo Fisher,USA)檢測卵巢組織和卵泡中SMAD2/3/4 mRNA的表達水平,以GAPDH 為內參。PCR 體系包括10 μL 2×SYBR? Green PremixPro Taq HS qPCR Kit(AG11720,艾科瑞),上、下游引物各0.4 μL,7.2 μLddH2O,2 μL cDNA, 3次重復。PCR程序為95 ℃3 min;95 ℃ 10 s,60 ℃ 30s,72 ℃ 30 s, 40 個循環;95 ℃ 15 s,60 ℃ 60 s,95 ℃ 15 s。按照梁維煒等[21]方法對RT-qPCR結果進行計算。
1.3 數據分析
使用Image J 軟件統計Western blot 結果,使用GraphPad Prism8.0軟件對數據進行獨立樣本t檢驗和單因素方差分析。
2 結果與分析
2.1 SMAD2、SMAD3 和SMAD4 蛋白的理化性質
ExPASy-ProtParam tool 在線工具分析發現,SMAD2、SMAD3 和SMAD4 蛋白分子式分別為C2 168H3 368N602O649S22、C2 133H3 298N594O626S25和C2 675 H4 140-N764O802S23,原子總數為6 809、6 676和8 404,氨基酸數量為437、425和553,蛋白的相對分子質量為48 955.56、48 080.75 和60 572.32 kDa,理論等電點為6.67、6.73 和6.50,脂肪族指數為75.58、74.52 和76.06,平均親水性指數為? 0.437、?0.447 和?0.389,不穩定指數(Ⅱ)為54.84、53.26和50.95。
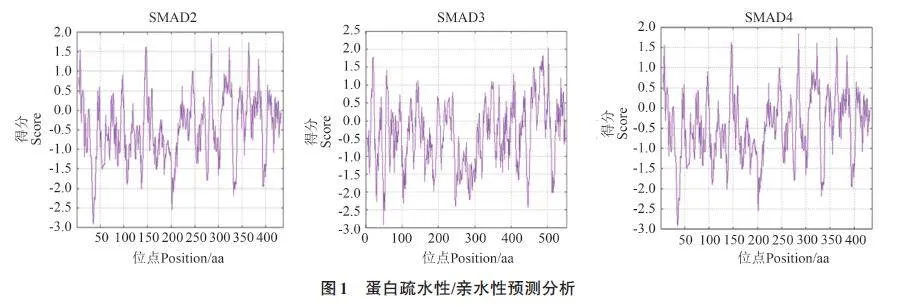
2.2 SMAD2、SMAD3 和SMAD4 蛋白的親疏水性
由圖1可知,高峰值(正值)區域表示疏水,而負值的“ 低谷”區域為親水區域,總體來看,SMAD2、SMAD3 和SMAD4 蛋白的親水性氨基酸明顯多于疏水性氨基酸,均屬于親水性蛋白。
2.3 SMAD2、SMAD3 和SMAD4 蛋白的亞細胞定位
亞細胞定位分析發現,SMAD2蛋白主要分布在細胞膜和細胞核;MAD3蛋白主要分布在細胞膜、細胞質和細胞核;SMAD4蛋白主要分布在細胞質和細胞核。
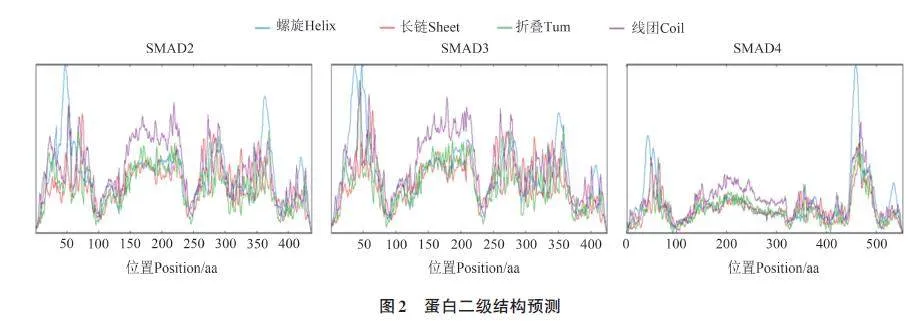
2.4 SMAD2、SMAD3 和SMAD4 蛋白的二級結構
通過在線網站SOPMA 對SMAD2、SMAD3和SMAD4蛋白的二級結構進行預測,結果(圖2)表明,SMAD2、SMAD3 和SMAD4 蛋白中α 螺旋(alpha helix)的占比分別為24.03%、23.53% 和24.41%,有105、100 和135 個氨基酸;延伸鏈(extended strand)的占比分別為16.93%、18.12%和15.55%,有74、77和86個氨基酸;β-折疊結構(beta turn) 的占比分別為3.89%、3.76%和6.69%,有17、16和37個氨基酸;無規線團(random coil)的占比分別為55.15%、54.59%和53.35%,有241、232和295個氨基酸。
2.5 SMAD2、SMAD3 和SMAD4 蛋白互作的GO 和KEGG 富集分析
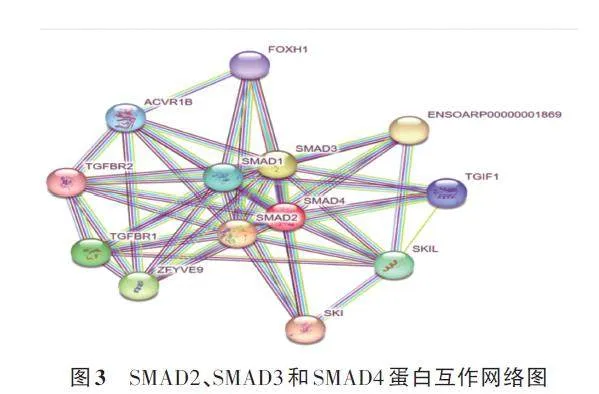
由圖3可知,與 SMAD2、SMAD3和SMAD4蛋白互作的蛋白共有10個(FOXH1、ACVR1B、SMAD1、TGFβR1、TGFβR2、ZFYVE9、SKI、SKIL、TGIF1、ENSOARP0000001869),存在52條互作關系。
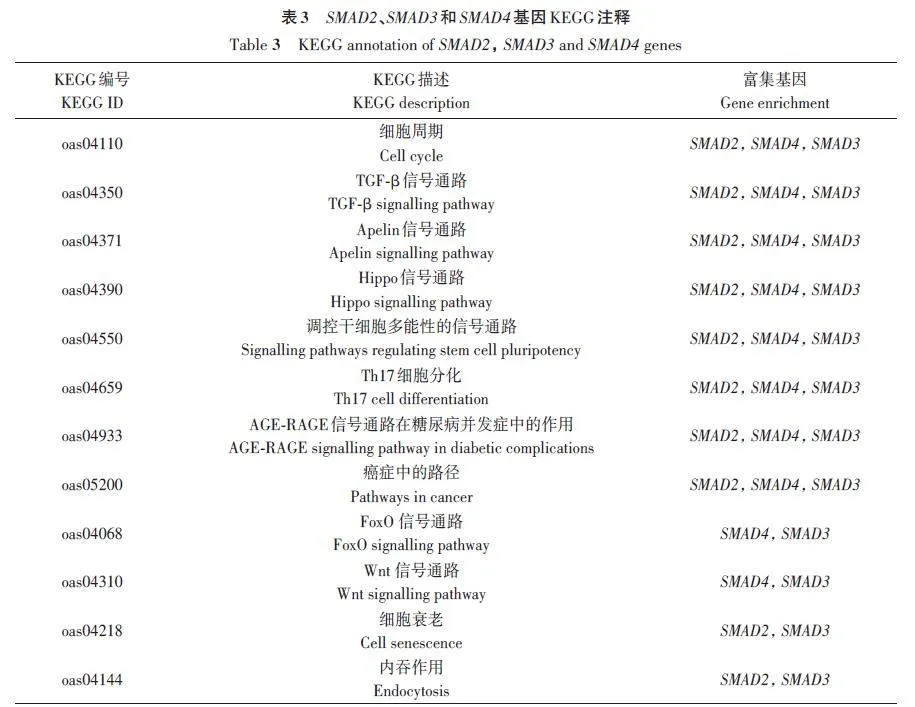
SMAD2、SMAD3 和SMAD4 基因的GO 的功能條目主要有TGF-β受體信號通路(GO∶0007179)、TGF-β受體結合(GO∶0005160)、TGF-β激活受體活性(GO∶0005024)(表2),在KEGG富集分析發現SMAD2、SMAD3 和SMAD4 基因主要富集于TGF-β信號通路、Apelin信號通路、Hippo信號通路等信號通路(表3)。這些都可能與卵巢發育有關。
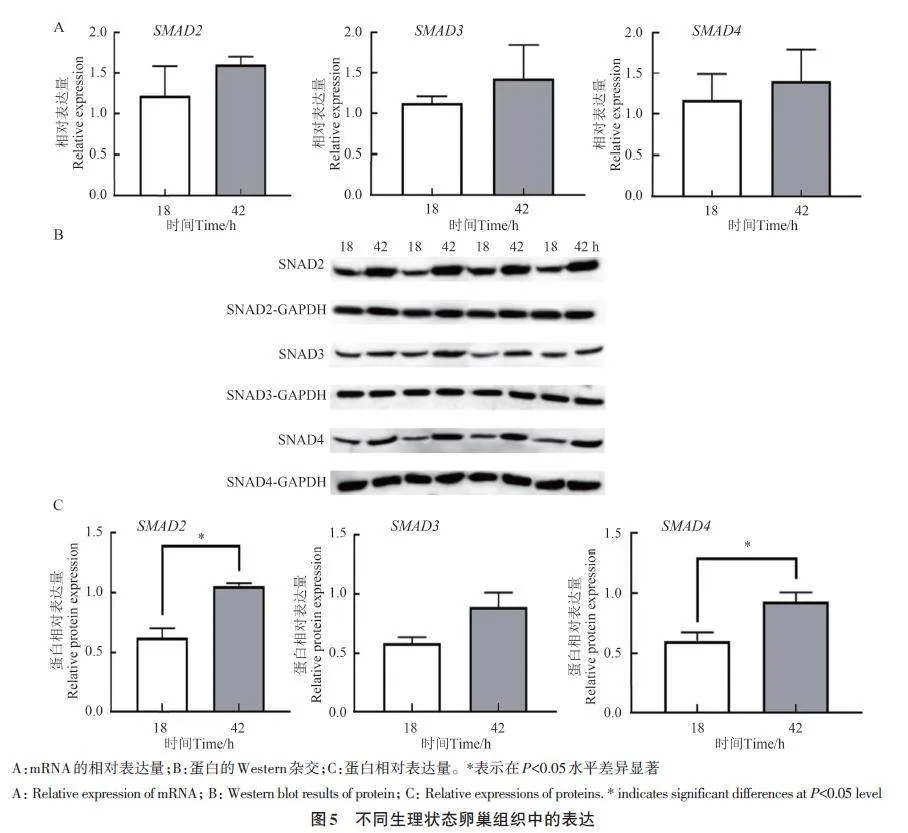
2.6 SMAD2、SMAD3 和SMAD4 蛋白在不同生理狀態卵巢組織中的陽性表達
免疫組織化學試驗結果如圖4 所示。SMAD2、SMAD3和SMAD4蛋白在撤栓后18和42 h的卵巢組織中均有陽性表達;且主要位于卵母細胞、卵泡膜細胞、顆粒細胞。
2.7 SMAD2、SMAD3 和SMAD4 基因在不同生理狀態卵巢組織中的表達
采用RT-qPCR 和Western blot技術檢測撤栓后18 和42 h 的卵巢組織中SMAD2、SMAD3 和SMAD4 基因mRNA及其編碼蛋白表達水平,結果(圖5)表明,在撤栓后18和42 h的卵巢組織中均能檢測到SMAD2、SMAD3 和SMAD4 基因與蛋白的表達,且在撤栓后42 h卵巢組織中mRNA及其編碼蛋白的表達量均高于18 h,其中,SMAD2 和SMAD4蛋白在撤栓后42 h卵巢組織中的表達量顯著高于18 h,而mRNA表達差異不顯著;SMAD3基因及其編碼蛋白在撤栓后18和42 h間差異均不顯著。
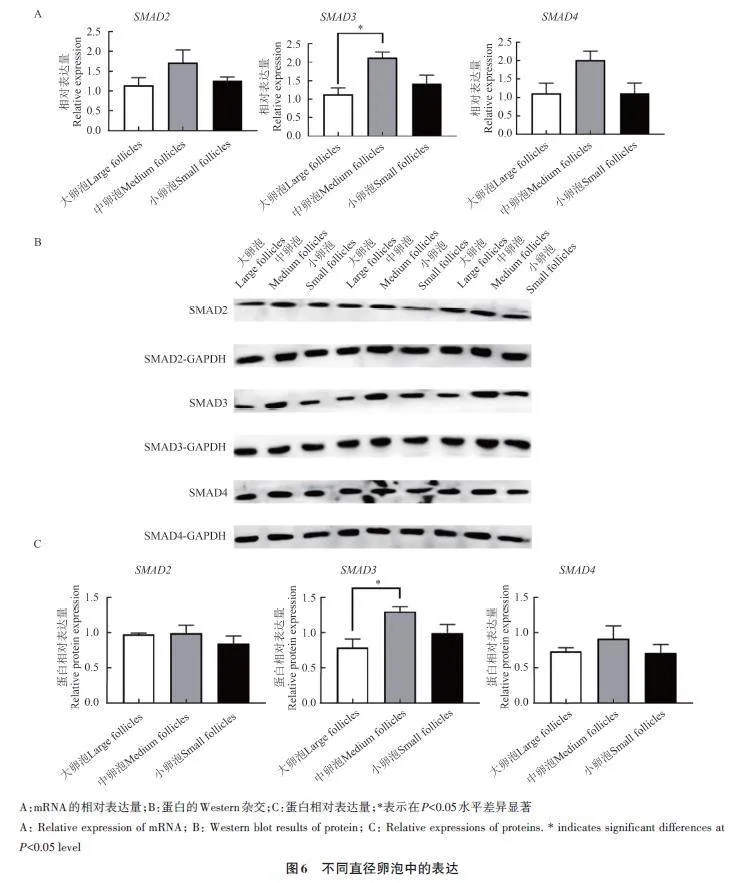
2.8 SMAD2、SMAD3 和SMAD4 基因在不同直徑卵泡中的表達
采用RT-qPCR 和Western blot技術檢測不同直徑卵泡中SMAD2、SMAD3 和SMAD4 基因mRNA及其編碼蛋白的表達水平,結果(圖6)表明,SMAD2、SMAD3 和SMAD4 基因及其蛋白在大、中、小卵泡中均表達。其中SMAD3 基因mRNA 及其編碼蛋白在中卵泡的表達量顯著高于大卵泡,然而大卵泡與小卵泡、中卵泡與小卵泡間差異不顯著。SMAD2 和SMAD4 基因及其蛋白在不同直徑卵泡中表達量差異均不顯著。
3 討論
TGF-β超家族信號通路對卵泡發育、卵母細胞生長以及顆粒細胞增殖發揮重要作用。SMAD2、SMAD3 和SMAD4 基因是SMAD 基因家族參與哺乳動物TGF-β信號傳導的重要成員,但其在綿羊卵巢周期性活動中的生物學功能尚不明確。本研究利用生物信息分析發現,SMAD2、SMAD3 和SMAD4 蛋白均為親水性蛋白,理論等電點為6.67、6.73和6.50,可以與某些帶有電荷的基團結合,從而發揮其生物學功能;亞細胞定位分析顯示,SMAD2、SMAD3 和SMAD4 蛋白在細胞膜、細胞質和細胞核中發揮生物學作用,且二級結構中α螺旋和無規卷曲的占比較高;與FOXH1、ACVR1B、SMAD1、TGFβR1、TGFβR2、ZFYVE9、SKI、SKIL、TGIF1和ENSOARP0000001869蛋白存在52條互作關系;GO分析表明,SMAD2、SMAD3和SMAD4 基因在TGF-β受體信號通路、TGF-β受體結合、TGF-β激活受體活性中發揮生物學功能,KEGG 富集分析發現,SMAD2、SMAD3 和SMAD4基因在TGF-β信號通路富集,而TGF-β信號通路在卵巢中發揮著重要作用,因此,推測SMAD2、SMAD3 和SMAD4 基因與卵巢的周期性變化有關。
湯繼順[22]研究表明,實施同期發情后的小尾寒羊在撤栓后18 h開始發情,在36 h時發情率達到90%以上,在48 h時發情率達到100%;撤栓后48~52 h 卵母細胞排出。為了進一步驗證SMAD2、SMAD3 和SMAD4 基因在卵巢中的功能,本研究分別采集撤栓后18和42 h的卵巢組織,采用免疫組織化學法發現,在卵母細胞、卵泡膜細胞、顆粒細胞中均有SMAD2、SMAD3和SMAD4蛋白的陽性表達;RT-qPCR和WB也檢測到SMAD2、SMAD3 和SMAD4 基因mRNA及其編碼蛋白在卵巢組織中表達,且SMAD2、SMAD3 和SMAD4 基因mRNA及其編碼蛋白在42 h卵巢中的表達量高于18 h,其中SMAD2 和SMAD4 蛋白表達量差異顯著。蓋玉強等[23]研究表明,敖漢細毛羊在發情期中SMAD4 基因mRNA表達量顯著高于發情前期;He等[24]研究發現,SMAD2 基因在黃鰻卵巢發育過程中表達,且表達量持續增加,在卵黃形成早期達到峰值;苗竹林等[25]發現,隨著大鼠卵巢的發育,SMAD4 基因的表達量也逐漸增加;與本研究結果一致,即SMAD2 和SMAD4 基因參與小尾寒羊發情初期至排卵這一過程中卵巢的生理變化。
雌性綿羊的卵母細胞進入減數分裂后一直被阻斷在第一次減數分裂前期的雙線期,直到發情時,才在垂體促性腺激素的調節下重新恢復減數分裂。與此同時,卵巢上的卵泡快速發育,隨著卵泡的不斷增大,雌激素分泌增多,從而引起性欲;在此期間,只有少數卵泡會變成優勢卵泡破裂排卵,大多數卵泡會發生閉鎖;排卵后雌激素顯著減少,孕酮(progesterone,P4)快速增加,導致停止發情[26]。鄭健[27]研究發現,在湖羊垂體上調控SMAD2基因表達能夠影響垂體細胞的激素分泌,調節卵巢卵泡發生和排卵。李碧筠等[28]發現,抑制山羊卵巢中SMAD2 基因表達,會抑制TGF-β/SMAD信號通路的傳導,從而抑制雌二醇(estradiol,E2)分泌,促進孕酮的合成。Nomura等[29]發現,在人卵巢中SMAD2 基因可通過調控CYP19A1的表達,影響雌激素分泌。Yu等[30]在小鼠中研究發現,SMAD4 基因是LH刺激ERK1/2激活和排卵相關基因表達所必需的,敲除SMAD4基因會阻斷LH誘導的卵丘擴張和卵泡破裂,還會降低Nppc 和Npr2 的表達,使其維持卵母細胞減數分裂停滯的作用減弱。絕經過渡期大鼠卵巢功能衰退與SMAD2基因表達下調密切相關,顆粒細胞中SMAD4 基因的表達下調也是其部分原因[31?32]。基于以上研究,推測SMAD2和SMAD4 基因能夠通過調控雌激素、孕激素分泌和阻斷LH的誘導作用來調控小尾寒羊發情初期至排卵前卵巢的生理變化。卵泡的發育及卵母細胞的成熟和排卵是雌性動物發情周期的關鍵。伴隨著動物發情,卵巢中的卵泡也不斷發育至成熟,SMAD2 和SMAD4 基因是否能夠參與卵泡發育的優勢化過程,還需進一步驗證。
分離并采集不同直徑的卵泡,檢測大、中、小卵泡中SMAD2、SMAD3 和SMAD4 基因mRNA及其編碼蛋白的表達水平,結果發現,SMAD3 基因mRNA及其編碼蛋白在中卵泡中的表達量顯著高于大卵泡,在大卵泡與小卵泡、中卵泡與小卵泡間無顯著差異;SMAD2 和SMAD4 基因mRNA及其編碼蛋白在不同直徑的卵泡中的表達量均無顯著差異。綜上所述,SMAD2 和SMAD4 基因參與小尾寒羊發情過程中卵巢的生理變化,但不參與卵泡發育;而SMAD3 基因參與卵泡發育。研究表明,SMAD3 基因是合成卵泡刺激素(follicle-stimulatinghormone,FSH)的必需基因[33]。Li 等[34] 發現,SMAD3 基因在大鼠不同階段卵泡中差異表達,過表達SMAD3 基因會促進雌激素的產生和增殖,抑制顆粒細胞的凋亡,調節卵泡的發育與閉鎖。Gry等[35]發現,人SMAD3 基因在卵泡生長開始就參與了卵泡發育。Li等[36]發現,敲除SMAD3 基因會導致雌鼠的卵泡發育受阻,最終導致卵泡閉鎖、生殖能力顯著下降。Zhou 等[37] 發現,內含子microRNAlet-7可降低豬卵巢顆粒細胞中SMAD3蛋白磷酸化水平來促進顆粒細胞凋亡和卵泡閉鎖。本研究結果也表明,SMAD3 基因在卵泡發育過程中起重要調控作用;然而該基因是否能夠通過調控小尾寒羊卵巢顆粒細胞增殖或凋亡來影響卵泡發育,還需要進一步研究。綜上所述,SMAD2、SMAD3 和SMAD4 基因在小尾寒羊卵巢周期性活動中的生物學功能存在差異,SMAD2 和SMAD4 基因參與小尾寒羊發情初期至排卵前的卵巢生理變化,但不參與卵泡發育; SMAD3 基因參與卵泡發育。
參考文獻
[1] 國家畜禽遺傳資源委員會.中國畜禽遺傳資源志:羊志[M].北京:中國農業出版社,2011.
[2] JUENGEL J L, FRENCH M C, QUIRKE L D, et al ..Reproduction differential expression of cart in ewes with differingovulation rates [J]. Soc. Study Fert., 2017, 153(4):471-479.
[3] SEKELSKY J J, NEWFELD S J, RAFTERY L A, et al ..Genetic characterization and cloning of mothers against dpp, agene required for decapentaplegic function in Drosophilamelanogaster [J/OL]. Genetics, 1995, 139(3): 1347 [2022-11-20]. https://doi.org/10.1007/BF01435010.
[4] 嚴曉華,章雋宇,陳曄光.抑制性Smad蛋白對TGF-β超家族信號轉導的調控及其生理意義[J].細胞生物學雜志,2009,31(2):4-13.
YAN X H, ZHANG J Y, CHEN Y G. Regulation of TGF- βsuperfamily signaling by inhibitory Smad [J]. Chin. J. CellBiol., 2009,31(2):4-13.
[5] MULSANT P, LECERF F, FABRE S, et al .. Mutation in bonemorp-hogenetic protein receptor-IB is associated with increasedovulation rate in Booroola Merino ewes [J]. Proc. Natl. Acad.Sci. USA, 2001, 98:5104-5109.
[6] ZHANG Y, MUSCI T, DERYNCK R. The tumor suppressorSmad4/DPC 4 as a central mediator of Smad function [J].Current Biol. Cb, 1997, 7(4):270-276.
[7] MING Z, LOPA M, CHU X D. The role of TGF- β/SMAD4signaling in cancer [J]. Int. J. Biol. Sci., 2018, 14(2):111-123.
[8] 廖火城,劉勇,周彬,等.四逆湯對異丙腎上腺素誘導的大鼠心肌纖維化Smad2和Smad7的影響[J].中國中西醫結合雜志,2012,32(7):934-938.
LIAO H C, LIU Y, ZHOU B, et al .. Effects of Sin decoction onthe expressions of Smad2 and Smad7 in isoproterenol inducedmyocardial fibrosis rats [J]. Chin. J. Integrative Med., 2012, 32(7):934-938.
[9] LIU C, LI W, ZHANG X, et al .. The critical role of myostatinin differentiation of sheep myoblasts [J]. Bioch. Biophy. Res.Comm., 2012, 422(3):381-386.
[10] 張秉芬,周勝紅,王哲.延齡草皂苷通過抑制TGF-β/Smad3與Wnt/β-catenin信號通路改善大鼠肺纖維化[J].山東大學學報(醫學版),2022,60(8):23-29.
ZHANG B F, ZHOU S H, WANG Z. Trillium saponinsameliorates pulmonary fibrosis in rats by inhibiting TGF- β/Smad3 and Wnt/β-catenin signaling pathways [J]. J. ShandongUniv. (Health Sci.), 2022, 60(8):23-29.
[11] 范李靜,張苗,鄭瑛紅,等.miR-34a-5p靶向Smad4抑制子宮內膜纖維化的機制研究[J]. 現代婦產科進展,2022,31(9):678-682.
FAN L J, ZHANG M, ZHENG Y H, et al .. Inhibitory effect ofmiR-34a-5p on fibrosis of endometrial by down-regulatingSmad4 [J]. Prog. Obstet. Gynecol., 2022, 31(9):678-682.
[12] 王雪,張景萍,郭麗麗,等.TGF-β/SMAD信號通路在哺乳動物卵巢發育調控中的作用研究進展[J].中國畜牧雜志,2023,59(3):61-69.
WANG X, ZHANG J P, GUO L L, et al .. Research progress onthe regulation of TGF-β/Smad signaling pathway in mammalianovarian development [J]. Chin. J. Anim. Sci., 2023, 59(3):61-69.
[13] LIU Y, DU S Y, DING M, et al .. The BMP4-Smad signalingpathway regulates hyperandrogenism development in a femalemouse model [J]. J. Biol. Chem., 2017, 292(28):11740-11750.
[14] OSTERLUND C. TGFbeta receptor types Ⅰ and Ⅱ and thesubstrate proteins Smad 2 and 3 are present in human oocytes[J/OL]. Mol. Human Reprod., 2000, 6(6): 498 [2022-11-20].https://doi.org/10.1093/molehr/6.6.498.
[15] ZHANG K, RAJPUT S K, LEE K B, et al .. Evidencesupporting a role for smad2/3 in bovine early embryonicdevelopment: potential implications for embryotropic actions offollistatin [J/OL]. Biol. Reprod., 2015, 86: 130278 [2022-11-20]. https://doi.org/10.1095/biolreprod.115.130278.
[16] GUERIPEL X, BENAHMED M, GOUGEON A. Sequentialgonadotropin treatment of immature mice leads to amplificationof transforming growth factor β action, via upregulation ofreceptor-type1, Smad2 and 4, and downregulation of Smad6 [J].Biol. Reprod., 2004, 70(3):640-648.
[17] PANGAS S A, LI X, ROBERTSON E J, et al ..Prematureluteinization and cumulus cell defects in ovar-ianspecificSmad4 knockout mice [J]. Mol. Endocrinol., 2006,20(6):1406-1422,.
[18] FINDIAY J K, DRUMMOND A E, DYSON M, et al .. Productionand actions of inhibin and activin during folliculogenesisin the rat [J]. Mol. Cell Endocr-inol., 2001, 180(1-2):139-144.
[19] JING J, JIANG X, CHEN J, et al .. Notch signaling pathwaypromotes the development of ovine ovarian follicular granulosacells [J]. Anim. Reprod. Sci., 2017, 181(1):69-78.
[20] CHOU K C, SHEN H B. A new method for predicting thesubcellular localization of eukaryotic proteins with both singleand multiple sites: Euk-mPLoc 2.0 [J/OL]. PloS One, 2010,5(4): e9931[2022-11-20].https://doi.org/10.1371/journal.pone.0009931.
[21] 梁維煒,李明娜,羅玉柱,等.性成熟期遼寧絨山羊與子午嶺黑山羊睪丸發育比較[J].畜牧獸醫學報,2021,52(12):3461-3470.
LIANG W W, LI M N, LUO Y Z, et al .. Comparation of thetestes development between Liaoning cashmere goat andZiwuling blackgoat at swxual matreity [J]. J. Anim. Husb.Vet. Med., 2021, 52(12):3461-3470.
[22] 湯繼順.利用轉錄組測序和蛋白質組學分析篩選綿羊多羔候選基因的研究[D].北京:中國農業科學院,2019.
TANG J S. Study on screening polytocous candidate genes insheep based on transcriptome sequencing and proteomics analysis[D]. Beijing: Chinese Academy of Agricultural Sciences, 2019.
[23] 蓋玉強,杜寶霞,馬龍,等.不同發情時期Smad4 基因在綿羊卵巢中表達規律的研究[J].吉林畜牧獸醫,2020,41(10):1-2,4.
[24] HE Z, DENG F, XIONG S, et al .. Expression and regulation ofSmad2 by gonadotropins in the protogynous hermaphroditicricefield eel (Monopterus albus) [J/OL]. Fish Physiol. Biochem.,2020, 4: 9 [2022-11-20]. https://doi. org/10.1007/s10695-020-00778-9.
[25] 苗竹林,王自能,章韻,等.Smad4蛋白及mRNA在卵巢不同發育階段的表達[J].中國病理生理雜志,2005,21(5):1009-1013.
MIAO Z L, WANG Z N, ZHANG Y, et al .. Expression of Smad4protein and mRNA in different developmental stages of the ratovary [J]. Chin. J. Pathophysiol., 2005, 21(5):1009-1013.
[26] 劉利杰.山羊卵母細胞減數分裂機制的初步研究[D].楊凌:西北農林科技大學,2008.
LIU L J. The study on the regulation of meiotic of goat oocyte[D]. Yangling: Northwest A amp; F University, 2008.
[27] 鄭健.高低繁湖羊垂體差異表達lncRNA/mRNA篩選及候選基因SMAD2 的相關研究[D].南京:南京農業大學,2019.
ZHENG J. Pituitary transcriptomic study reveals the differentialregulation of incRNAs/mRNAs related to prolificacy in sheep andstudy on the candidate gene SMAD2 [D]. Nanjing: NanjingAgricultural University, 2019.
[28] 李碧筠,黃思藝,王鈺錕,等.SMAD7 對山羊卵泡顆粒細胞增殖、凋亡的影響[J].畜牧獸醫學報,2022,53(8):2548-2557.
LI B J, HUANG S Y, WANG Y K, et al .. Effect of SMAD7 onproliferation and apoptosis of goat follicular granulosa cells [J].J. Anim. Husb. Vet. Med., 2022, 53(8):2548-2557.
[29] NOMURA M, SAKAMOTO R, MORINAGAH, et al .. Activinstimulates CYP19A gene expression in human ovarian granulosacell-like KGN cells via the SMAD2 signaling pathway [J].Biochem. Biophys. Res. Comm., 2013, 436(3):443-448.
[30] YU C, ZHANG Y L, FAN H Y. Selective Smad4 knockout inovarian preovulatory follicles results in multiple defects inovulation [J]. Mol. Endocrinol., 2013, 27(6):966-978.
[31] 張娟.Smad2、Smad3及Smad7蛋白在絕經過渡期大鼠卵巢中的表達及意義[D].張家口:河北北方學院,2017.
ZHANG J. The expression and significance of Smad protein inthe ovary of the rat during menopausal transition [D].Zhangjiakou: Hebei North College, 2017.
[32] 袁麗娟,任君旭,姬宏宇,等.轉化生長因子-β和Smad4在絕經過渡期大鼠卵巢顆粒細胞中的表達[J].解剖學報, 2018,49(1):108-112.
YUAN L J, REN J X, JI H Y, et al .. Expression of transforminggrowth factor- β and Smad4 in ovarian granulosa cells inmenopausal transitional rat [J]. J. Anatomy, 2018, 49(1):108-112.
[33] LI Y, SCHANG G, BOEHM U, et al .. SMAD3 regulates folliclestimulatinghormone synthesis by pituitary gonadotrope cells invivo [J]. J. Biol. Chem., 2017, 292(6):2301-2314.
[34] LI Y, JIN Y, LIU Y, et al .. SMAD3 regulates the diversefunctions of rat granulosa cells relating to the FSHR/PKAsignaling pathway [J/OL]. Reproduction, 2013, 146(2): 0325[2022-11-20]. https://doi.org/10.1530/rep-12-0325.
[35] GRY K S, KASPER A, ALEXANDRO C C, et al .. Expressionof TGF-beta superfamily growth factors, their receptors, theassociated SMADs and antagonists in five isolated sizematchedpopulations of pre-antral follicles from normal humanovaries [J]. Mol. Human Reprod., 2014, 20(4):293-308.
[36] LI Q L, PANGAS S A, JORGEZ C J, et al .. Redundant roles ofSMAD2 and SMAD3 in ovarian granulosa cells in vivo [J]. Mol.Cell Biol., 2008, 28(23):7001-7011.
[37] ZHOU J L, LIU J Y, PAN Z X, et al .. The let-7g microRNApromotes follicular granulosa cell apoptosis by targetingtransforming growth factor- β type 1 receptor [J]. Mol. CellularEndocrinol., 2015, 409(7):103-112.
基金項目:國家自然基金項目(31960664);甘肅農業大學學科團隊項目(GAU-XKTD-2022-21);甘肅省自然基金項目(21JR7RA809);甘肅省基礎研究創新群體項目(22JR5RA829);蘭州市科技計劃項目(2021-1-162)。

