從學科素養角度闡釋2024高考中的氧族元素

核心素養視角下的試題命制要以核心素養為測試宗旨,以實際問題為測試任務,以真實情境為測試載體,以化學知識為解決問題的工具,本文結合氧族元素及其化合物對核心素養中的“宏觀辨識與微觀探析”“變化觀念與平衡思想”“證據推理與模型認知”“科學探究與創新意識”“科學態度與社會責任”5個維度進行分述,以期與新高考命題的新思路接軌.
維度一 宏觀辨識與微觀探析
視角1:能從不同角度認識物質的多樣性,并對物質進行分類.
視角2:能從元素和原子、分子水平認識物質的組成、結構、性質和變化,形成“結構決定性質”的觀念.
例題1 (2024.湖北卷)O2在超高壓下轉化為平行六面體的O8分子(結構如圖1所示).下列說法錯誤的是( ).
A.O2和O8互為同素異形體
B.O8中存在不同的氧氧鍵
C.O2轉化為O8是熵減反應
D.常壓低溫下O8能穩定存在
解析O2和O8是氧元素形成的不同單質,兩者互為同素異形體,A項正確;O8分子為平行六面體,由其結構知,O8中存在2種氧氧鍵:上下底面中的氧氧鍵、上下底面間的氧氧鍵,B項正確;O2轉化為O8可表示為:
4O =超高壓 O8
氣體分子數減少,故O2轉化為O8是熵減反應,C項正確;O2在超高壓下轉化成O8,則在常壓低溫下O8會轉化成O2,不能穩定存在,D項錯誤.答案:D
素養啟迪 該題以新穎的視角、凝練的語言、直觀的圖形考查了最新合成的O8單質,考查了基本概念、物質結構、化學方程式的構建和對題意的領悟遷移能力,基礎之中見能力,樸實之中顯功力.
維度二 變化觀念與平衡思想
視角1:能認識物質是運動和變化的,知道化學變化需要一定條件,并遵循一定的規律.
視角2:認識化學變化的本質是有新物質生成,并伴有能量的轉化;認識化學變化有一定限度,是可以調控的.
視角3:能多角度、動態的分析化學反應,運用化學反應原理解決實際問題.
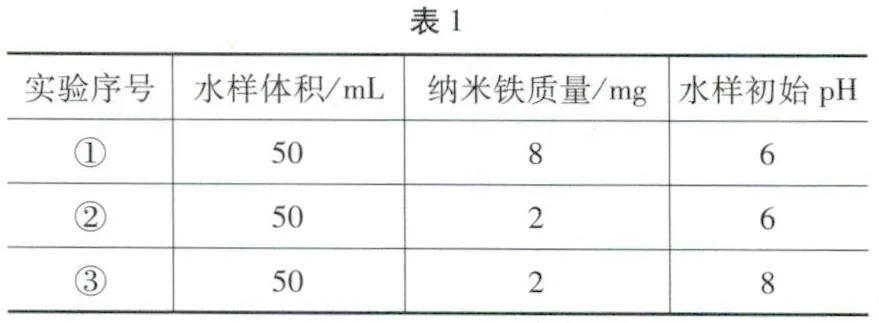
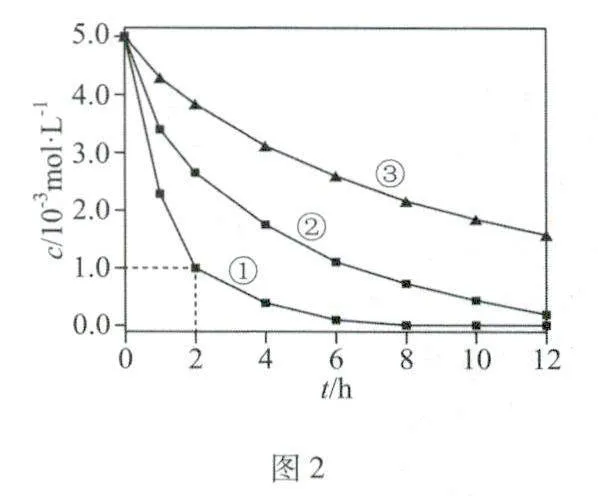
例題2 (2024.安徽卷)室溫下,為探究納米鐵去除水樣中SeO2-4的影響因素,測得不同條件下SeO2-4濃度隨時間變化關系如圖2所示.
下列說法正確的是( ).
A.實驗①中,0-2h內平均反應速率v(SeO2-4)=2.0 mol·L-1·h-1
B.實驗③中,反應的離子方程式為:2Fe+ SeO2-4+ 8H+=2Fe3+ + Se +4H2O
C.其他條件相同時,適當增加納米鐵質量可加快反應速率
D.其他條件相同時,水樣初始pH越小,SeO2-4的去除效果越好
解析 A.實驗①中,0-2小時內平均反應速率v(SeO2-4)=(5.0×10-3-1.0×10-3)mol·L-1/2h=2.0×10-3mol·L-1·h-1,A不正確;B.實驗③中水樣初始pH =8,溶液顯弱堿性,發生反應的離子方程式中不能用H+配電荷守恒,B不正確;C.綜合分析實驗①和②可知,在相同時間內,實驗①中SeO2-4濃度的變化量大,因此,其他條件相同時,適當增加納米鐵質量可加快反應速率,C正確;D.綜合分析實驗③和②可知,在相同時間內,實驗②中SeO2-4濃度的變化量大,因此,其他條件相同時,適當減小初始pH,SeO2-4的去除效果越好,但是當初始pH太小時,H+濃度太大,納米鐵與H+反應速率加快,會導致與SeO2-4反應的納米鐵減少,因此,當初始pH越小時SeO2-4的去除效果不一定越好,D不正確,答案:C
素養啟迪 硒酸(H2SeO4)的性質與硫酸類似,但比硫酸酸性弱;亞硒酸(H2SeO3)的性質與亞硫酸類似,既具有氧化性,也具有還原性.以硫及其化合物的性質為知識原型,運用同主族元素性質具有相似性和遞變性這一知識模型可以把碎片化的知識和內容變得厚實、完整和系統.
維度三 證據推理與模型認知
視角1:具有證據意識,能基于證據對物質組成、結構及其變化提出可能的假設,通過分析推理加以證實或證偽.
視角2:建立觀點、結論和證據的邏輯關系.
視角3:通過分析、推理等方法認識研究對象的本質特征、構成要素及其相互關系,從而建立模型.
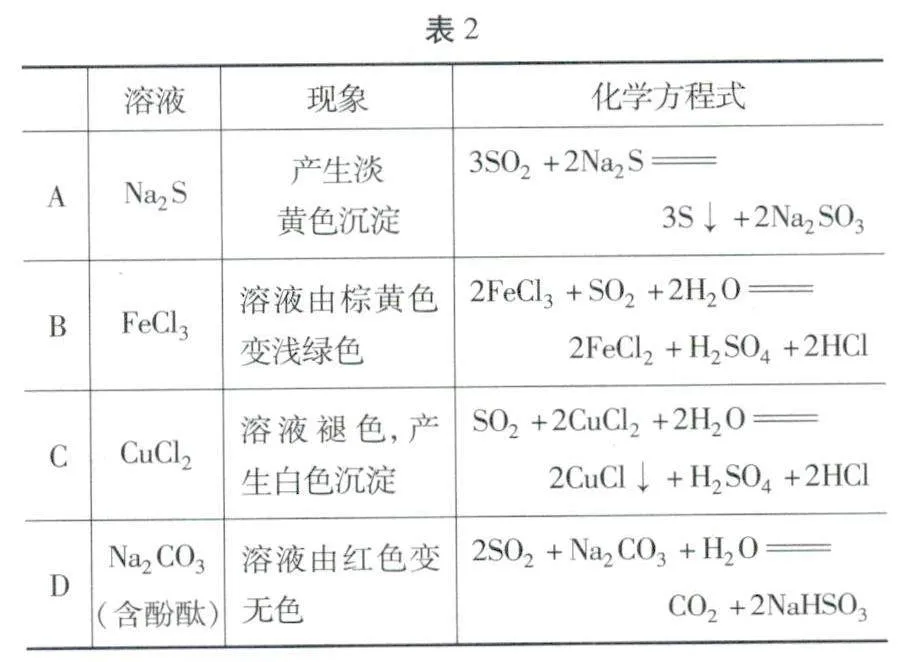
例題3 (2024·湖北卷)過量SO2與以下0.1 mol·L-1的溶液反應(見表2),下列總反應的化學方程式錯誤的是( ).
解析 過量SO2與0.1 mol·L-1的Na2S溶液反應,生成的淡黃色沉淀是S,還生成NaHSO3,SO2過量不能生成Na2SO3,因此,總反應的化學方程式為:SSO2 +2Na2S +2H2O =3S↓+4NaHSO3A錯誤;過量SO2與0.1 mol·L-1的FeCl2溶液反應,生成FeCl2、H2SO4、HCl,總反應的化學方程式為:2FeCl3 +SO2 +2H2O =2FeCl2 +H2SO4 +2HClB正確;過量SO2與0.1 mol·L-1的CuCl2溶液反應,生成的白色沉淀是CuCl,總反應的化學方程式為:SO2 +2CuCl2 +2H2O=2CuCl↓+H2SO4 +2HClC正確;Na2CO3水解使溶液顯堿性,其水溶液能使酚酞變紅;過量SO2與0.1 mol·L-1的Na2CO3溶液反應,生成CO2、NaHSO3,NaHSO3溶液顯酸性,因此,溶液由紅色變無色,總反應的化學方程式為:2SO2+ Na2CO3+ H2O =CO2 ↑+2NaHSO3.D正確.答案:A
素養啟迪 過量二氧化硫與亞硫酸鈉不共存,很容易判斷A項錯誤;本題的易錯選項是C項,學生若忽略CuCl2溶液中的Cu2+具有氧化性,對于CuCl是白色沉淀存在知識盲區,很容易落人命題陷阱,這就要求學生重點把握銅的變價性質及其構建Cu2+具有弱氧化性的知識體系,豐盈自己的知識儲備,方可在高考中得心應手.
維度四 實驗探究與創新意識
視角1:能發現和提出有探究價值的問題,能從問題和假設出發,確定探究目的,設計探究方案,進行實驗探究.
視角2:在科學探究中學會合作,面對“異常”現象敢于提出自己的見解.
例題4 (2024.黑吉遼卷)H2O2分解的“碘鐘”反應美輪美奐,將一定濃度的3種溶液(①H2O2溶液;②淀粉、丙二酸和MnSO4混合溶液;③KIO3、稀硫酸混合溶液)混合,溶液顏色在無色和藍色之間來回振蕩,周期性變色;幾分鐘后,穩定為藍色,下列說法錯誤的是( ).
A.無色一藍色:生成I2
B.藍色一無色:I2轉化為化合態
C.H2O2起漂白作用
D.淀粉作指示劑
解析分析該“碘鐘”反應的原理:①在Mn2的催化下H2O2與IO3-反應生成I2,在淀粉指示劑的作用下溶液變藍色;②生成的I2又會與H2O2反應生成IO3-,使溶液變回無色;③生成的I2可以與丙二酸反應生成琥珀色的ICH(COOH)2,溶液最終會變成藍色.A.根據分析,溶液由無色變為藍色說明有I:生成,A正確;溶液由藍色變為無色,是將I:轉化為IO3-,I2轉化為化合態,B正確;H2O2在此過程中參加反應,不起到漂白作用,C錯誤;在此過程中,因為有I2的生成與消耗,淀粉在這個過程中起到指示劑的作用,D正確,答案:C.
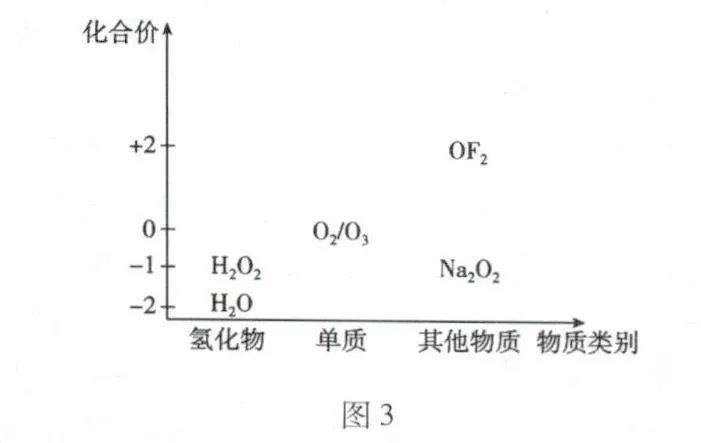
素養啟迪 過氧化氫既有氧化性又有還原性,在遇到不同的物質時,其性質隨時而變,要建立起變化觀念和證據推理的學科素養來看待雙氧水的多重角色;同時要從價類二維觀念建構氧氣及其常見化合物的性質及其轉化關系,如圖3所示.
維度五 科學態度與社會責任
視角1:具有嚴謹求實的科學態度,具有探索未知、崇尚真理的意識.
視角2:贊賞化學對社會發展的重大貢獻,具有可持續發展意識和綠色化學觀念,能對與化學有關的社會熱點問題做出正確的價值判斷.
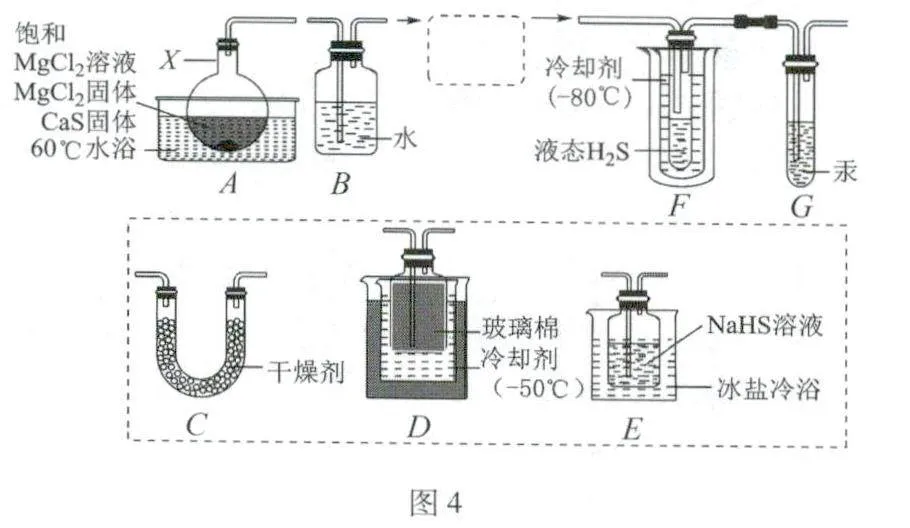
例題5 (2024.浙江高考1月卷)H2S可用于合成光電材料.某興趣小組用CaS與MgCl2反應制備液態H2S,實驗裝置如圖4所示,化學方程式為:
CaS+ MgCl2 +2H2O =CaCl2+Mg(OH)2+H2S↑
已知:①H2S的沸點是- 61℃,有毒;②裝置A內產生的H2S氣體中含有酸性氣體雜質.
請回答:
(1)儀器X的名稱是____.
(2)完善虛框內的裝置排序:
A→B→_____→F→G
(3)下列干燥劑,可用于裝置C中的是____.
A.氫氧化鉀 B.五氧化二磷
C.氯化鈣 D.堿石灰
(4)裝置G中汞的2個作用是:
①平衡氣壓;②____.
(5)下列說法正確的是____.
A.該實驗操作須在通風櫥中進行
B.裝置D的主要作用是預冷卻H2S
C.加入的MgCl2固體,可使MgCl2溶液保持飽和,有利于平穩持續產生H2S
D.該實驗產生的尾氣可用硝酸吸收
(6)取0.680 g H2S產品,與足量CuSO4溶液充分反應后,將生成的CuS置于已恒重、質量為31. 230 g的坩堝中,煅燒生成CuO,恒重后總質量為32. 814 g.產品的純度為____.
解析 A作為H2S的發生裝置,由于不能驟冷,所以D、E都是冷卻H2S的裝置,C裝置干燥H2S,F冷卻并收集H2S,G作為平衡氣壓和尾氣處理裝置.(1)儀器X的名稱是圓底燒瓶;(2)制備氣體的裝置包括發生裝置,除雜裝置,收集裝置和尾氣處理,由于不能驟冷,要逐步冷卻,所以B連E,E連C,C連D,D連F;(3)H2S是酸性氣體,不可以用堿性干燥劑,所以不可以用氫氧化鉀和堿石灰,故選BC;(4)裝置G中汞的2個作用是:①平衡氣壓:②處理尾氣H2S;(5)A.H2S有毒,該實驗操作須在通風櫥中進行,故A正確;B.氣體不能驟冷,裝置D的主要作用是預冷卻H2S,故B正確;C.加入的MgCl2固體,可使MgCl2溶液保持飽和,有利于平穩持續產生H2S,故C正確;D.該實驗產生的尾氣不可用硝酸吸收,硝酸的氧化性雖然可以把H2S氧化為S單質,但是稀硝酸產生的NO或者濃硝酸產生的NO2,會污染空氣,故D錯誤;故選ABC. (6)氧化銅的質量為32. 814 g - 31. 230 g=1.584 g,則氧化銅物質的量為0. 0198 mol,根據銅元素守恒關系有:
CuS~Cu0
1 1
n 0. 0198 mol
硫化銅物質的量為0. 0198 mol,則H:S物質的量為0. 0198 mol,H2S的質量為0.6732 g,產品純度為0.06732g/0.680×100% =99%.
答案:(1)圓底燒瓶 (2)E→C→D (3)BC
(4)處理尾氣H2S (5)ABC (6)99%
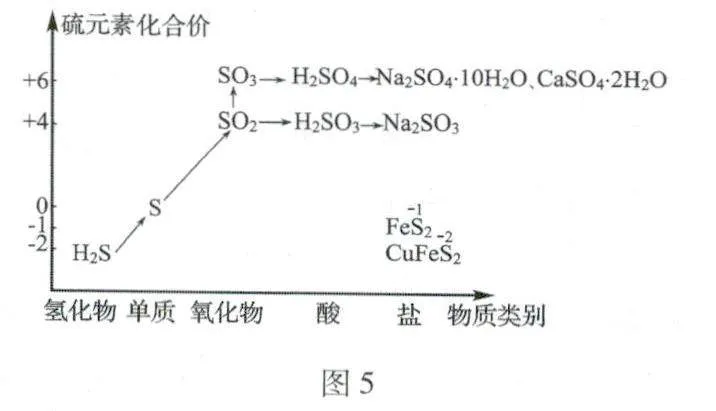
素養啟迪 1.從化合價角度理解硫化氫的還原性;硫及化合物轉化關系如圖5所示.
2.產品純度或者物質含量計算的要點:根據元素質量守恒法、關系式法、得失電子守恒法等,求出混合物中某一成分的質量,再除以樣品的總質量,即可得出其純度或者百分含量.
(收稿日期:2024 -06 - 16)

