嬰幼兒谷類輔助食品中亞硝酸鹽含量的測定
摘 要:由于嬰幼兒谷類輔助食品中含有淀粉類物質,導致其在前處理階段的樣液渾濁而影響亞硝酸鹽的準確測定。本文通過優化酶解過程和方法學驗證建立一種能準確測定嬰幼兒谷類輔助食品亞硝酸鹽含量的方法。結果表明,選擇α-淀粉酶,在70 ℃酶解14 min,可有效解決樣品濾液渾濁問題。亞硝酸鹽含量在0~
12.5 μg線性關系良好,回歸方程y=0.014 2x-0.000 1,相關系數r=0.999 8,加標回收率為91.0%~98.2%。該方法操作簡單,結果準確,可用于嬰幼兒谷類輔助食品中亞硝酸鹽含量的測定。
關鍵詞:嬰幼兒谷類輔助食品;亞硝酸鹽;淀粉酶
Determination of Nitrite Content in Cereal Complementary Foods for Infants and Young Children
LUN Qijing1,2, LUO Peiyan1,2
(1.Guangdong Food Industry Research Institute Co., Ltd., Guangzhou 511442, China;
2.Provincial Food Quality Supervision and Inspection Station, Guangzhou 511442, China)
Abstract: Due to the presence of starchy substances in cereal supplements for infants and young children, the sample solution becomes turbid during the pre-treatment stage, which affects the accurate determination of nitrite. This article establishes an accurate method for determining the nitrite content in infant cereal supplements by optimizing the enzymatic hydrolysis process and verifying the methodology. The results showed that selecting alpha amylase for enzymatic hydrolysis at 70 ℃ for 14 min can effectively solve the problem of turbidity in the sample filtrate. The nitrite had a good linear relationship between 0~12.5 μg, the regression equation y=0.014 2x-0.000 1, the correlation coefficient r=0.999 8, and the recovery rate was 91.0%~98.2%. This indicates that the method is simple to operate, accurate in results, and can be used for the determination of nitrite content in infant cereal supplements.
Keywords: cereal supplementary food for infants and young children; nitrite; amylase
亞硝酸鹽是一種在自然界中普遍存在的化合物,它可以在特定條件下由硝酸鹽還原形成。在食品工業中,亞硝酸鹽可以抑制微生物的生長,延長食品的保質期,經常被用作防腐劑[1]。嬰幼兒谷類輔助食品的生產過程和儲存條件通常可以保證產品的質量安全,不需要額外添加亞硝酸鹽來防腐。因此,嬰幼兒谷類輔助食品中存在的亞硝酸鹽通常不是有意添加的成分,可能是原料污染或加工過程中的交叉污染造成的[2-3]。
嬰兒由于身體尚未發育完全,腸道壁較薄,更容易吸收亞硝酸鹽,導致即使是微量的亞硝酸鹽也可能使嬰兒面臨中毒的風險。此外,亞硝酸鹽在體內可以轉化為亞硝胺,而亞硝胺是一種強烈的致癌物質,可能增加人體患食管癌、胃癌、肝癌和大腸癌等疾病的風險[4-7]。亞硝酸鹽的檢測方法包括高效液相色譜法[8-10]、離子色譜法[11-12]、分光光度法[13-14]等。目前,《食品安全國家標準 食品中亞硝酸鹽與硝酸鹽的測定》(GB 5009.33—2016)是國家強制性標準檢測方法。其中,第一法(離子色譜法)靈敏度高、準確性好,但其檢測成本較高,且檢測時間長;第二法(分光光度法)具有檢測速度快、適用范圍廣(涵蓋所有基質)、檢測成本低等優勢,是目前普遍使用的一種檢測方法。但由于嬰幼兒谷類輔助食品中普遍含有淀粉物質,采用GB 5009.33—2016中第二法(分光光度法)的前處理方法得到的濾液十分渾濁,甚至無法通過過濾來澄清,這導致無法正常進行比色,從而嚴重影響實驗結果的可靠性。針對這種情況,本文使用淀粉酶把淀粉物質分解,使樣液變澄清,從而確保實驗測定樣品亞硝酸鹽含量的準確性,為嬰幼兒谷類輔助食品的亞硝酸鹽測定提供技術支撐[15]。
1 材料與方法
1.1 材料與試劑
嬰幼兒谷類輔助食品1(樣品1)、嬰幼兒谷類輔助食品2(樣品2)、嬰幼兒谷類輔助食品3(樣品3)。亞鐵氰化鉀、乙酸鋅、硼酸鈉,均為分析純,佛山西隴化工有限公司;對氨基苯磺酸、鹽酸萘乙二胺,廣東翁江化學試劑有限公司;水中亞硝酸鹽標準物質(1 000 μg·mL-1),上海安譜璀世標準技術服務有限公司;α-淀粉酶、β-淀粉酶,默克制藥(江蘇)有限公司;實驗室用水由Milli-Q Integral 15純水機制備。
1.2 儀器與設備
FA2004十萬分之一電子天平;T9雙光束紫外可見分光光度計;電熱恒溫水浴鍋;Milli-Q Integral 15純水機。
1.3 實驗方法
1.3.1 實驗試劑配制
亞鐵氰化鉀溶液:稱取10.6 g亞鐵氰化鉀于100 mL容量瓶中,加水溶解后,定容至刻度。乙酸鋅溶液:稱取22.0 g乙酸鋅于100 mL容量瓶中,用3 mL冰乙酸溶解后,加水定容至刻度。飽和硼砂溶液:稱取10.0 g硼酸鈉,加入150 mL熱水,攪拌至完全溶解,冷卻,加水定容至200 mL。對氨基苯磺酸溶液:準確稱取0.2 g對氨基苯磺酸,溶于50 mL 20%鹽酸中,超聲振蕩10 min,于避光處儲存。鹽酸萘乙二胺溶液:準確稱取0.1 g鹽酸萘乙二胺,溶于50 mL水中,超聲振蕩10 min,于避光處儲存。
1.3.2 水中亞硝酸鹽儲備液配制
精確吸取0.5 mL水中亞硝酸鹽標準物質于100 mL容量瓶中,用水定容至刻度,制成5.0 μg·mL-1亞硝酸鹽溶液,現用現配。
1.3.3 標準曲線的測定
精確移取0 mL、0.2 mL、0.4 mL、0.6 mL、0.8 mL、1.0 mL、1.5 mL、2.0 mL和2.5 mL亞硝酸鹽標準使用液于50 mL比色管中,加入25.0 mL水,搖勻后,加入2.0 mL對氨基苯磺酸溶液搖勻,靜置5 min,加入1.0 mL鹽酸萘乙二胺溶液,加水定容至刻度后搖勻,靜置15 min,得到亞硝酸鹽質量為0 μg、1.0 μg、2.0 μg、3.0 μg、4.0 μg、5.0 μg、7.5 μg、10.0 μg和12.5 μg的溶液。以零管調節零點,以亞硝酸鹽含量為橫坐標,吸光度為縱坐標,用光程10 mm的比色皿于波長538 nm處測定吸光度并繪制標準曲線。
1.3.4 樣品測定
準確稱取2.50 g樣品于200 mL碘量瓶中,加水50.00 mL,搖勻后加入0.10 g淀粉酶和6.25 mL飽和硼砂溶液,搖勻。于70 ℃水浴加熱15 min后沸水浴15 min,取出冷卻至室溫。將樣液轉移至100 mL容量瓶中,加入2.50 mL亞鐵氰化鉀溶液,搖勻,靜置3 min后,加入2.50 mL乙酸鋅溶液,加水定容至100 mL,搖勻,靜置30 min后過濾,濾液備用。若樣品濾液自帶顏色,可加入少量活性炭,以減少其對比色的干擾[16]。吸取40.00 mL上述濾液于50 mL帶塞比色管中,加入2.0 mL對氨基苯磺酸溶液,靜置5 min,加入1.0 mL鹽酸萘乙二胺溶液,加水定容至刻度后搖勻,靜置15 min,待測,同時進行空白實驗。
1.3.5 重復性測定
對3種不同樣品各自重復稱量6次,按1.3.4的實驗方法測定樣品中亞硝酸鹽含量。
1.3.6 加標回收實驗
在已經稱量完成的碘量瓶中,對3個樣品進行3個濃度的加標,加標水平為1 mg·kg-1、5 mg·kg-1、25 mg·kg-1,按1.3.4方法進行加標樣品中亞硝酸鹽含量的測定并計算回收率。
2 結果與分析
2.1 淀粉酶種類及酶解時間的選擇
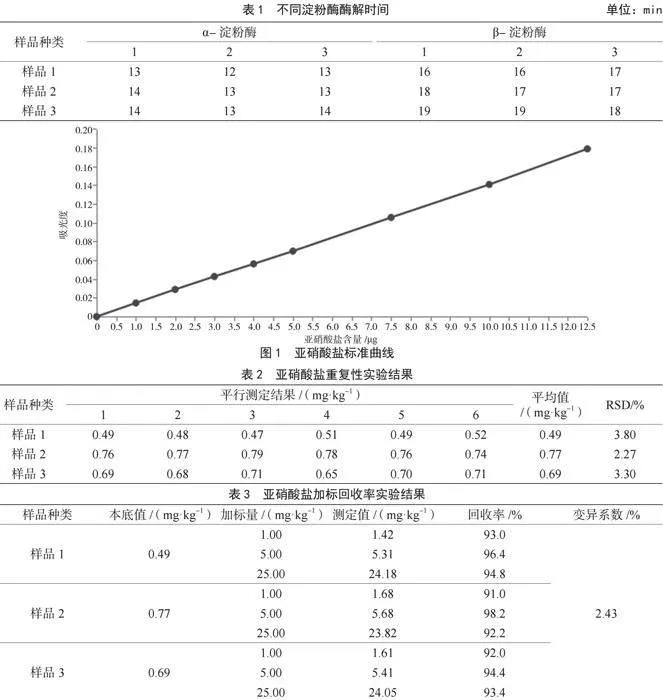
本研究選擇常見的2種淀粉酶(α-淀粉酶、β-淀粉酶)進行酶解。稱取樣品2.5 g于燒杯中,加入50 mL水和3 mL碘液混勻后,加入0.1 g淀粉酶。將燒杯分別置于α-淀粉酶和β-淀粉酶的最適溫度條件下進行反應,觀察藍色消失所需時間并記錄,對3個樣品各進行3次測定。由表1可知,兩種酶都能有效解決濾液渾濁的問題,但α-淀粉酶需要的酶解時間更短,且用時均≤14 min,說明樣品加入α-淀粉酶后,在最適溫度下14 min內能完全酶解樣品。本實驗使用的α-淀粉酶最適溫度為70 ℃,所以本實驗選擇用α-淀粉酶于70 ℃下酶解樣品14 min。
2.2 標準曲線
由圖1可知,亞硝酸鹽的線性回歸方程為y=0.014 2x-0.000 1,相關系數r=0.999 8,亞硝酸鹽在0~12.5 μg線性關系良好。
2.3 重復性實驗
由表2可知,3種樣品的相對標準偏差(Relative Standard Deviation,RSD)分別為3.80%、2.27%和3.30%,均小于5%,表明本方法測定結果穩定性好、重復性高。
2.4 回收率實驗
由表3可知,回收率在91.0%~98.2%,變異系數為2.43%,符合標準《實驗室質量控制規范 食品理化檢測》(GB/T 27404—2008)對實驗室內變異系數的要求(≤5.3%)。表明本方法檢測嬰幼兒谷類輔助食品中亞硝酸鹽含量具有良好的回收率和精密度。
3 結論
在嬰幼兒谷類輔助食品中,由于淀粉或其類似物質的存在,傳統的亞硝酸鹽測定方法難以應用。因此,本文探索了一種新的測定方法,即通過優化酶解處理過程以準確測定亞硝酸鹽含量。結果顯示,選擇α-淀粉酶,在70 ℃酶解14 min,可有效解決樣品濾液渾濁問題。而且通過方法學驗證,亞硝酸鹽在0~12.5 μg線性關系良好,回收率在91.0%~98.2%,重復性和穩定性好,精密度高,適用于準確檢測嬰幼兒谷類輔助食品中的亞硝酸鹽含量,可為嬰幼兒食品的質量安全提供技術參考。
參考文獻
[1]朱效兵,石晶紅.亞硝酸鹽與人體健康[J].河套大學學報,2007(4):66-69.
[2]趙永杰.關于亞硝酸鹽的來源、危害的討論[J].課程教育研究(新教師教學),2014(22):294-295.
[3]李婷.正確認識食物中的亞硝酸鹽[J].現代食品,2019(14):96-99.
[4]陳長宏,張科.食品中硝酸鹽和亞硝酸鹽的污染及預防[J].現代農業科技,2013(7):327.
[5]魏紅.食品中的亞硝酸鹽與人體健康[J].中國初級衛生保健,2004,18(3):59.
[6]徐銀,蓋圣美,劉登勇.食物中亞硝酸鹽的來源及其控制[J].農技服務,2008,25(9):168-169.
[7]徐國財.亞硝酸鹽與健康[J].新課程(教研),2010(8):406-407.
[8]沈龔鳴,龐貝妮,陸志蕓,等.高效液相色譜柱前衍生法測定乳制品中亞硝酸鹽的含量[J].包裝與食品機械,2019,37(6):63-67.
[9]陳國亮,厲志玉,汪志華.超聲萃取反相離子對高效液相色譜法測定食品中亞硝酸鹽和硝酸鹽含量[J].中國衛生檢驗雜志,2007,17(12):2151-2152.
[10]蔡志斌,張英,劉麗.高效液相色譜法快速測定乳粉中硝酸鹽和亞硝酸鹽[J].中國衛生檢驗雜志,2009,19(3):584-585.
[11]鄭小玲,郭小喜,李曉華,等.離子色譜法測定嬰幼兒米粉中硝酸鹽和亞硝酸鹽[J].食品研究與開發,2018,39(4):152-156.
[12]冷桃花,萬麗佳,施依文,等.乙腈沉淀-離子色譜法測定嬰幼兒米粉中硝酸鹽和亞硝酸鹽[J].食品安全質量檢測學報,2021,12(10):4095-4099.
[13]亢美娟,黃思棋,劉芳玉,等.嬰幼兒配方乳粉中亞硝酸鹽檢測方法的優化[J].中國乳品工業,2022,50(8):53-57.
[14]丁楊,鄧美榮,孫中華,等.嬰幼兒奶粉及米粉中亞硝酸鹽的檢測[J].黑龍江醫學,2016,40(11):1029-1030.
[15]張宓靈.分光光度法檢測乳制品中亞硝酸鹽的影響因素[J].中國標準化,2021(12):217-220.
[16]楊琳,許容年,秦志榮,等.嬰兒米粉中亞硝酸鹽測定前處理方法的改進[J].理化檢驗(化學分冊),2009,45(7):867.

