缺血修飾白蛋白在經皮冠脈介入治療術中的變化及意義
宋 濤,賈永平,呂吉元,范春雨,高宇平,王 睿
經皮冠脈介入治療(percutaneous coronary intervention,PCI)已成為冠心病一種有效的治療方法,但它畢竟是一種微創手術,可能會造成心肌微小損傷[1]。迄今為止,臨床常用肌鈣蛋白、心肌酶等作為心肌損傷的生化標記物。
近年來,缺血修飾白蛋白(ischemia modified albumin,IMA)作為心肌缺血的一種敏感性指標日益受到關注,是診斷心肌缺血的一個新的生化指標,具備理想標志物的特征[2]。IMA通過白蛋白-鈷結合試驗(ACB)測定。基于此基礎的ACB試驗有助于檢測心肌缺血。冠心病患者PCI術中心肌發生一過性缺血缺氧損傷,血液循環中IMA升高[3]。本研究探討冠心病患者PCI術所誘導的短暫性心肌缺血后12 h內IMA的變化,并將其與肌酸激酶同工酶(CK-MB)、心肌肌鈣蛋白I(cTnI)進行對比,分析這些生化指標在PCI術后的變化及意義。
1 資料與方法
1.1 病例選擇 2009年6月—2009年9月于我院行PCI的冠心病患者40例(PCI組),同期在本院行冠脈造影術(coronary angiography,CAG)證實為冠心病但未進行介入治療者20例(冠造組)。PCI組中急性心肌梗死穩定期25例,不穩定型心絞痛15例,其中合并高血壓25例,糖尿病10例,高脂血癥 15例,有吸煙史32例;年齡35歲~78歲(58.8歲±10.2歲),女9例,男31例。冠造組中急性心肌梗死穩定期10例,不穩定型心絞痛10例;合并高血壓12例,糖尿病 7例,高脂血癥 11例,有吸煙史9例;年齡34歲~77歲(56.9歲±10.9歲),女6例,男14例。兩組患者在性別、年齡、病情程度等方面無統計學意義。入選病例均除外肝、腎、肺、腦等疾病、妊娠、外周血管疾病、血液性及腫瘤性疾病,同時血漿白蛋白濃度(20~55)g/L。除冠狀動脈造影外,2周內無任何外傷及其他有創操作。
1.2 觀察指標 對接受PCI術的患者,術前2 d無心絞痛、惡性心律失常發作,術中詳細記錄球囊擴張總壓力、擴張次數、植入支架數、手術時間及有無胸痛、心律失常等發生,仔細比較術前和術后造影片,記錄有無內膜撕裂和夾層、分支血管阻塞等情況(由兩名經驗豐富的心臟病介入醫師決定球囊、支架的選擇和使用,并閱術前術后的造影片);術后3 d內觀察其有無心絞痛、心肌梗死、惡性心律失常等惡性事件的發生。
1.3 常規治療 以橈動脈為穿刺徑路行冠狀動脈造影及PCI治療的患者,術前5 d給阿司匹林100 mg,氯吡格雷75 mg,1次/日,低分子肝素鈣針4 100 U皮下注射,2次/日。術后氯吡格雷連續服用至少1年,阿司匹林長期服用。橈動脈穿刺成功后經動脈鞘管注入肝素3 000 U,支架植入前追加肝素至8 000 U~10 000 U,術中若出現冠脈痙攣,可注入硝酸甘油100 μ g~300μ g。采用Judkins6F指引導管,球囊預擴張后均給予支架植入術。
1.4 樣本采集及測定方法
1.4.1 樣本采集 PCI組,在PCI術前及術后30 min、6 h、12 h分別采血4 mL,放入肝素抗凝管中。冠造組僅在冠狀動脈造影術前及術后30 min、12 h采血,采集后2 h內分離血漿,分裝于-20℃冰箱保存備測,2d內測定cTnI和CK-MB濃度,擇期測定IMA。
1.4.2 IMA、cTnI及CK-M B測定方法 IM A由ACB試驗測定:測定血漿標本應無沉淀,無纖維蛋白凝塊和血細胞沉淀。取12 mm×100 mm試管2支,標明測定管和空白管,2管均加血漿 200 μ L,0.1%氯化鈷試劑(CoCl2?6H2O)50 μ L,輕輕搖勻,置室溫10 min,于測定管加二硫蘇糖醇(DTT)試劑 50 μ L,空白管加蒸餾水50 μ L,代替DTT試劑,輕輕搖勻,放室溫2 min,各加生理鹽水1.0 mL。于U-2001型號日本日立公司的紫外可見光分光光度計,470 nm波長,5 mm光徑比色皿,空白管調“0”,讀取測定管吸光度,將結果乘以2即為吸光度單位(ABSU)。氯化鈷試劑由Sigma-Aldrich公司提供,DTT試劑由上海生工公司提供。正常參考值:IM A<0.500。cTnI采用免疫比濁法測定:正常參考值 0~0.5 μ g/L;CK-M B采用免疫抑制法測定:正常參考值:0~25 U/L。兩者均采用日立7060全自動生化儀,嚴格按照試劑盒及儀器的要求操作。
1.5 統計學處理 用SPSS 13.0軟件分析。計量資料用均數±標準差(±s)表示,組內比較采用重復測量數據的方差分析。
2 結 果
2.1 PCI術結果 40例患者球囊擴張血管64支,植入支架79枚,所有手術患者無內膜撕裂和夾層、分支血管阻塞等情況,術后24 h內無心絞痛發作及心電圖改變。
2.2 IMA、cTnI及CK-MB測定結果 PCI組與冠造組術前IMA、cTnI及CK-MB均在正常參考值范圍以內。冠造組所有患者IM A、cTnI及CK-MB在術前、術后無明顯變化。PCI組IMA在 PCI術后30 min均較術前明顯升高(P<0.05),其中34例超過正常值(>0.5ABSU),在6 h漸降到正常范圍內,12 h基本恢復到基線水平;cTnI術后升高20例,6 h較術前明顯升高(>0.5 μ g/L),平均12 h達峰,但升高值不超過正常值的2倍,6 h、12 h與術前比較有統計學意義(P<0.05),且均發生在IMA升高的患者中;CK-MB術前術后均無明顯改變(P>0.05)。詳見表 1。
表1 PCI術前后血漿心肌損傷標志物變化(±s)
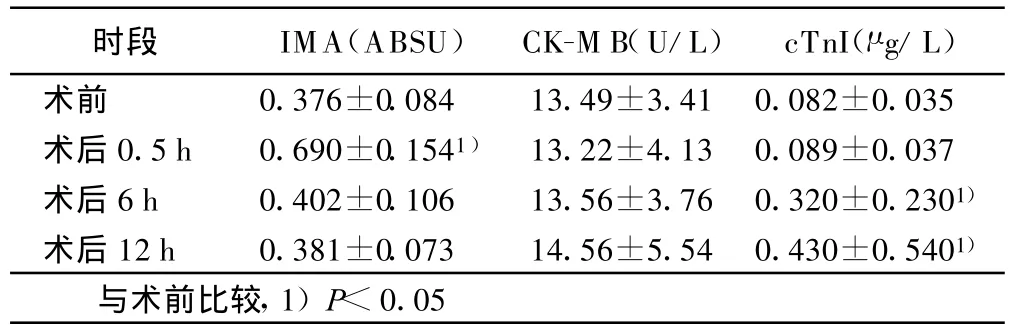
表1 PCI術前后血漿心肌損傷標志物變化(±s)
時段 IMA(ABSU)CK-M B(U/L)cTnI(μ g/L)術前 0.376±0.084 13.49±3.41 0.082±0.035術后0.5 h 0.690±0.1541) 13.22±4.13 0.089±0.037術后6 h 0.402±0.106 13.56±3.76 0.320±0.2301)術后12 h 0.381±0.073 14.56±5.54 0.430±0.5401)與術前比較,1)P<0.05
2.3 血漿IMA升高的相關因素 在40例中,回旋支病變14例,前降支35例,右冠 26例植入1個或更多個支架;PCI中 10例球囊擴張<2次,30例擴張≥2次。球囊擴張次數中位數是4,球囊總擴張壓為(16.77±7.84)atm。IMA在所有患者中,術后30min均較術前明顯升高(P<0.05),與術中擴張壓(r=0.482,P<0.01)和擴張次數(r=0.406,P<0.05)呈正相關。球擴壓越大、擴張次數越多,IMA升高越明顯。IMA升高水平與患者年齡、性別、處理的血管及冠心病的危險因素(如吸煙、糖尿病、高血壓和高脂血癥等)無關。
3 討 論
PCI在球囊擴張及支架植入時冠脈發生了短暫的急性閉塞,導致心肌缺血發生心肌微小損傷(M MD)。與M MD相關的機制主要有:PCI術中被擴張狹窄冠脈及其相關的側支短暫性閉塞[4];PCI術中出現的血管微顆粒,如斑塊微顆粒、血管內纖維物質的碎屑、血凝塊及膽固醇結晶等所致的微小栓塞有關;在球囊擴張過程中,由于暫時性冠脈血供與心肌代謝失衡,也可引起心肌缺血缺氧,致心肌微小損傷。僅靠臨床癥狀、體征和心電圖檢查難以發現,僅能通過靈敏的心肌缺血損傷標志物來診斷。CK-MB及cTnI是在心肌發生不可逆損傷壞死時出現,而IMA產生于心肌發生可逆損傷時。IM A產生機制可能是:人白蛋白N-Asp-Ala-His-Lys序列在PCI術中發生心肌缺血和/或再灌注時所致的缺氧、酸中毒、自由基損傷、膜鈉泵和鈣泵的破壞以及游離鐵和銅離子的暴露,使白蛋白N末端的結構發生變化,與過渡性金屬鈷離子結合的能力下降,從而使血液循環中的IMA升高[5,6]。本研究中,IMA在PCI術后30 min明顯升高,6 h漸降至正常,12 h恢復到基線水平;CK-MB術前術后無明顯變化;cTnI在術后6 h開始升高,12 h達高峰,升高值不超過正常值2倍,而且cTnI升高均發生在IMA升高組的患者中。這提示在PCI術中,血漿白蛋白經歷了與金屬鈷離子結合能力下降的過程,血液循環中IMA升高,并早于cTnI,是診斷心肌缺血的一個早期生化指標[7]。IMA升高也見于休克、終末期腎病和某些腫瘤患者,但不見于外傷、組織缺氧、骨骼肌缺血或外周血管疾病患者[8]。
本研究還發現,IMA升高與術中球囊擴張次數、擴張壓力呈正相關,這提示球囊擴張次數越多、擴張壓越大,心肌缺血缺氧程度也就越重,IMA升高水平也隨之越高;而與年齡、性別、高血壓、高血脂、血管病變支數和狹窄程度等因素無明顯相關。這說明在PCI術中,IMA值越高,PCI術的心肌缺血程度也越嚴重,是心肌損傷程度的一個生化指標,有助于評價PCI術對心肌的影響,但仍需更多的臨床研究來證實。
[1]Sala M,Mohd A,Samia H,et al.Minor myocardial injury after elective uncomplicated successful P TCA with or without stenting:Detection by cardiac troponins[J].Cathet Cardiovasc Interv,2005,53:188-192.
[2]Aparci M,Kardesoglu E,Ozmen N,et al.Prog nostic significance of ischemia modified albumin in patients with acute coronary syndrome[J].Coron Artery,2007,18(5):367-373.
[3]Sinha MK,Gaze DC,Tippins JR,et al.Ischemia modified albumin is a sensitive marker of myocardial ischemia after percutaneous coronary intervention[J].Circulation,2003,107(19):2403.
[4]李素姣,黃振文,陳磊,等 缺血修飾白蛋白在經皮冠狀動脈介入治療術中的變化及意義[J].實用診斷與治療雜志,2006,20(3):180-184.
[5]Bar OD,Lau E,Rao N,et al.Reduction in cobalt binding capacity of human album in with myocardial ischemia[J].Ann Emerg Med,1999,34(4 Suppl):56.
[6]Wu AH,Morris DL,Fletcher DR,et al.Analysis of the album in cobalt binding(ACB)test as an adjunct to cardiac troponin I fo r the early detection of acute myocardial infarction[J].Cardiovascular T oxicology,2001,1(2):147.
[7]Montagnana M,Lippi G,Volpe A,et al.Evaluation of cardiac laboratory markers in patients with systemic sclerosis[J].Clin Biochem,2006,39(9):913-917.
[8]Roy D,Quiles J,Sharma R,et al.Ischemia modified albumin concentrations in patients with peripheral vascular disease and exercise induced skeletal muscule ischemia[J].Clin Chem,2004,50(9):1656-1660.

