用氧化還原滴定法測定模擬炒菜時食鹽中碘含量
呂寶華,李玉珍,王 瑛
(1.運城學院應用化學系,山西運城 044000;2.運城學院機電公共實驗中心,山西運城 044000)
用氧化還原滴定法測定模擬炒菜時食鹽中碘含量
呂寶華1,李玉珍2,王 瑛1
(1.運城學院應用化學系,山西運城 044000;2.運城學院機電公共實驗中心,山西運城 044000)
采用氧化還原滴定法測定模擬炒菜時食鹽中碘的含量.結果表明,模擬炒菜樣品在經過不同高溫和加入佐料處理后,食鹽中的碘含量都或多或少地流失.該方法設備簡單,費用低,操作簡便,方法準確、可靠.
碘 食鹽 氧化還原滴定法
碘是人體內合成甲狀腺素所必需的微量元素.它與人的生長發育和新陳代謝密切相關,特別是對大腦的發育起著重要作用.人體攝入碘不足或過高,都會引起疾病.食鹽中的碘是以碘酸鉀形式存在,食鹽含碘量的測定方法很多[1],如分光光度法[2-5],原子吸收光譜法[6],流動注射電位法[7]等.這些方法各有特點,有些需使用昂貴的儀器,有些操作繁瑣.另外,在實際烹飪過程中,食鹽中的碘總會部分流失[8].因此,模擬炒菜過程中食鹽中碘含量的測定對我們如何合理用鹽具有重要的指導意義.為此,筆者根據在酸性條件下,IO3-易被I-還原生成I2,游離的I2遇淀粉顯藍色原理,以氧化還原滴定法[9]測定模擬炒菜時碘的含量.
1 材料與方法
1.1 儀器與試劑
電子天平;堿式滴定管.7.8×10-4mol/L碘酸鉀標準溶液:用電子天平稱取碘酸鉀 (KIO3,分析純) 0.165 8 g,溶于1 L容量瓶中,用蒸餾水稀釋至刻度,此溶液1 mL含100 μg碘;7.8×10-4mol/L碘化鉀溶液:用電子天平稱取碘化鉀 (KI,分析純)0.130 8g,溶于1 L容量瓶中,用蒸餾水稀釋至刻度.此溶液1 mL含100 μg碘;10 g/L淀粉溶液:用托盤天平稱取可溶性淀粉1.0 g,加入水5 mL攪拌成渾濁液,再緩慢倒入沸水95 mL,冷卻后即可使用;0.004 mol/L Na2S2O3溶液:用托盤天平稱取5.0 g Na2S2O3·5H2O,溶解于無CO2的蒸餾水中,儲存于500 mL棕色容量瓶中,用無CO2的蒸餾水稀釋至刻度,靜置一段時間后,用移液管取上清液50 mL于500 mL棕色容量瓶中,加入0.1 g硫酸鈉溶解后,用無CO2的蒸餾水稀釋至500 mL(待標定);食鹽(市售).
1.2 試驗原理
碘酸鉀中的IO3-在酸性條件下易被I-還原成I2:IO3-+5I-+6H+=3I2+3H2O(1);游離的I2遇淀粉顯藍色,用硫代硫酸鈉標準溶液滴定至藍色消失:I2+2S2O32-=2I-+S4O62-(2),結合(1)和(2),即:IO3-+6S2O32-+6H+=I-+3S4O62-+3H2O(3),根據硫代硫酸鈉標準溶液的用量計算碘的含量.
1.3 Na2S2O3標準溶液的標定
用移液管取10.00 mL配制好的7.8×10-4mol/L KIO3標準溶液,于250 mL碘量瓶中,加入1.00 mL mol/L H2SO4溶液,搖勻后加入5.00 mL 7.8×10-4mol/ L的KI溶液,立即用Na2S2O3標準溶液滴定,至溶液呈現淺黃色時,加5.00 mL 10g/L的淀粉溶液,繼續滴定至藍色恰好消失為止,記錄消耗的Na2S2O3標準溶液的體積,平行測定3次,求平均值.如果發現溶液變渾或析出硫,就應該過濾后再標定,或者另配溶液[10].
1.4 樣品碘含量分析
1.4.1 含碘食鹽中碘含量分析
稱取食鹽50.0 g,放入250 mL的碘量瓶中,加入90 mL蒸餾水,溶解后,加入1.00 mL 1mol/L H2SO4溶液,搖勻后加入5.00 mL 7.8×10-4mol/L的KI溶液,立即用Na2S2O3標準溶液滴定,至溶液呈現淺黃色時,加5.00 mL 10g/L的淀粉溶液,繼續滴定至藍色恰好消失為止,記錄消耗的Na2S2O3標準溶液體積,平行測定3次求平均值,然后根據公式:CI=CNa2S2O3×VNa2S2O3×21.17×1000/m樣品,即可求出碘鹽中碘的含量,CI的單位為mg/kg.
1.4.2 模擬炒菜時不同過程的樣品中碘含量分析
稱取4份50.0 g食鹽樣品,分別經過如表1所示的過程.其余操作同1.4.1.

表1 模擬炒菜時所得不同樣品的操作過程
2 結果與分析
2.1 Na2S2O3標準溶液的標定
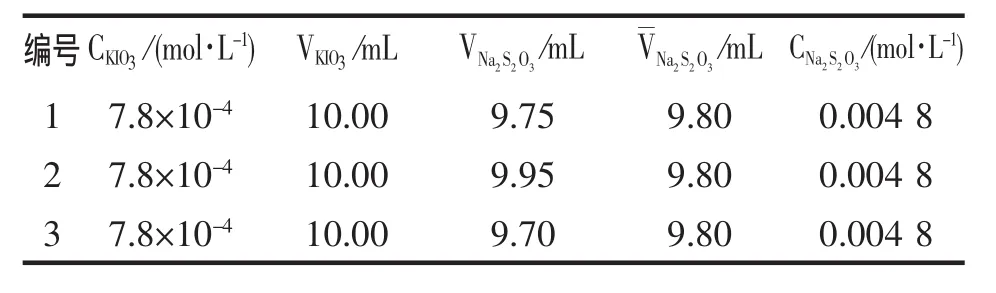
表2 Na2S2O3標準溶液的標定
經標定后測得 Na2S2O3標準溶液的濃度為0.004 8 mol/L,見表2.
2.2 佐料顏色對實驗的影響
氧化還原滴定法測定含碘食鹽中碘含量的時候,佐料醋、醬油的顏色會覆蓋氧化還原反應的顏色變化,無法確定反應是否發生和滴定是否到達終點,因此本實驗加入佐料應該為無色.
2.3 樣品分析結果
從表3可以看出,含碘食鹽及不同樣品中的碘含量的大小順序為:含碘食鹽>a>b>c>d.這表明,在沸水中,隨著時間的增加,碘鹽中的碘含量在逐漸減少;在相同的加熱時間條件下,加入佐料味精的樣品的碘含量要比沒有加入佐料的樣品低,說明佐料對碘鹽的損失產生了影響.
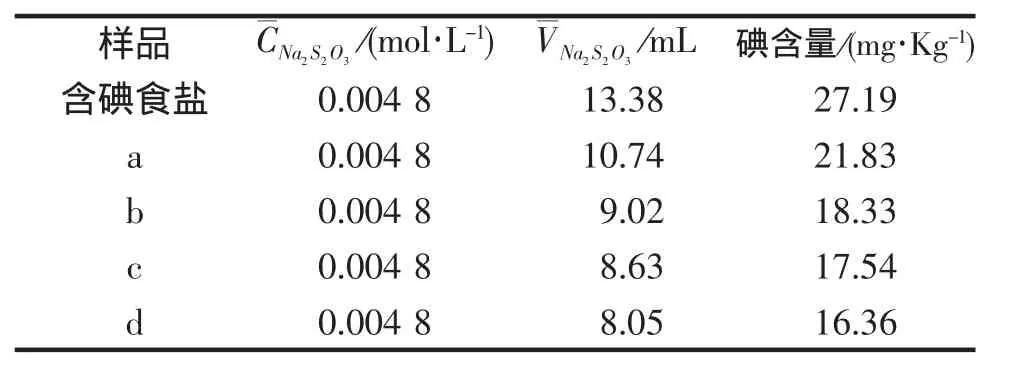
表3 含碘食鹽及模擬炒菜時所得不同樣品中碘含量測定結果
3 結論
碘鹽加熱時間的不同以及加入佐料,都會造成含碘食鹽碘含量的減少,引起碘的損失.
[1]李詠梅,李人宇.食品中碘含量分析方法研究進展[J].理化檢驗:化學分冊,2007,43(11):987-991.
[2]韓長秀,馮尚彩.二甲基黃褪色光度法測定微量碘[J].理化檢驗:化學分冊,2004,40(7):384-385.
[3]朱金坤,方艷夕.光度法測定食鹽碘含量的條件研究[J].安徽科技學院學報,2006,20(3):24-26.
[4]王末肖,高磊紅,劉春艷,等.吸光光度法測定碘酸鉀的研究[J].理化檢驗:化學分冊,2002,38(5):243-244.
[5]呂寶華,朱運德,王瑛.基于分光光度法的模擬炒菜時食鹽中碘含量測定[J].安徽農業科學,2009,37(31):15095-15096.
[6]孫漢文,孫智敏,張得強.火焰原子吸收光譜法間接測定碘[J].光譜學與光譜分析,2000,20(4):537-538.
[7]Saeed S B,Mohammad K A.A Simple and Selective Flow-Injection Potentiometric Method for Determination of Iodide Based on a Coated Glassy Carbon Electrode Sensor[J].Int J Electrochem Sci,2007(2):778-787.
[8]Wisnl C.Determination of Iodine Species Content in Iodized Salt and Foodstuff During Cooking[J].International Food Research Journal, 2008,15(3):325-330.
[9]譚江濤.食用鹽及品種鹽中碘測定方法的討論[J].中國井礦鹽,2009,40(3):33-35.
[10]武漢大學.分析化學[M].北京:高等教育出版社,2000:163-164.
Abstract:The iodine content of table salt in cooking simulation was determined by Oxidation-reduction titration.The results showed that after different cooking temperatures and adding seasoning of cooking simulation samples,all the iodine content of iodized salt was lost.
Key words:iodine;table salt;oxidation-reduction titration
〔編輯 楊德兵〕
Iodine Content Determination of Table Salt in Cooking Simulation Based on Oxidationreduction Titration
LU Bao-hua1,LI Yu-zhen2,WANG Yin1
(1.Department of Applied Chemistry,Yuncheng University,Yuncheng Shanxi,044000;2.Experimental Center of Electrical and Mechanical,Yuncheng University,Yuncheng Shanxi,044000)
O657.32
A
1674-0874(2010)05-0036-02
2010-07-12
運城學院院級科研項目[2009007]
呂寶華(1982-),男,山西文水人,碩士,研究方向:無機及分析材料性能測定.

