甘遂藥材有毒成分、有效成分及其質量控制標準研究現狀△
程顯隆,劉軍玲,肖新月*,馬雙成
(1.中國藥品生物制品檢定所,北京 100050;2.安徽省食品藥品檢驗所,安徽 合肥 230051)
甘遂藥材有毒成分、有效成分及其質量控制標準研究現狀△
程顯隆1,劉軍玲2,肖新月1*,馬雙成1
(1.中國藥品生物制品檢定所,北京 100050;2.安徽省食品藥品檢驗所,安徽 合肥 230051)
綜述了甘遂的化學成分、生物活性、分析方法及其質量標準方法的研究進展,為更深入研究開發甘遂及建立安全有效質量標準提供理論依據。
甘遂;化學成分;生物活性;分析方法;質量標準
甘遂始載于 《神農本草經》,列為下品。現行《中國藥典》收載的甘遂為大戟科(Euphobiaceae)大戟屬(Euphorbia)植物甘遂 Euphorbia kansui T.N.Liou ex T.P.Wang的干燥塊根。性寒,味苦;有毒。具有瀉水逐飲的功能。用于水腫脹滿,胸腹積水,痰飲積聚,氣逆咳喘,二便不利[1]。通常認為其毒性較強,臨床使用劑量十分有限,過量則引起腹痛、腹瀉,嚴重時會出現劇烈嘔吐、血壓下降、脫水和呼吸衰竭等癥狀。炮制后可降低其毒性,緩和峻瀉作用[2]。現代研究表明,甘遂化學成分具有抗癌抗腫瘤活性、抗生育、抗病毒、抗胰腺炎等作用,可影響免疫系統的特異性[3]。由于 《中國藥典》(2005年版)甘遂項下只收載了性狀、顯微鑒別、薄層鑒別、水分、灰分、浸出物項,無法有效控制其質量,為此我們開展了甘遂的有毒成分、有效成分及其檢測方法和甘遂藥用安全性、有效性的質量控制標準研究。本文就甘遂的化學成分及其生物活性的研究進展、質量評價標準情況進行綜述。
1 甘遂化學成分研究
甘遂主要含有巨大戟二萜醇型(Ingenane)、假白欖酮型(Jatrophane)二萜類化合物,大戟醇型(Euphane)、甘遂醇型(Triucallane)三萜類化合物及其他成分[3]。
1.1 二萜類成分
1.1.1 巨大戟烷型二萜類化合物 巨大戟烷型二萜醇型化合物(化合物1~28)多為13-Oxyingenol(13-氧化巨大戟萜醇)和20-Deoxyingenol(20-去氧巨大戟萜醇)的衍生物,屬于多氧二萜化合物,其基本母核是由5/7/7/3 4個環稠合而成,C-8和 C-10間通過酮基橋而連接[4],C-1,2的雙鍵存在于B環,C-4為β-羥基,A/B環為反式駢環一個環丙烷構成D環。化合物1~28的結構式見圖1。
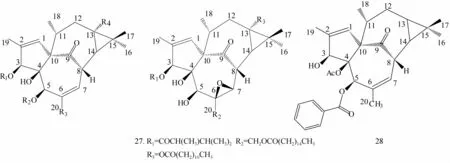

圖1 化合物1~28的結構圖
1.1.2 假白欖酮型二萜類化合物 假白欖酮型二萜類化合物(化合物29~37)也是甘遂中的二萜類成分之一,多為一個5元環與一個12元環駢合在一起而形成,同時某些位置的羥基形成醚或酯橋。化合物29~37的結構式見圖2。
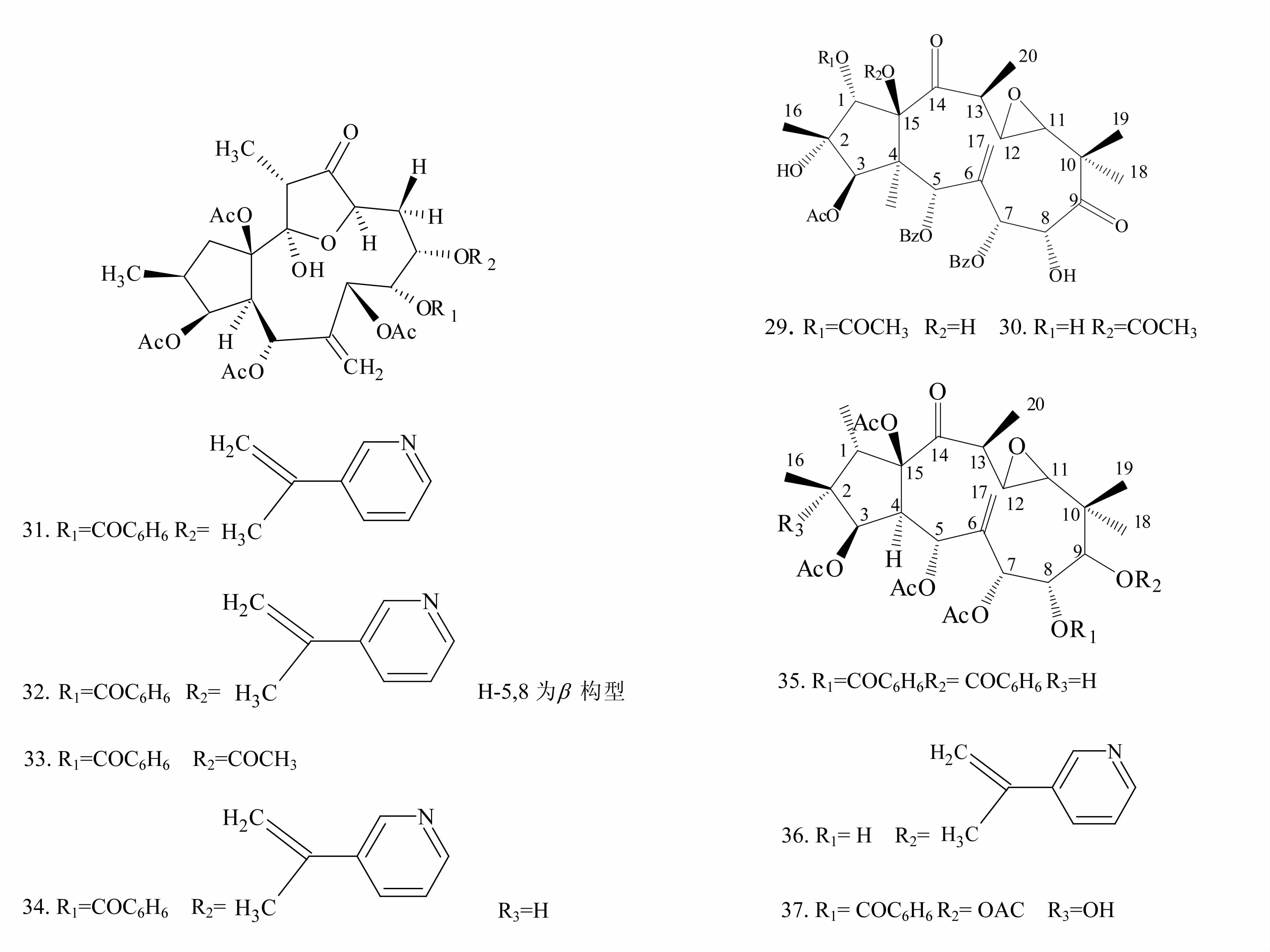
圖2 化合物29~37的結構圖
甘遂中的二萜類成分匯總見表1。
1.2 三萜類化學成分
三萜類化合物(38~44)均為四環三萜類化合物,分為兩種類型,Euphane型化合物和Ttirucallane型化合物。二者區別在于21位甲基取向為α的為Euphane型,21位甲基取向為β的為Tirucallane型。通常在17位的長側鏈上有雙鍵,羰基出現在7位時,在8,9位出現雙鍵。化合物39~44的結構式見圖3。
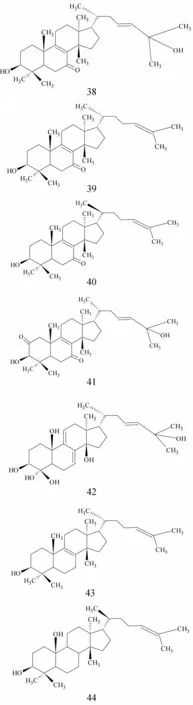
圖3 化合物39~44的結構圖

表1 甘遂中的二萜類成分
甘遂中三萜類成分見表2。

表2 甘遂中的三萜類成分
1.3 其他類成分
王立巖等[11]還從甘遂分離得到了 Stigmast-5-ene-3β,7β-diol和 Stigmast-5-ene-3β,7α-diol,異東莨菪素(Isoscopoletin),β-谷甾醇(β-sitosterol)。此外甘遂中還含有棕櫚酸(Palmitic acid)、檸檬酸(Critic acid)、草酸(Oxalic acid)、鞣質、樹脂等[3]。
2 甘遂化學成分的生物活性研究
2.1 三萜類成分的生物活性
從甘遂引產有效成分的研究中,發現從甘遂中分離得到的大戟腦(mp116~117℃ )均有興奮子宮的作用[26]。
甘遂中的三萜成分具有阻止細胞分裂的功能[27],其中7位有酮羰基的化合物表現出了一定的細胞分裂抑制活性和很強的NO抑制活性,如Kansenone;而7位無酮羰基的化合物沒有表現出明顯的細胞分裂抑制活性,如大戟二烯醇。但是Epi-Kansenone在30μg·mL-1時表現明顯的細胞毒性,而Kansenonol則沒有表現出明顯的細胞毒性,推測可能是由于該化合物側鏈上25位羥基的存在造成毒性降低[11]。
Yasukawa K等[24]從甘遂中分離出13種三萜類成分,這些成分均具有抗腫瘤的活性,其中以大戟二烯醇的活性最強。
大戟二烯醇對血壓有調節作用。其對麻醉后血壓正常的狗及小鼠具有降血壓的作用;對使用過阿托品、安替斯丁、β-阻斷劑等降壓藥物的狗及頸動脈竇切除的動物未產生降壓作用,對脊柱切斷、內臟去除、神經中樞阻斷的狗的降血壓作用增強。小鼠靜脈注射大戟二烯醇的半數致死量為1 500mg·kg-1,小鼠口服大戟二烯醇的半數致死量為 2g·kg-1[28]。
2.2 二萜類成分的生物活性
2.2.1 抑制細胞分裂的活性 王立巖等[5]利用蛙卵動物極細胞分裂抑制活性實驗,對從甘遂中分離得到的12種二萜醇類化合物進行了測試,認為其中9個巨大戟二萜醇型化合物和1個假白欖酮型化合物Kansuinin B具有抑制細胞分裂活性。
2.2.2 抗驅線蟲活性 甘遂中的3個巨大戟二萜醇型化 合 物,20-O-acetyl-3-O-(2′E,4′Z-decadienoyl)ingenol、20-O-acetyl-5-O-(2′E,4′Z-decadienoyl)ingenol、3-O-(2′E,4′Z-decadienoyl)ingenol具有抗驅線蟲活性[6]。
2.2.3 抗病毒活性 甘遂中的二萜醇類化合物,如KansuiphorinA、KansuiphorinB[29],甘遂大戟萜酯 A,13-十一酰基-3-(2,4-二甲基丁酰基)巨大戟萜酯,3-(癸-2,4-二烯酰基)巨大戟萜酯及甘遂萜酯A[30]具有抗病毒的活性,且這種活性與C-3和C-20位有無酰化基團的存在有關。這些成分的體內抗病毒活性可能是通過刺激淋巴細胞的增殖,增強殺傷病毒感染細胞能力來實現[31]。另外,發現甘遂醇提物中的巨大戟二萜醇型二萜酯類化合物有很強的抑制人類免疫缺陷病毒(HIV)增殖作用[32]。
2.2.4 抗癌和抗腫瘤活性 從甘遂中分離得到的兩個巨大戟二萜醇型二萜酯[20],甘遂大戟萜酯A及甘遂大戟萜酯 B,對白血病(HL-60TB)、肺癌(H-322)、結腸癌(SW-620)、黑色素瘤(SK-MEL-5)和腎臟癌細胞(A-498)等某些人體癌細胞有選擇性細胞毒作用。二萜醇類化合物的酯酰化取代基是影響其抗癌活性強度的主要官能團[33]。Yu FR[34]研究了從甘遂中提取得到的甲酯及其衍生物對于人胃癌細胞株(SGC-7901)的細胞凋亡和細胞周期的作用;其中6種甲酯及衍生物能夠導致癌細胞生長抑制和凋亡。
2.2.5 對免疫系統作用 從甘遂中得到的3-O-2,3-二甲基丁酰基13-O-癸酰基巨大戟二萜醇對免疫性疾病具有潛在的治療作用,是通過抑制IgE引導的肥大細胞的活化作用來實現的[35]。甘遂水煎劑醇沉物能使小鼠胸腺減輕和脾臟加重,能明顯抑制小鼠抗羊紅細胞(SRBC)抗體產生,提示甘遂對免疫系統有明顯的抑制作用[36]。甘遂的熱水提取物能提高免疫復合物(GAG)與巨噬細胞的結合能力。從甘遂中分離得到的 3-O-(2′E,4′Z-癸二烯酰基)巨大戟二萜醇及3-O-(2,3-二甲基丁酰基)-13-O-十二烷酰基巨大戟二萜醇能提高免疫復合物GAG(葡萄糖氧化酶-抗葡萄糖氧化酶復合物)與巨噬細胞的結合能力,且表現出量效關系[37-38]。
2.2.6 抗生育作用 王秋靜等[36]對復方甘遂制劑宮內給藥終止動物中期妊娠及毒性進行了研究,認為甘遂藥材和復方皆對小鼠有終止中期妊娠作用。
從甘遂中提取得的巨大戟二萜醇對非洲蟾蜍胞胚期的細胞分裂有明顯的抑制作用,同時也能抑制拓撲異構酶Ⅱ的活性。修彥鳳等[38]認為甘遂終止妊娠的首要機制不是增加子宮收縮,而可能是對滋養細胞的選擇性損害。
2.3 甘遂的急性長期毒性實驗
韓向陽[39]研究發現,家兔連續給藥7d(10mg·kg-1),第8天處死病檢,心肝腎有一定的中毒性組織學改變。王秋靜等[36]認為甘遂的急性長期毒性實驗,雖然對心、腎顯示出一定的病理變化,但均為變性改變,屬于可逆性病理變化。
3 甘遂化學成分的分析方法研究
任樹林等[40]研究甘遂在炮制前后化學成分的整體變化,以揭示炮制減毒、增效的物質基礎,結果發現甘遂經過炮制后水煎液和醇提取液中,有的成分含量顯著下降甚至消失,有成分的含量顯著上升,還有新成分出現。作者認為甘遂炮制增效、減毒的物質基礎可能是有毒成分的消失或含量減少,這些消失或含量減少的成分轉變成了新成分或者在水中溶解度小而在醇中溶解度大的成分。
束曉云等[41]建立了甘遂飲片及其炮制品的指紋圖譜。采用HPLC法,以胡薄荷酮作為內標參照品,乙腈-水為流動相梯度洗脫,結果甘遂飲片及其醋制品共有17個共有峰。炮制品與生品比較,有2種成分含量增加約40%左右,1種成分含量減少達70%;17個共有峰的相似度均在0.95以上。
修彥鳳等[42]比較甘遂炮制前后成分的變化,以3-O-(2,3二甲基丁酸基)-13-O十一烷酸基巨大戟二萜醇為對照,建立生、制甘遂的HPLC-ELSD特征指紋譜并進行比較,結果發現在選定的色譜條件下,生、制甘遂的特征色譜峰分別為31、19個;甘遂炮制后大部分成分含量下降;不同成分間的含量比例有變化,成分的種類沒有變化。
張麗等[43]建立了以甘遂的毒效成分之一3-O-(2′E,4′Z-癸二烯酸基)-2-O-乙酰基巨大戟二萜醇為指標的HPLC測定法,用于考察醋甘遂飲片的最佳炮制上藝。
本課題組[44]對甘遂中含有的2個有效成分大戟二烯醇及其同分異構體表大戟二烯醇含量測定方法進行了研究,建立了HPLC法,同時測定兩成分的含量。
4 安全性和質量相關標準情況[1]
《中國藥典》1963年版一部收載的甘遂為大戟科(Euphobiaceae)植物甘遂Euphorbia sp.的干燥根。均系野生,主產于陜西、山西、河南等地。藥材檢測項只有性狀項;并規定 “以肥大飽滿、表面潔白或黃色、細膩、斷面粉性足、無纖維為佳。”
《中國藥典》1977年版一部,收載的甘遂來源改為大戟科植物甘遂Euphorbia Kansui T.N.Lion ex T.P.wang.的干燥塊根。將性狀項下修訂為 “以肥大、色白、粉性足者為佳”,并增訂了粉末顯微鑒別項。《中國藥典》1985年版、1990年版、1995年版、2000年版未作修訂。《中國藥典》2005年版增訂了以甘遂對照藥材為對照的薄層色譜鑒別項,增訂了水分、總灰分、酸不溶性灰分檢查項和浸出物測定項。
國務院1988年12月27日發布的 《醫療用毒性藥品管理方法》中規定,毒性中藥管理品種常用劑量:生甘遂0.5~1g。現行 《中國藥典》甘遂標準【用法用量】項下規定 “0.5~1.5g,炮制后多入丸散用”。
5 討論
總之,目前對甘遂的化學成分研究報道較多。研究表明甘遂的化學成分主要是二萜類和三萜類化合物。目前活性研究主要是針對單體化學成分進行的。其中,二萜類化合物有較強的刺激作用,也有抗腫瘤作用;提示其毒性成分與有效成分之間有一定的內在聯系。三萜類成分也是有效成分,但未見毒性方面的報道。另外,現代毒理學研究結果表明,甘遂的毒性是可逆的。提示我們在毒性藥材研究中,既要繼承,也要以科學、辨證的態度進行驗證,不盲從古人的說法。開展甘遂毒性及有效成分研究,制定相關安全與有效性標準,極為重要。
[1]國家藥典委員會.中國藥典(一部)[S].北京:化學工業出版社,2005:60.
[2]葉定江.中藥炮制學[M].上海:上海科學技術出版社,1996:248.
[3]郭曉莊.有毒中草藥大辭典[S].天津:天津科技翻譯出版公司,1992:739.
[4]Evan F J,Taylor S E.Progress in the Chemistry of Organic Natural Products[M].NY:Springer-Verlag,1983,44:1-99.
[5]Wang LY,Wang NL,Yao XS,et al.Diterpenes from the roots of Euphorbia kansuiand their in vitro effects on the cell division of Xenopus[J].J Nat Prod.,2002,65(9):1246-1251.
[6]Shi JX,Li ZX,Nitoda T,et al.Three antinematodal diterpenes from Euphorbia kanbsui[J].Biosci Biotechnol Biochem,2007,71(4):1086-1089.
[7]Matsumoto T,Cyoun JC,Yamada H.Stimulatory effects of ingenols from Euphorbia kansuion the expression ofmacrophage Fc receptor[J].Planta Med.,1992,58:255-258.
[8]Shi J.G,Jia Z.J,Yang.L.Lathyrance and ingenane diterpenoids from Euphorbia micractina[J].Planta Med.,1994,60:588-589.
[9]潘勤,閔知大.甘遂中巨大戟萜醇型二萜酯類化學成分的研究[J].中草藥,2003,34(6):489-492.
[10]Bernd S.,Erich H..Chemisty of ingenol.Ⅱ.Esters of ingenol and 7,8-isoingenol.Zeitschrift fuer Naturforschung,Teil B:Anorganische Chemie[J].Organische Chemie,1982,37B(6):748-756.
[11]王立巖.甘遂的化學成分及其生物活性研究[D].沈陽:沈陽藥科大學博士學位論文,2000.
[12]Uemura D.,Ohwaki H.,Chen Y.,et al.Isolation and structures of 20-deoxyingenol new diterpene,derivatives and ingenol derivative obtained from kansui[J].Tetrahedron Lett,1974,(29):2527-2528.
[13]Wang LY,Wang NL,Yao XS,et al.Diterpenes from the roots of Euphorbia kansui and their in vitro effects on the cell division of Xenopus(part 2)[J].Chem Pharm Bull(Tokyo),2003,51(8):935-941.
[14] Ott HH.,Hecker E..Highly irritant ingenane type diterpene esters from Euphorbia cyparissias L[J].Experientia,1981,37:88-91.
[15]Wu TS,Lin YM,Haruna M,etal.Antitumor agents,119.Kansuiphorins A and B,two novel antileukemic diterpene esters from Euphorbia kansui[J].JNat Prod.,1991,54(3):823-829.
[16]Pan D.J,HU C.O,Chang J.j,et al.Kanuiphorin C and D cytotoxic diterpenes from Euphorbia Kansui[J].Phytocehmistry,1991,30:1018-1020.
[17]王玉波,李穎玉,王紅兵,等.甘遂的化學成分[J].中國天然產物,2007,5(3):182-185.
[18]LiCF,Wang JH,Cong Y,etal.A new diterpene from the processed roots of Euphorbia Kansui[J].JAsian Nat prod Res.,2008,10(1-2):101-104.
[19]Uemura D,Kitayama C.K,ansuinin B.A novel multioxygenated diterpene from Euphorbia Kansui Liu[J].Tetrahedron Lett,1975,(10):1703-1706.
[20]陳云利,袁丹,徐鑫.甘遂中麻風樹烷型大環二萜類化學成分的研究[J].中國中藥雜志,2008,33(15):1836-1839.
[21]Pan Q,Ip Fc,Ip NY,et al.Activity of macrocyclic jatrophane diterpenes from Euphorbia kansui in a TrkA fibroblast survival assay[J].JNat Prod.,2004,67(9):1548-1551.
[22]Bernd S,Erich H.Chemisty of ingenol.Ⅱ.Esters of ingenol and 7,8-isoingenol.Zeitschrift fuer Naturforschung,Teil B:Anorganische Chemie[J].Organische Chemie,1982,37B(6):748-756.
[23]GewallMB,HattoriM,Tezuka Y,etal.Constituents of the latex of Euphorbia antiquorum[J].Phytochemistry,1990,29:1625-1628.
[24]Yasukawa K,Akihisa T,Yoshida ZY,et al.Inhibitory effect of euphol,a triterpene alcohol from the roots of Euphorbia kansui,on tumour promotion by 12-O-tetradecanoylphorbol-13-acetate in two-stage carcinogenesis in mouse skin[J].J Pharm Pharmacol,2000,52(1):119-124.
[25]Itoh T,Tamura T,Matusumoto T,et al.A new triterpene alcohol from tea seed oil[J].Lipids,1975,11(6):434-441.
[26]陳希琛.甘遂引產成分的初步研究[J].藥學通報,1982,17(6):43.
[27] Wang LY,Wang NL,Yao XS,et al.Euphane and tirucallane triterpenes from the roots of Euphorbia kansui and their in vitro effects on the cell division of Xenopus.J Nat Prod[J].2003,66(5):630-633.
[28] Singh G.B.,Singh Surjeet,Sharma M.L.,et al.Hypotensive activity of 8,24-euphadien-3β-ol(euphol)[J].Panta Med.,1989,55(6):498-500.
[29]ZhengWF,Cui Z,Zhu Q.Cytotoxicity and antiviralactivity of the compounds from Euphorbia kansui[J].Planta Med.,1998,64:754-756.
[30]鄭維發.甘遂醇提物中4種二萜類化合物的體內抗病毒活性研究[J].中草藥,2004,35(1):65-68.
[31]鄭維發,陳才法,朱愛華.甘遂醇提物抗流感病毒FM1有效部位的篩選[J].中成藥,2002,24(5):362-365.
[32]Fujiwara M,Ijichi K,Konno K,et al.Ingenol Derivatives,Ingredient of Kansui are Highly Potent Inhibitor of HIV[J].Antiviral Res.,1995,26(3):228.
[33]史海明,閔知大,屠鵬飛,等.中國大戟屬植物中二萜成分的化學及生物活性[J].化學進展,2008,20(2/3):375-385.
[34]Yu FR,Lian XZ,Guo HY,et al.Isolation and characterization of methyl esters and derivatives from Euphorbia kansui(Euphorbiacead and their inhibitory effects on the human SGC-7901 cells[J].JPharm Sci,2005,278(3):528-535.
[35]Nunomura S,Kitanak S,Ra C.3-O-(2,3-dimethylbutanoyl)-13-O-decanoylingenol from Euphorbia kansui suppresses IgE-mediatedmast cell activation[J].Biol Pharm Bull,2006,29(2):286-290.
[36]王秋靜,于曉風,劉宏雁,等.復方甘遂制劑宮內給藥終止動物中期妊娠及毒性實驗[J].白求恩醫科大學學報[J],1994,20(5):461-463.
[37]Matsmnoto T,Cyoun JC,Yamada H.Stimulatary effects of ingenols from Euphorbia kansui on the expression ofmacrophage Fc recepter[J].Planta Med,1992,58(3):255-258. [38]修彥鳳,曹艷華,張永太.甘遂的藥理作用研究進展[J].上海中醫雜志,2008,42(4):79-81.
[39]韓向陽.甘遂的毒性研究 [J].醫學研究通訊,1980,(5):8.
[40]任樹林,張楠楠,劉竹蘭,等.甘遂炮制前后整體化學成分變化的研究 [J].中藥材,2007,30(6):639-641.
[41]束曉云,丁安偉,張麗,等.內標法研究甘遂及其炮制品的指紋圖譜 [J].廣東藥學院學報,2007,23(6):638-640.
[42]修彥鳳,吳弢,王海穎,等.HPLC-ELSD指紋譜法研究甘遂炮制前后成分差異 [J].中成藥,2009,31(2):249-252.
[43]張麗,束曉云,唐于平,等.醋甘遂飲片炮制工藝研究[J].中國中藥雜志,2009,34(6):681-683.
[44]程顯隆,肖新月,李廣華,等.甘遂中大戟二烯醇及其同分異構體表大戟二烯醇的含量測定 [J].藥物分析雜志,2009,29(9):4-7.
國家科技支撐計劃項目(2006BAI14B01)——常見與重要藥品安全標準研究
*肖新月,Tel:(010)67095432,E-mail:xiaoxy@nicpbp.org.cn
2010-01-14)

