響應面法優化鯽魚魚鱗酸溶性膠原蛋白提取工藝
朱秀靈,戴清源,蔡為榮,王 建
(安徽工程科技學院生物化學工程系,安徽蕪湖241000)
響應面法優化鯽魚魚鱗酸溶性膠原蛋白提取工藝
朱秀靈,戴清源,蔡為榮,王 建
(安徽工程科技學院生物化學工程系,安徽蕪湖241000)
在單因素實驗基礎上,采用響應面法對影響酸溶性膠原蛋白(acid-soluble collagen,ASC)提取效果的3個因素即乙酸濃度、液料比和提取時間進行了優化,建立并分析了各因素與ASC得率關系的數學模型。結果表明:ASC最佳提取工藝條件為:乙酸濃度0.41mol/L,液料比12mL/g,提取時間54.81h,在此工藝條件下,ASC最高得率(以干基計)理論值為20.97%,而實測值可達20.68%,與理論預測值相比,相對誤差為1.38%。ASC的相對溶解度在pH4時最大,當NaCl濃度低于3%(mg/mL)時,ASC的相對溶解度基本不變,當NaCl濃度大于3%(mg/mL)時,相對溶解度迅速降低,但都在40%以上。
酸溶性膠原蛋白,響應面法,優化,魚鱗
膠原蛋白不僅是構成生物體的重要成分(如動物皮膚、骨骼、肌腱、韌帶、軟骨及血管等)[1],而且作為原料已被廣范應用到食品、醫藥及化妝品等眾多領域[2-3]。膠原蛋白的主要來源最初僅限于陸生動物如牛、豬等的骨骼和皮膚[4]。然而,近幾年來,由于瘋牛病及口蹄疫等疾病的爆發使人們對這些來源的膠原蛋白的安全性甚是擔憂[5]。歐美、日本等國家相繼出臺了不少法規,限制從牛等哺乳動物皮骨中的提取物用于食品、醫藥等對人體直接影響的產品中[6]。另外,來源于豬的膠原蛋白由于宗教信仰問題,其應用也受到限制[7]。基于此,必須尋找新的膠原蛋白來源。魚類加工副產物——皮膚、骨、魚鱗等富含膠原蛋白,以此為原料提取膠原蛋白的報道較多,但大多以深海魚類為主,而以淡水魚魚鱗為原料的報道尚少[8]。本實驗以淡水魚鯽魚魚鱗為原料,采用傳統的酸法提取工藝,利用響應面分析法對酸溶性膠原蛋白(acid-soluble collagen,ASC)提取工藝進行優化,并初步探討pH及NaCl濃度對ASC溶解度的影響。
1 材料與方法
1.1 材料與儀器
魚鱗 購于本地集貿市場,活魚屠宰后的魚鱗用清水洗凈,真空干燥(25℃),粉碎過80目篩,4℃保存,備用;乙二胺四乙酸二鈉(EDTA-2Na)、乙酸、鹽酸、檸檬酸、乳酸、氯化鈉等 均為國產分析純;牛血清白蛋白(BSA) 廣州蕊特生物科技公司。
SP-754型紫外分光光度計 上海光譜儀器有限公司;DZX-型(60508)真空干燥箱 上海福瑪實驗設備有限公司;L-550臺式大容量離心機 湘儀離心機有限公司;PHS-2C數顯酸度計 上海雷磁儀器廠。
1.2 實驗方法
1.2.1 鯽魚魚鱗中ASC的提取工藝流程 魚鱗粉(質量m1,g)→堿液處理→脫脂→脫鈣→酸解→鹽析→透析→真空干燥(質量為m2,g)
具體操作參照文獻[3,9]進行,則 ASC得率η(%,以干基計)=m2/m1×100%。
1.2.2 響應面法優化提取工藝 應用Box-Behnken中心組合方法進行三因素三水平的實驗設計。在單因素實驗基礎上,以酸液濃度,液料比,提取時間3個因素為自變量,分別以x1、x2、x3表示,按方程Xi=(xi-x0)/△x對自變量進行編碼(Xi為自變量的編碼值,xi為自變量的真實值,x0為實驗中心點處自變量的真實值,△x為自變量的變化步長)。并以自變量的編碼值+1、0、-1分別代表自變量的高、中、低水平,ASC得率Y為響應值,實驗自變量因素編碼及水平見表1。

表1 實驗因素編碼及水平表
1.2.3 紫外可見光譜分析 準確稱取一定質量的ASC溶于0.02mol/L乙酸水溶液,得到2mg/mL ASC溶液[10-11]。在波長范圍190~400nm下測定其吸光度,記錄最大吸收波長。
1.2.4 ASC溶解度實驗 參照文獻[10,12-13]進行,先用0.5mol/L乙酸溶解膠原蛋白配制成質量濃度分為3mg/mL和6mg/mL的膠原蛋白溶液。然后分別考察 pH及 NaCl濃度對膠原蛋白溶解度的影響。
1.2.4.1 pH對ASC溶解度的影響 取10支離心管,各加入 8mL 3mg/mL的 ASC溶液,并用 6mol/L NaOH或6mol/L HCl溶液調節pH分別為1.0、2.0、3.0、4.0、5.0、6.0、7.0、8.0、9.0和10.0,然后加入蒸餾水(將其pH調整到與膠原蛋白pH相同)至溶液體積為10mL,磁力攪拌 30min后進行離心(30min,1000r/min)。測定上清液中蛋白質含量(mg/mL),計算ASC相對溶解度。
1.2.4.2 NaCl濃度對ASC溶解度的影響 將NaCl溶解于0.5mol/L乙酸中,制得質量濃度分別為0%、2%、4%、6%、8%、10%、12%(mg/mL)的NaCl溶液。分別取5mL不同質量濃度的NaCl溶液于離心管中,各加入5mL 6mg/mL的ASC溶液,混勻,則混合溶液中NaCl質量濃度分別為0%、1%、2%、3%、4%、5%、6%(mg/mL)。然后離心(30min,1000r/min),測定上清液中蛋白質含量(mg/mL),計算ASC相對溶解度。
1.2.4.3 ASC相對溶解度計算 以牛血清白蛋白為標準,參照文獻[14]對上清液中蛋白質含量(mg/mL)進行測定。

式(1)中:V1為ASC溶液的體積,mL;C1為ASC溶液的濃度,mg/mL;V2為離心后上清液的體積,mL;C2為上清液中蛋白質含量,mg/mL。
2 結果與分析
2.1 紫外可見吸收光譜分析
通過測定ASC在波長190~400nm下的吸光度,得知最大吸收波長為222nm,這與ASC多肽鏈中含有的C=O、COOH、CONH2基團有關[10]。絕大部分蛋白質因含有一定量的酪氨酸和色氨酸,因此在280nm處具有最大吸收峰。苯丙氨酸在251nm處有最大吸收峰。而膠原蛋白在280nm及251nm處無顯著吸收峰[11]。因此,實驗所得蛋白質為膠原蛋白。
2.2 不同酸對ASC得率的影響
稱取4份質量均為5g的魚鱗,按照1.2.1操作,分別以0.5mol/L的鹽酸、乙酸、檸檬酸、乳酸為提取劑,液料比為10mL/g,提取時間為72h,ASC得率見圖1。由圖1看出,不同酸液提取ASC得率不同,按得率由大到小依次為乙酸、檸檬酸、鹽酸、乳酸。故實驗選擇乙酸作為ASC的提取劑。

圖1 酸對ASC得率的影響
2.3 乙酸濃度對ASC得率的影響
稱取5份質量均為5g的魚鱗,以液料比為10mL/g分別加入濃度為 0.20、0.35、0.50、0.65、 0.80mol/L的乙酸,提取時間為72h,按1.2.1操作進行提取,結果如圖2所示。
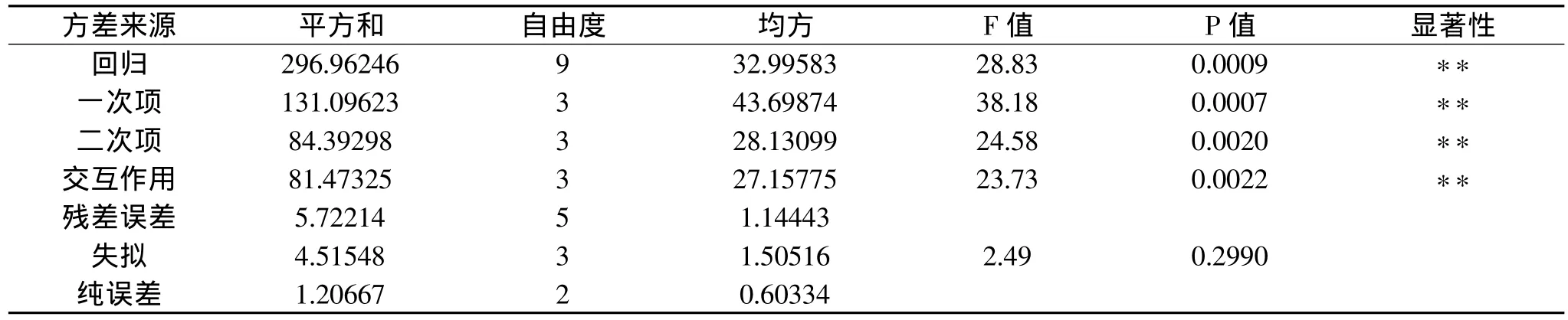
表3 回歸方程的方差分析
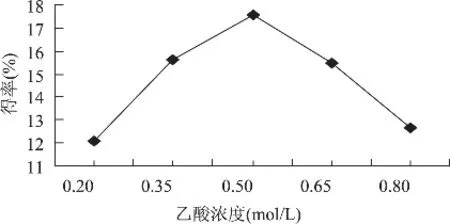
圖2 乙酸濃度對ASC得率的影響
乙酸濃度對ASC得率的影響如圖2,乙酸濃度為0.2~0.5mol/L時,ASC得率隨著乙酸濃度的增加而增大;當乙酸為0.5mol/L時,得率最大為17.58%;當乙酸濃度大于0.5mol/L時,得率反而下降。這可能是隨著乙酸濃度增大,溶液pH降低,膠原蛋白變性,致使溶解度降低,其得率也相應降低。故乙酸濃度以0.50mol/L較為合適。
2.4 液料比對ASC得率的影響
稱取5份質量均為5g的魚鱗,以液料比為5、10、15、20、25mL/g分別加入0.50mol/L的乙酸,提取時間為72h,按1.2.1操作進行提取,結果如圖3所示。當液料比為5~10mL/g時,ASC得率急劇增加,液料比為10~15mL/g時,得率增加也較快,但相對于前者增加幅度較小;當液料比為15~25mL/g時,得率趨于平緩。考慮到酸液使用量大,后處理困難及成本高等問題,故液料比以10~15mL/g為合適范圍。
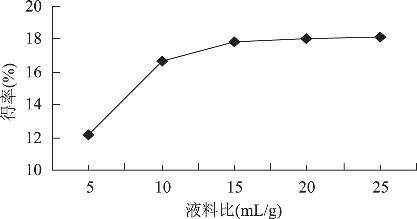
圖3 液料比對ASC得率的影響
2.5 提取時間對ASC得率的影響
稱取7份質量均為5g的魚鱗,以液料比10mL/g加入0.50mol/L的乙酸,提取時間分別為24、36、48、60、72、84、90h,按1.2.1操作進行提取,結果如圖4所示。
由圖4得知,當提取時間為24~60h,ASC得率隨著提取時間的延長而快速增加;當提取時間為60h時,得率達到17.45%;當提取時間大于60h,再隨著時間延長,得率增加不明顯。故提取時間以60h為最佳。
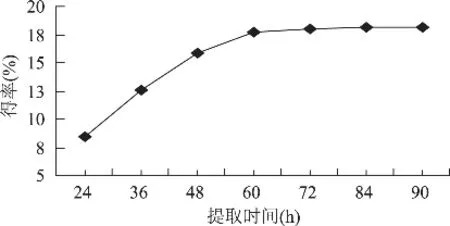
圖4 提取時間對ASC得率的影響
2.6 鯽魚魚鱗中ASC提取工藝優化
在單因素實驗基礎上,以乙酸濃度、液料比和提取時間3因素3水平進行響應面實驗設計及分析,實驗因素編碼及水平表見表1,實驗設計及結果見表2。以編碼值X1,X2,X3為自變量,以ASC得率Y為響應值,采用SAS RSREG程序進行響應面分析實驗,結果見表3,因子經過回歸擬合,解得回歸方程為:
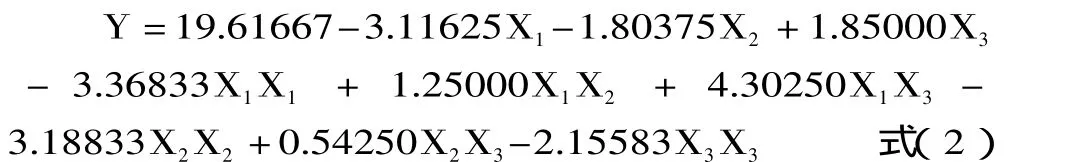
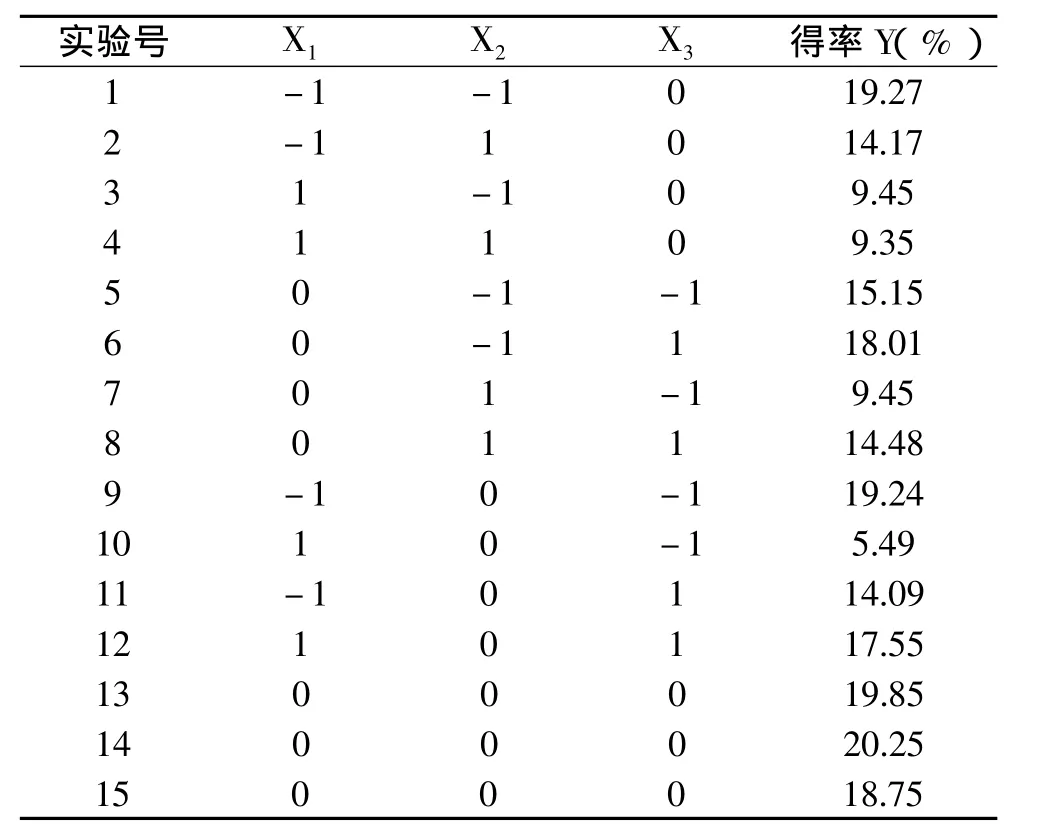
表2 ASC提取實驗設計與結果
回歸方程(2)的方差分析和參數估計分別見表3、表4。由表3可知,模型回歸P為0.0009,說明模型回歸高度顯著可靠;一次項、二次項交互作用高度顯著,說明各因素之間不是簡單的線性關系,而是二次關系;失擬項F值較小,失擬項P為0.2990,表明失擬項不顯著,說明該方程對實驗擬合好,實驗誤差小。因此可以用該回歸方程代替實驗真實點對實驗結果進行分析。由表4知,對方程影響顯著程度由大到小依次為乙酸濃度、提取時間和液料比,三者對ASC得率的影響均高度顯著,說明三者取值大小直接關系到ASC得率。模型的回歸系數R2為0.9811,說明模型響應值即ASC得率的變化98.11%來自所選因變量,即乙酸濃度、液料比和提取時間的值,因此,回歸方程可以較好地描述隨機因子與響應值之間的關系,可以利用該回歸方程確定最佳提取工藝條件。
圖5~圖7反映了乙酸濃度、液料比和提取時間三因素交互作用對響應值的影響。由圖5可知,當液料比X2一定時,隨著乙酸濃度X1的增加,膠原蛋白得率先是逐漸增大然后又逐漸減少;當乙酸濃度一定時,膠原蛋白得率隨著液料比的增大也是先逐漸增大而后又逐漸減少。如編碼X3為0,X1為-0.5時,當編碼X2為-0.62時,ASC得率為20.60%,X2為-0.40時,得率為20.79%,X2為-0.09時,得率為20.55%,X2為0.20時得率又降低為19.77%。

表4 參數估計
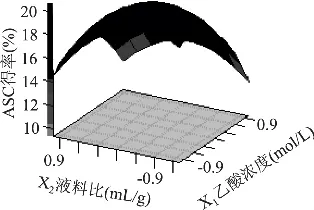
圖5 乙酸濃度和液料比對ASC得率影響的響應曲面(X3=0)

圖6 液料比和提取時間對ASC得率影響的響應曲面(X1=0)
圖6表明,提取時間不變,隨著液料比的增大,ASC得率先是逐漸增大而后又逐漸下降;當液料比一定時,提取時間編碼X2在-1至1范圍內變化,在一定時間內延長提取時間有利于ASC得率的提高,但超過一定值后ASC得率隨時間延長變化不明顯。由圖7得知,乙酸濃度不變時,隨著提取時間的延長,ASC得率也是先增加而后又逐漸減少。而提取時間不變時,隨著乙酸濃度的增大,ASC得率呈下降趨勢。
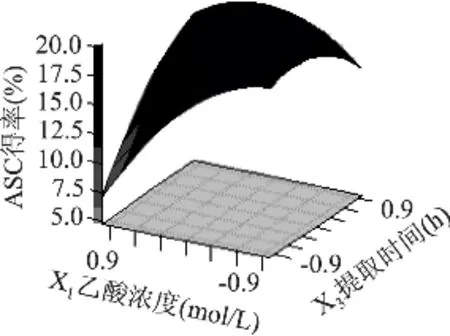
圖7 乙酸濃度和提取時間對ASC得率影響的響應曲面(X2=0)
圖5~圖7表明,ASC得率與乙酸濃度、液料比和提取時間三個因素有關,且這三個因素存在最佳參數組合可以滿足ASC得率達到理論最大值。再對三維非線性回歸模型(2)取一階偏導數等于零,得到如下方程組:

解方程組得X1=-0.8871,X2=-0.5009和X3= -0.5192,根據編碼值與非編碼值的轉換式解得x1= 0.41mol/L,x2=12mL/g,x3=54.81h。即鯽魚魚鱗中ASC最佳提取工藝為乙酸濃度0.41mol/L,液料比12mL/g,提取時間54.81h,由回歸方程可得ASC最高得率理論值可達到20.97%。在該提取工藝條件下,實際測得ASC得率為20.68%(三次平行實驗的平均值,即 n=3),與理論預測值相比,相對誤差為1.38%,因此,采用響應曲面分析法優化得到的提取工藝參數準確可靠,具有實用價值。
2.7 ASC的溶解度
按照1.2.4操作,pH及氯化鈉對ASC的影響分別見圖8、圖9。
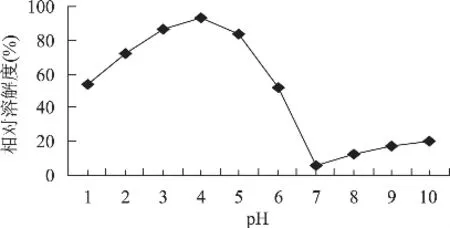
圖8 pH對ASC溶解度的影響
pH對ASC溶解度影響(見圖8)較大,當pH為4時,ASC相對溶解度最大為93.63%;當pH為7時,相對溶解度最小;而pH在7~10范圍內,相對溶解度又隨著pH增大而逐漸增大。其原因可能是膠原蛋白等電點在7附近,當pH接近蛋白質的等電點時,蛋白質所帶凈電荷接近零及蛋白質肽鏈間疏水相互作用增強,導致蛋白質分子聚集、沉淀,相對溶解度降低[13]。當pH偏離等電點時,蛋白質帶有較多凈電荷,蛋白質分子間相互排斥,因此蛋白質相對溶解度較高。
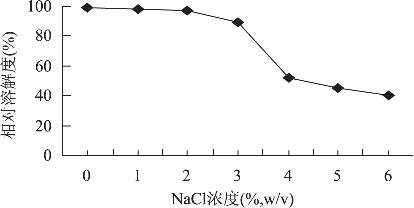
圖9 NaCl對ASC溶解度的影響
由圖9看出,當溶液中 NaCl濃度低于 3%(mg/mL)時,ASC在0.5mol/L乙酸中的溶解度稍微高于在 NaCl溶液中的溶解度;當 NaCl濃度為3%~4%時,相對溶解度隨著NaCl濃度增大而迅速下降;當NaCl濃度大于4%時,相對溶解度緩慢下降;但是,ASC在NaCl溶液(1%~6%,mg/mL)中的相對溶解度均在40%以上。蛋白質在NaCl溶液中溶解度降低原因主要是由于較高離子濃度導致蛋白質分子間疏水相互作用增強,蛋白質與蛋白質發生聚集沉淀而使溶解度降低[15]。
3 結論
利用SAS9.1軟件,采用響應面法(RSM)建立了鯽魚魚鱗ASC提取工藝條件的二次多項式數學模型,分析了各因素對響應值的影響。并對ASC在不同pH及NaCl溶液中的溶解度進行了初步分析。
結果表明:對響應值影響顯著程度由大到小依次為乙酸濃度、提取時間和液料比;二次多項式數學模型擬合程度高,實驗誤差小。對響應回歸方程進行一階偏導數等于零,求出最佳提取工藝條件為:乙酸濃度0.41mol/L,液料比12mL/g,提取時間54.81h,在此條件下,ASC最高得率理論值為20.97%,而實測值可達20.68%,與理論預測值相比,相對誤差為1.38%。ASC溶解度與溶液pH及離子強度(NaCl溶液)有關。當pH在等電點時,相對溶解度較低,偏離等電點時,相對溶解度增大,當pH為4時,相對溶解度最大為93.63%;當NaCl濃度低于3%,離子強度對ASC相對溶解度影響較小,當NaCl濃度大于3%時,相對溶解度先是迅速下降而后又趨于平緩,但都在40%以上。
[1]Senaratne LS,Park PJ,Kim SK.Isolation and characterization of collagen from brown backed toadfish(Lagocephalus gloveri)skin[J].Bioresource Technology,2006,97(2):191-197.
[2]Morimura S,Nagata H,Uemura Y,et al.Development of an effective process for utilization of collagen from livestock and fish waste[J].Process Biochemistry,2002,37(12):1403-1412.
[3]Ogawa M,Portier RJ,Moody MW,et al.Biochemical properties ofbone and scale collagens isolated from the subtropical fish black drum(Pogonia cromis)and sheepshead seabream(Archosargus probatocephalus)[J].Food Chemistry,2004,88(4):495-501.
[4]Jongjareonrak A,Benjakul S,Visessanguan W,et al.Isolation and characterisation of acid and pepsin-solubilised collagens from the skin of Brownstripe red snapper(Lutjanus vitta)[J].Food Chemistry,2005,93(3):475-484.
[5]Kittiphattanabawon P,Benjakul S,Visessanguan W,et al. Characterisation of acid-soluble collagen from skin and bone of bigeye snapper(Priacanthus tayenus)[J].Food Chemistry,2005,89(3):363-372.
[6]胡業麗,吳潔,張瑞,等.酸法提取人工養殖鱘魚皮中膠原蛋白工藝的研究[J].食品科技,2008,33(2):209-212.
[7]Sadowska M,Kolodziejska I,Niecikowska C.Isolation of collagen from the skins of Baltic cod(Gadus morhua)[J].Food Chemistry,2003,81(2):257-262.
[8]Zhang J,Duan R,Tian Y,et al.Characterisation of acidsoluble collagen from skin of silver carp(Hypophthalmichthys molitrix)[J].Food Chemistry,2009,116(1):318-322.
[9]Duan R,Zhang J,Du X,et al.Properties of collagen from skin,scale and bone of carp(cyprinus carpio)[J].Food Chemistry,2009,112(3):702-706.
[10]Zeng S,Zhang C,Lin H,et al.Isolation and characterisation of acid-solubilised collagen from the skin of Nile tilapia(0reochromis niloticus)[J].Food Chemistry,2009,116(4):879-883.
[11]Yan M,Li B,Zhao X,et al.Characterization of acid-soluble collagen from the skin of walleye pollock( Theragra chalcogramma)[J].Food Chemistry,2008,107(4):1581-1586.
[12]Nalinanon S,Benjakul S,Visessanguan W,et al.Use of pepsin for collagen extraction from the skin of bigeye snapper(Priacanthus tayenus)[J].Food Chemistry,2007,104(2):593-601.
[13]Montero P,Jiménez-Colmenero F,Borderìa J,et al.Effect of pH and the presence of NaCl on some hydration properties of collagenous material from trout(Salmo irideus Gibb)muscle and skin[J].Journal of the Science of Food and Agriculture,1991,54(1):137-146.
[14]LowryOH,RosebroughNJ,FarrAL,etal.Protein measurement with the folin phenol reagent[J].Journal of Biological Chemistry,1951,193(1):256-275.
[15]Fennema OR著.食品化學[M].第三版.王璋,許時嬰等譯.北京:中國輕工業出版社,2003:307-308.
Optimization of extraction acid-soluble collagen from crucian carp scale by response surface methodology
ZHU Xiu-ling,DAI Qing-yuan,CAI Wei-rong,WANG Jian
(Department of Biochemistry Engineering,Anhui University of Technology and Science,Wuhu 241000,China)
Based on the single factor experiments,the effects of acetic acid concentration,ratio of solvent to solid and extraction time on the yield of acid-soluble collagen(ASC)from crucian carp scale were optimized with response surface methodology.A methematical model was established and analyzed to describe the relationships between the factors and the response of the yield of ASC from crucian carp scale.The results showed that the optimum extracting conditions for ASC were as follows:the concentration of acetic acid 0.41mol/L,the ratio of solvent to solid 12mL/g and extraction time 54.81h.Under the optimum conditions,the predictive maximum yield of ASC on the dry weight basis was 20.97%and experimental value was 20.68%.Comparing predictive value with experimental value,the relative error was 1.38%.The highest relative solubility of ASC from crucian carp scale was obtained at pH4.No changes in solubility were found in the presence of NaCl up to 3%(mg/mL).However,a sharp decrease but no less than 40%in solubility was observed with NaCl above 3%(mg/mL).
acid-soluble collagen(ASC);response surface methodology;optimization;scale
TS254.1
B
1002-0306(2010)11-0247-05
2009-11-25
朱秀靈(1978-),女,碩士,講師,研究方向:農副產品資源開發與利用。
安徽省高等學校省級自然科學研究項目(KJ2009B091);安徽工程科技學院青年基金項目(2008YQ050)。

