堿性蛋白酶水解蠶豆蛋白的條件優化
白小佳,宋慶明,肖萍,王艷萍
(天津市食品營養與安全重點實驗室,天津科技大學食品工程與生物技術學院,天津 300457)
堿性蛋白酶水解蠶豆蛋白的條件優化
白小佳,宋慶明,肖萍,王艷萍*
(天津市食品營養與安全重點實驗室,天津科技大學食品工程與生物技術學院,天津 300457)
采用堿性蛋白酶酶解蠶豆分離蛋白,通過正交試驗確定最佳酶解反應條件:反應溫度為50℃,pH值為8.5,酶與底物比為16000 U/g,底物濃度為60 g/L。在此條件下,水解度可以達到15.55%。
蠶豆蛋白;酶解;優化
近年來多肽越來越受到重視,現代生物學試驗已經證明,多肽與蛋白質和氨基酸相比具有更多的優點:多肽在腸道中的吸收率最好[1],一些低肽如二肽、三肽的吸收速度比氨基酸快;一些多肽具有強化機體免疫、促進人體新陳代謝的作用;多肽具有低抗原性、促進脂質代謝、降低膽固醇、促進礦物質吸收、降血壓、抗氧化、促進微生物生長等生理功能;多肽具有較好的酸、熱穩定性、水溶性[2]。這些功能使蛋白質的分解產物作為高效氮源受到國際營養界和食品產業的高度重視。乳蛋白的分解物、大豆蛋白的分解產物、畜血蛋白的分解產物和玉米蛋白的分解產物都已經成為運動飲料、功能食品和醫療食品的重要原料。
蠶豆的蛋白質含量高,是我國重要的糧食、蔬菜和副食品。蠶豆的微量元素含量較高,尤其是磷、鎂、硒的含量居常食幾種豆類之首,成熟的蠶豆中B族維生素的含量比其他豆類都高,而未成熟蠶豆則是VA和VC的上等來源。蠶豆種子不僅蛋白質含量高。而且蛋白質中氨基酸種類全,人體內不能合成的8種必需氨基酸中,除色氨酸和蛋氨酸含量稍低外,其余6種含量都高,尤其以賴氨酸含量豐富,比谷物中高出3倍,所以蠶豆被譽為植物蛋白質的新來源[3]。因此,許多國家都很重視對蠶豆的研究,并對相應發展起來的蠶豆加工業也加倍關注。
本課題組已經對蠶豆蛋白的超聲提取工藝進行了研究,取得了較好的效果[4]。本試驗通過對堿性蛋白酶酶解蠶豆蛋白的條件進行優化,制取蠶豆蛋白水解產物,提高了蠶豆的營養價值,為今后對蠶豆蛋白水解物生物活性的研究打下基礎。
1 材料與方法
1.1 材料
1.1.1 原料
蠶豆:購于天津北塘市場。
1.1.2 試劑
堿性蛋白酶:天津市諾奧科技發展有限公司(2×105U/g);其它試劑均為分析純。
1.1.3 儀器
DELTA-320型pH計:瑞士METTLER TOLEDO公司;78HW-1型恒溫磁力攪拌器:杭州儀表電機廠;VIS-7220型分光光度計:北京瑞利分析儀器公司;LRH-250生化培養箱:天津市達北實驗儀器廠。
1.2 方法
1.2.1 蠶豆分離蛋白的制備流程
市售蠶豆,50℃~60℃水溶漲24 h,去皮后,將蠶豆置于55℃烘箱中烘干,所得蠶豆仁用粉碎機粉碎后過60目篩,得到的蠶豆粉置于4℃冰箱中儲存備用。經超聲提取蠶豆粉中蛋白質,調pH至4.2,離心保留沉淀,冷凍干燥24 h,得到蠶豆分離蛋白[4]。
1.2.2 蛋白質含量的測定
凱氏定氮法,參照GB5009.5-1985《食品中蛋白質的測定方法》[5]。
1.2.3 水解度(DH)的測定
蛋白水解度(DH)以水解斷裂的肽鍵數目(h)占總肽鍵數目(htot)的百分數來表示,即DH=h/htot×100%,由于pH-stat法[6]具有操作簡單,連續測定的優點,因此主要采用該法來檢測蠶豆分離蛋白的水解度。
蛋白水解度可根據水解過程中NaOH的消耗量來進行計算,計算公式如下:
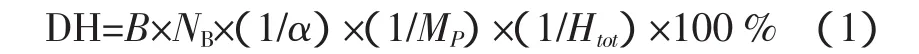
式中:B為水解過程中所消耗的NaOH的溶液量,mL;NB為-溶液的當量濃度,(mol/L);α 為水解時 α-氨基平均解離度,1/α=1+10(pK-pH);pK 為蛋白質 α-氨基的pK值;pH為水解溶液的pH值;MP為底物蛋白質的總量,g;Htot為每克原料蛋白質中肽鍵的毫摩爾數,Htot取 7.75 mmol/L[7]。
1.2.4 蠶豆分離蛋白的酶解反應
準確稱取適量蠶豆分離蛋白于100 mL蒸餾水中混勻,放入集熱式磁力攪拌器中,調節溫度、pH值,加入一定量蛋白酶進行水解,通過加入2 mol/L氫氧化鈉來保持pH值不變,記錄堿液消耗量,換算成DH值,反應時間 1 h(pH變動范圍 ±0.1),到達時間后,調節溶液pH值到4.0,并在85℃水浴中維持20 min,對酶進行滅活,然后迅速冷卻至室溫,在4000 r/min下離心20 min,傾倒出上清液,調pH到7.0,凍干備用。
記錄NaOH溶液的滴加量,利用公式(1)pH-stat法計算水解度。
1.2.5 溫度對水解反應的影響
精確稱取6 g蠶豆分離蛋白,溶于100 mL蒸餾水中,加入 84000 U 堿性蛋白酶,分別在 40、50、60、70 ℃溫度,pH值為8.0的條件下進行水解反應,記錄消耗的氫氧化鈉的體積,研究溫度對水解的影響。
1.2.6 pH對水解反應的影響
精確稱取6 g蠶豆分離蛋白,溶于100 mL蒸餾水中,加入84000 U堿性蛋白酶,反應溫度為60℃,分別在 pH 為 8.0、8.5、9.0、10.0的條件下進行水解反應,記錄消耗的氫氧化鈉的體積,研究pH對水解的影響。
1.2.7 底物濃度對水解反應的影響
分別精確稱取 4、5 、6、7、8、9 g 的蠶豆分離蛋白,溶于100 mL蒸餾水中,加入84000 U堿性蛋白酶,反應溫度為60℃,pH為8.0條件下進行水解反應,記錄消耗的氫氧化鈉的體積,研究底物濃度對水解的影響。
1.2.8 酶與底物濃度比對水解反應的影響
分別精確稱取6 g蠶豆分離蛋白,溶于100 mL蒸餾水中,分別加入 60000、72000、84000、96000 U 堿性蛋白酶,使酶與底物濃度比為10000、12000、14000、16000 U/g,反應溫度為60℃,pH為8.0條件下進行水解反應,記錄消耗的氫氧化鈉的體積,研究酶與底物濃度比對水解的影響。
1.2.9 酶解條件的優化
正交試驗[8-9]具有試驗次數少、代表性強和綜合可比的優點。根據酶解的單因素試驗結果,選擇溫度、底物濃度、pH值、酶與底物比為正交試驗的因素,擬通過L16(45)正交試驗來確定最佳水解反應條件,以DH為指標,確定蠶豆分離蛋白最佳水解工藝參數,表1為正交試驗因素水平編碼表。
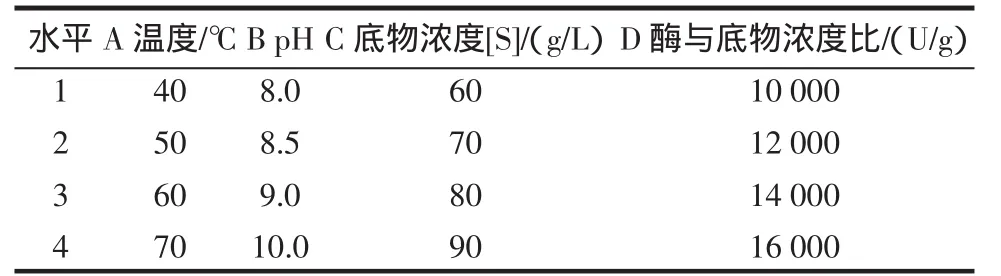
表1 L16(45)正交試驗因素水平設計表Table1 Factorsandlevelsdesignoforthogonaltest
2 結果與分析
2.1 蠶豆分離蛋白的提取
將蠶豆粉按照1∶12的料液比溶于蒸餾水中,調節pH到8.0,功率660 W下超聲提取20 min,2000 r/min離心5 min,取上清液,調節pH到4.2,沉淀蠶豆蛋白,3500 r/min離心10 min,取沉淀,冷凍干燥24 h,得到蠶豆分離蛋白,此條件下提取的蠶豆分離蛋白中蛋白質含量為89.32%。
2.2 反應溫度對水解的影響
各種催化反應都有最適的溫度,此時,酶的反應速度最快。與普通化學反應一致,在酶的最適溫度以下,隨著溫度的升高,反應物能量增加,單位時間內分子間有效接觸次數增加,反應速度越快。如果反應體系溫度超過酶的最適溫度,酶分子吸收了過多的能量,引起維持酶分子結構的次級鍵解體,導致變性,因而使酶活性減弱甚至喪失催化能力。
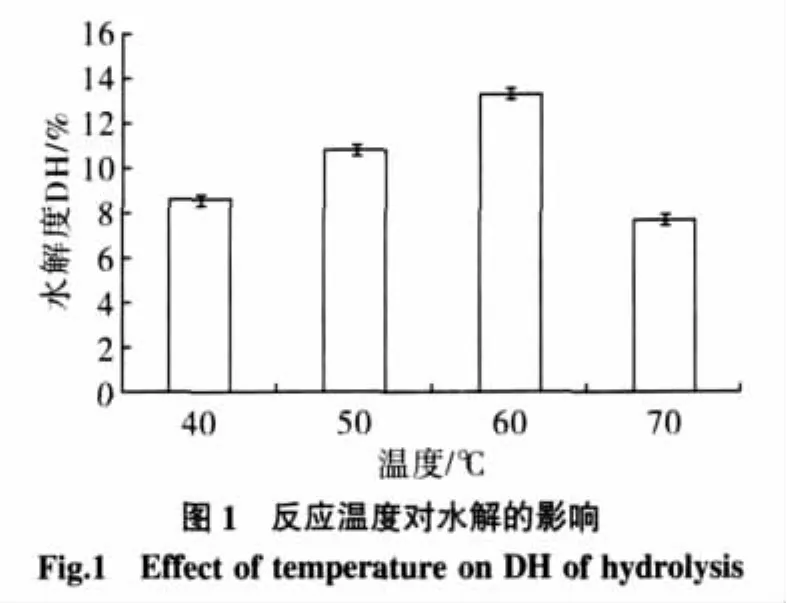
圖1可知,在溫度<60℃時,隨溫度升高DH增大;當溫度為60℃時,DH達到最大值;但溫度>60℃時,DH隨溫度增加而降低,因此,本試驗條件下,堿性蛋白酶水解蠶豆分離蛋白的最適溫度60℃。
2.3 反應pH對水解的影響
酶分子是一種特殊的蛋白質分子,具有一個或若干個活性部位,酶的活性部位由結合部位和催化部位組成。結合部位的功能是直接與底物相結合,而催化部位則催化底物進行特定的反應。活性部位中的基團在蛋白質的一級結構所處的位置通常相距較遠,也許可能位于不同的肽鏈上,但是它們在酶的空間結構卻必須按一定的相對位置靠近在一起,形成活化中心(活性部位)。因此酶的活性部位只有在酶蛋白保持一定的空間構象時才能存在,并發揮其催化作用。結合部位和催化部位的基團對反應體系的pH值變化比較敏感,其解離狀態隨pH的變化而變化,這些變化影響了酶分子的特殊構象。另外體系中作為底物的蠶豆分離蛋白隨著pH值變化也表現出不同的解離狀態,因此,pH值直接影響了酶與底物的結合和催化,是酶催化反應的主要因素之一。反應pH對水解的影響見圖2。
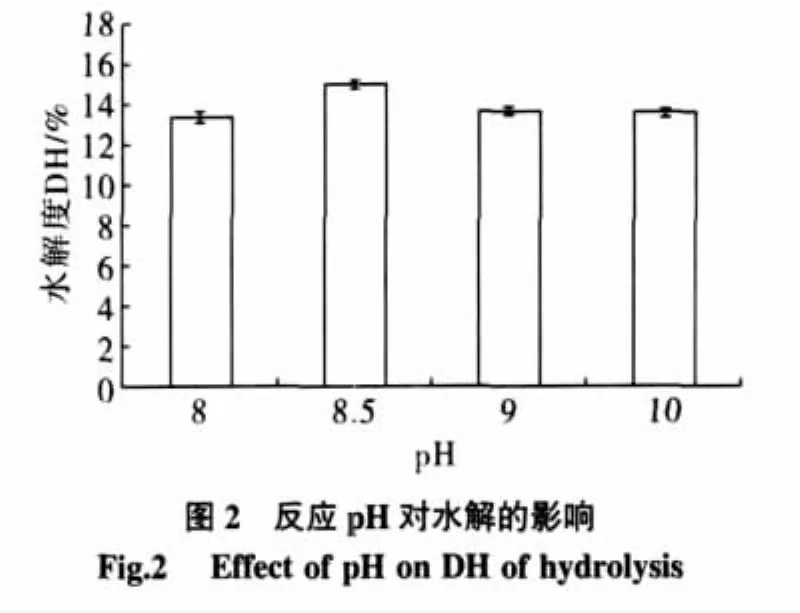
由圖2可知,在pH小于8.5時,隨pH升高,DH升高;在pH大于8.5時,隨pH升高而DH降低;而在pH為8.5時,DH達到最大。本反應體系下,堿性蛋白酶催化蠶豆分離蛋白水解的最適pH值為8.5。
2.4 底物濃度對水解反應的影響
酶與底物反應速度在一定程度上取決于底物濃度,由圖3可知,DH隨底物濃度的增大而呈下降趨勢。
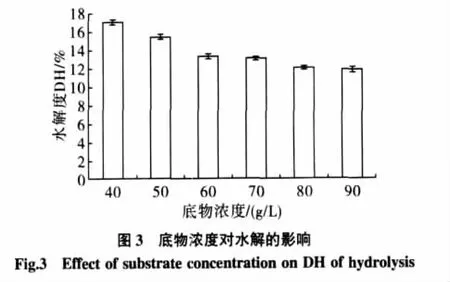
底物濃度在不斷受熱情況下,蠶豆蛋白分子易于產生交鏈聚合現象。使酶分子與蛋白分子之間的接觸機會減少,從而導致DH的下降,且溶解性差,黏度增大,影響反應速度。但底物濃度過低時,產品的得率和生產效率不高,經濟效益差。綜合考慮,選用底物濃度為60 g/L作為最適底物濃度。
2.5 酶與底物濃度比對水解的影響
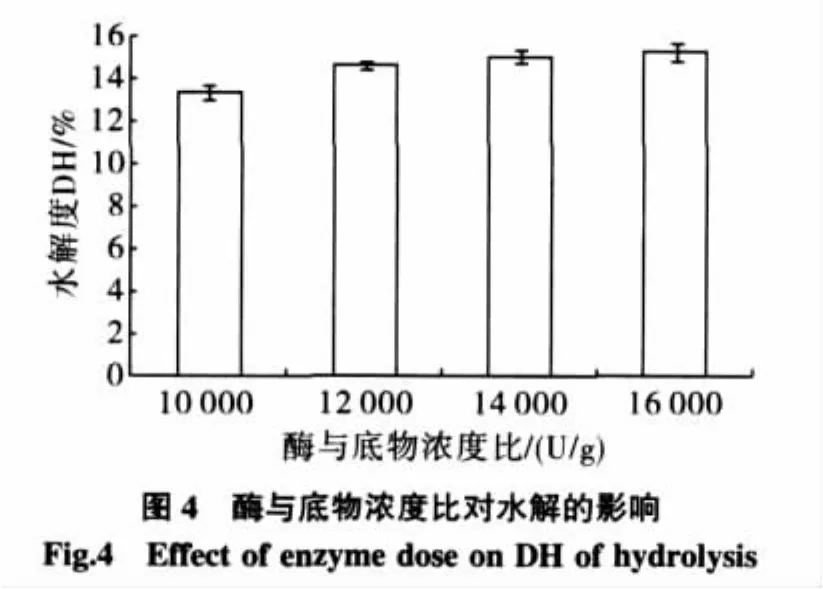
在底物蠶豆分離蛋白濃度一定時,底物的轉化率取決于酶濃度,酶濃度越大,酶與蛋白質分子肽鏈接觸幾率增加,底物轉化為產物可溶性肽也就相應地增加。所以高劑量的酶可提高轉化率,但酶成本較高,適當添加可降低成本。綜合考慮,水解反應速率、蛋白質水解度及生產成本之間的相互作用,確定一個最佳酶用量,以達到低成本高效率,同時又能達到目標水解度的要求。酶與底物濃度的對水解的影響見圖4,由圖4結果可知,隨著酶與底物濃度比的增加,DH增加。但16000 U/g與14000 U/g相比,DH相差不大,酶與底物濃度比無需再增加。
2.6 酶解條件的優化分析
按照1.2.9的方法進行正交試驗,結果如表2所示。
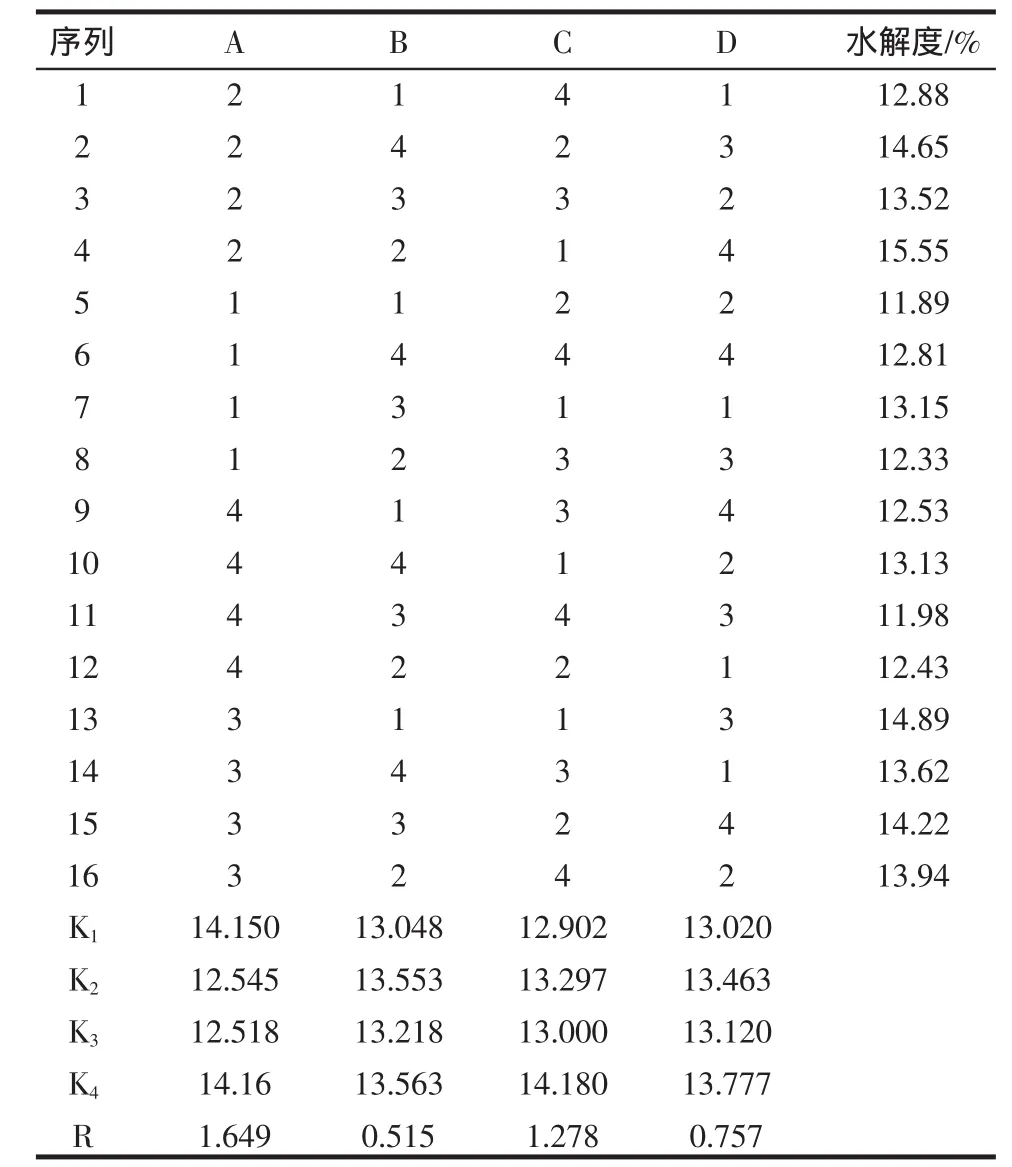
表2 L16(45)正交試驗設計表及試驗結果分析Table2 L16(45)Orthogonalexperimentaldesignandresult
根據各因子3個水平極差大小得出對水解度影響的主次順序為:溫度>底物濃度>酶與底物濃度比>pH。堿性蛋白酶水解蠶豆分離蛋白的最佳條件為:溫度為50℃,pH值為8.5,酶與底物比為16000 U/g,底物濃度為60 g/L,水解度達到15.55%。
3 結論
以水解度為指標,使用堿性蛋白酶水解蠶豆分離蛋白,根據單因素試驗結果,做正交試驗得出堿性蛋白酶水解蠶豆分離蛋白的最佳工藝條件為:反應溫度為50℃,pH值為8.5,酶與底物比為16000 U/g,底物濃度為60 g/L,水解度達到15.55%。可利用該蠶豆蛋白水解物為原料開發多種產品,具有較好的應用前景。
[1]陳雪梅,嚴丹紅,農向,等.牛乳源活性肽及其研究進展[J].西南民族大學學報,2006,32(2):226-229
[2]高福成.食品分離重組工程技術[M].北京:中國輕工業出版社,1998:95-802
[3]孫遠明.食品營養學[M].北京:科學出版社,2006:103-105
[4]王艷萍,李雙喜,程巧玲.超聲提取蠶豆蛋白的研究[J].食品研究與開發,2008,29(5):71-72
[5]中華人民共和國衛生部.GB5009.5-1985食品中蛋白質的測定方法[S].1985
[6]Magdalena Karama,Ryszard Amarowice,Henryk Kostyra.Effect of Temperature and Enzyme Substrate Ratio on the Hydrolysis of Pea Protein Isolates by Trypsin[J].Czeeh J.Food Sci.,2002(20):1-6
[7]Adler-Nissen Jens.Enzymatic hydrolysis of food proteins[M].London:Elsevier applied science publishers,1986:12-14
[8]北京大學數學力學系數學專業概率統計組.正交設計[M].北京:人民教育出版社,1976:85-89
[9]彭志英.食品酶學導論[M].北京:中國輕工業出版社,2002:162-163
Optimizing Hydrolysis Conditions of Broad Bean Protein by Alkaline Protease
BAI Xiao-jia,SONG Qing-ming,XIAO Ping,WANG Yan-ping*
(Tianjin Key Laboratory of Food Nutrition and Safety,Faculty of Food Engineering and Biotechnology,Tianjin University of Science and Technology,Tianjin 300457,China)
Alkaline protease hydrolysis of broad bean protein was investigated in this research.The result indicated that the hydrolysis degree was 15.55%under the optimized conditions of the hydrolysis temperature 50℃,the solution pH 8.5,enzyme and substrate ratio 16000 U/g,and the substrate concentration 60 g/L.
Broad bean protein;hydrolysis;optimization
白小佳(1975—),女(漢),副教授,博士,研究方向:食品生物技術。
*通訊作者
2009-09-04

