6個新的STR基因座復合擴增體系的建立及應用
劉俊宏,邵偉波,李 莉,楊 穎
(1.華東政法大學,上海200042;2.蘇州大學 醫學部法醫學系,江蘇 蘇州215123;3.司法部司法鑒定科學技術研究所,上海市法醫學重點實驗室,上海200063;4.上海市血液中心,上海200051)
短串聯重復序列(short tandem repeat,STR)通常是由長度為2~5個堿基的核心序列串聯重復而成,具有分布廣泛、多態性高及易于擴增等特性[1],STR分型已成為法醫物證檢驗的主要技術手段。目前我國廣泛使用的試劑盒主要為Identifiler○R,SinofilerTM和Powerplex○R16 System,基本上可以滿足個體識別和親子鑒定的需要,但在突變和特殊案件中,需要檢測更多的STR基因座來補充當前STR系統的不足。本研究選擇了非CODIS系統的6個基因座,即D4S2366、
D3S3045、D18S1002、D20S481、D22S689、D4S2639,建立了熒光復合擴增檢測體系,并將該體系應用于224名華東漢族無關個體的基因型檢測,評估了其作為新的遺傳標記在華東漢族人群中的法醫學價值。
1 材料和方法
1.1 樣本
224份血斑(每份約3mm×3mm大小),分別來源于華東地區漢族無關個體,Chelex-100法[2]提取血液DNA。
1.2 引物
6個基因座的熒光引物序列來自GDB基因組數據庫,其具體信息和熒光素標記見表1。所有引物由上海生工生物工程技術有限公司合成。
1.3 PCR復合擴增體系及產物檢測
PCR復合擴增體系為20μL,內含10×PCR buffer 2 μL,2 mmol/L dNTPs 2 μL,25 mmol/L Mg2+2 μL,primer pair mix 2μL,AmpliTaq GoldR○DNA聚合酶0.5 μL,DNA模板量5μL,純水6.5μL。采用9700型擴增儀(美國AB公司)進行擴增,循環參數為:95℃15min;94℃30s,56℃90s,72℃60s,循環30次;60℃60min;4℃保存。
取PCR擴增產物1μL、去離子甲酰胺(美國AB公司)10μL、內標SIZ-350(無錫中德美聯生物技術有限公司)0.3μL混合,95℃變性3min,冰浴3min,使用3130遺傳分析儀(美國AB公司)電泳檢測。
1.4 等位基因測序、命名
根據在GALAXY網站上查到的DNA序列,采用Primer premier5.0軟件設計用于克隆測序的PCR引物,其具體信息見表2。設計好的引物由上海生工生物工程技術有限公司合成。選取每個基因座各個等位基因的樣本,用所合成的測序引物分別對其進行PCR擴增,產物送上海生工生物工程技術有限公司進行測序,根據各等位基因的測序結果,確定核心序列重復次數,按照國際法醫血液遺傳學會DNA委員會ISFH推薦的命名原則進行命名[3~4]。

表1 復合擴增體系中6個基因座的引物特征

表2 6個基因座的測序引物特征
1.5 等位基因梯度標準(Allelic Ladder)的制備
選取各基因座含不同等位基因的樣本,用熒光標記引物單獨擴增后,通過多次調節模板量濃度、擴增次數及混合比例,制備Allelic Ladder。
1.6 靈敏度檢測
將標準品DNA 9947A(10ng/μL)稀釋成如下濃度梯度:2 ng/μL、1ng/μL、0.5ng/μL、0.25ng/μL、0.125ng/μL、0.0625 ng/μL、0.03125 ng/μL、0.015625 ng/μL,用復合擴增體系進行擴增,擴增產物在3130遺傳分析儀上電泳檢測。
1.7 統計學分析
運用PowerStats V12.xls[5]軟件統計分析D4S2366等6個非CODIS STR基因座的等位基因頻率、雜合度(H)、個體識別能力(DP)和多態信息含量(PIC)等參數,采用Cervus2.0軟件統計分析二聯體非父排除率(PED)和三聯體非父排除率(PET),并進行Hardy-Weinberg平衡檢驗,檢驗水準α=0.05。
1.8 排除效能統計
運用所建立的復合擴增體系,對93個經Sinofiler試劑盒(美國AB公司)檢測已排除非父的二聯體案例進行分析,討論其在實際案例中的運用價值。
2 結果
2.1 6個STR基因座的熒光標記復合擴增體系
本文構建的6個非CODIS STR基因座熒光標記復合擴增體系分型穩定,具有種屬特異性,且適用于各類生物學檢材。標準品DNA 9947A的分型結果見圖1。
2.2 6個STR基因座各等位基因測序結果
通過測序得到6個STR基因座每個等位基因的核心重復序列(見表3),按國際法醫遺傳學會推薦原則,以核心序列重復次數命名等位基因。
2.3 Ladder制備結果
將6個STR基因座的各個等位基因用熒光標記引物進行擴增,依照熒光強度調節各個PCR產物的比例,制成Ladder見圖2。
2.4 靈敏度檢測結果
將標準品DNA 9947A(10ng/μL)稀釋成如下濃度梯度:2ng/μL、1ng/μL、0.5ng/μL、0.25ng/μL、0.125ng/μL、0.0625ng/μL、0.03125ng/μL、0.015625ng/μL,用復合擴增體系進行擴增,擴增產物在3130遺傳分析儀上電泳分離,使用Genemapper軟件分析結果。在四種熒光素中,ROX產生的峰高普遍低于其它熒光素,通過觀察用ROX標記的基因座的峰高,發現20 μL體系中模板DNA濃度為0.125ng/μL時效果最好,但濃度低至0.03125ng/μL時仍能得到正確的分型結果,提示該體系的靈敏度為156.25pg。
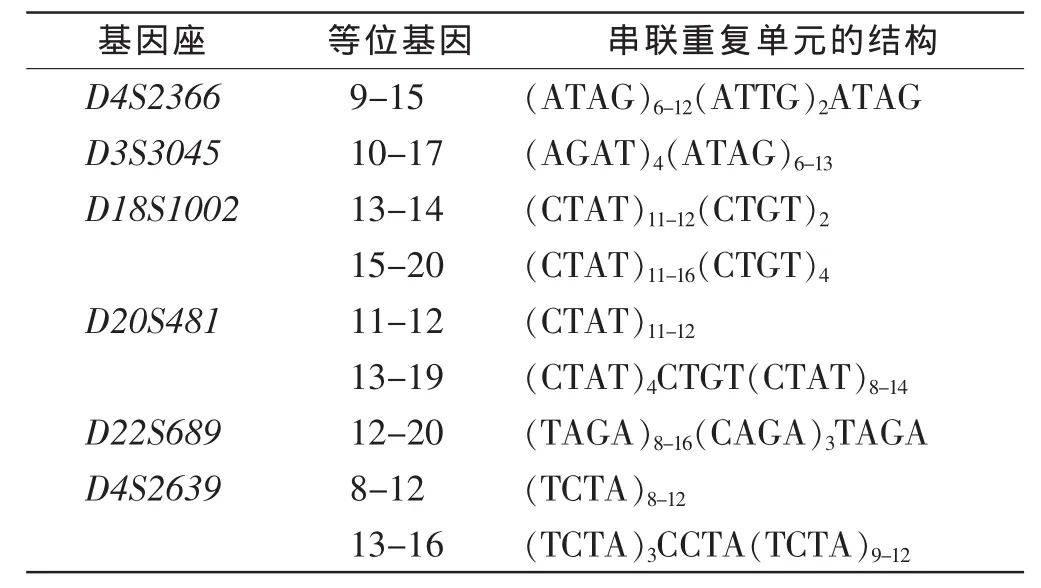
表3 6個STR基因座各等位基因的序列特征
2.5 6個基因座的等位基因頻率分布

圖1 標準品DNA9947A分型圖
在華東地區漢族 224名無關個體中,6個非CODIS STR基因座共檢出52個等位基因,各等位基因頻率見表4。

圖2 6個STR基因座的Allelic Ladder
2.6 法醫學參數
經過統計分析,D4S2366等6個STR基因座的雜合度(H)分布為 0.714~0.808,個體識別率(DP)為0.874~0.934,二聯體非父排除率(PED)為0.310~0.453,三聯體非父排除率(PET)為0.485~0.628,多態信息含量(PIC)為0.672~0.784,基因型頻率分布通過Hardy-Weinberg平衡檢驗(P>0.05),見表5。6個STR基因座的二聯體累積非父排除率(CPED)為0.947689,三聯體累積非父排除率(CPET)為0.993345,累積個人識別能力(CDP)為0.999999543。
2.7 實際案例應用
將復合擴增體系應用于93例二聯體排除案例,每個基因座的排除概率(見表6)與其二聯體非父排除率(PED)指標(見表5)基本一致。
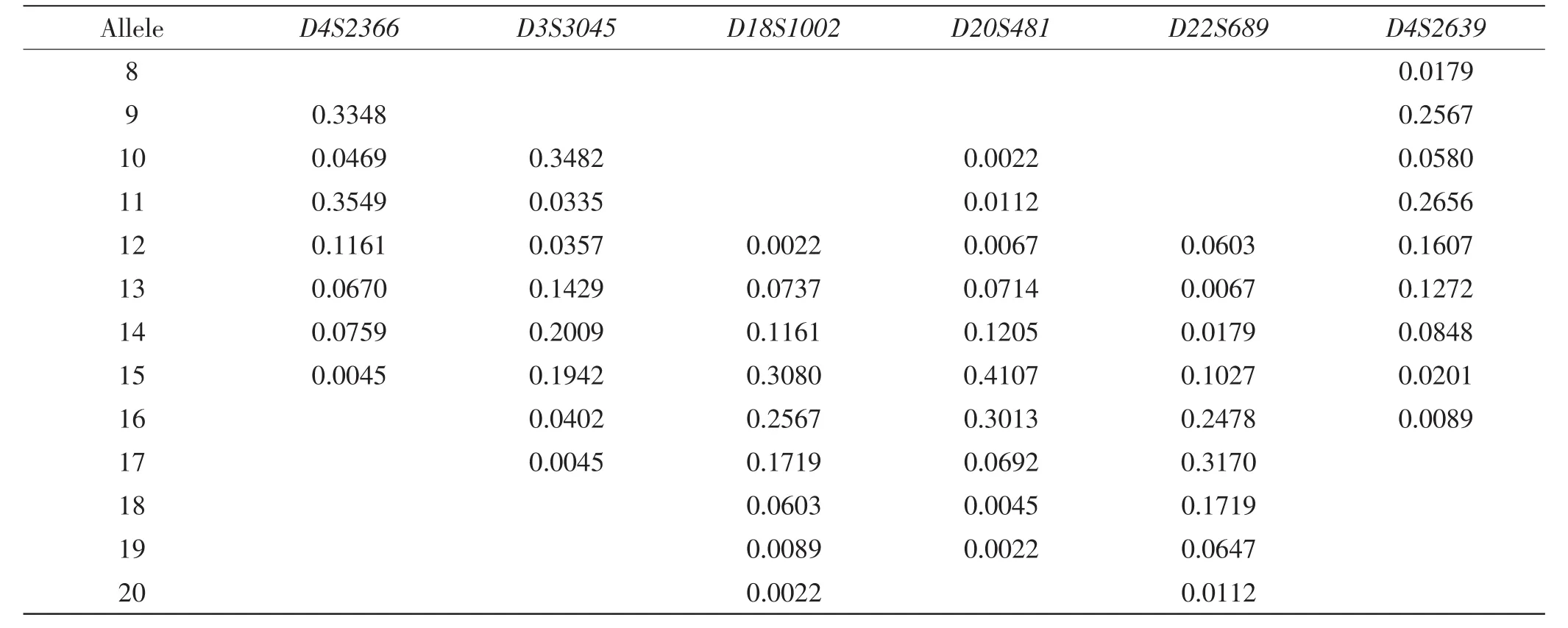
表4 6個STR基因座在華東漢族人群的等位基因頻率分布 (n=224)
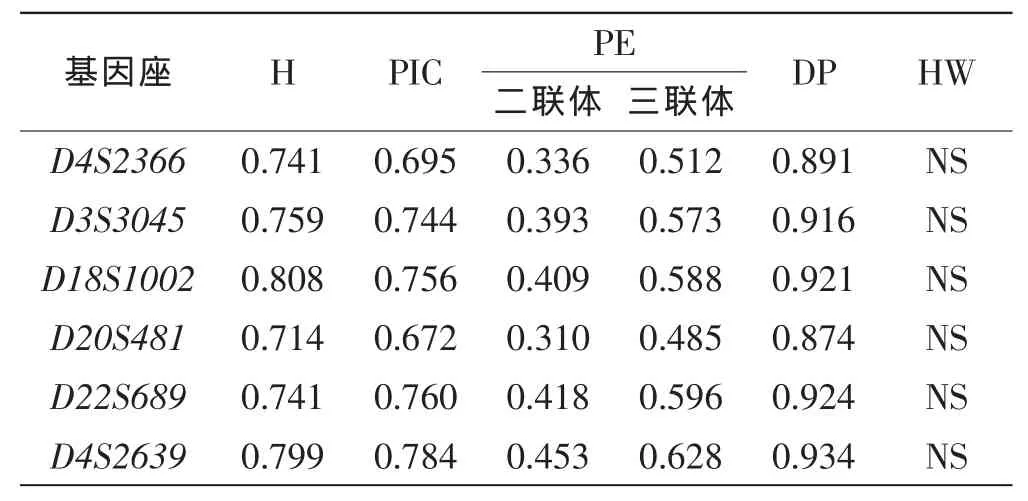
表5 華東漢族人群6個STR基因座的相關法醫學參數(n=224)
3 討論
構建熒光標記復合擴增體系的主要步驟包括基因座的選擇、引物設計、擴增體系和擴增條件的優化。引物的設計選擇要有高度特異性,不同引物之間不能互相干擾,應避免引物二聚體、發夾結構等,同時還需要考慮片段大小等因素。本研究采用的是多重PCR擴增體系,作者通過大量實驗調整各個基因座的引物量,最終得到了比較理想的配比方案。同時,對退火溫度及循環次數也進行了梯度試驗,建立了合適的PCR擴增方法。復合PCR體系中,模板濃度的最低量為0.03125ng/μL,各個STR基因座的擴增片段大小均小于350bp,因此適用于降解檢材的DNA分型。
本文選擇的是6個非CODIS STR基因座,通過對華東漢族224個無關個體的檢測,在D4S2366、D3S3045、D18S1002、D20S481、D22S689、D4S2639STR基因座分別檢出 7、8、9、10、9、9個等位基因和 21、26、21、23、28、32種基因型,各基因座的基因型均符合Hardy-Weinberg平衡。6個基因座中,D4S2639非父排除率最高,D20S481非父排除率最低,各基因座平均雜合度(H)為 0.760,平均個體識別率(DP)為0.910,平均多態信息含量(PIC)為0.735,二聯體累積非父排除率(CPED)為0.947689,三聯體累積非父排除率(CPET)為 0.993345,累積個人識別能力(CDP)為0.999999543,表明上述6個STR基因座在中國漢族人群中具有高度的多態性,其復合擴增體系的效能適用于法醫學個人識別。另外,作為常規STR標記的補充,上述6個基因座可用于存在突變情形的二聯體、三聯體鑒定,也可用于因累積親權指數低于標準值[6]而不能明確鑒定意見的親權鑒定案件。

表6 6個基因座在實際案例中的排除率 (n=93)
[1]Schuler GD,Boguski MS,Stewart EA,et al.A gene map of the human genome[J].Science,1996,274(5287):540-546.
[2]Walsh P S,Metzger D A,Higuchi R.Chelex-100 as a medium for simple xtraction of DNA for PCR-based typing from forensic materia[J].Biotechniques,1991,10:506-513.
[3]Lincoln P J.DNA recommendations-further report of the DNA Commission of the ISFH regarding the use of short tandem repeat systems.Forensic Sci Int.1997 Jun 23,87(3):181-184.
[4]B?r W,Brinkmann B,Budowle B,et al.DNA recommendations.Further report of the DNA Commission of the ISFH regarding the use of short tandem repeat systems.International Society for Forensic Haemogenetics[J].Int J Legal Med,1997,110(4):175-176.
[5]Promega Biotech Co.,Ltd.Powerstates V12.xls.[EB/OL] http://www.promega.com/geneticidtools/.
[6]司法部司法鑒定技術規范[S].SF/Z JD0105001-2010.

