肉豆蔻炮制品的化學成分分離與鑒定
趙光云,王曉霞,高慧媛
(沈陽藥科大學教育部基于靶點的藥物設計與研究重點實驗室,遼寧 沈陽 110016)
化學
肉豆蔻炮制品的化學成分分離與鑒定
趙光云,王曉霞,高慧媛*
(沈陽藥科大學教育部基于靶點的藥物設計與研究重點實驗室,遼寧 沈陽 110016)
目的:對肉豆蔻Myristica fragrans Houtt.種仁炮制后的化學成分進行分離鑒定。方法:采用麥麩煨制法炮制肉豆蔻,Sephadex LH-20和ODS反相硅膠柱色譜等方法對制肉豆蔻的95%乙醇提取物進行化學成分分離,結合理化性質和波譜數據進行結構鑒定。結果:從麩制肉豆蔻中分離得到9個化合物,分別鑒定為消旋-去氫二異丁香酚[(±)-dehydrodiisoeugenol,1]、利卡靈-B(licarin-B,2)、愈創木素(guaiacin,3)、肉豆蔻醚(myristicin,4)、malabaricone A(5)、malabaricone B(6)、malabaricone C(7)、β-谷甾醇(β-sitosterol,8)、胡蘿卜苷(daucosterol,9)。結論:化合物5~7為馬拉巴酮衍生物,在生品中至今未見國內有分離報道,推測炮制使該類成分含量明顯增加。
肉豆蔻;炮制;化學成分;結構鑒定
肉豆蔻是肉豆蔻科肉豆蔻屬(Myristica)植物肉豆蔻Myristica fragransHoutt.的干燥成熟種仁,又名迦拘勒、豆蔻、肉果、頂頭肉等,分布于馬來西亞、印度尼西亞、西印度群島等地,我國臺灣、廣東、云南等地有引種栽培。肉豆蔻具有溫中行氣,澀腸止瀉的功能,用于脾胃虛寒,久瀉不止,脘腹脹痛,食少嘔吐等。現代藥理學研究表明,肉豆蔻具有抗菌、消炎、鎮靜、抗腫瘤等作用,但因種仁的油中富含有可致幻性的黃樟醚(safrol,油中含量>4%)、肉豆蔻醚(myristicin,油中含量>37%)等毒性物質,需經炮制后入藥,用于治療嘔吐、腹瀉、風濕病、霍亂、胃脹氣等。肉豆蔻的炮制方法有8種:包括面裹煨、麥麩煨、滑石粉煨、蒸制、蛤粉制、炒制、土制、制霜等,目前應用多以麥麩煨制為主,并收錄在《中國藥典》2010版,中醫理論認為肉豆蔻炮制的作用在于 “減毒增效”[1-4]。
肉豆蔻中除富含揮發油、脂肪油外,還有苯丙素及木脂素等成分,國內外對其生品、制品的揮發性組分研究報道較多[5-9],但對中等及大極性組分、尤其是炮制前后這些成分變化與藥效的相關性等研究還十分有限。楊秀偉等[10]從生品肉豆蔻中分離出多個新木脂素衍生物,也進一步說明肉豆蔻的其他藥效組分還待深入認識,這也是對其炮制原理進行深入認識的必要前提。課題在前期對生品肉豆蔻進行脫脂處理后,對其中大極性組分進行了化學研究[11],發現肉豆蔻炮制后乙醇可溶性組分的含量不但有明顯變化,而且有新成分產生。為做進一步認識,本文對炮制品脫脂后的95%乙醇提取物進行了化學分離,結合理化性質及譜學分析鑒定出9個化合物,分別為消旋-去氫二異丁香酚(1)、利卡靈-B(2)、愈創木素(3)、肉豆蔻醚(4)、malabaricone A(5)、malabaricone B(6)、malabaricone C(7)、β-谷甾醇(β-sitosterol,8)、胡蘿卜苷(daucosterol,9)。其中化合物5~7為馬拉巴酮衍生物,文獻記載有很好的抗炎活性[12],但國內至今未見其從生品中分離報道。化合物1~7的結構式見圖1。
1 儀器與材料
1.1 儀器與試劑
Bruker-ARX-300型、AV-600核磁共振儀(TMS內標,瑞士Bruker公司);FL-220高效液相色譜儀(浙江溫嶺福立分析儀器有限公司);101-1-BS-Ⅱ電熱恒溫鼓風干燥箱(上海躍進醫療器械廠);DK-98-1型恒溫水浴鍋(天津市泰斯特儀器有限公司)。柱色譜用硅膠(200~300目)、薄層色譜用硅膠GF254(10~40μm)和薄層色譜用硅膠 H(10~40μm),均為青島海洋化工有限公司生產。柱色譜用分析純試劑、液相用色譜純試劑均為市售。
肉豆蔻藥材購買于河北安國藥材市場,產地海南,經沈陽藥科大學中藥學院中藥學教研室孫啟時教授鑒定為肉豆蔻Myristica fragransHoutt.的干燥種仁。
1.2 藥材炮制品的制備
根據《中國藥典》(2010年版一部)[13]對肉豆蔻記述的炮制方法:取生品肉豆蔻用水浸泡6 h,用水量以浸沒藥材為度,然后取出稍晾,以無明顯水印為度,加入麩皮,麩制溫度150~160℃,時間15 min,至麩皮呈焦黃色,肉豆蔻呈棕褐色,表面有裂隙時取出,每100 g肉豆蔻用40 g麥麩,依法炮制肉豆蔻10 kg備用。
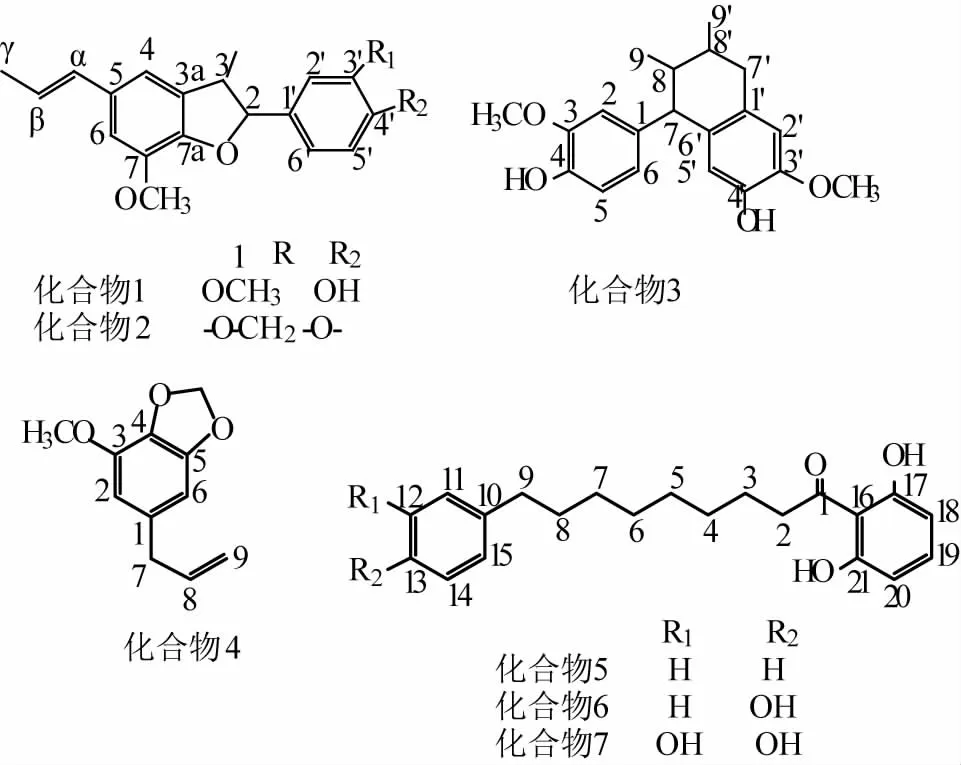
圖1 化合物1~7的化學結構
2 提取分離
取麩制品肉豆蔻(10 kg)粉碎后過20目篩,預先用8倍量石油醚(沸程60~90℃)熱回流提取3次,每次2 h,進行脫脂處理;藥渣用95%乙醇熱回流提取3次,每次2 h,提取液過濾合并,減壓回收乙醇至無醇味,得浸膏3 197 g,以蒸餾水將浸膏分散后,用等體積醋酸乙酯萃取3次,回收溶劑,得浸膏1 210 g。
取醋酸乙酯浸膏200 g,用石油醚-丙酮系統梯度洗脫(100∶0~1∶1)。對各流分進行硅膠、凝膠柱色譜等方法反復分離,得到化合物1(5.2 mg)、2(0.2 g)、3(5.3 mg)、4(9.5 mg)、5(20 mg)、6(18.5 mg)、7(23.2 mg)、8(15.6 mg)、9(1.6 g)。
3 結構鑒定
3.1 化合物1
白色結晶(石油醚),mp 134~136℃,[α]D±0°(c0.1,CHCl3)。1H-NMR(300 MHz,CDCl3):δH1.38(3H,d,J=6.8 Hz,C3-CH3),1.87(3H,dd,J=6.6,1.5 Hz,H-γ),3.45(1H,m,H-3),3.88(3H,s,C7-OCH3),3.89(3H,s,C3′-OCH3),5.10(1H,d,J=9.4 Hz,H-2),5.63(1H,s,C4′-OH),6.11(1H,m,H-β),6.36(1H,dd,J=15.7,1.5 Hz,H-α,6.77(1H,br.s,H-4),6.79(1H,br.s,H-6),6.88(1H,br.d,J=8.3 Hz,H-5′),6.91(1H,br.d,J=8.3 Hz,H-6′),6.97(1H,br.s, H-2′);13C-NMR(75 MHz, CDCl3)δC17.5(C3-CH3),56.0(C7-OCH3),56.0(C3-OCH3),18.4(C-γ),45.6(C-3),93.8(C-2),108.9(C-2′),109.2(C-6),113.3(C-4),114.0(C-5′),120.0(C-6′),123.5(C-β),130.9(C-(),132.1(C-1′),132.2(C-5),133.2(C-3a),144.1(C-7),145.8(C-4′),146.6(C-7a),146.6(C-3′),以上譜學數據與文獻[14]中的一致,故鑒定化合物1為消旋 -去氫二異丁香酚 [(±)-dehydrodiisoeugenol)]。
3.2 化合物2
白色結晶(石油醚-丙酮),mp 89~90℃,1HNMR(300 MHz,CDCl3)δH1.38(3H,d,J=6.8 Hz,C3-CH3),1.87(3H,dd,J=6.6,1.5 Hz,H-γ),3.42(1H,m,H-3),3.89(3H,s,C7-OCH3),5.10(1H,d,J=9.4 Hz,H-2),5.95(2H,s,C3′-OCH2O-C4′),6.11(1H,m,H-β),6.36(1H,dd,J=15.7,1.5 Hz,H-α,6.79(1H,br.s,H-4),6.76(1H,br.s,H-6),6.78(1H,br.d,J=7.9 Hz,H-5′),6.88(1H,br.d,J=7.9Hz,H-6′),6.93(1H,br.s,H-2′);13C-NMR(75 MHz,CDCl3) δC17.9(C3-CH3),55.9(C7-OCH3),18.4(C-γ),45.8(C-3),93.4(C-2),106.8(C-2′),109.2(C-6),134.3(C-4),108.0(C-5′),120.2(C-6′),123.5(C-β),130.9(C-α,134.3(C-1′),132.2(C-5),133.0(C-3a),144.1(C-7),147.6(C-4′),146.5(C-7a),147.9(C-3′),101.0(C3′-OCH2O-C4′),以上譜學數據與文獻[15]一致,故鑒定化合物2為利卡靈-B(licarin-B)。
3.3 化合物3
白色結晶,mp 169~171℃。1H-NMR(300 MHz,CDCl3)δH0.78(3H,d,J=5.7 Hz,H-9′),1.02(3H,d,J=5.8 Hz,H-9),1.49(2H,m,H-8,H-8′),2.64(1H,m,J=3.8 Hz,Ha-7′),3.29(1H,m,J=9.5 Hz,Hb-7′),3.35(1H,s,H-7),6.02(1H,s,H-6′),6.50(1H,dd,J=8.0,1.7 Hz,H-6),6.55(1H,s,H-3′),6.60(1H,d,J=1.7 Hz,H-2),6.70(1H,d,J=8.0 Hz,H-5);13C-NMR(75MHz,CDCl3)δC17.2(C-9),20.0(C-9′),35.3(C-8′),39.3(C-7′),43.1(C-8),53.3(C-7),55.6(C3′-OCH3),111.5(C-6′),113.0(C-2),115.3(C-5),116.3(C-3′),121.7(C-6),126.9(C-1′),132.7(C-2′),137.6(C-1),144.2(C-4′),144.8(C-4),145.7(C-5′),147.5(C-3),以上譜學數據與文獻[16]一致,故鑒定化合物3為愈創木素(guaiacin)。
3.4 化合物4
黃 色 油 狀 物,1H-NMR(300 MHz,CDCl3)δH3.28(2H,d,J=6.7 Hz,H-7),3.88(3H,s,C3-OCH3),5.06(2H,m,H-9),5.92(1H,m,H-8),5.92(2H,s,C4-OCH2O-C5),6.35(1H,br.s,H-2),6.38(1H,br.s,H-6);13C-NMR(75 MHz,CDCl3)δC40.1(C-7),56.4(C3-OCH3),101.1(C4-OCH2O-C5),102.6(C-6),107.5(C-2),115.8(C-9),133.3(C-4),134.5(C-1),137.3(C-8),143.4(C-5),148.7(C-3)。以上譜學數據與文獻[17]一致,鑒定其為肉豆蔻醚(myristicin)。
3.5 化合物5
白色針晶(甲醇)。1H-NMR(300 MHz,CDCl3)δH2.61(2H,t,J=7.5 Hz,H-9),3.12(2H,t,J=7.5 Hz,H-2),6.39(2H,d,J=8.1 Hz,H-18,H-20),7.19(1H,t,J=8.1 Hz,H-19),7.24(5H,m,H-11~H-15),9.50(2H,s,C17-OH,C21-OH),1.34(8H,H-5~H-8),1.66(4H,m,H-3,H-4);13C-NMR(75MHz,CDCl3)δC128.4(C-11,C-15),128.2(C-12,C-14),161.1(C-17,C-21),108.4(C-18,C-20),135.6(C-19),110.0(C-16),207.9(C-1),142.9(C-10),125.5(C-13),44.7(C-2),24.3(C-3),29.4(C-4,C-5),29.2(C-6,C-7),31.4(C-8),35.9(C-9),以上譜學數據與文獻[18]一致,鑒定其為 Malabaricone A。
3.6 化合物6
白色針晶(甲醇)。1H-NMR(300 MHz,CDCl3)δH2.54(2H,t,J=7.5 Hz,H-9),3.11(2H,t,J=7.5 Hz,H-2),6.39(2H,d,J=8.1 Hz,H-18,H-20),7.25(1H,t,J=8.1 Hz,H-19),6.78(2H,d,J=8.4Hz,H-11,H-15),7.05(2H,d,J=8.4 Hz,H-12,H-14),7.25(1H,t,J=8.1 Hz,H-19),9.42(2H,s,C17-OH,C21-OH),9.07(1H,s,C13-OH),1.32(8H,H-5~H-8),1.69(4H,m,H-3,H-4);13C-NMR(75 MHz,CDCl3)δC129.4(C-11,C-15),115.0(C-12,C-14),161.1(C-17,C-21),108.5(C-18,C-20),135.6(C-19),110.0(C-16),207.8(C-1),135.2(C-10),153.3(C-13),44.7(C-2),24.3(C-3),29.4(C-4~C-6),29.2(C-7),31.2(C-8),35.6(C-9)。以上譜學數據與文獻[18]一致,鑒定其為Malabaricone B。
3.7 化合物7
白色針晶(甲醇)。1H-NMR(600 MHz,DMSO-d6)δH2.61(2H,t,J=7.8 Hz,H-9),3.01(2H,t,J=7.2 Hz,H-2),6.35(2H,d,J=7.8 Hz,H-18,H-20),7.19(1H,t,J=7.8 Hz,H-19),6.54(1H,d,J=2.4 Hz,H-11),6.40(1H,dd,J=7.8,2.4 Hz,H-15),6.60(1H,d,J=7.8 Hz,H-14),7.19(1H,t,J=8.1 Hz,H-19),11.55(2H,s,C17-OH,C21-OH),8.54(2H,s,C12-OH,C13-OH),1.27(8H,H-5~H-8),1.58(2H,m,H-3),1.47(2H,m,H-4);13C-NMR(75 MHz,DMSO-d6)δC115.2(C-11),143.8(C-12),141.8(C-13),114.9(C-14),120.0(C-15),161.8(C-17,C-21),107.5(C-18,C-20),135.7(C-19),110.1(C-16),207.3(C-1),135.3(C-10),44.6(C-2),24.3(C-3),29.2(C-4~C-6),28.9(C-7),31.4(C-8),35.3(C-9)。以上譜學數據與文獻[18]一致,鑒定其為Malabaricone C。
3.8 化合物8
白色針晶(丙酮),mp 136~138℃。Lieberman-Burchard反應陽性,將該單體化合物與已知對照品β-谷甾醇共薄層,在3種溶劑系統下Rf值均一致,故鑒定化合物其為β-谷甾醇。
3.9 化合物9
白色粉末(甲醇),mp>300℃。Lieberman-Burchard反應陽性,Molish反應陽性。將該單體化合物與胡蘿卜苷對照品共薄層,在3種溶劑系統下Rf值一致,混合后測定熔點不下降,鑒定其為胡蘿卜苷。
4 討論
對肉豆蔻中的揮發性組分炮制前后的變化,楊秀偉等[19]以氣相、氣相-質譜(GC-MS)聯用技術對生品、炮制品都進行過分析研究,至今已檢出100余個化學成分,其中已鑒定出的化學結構有80余種。另外,根據肉豆蔻炮制后揮發油的變化情況,認為炮制后揮發油含量都有不同程度的降低,其顏色、比重、旋光度、折光率亦有改變,毒性成分黃樟醚、肉豆蔻醚的含量也有不同程度的降低。我們前期對肉豆蔻成分進行的研究中也發現,肉豆蔻炮制前后的甲醇提取物的化學成分及含量組成均有變化。國外學者從生品肉豆蔻的外種皮中分離得到了馬拉巴酮衍生物[20],且有很好的抗炎、抗菌活性,但至今未見國內有過分離報道,我們在前期的生品中也未能發現該類成分,推測其在原植物種仁中含量較少,但經炮制加工后,此類化合物卻易于分離得到,推測炮制帶來了含量的明顯變化,然而是否為基于內源性成分在炮制條件下進行的轉化卻不得而知,尤其是炮制帶來的 “減毒增效”作用是否與該類成分存在必然聯系,尚需深入研究才能得出正確的結論。
[1]代冬梅,賈天柱,徐洪亮,等.肉豆蔻炮制及現代研究進展[J].中成藥,2005,27(12):1416-1419.
[2]代冬梅,賈天柱,相宇,等.中藥肉豆蔻歷史沿革研究[J].時珍國醫國藥,2005,16(8):707-708.
[3]天津市藥品檢驗所中藥組.關于肉豆蔻炮制方面有關問題的探討[J].中草藥通訊,1979,10(1):16.
[4]俞永瓊.淺談肉豆蔻的炮制[J].云南中醫中藥雜志,2001,22(3):46.
[5]李鐵林,周杰,江文君,等.炮制對肉豆蔻揮發油成分及肉豆蔻醚含量影響的研究[J].中國中藥雜志,1990,15(8):23-25.
[6]賴聞玲,曾志,陳億新,等.中藥復方中瀉下組份化學成分研究(Ⅱ)肉豆蔻揮發油[J].中草藥,2002,33(7):596-598.
[7]劉博,陳開勛,陳渭萍,等.肉豆蔻超臨界二氧化碳萃取工藝及其精油的GC-MS分析研究[J].香料香精化妝品,2003,31(4):17-19.
[8]王瑩,楊秀偉,陶海燕,等.商品肉豆蔻揮發油成分的GCMS分析[J].中國中藥雜志,2004,29(4):339-342.
[9]王瑩,楊秀偉.印度尼西亞產肉豆蔻揮發油成分的GCMS分析[J].中華中醫藥雜志,2007,22(9):603-606.
[10]楊秀偉,黃鑫,艾合買提·買買提.肉豆蔻中新的新木脂素類化合物[J].中國中藥雜志,2008,33(4):397-402.
[11]李秀芳,吳立軍,賈天柱,等.肉豆蔻的化學成分[J].沈陽藥科大學學報,2006,23(11):698-701.
[12]Shinohara C, Mori S, Ando T, et al.Arg-gingipain inhibition and anti-bacterial activity selective for Porphyromonas gingivalis by malabaricone C[J].Biosci Biotechnol Biochem,1999,63(8):1475-1477.
[13]國家藥典委員會.中國藥典[S].一部.北京:中國醫藥科技出版社,2010:127.
[14]Enriquez R.G.,Chavez M.A.,ReynoldsW.F.Phytochemical investigations of plants of the genus aristolochia,Isolation and NMR spectral characterization of eupomatenoid derivatives[J].JNat Prod,1984,47(5):896-899.
[15]Wenkert E,Gottlieb H E,Gottlieb O R,et al.13C-NMR Spectroscopy of neolignans[J].Phytochem,1976,15(10):1547-1551.
[16]Fo R B,De Carvalho MG,Gottlieb O R.The chemistry of Brazilian Myristicaceae[J].Planta Med,1984,50(1):53-55.
[17]Benevides PJC,Sartorelli P,Kato MJ.Phenylpropanoids and neolignans from Piper regnellii[J].Phytochem,1999,52(2):339-343.
[18]Purushothaman K K,Sarada A,Connolly JD.Malabaricones A-D,Novel Diarylnonanoids from Myristica malabarica Lam(Myristicaceae)[J].JChem Soc,Perkin TransⅠ,1977,(5):587-588.
[19]黃鑫,楊秀偉.不同炮制品肉豆蔻揮發油成分的GC-MS分析[J].中國中藥雜志,2007,32(16):1669-1675.
[20]Orabi K Y,Mossa J S,EI-Feraly F S.Isolation and characterization of two antimicrobial agents from Mace(Myristica Fragrans)[J].J Nat Prod,1991,54(3):856-859.
Isolation and Identification of Chem ical Constituents from Processed Myristica fragrans Houtt.
ZHAO Guang-yun,WANG Xiao-xia,GAO Hui-yuan
(Key Laboratory of Structure-Based Drug Design&Discovery of Ministry of Education,Shenyang Pharmaceutical University,Shenyang611001,China)
Objective:To isolate the chemical constituents from the processed Myristica fragrans Houtt.,and identify their structures.MethodsMyristica fragransHoutt.was delt with the wheat bran processing method.Compoundswere isolated by Sephadex LH-20,ODS column chromatographies,and their structureswere identified on the basis of the physico-chemical properties and their spectral data.Results:Nine compoundswere obtained and they were elucidated as(±)-dehydrodiisoeugenol(1),licarin-B(2),guaiacin(3),myristicin(4),malabaricone A(5),malabaricone B(6),malabaricone C(7),β-sitosterol(8),daucosterol(9),respectively.Conclusion:Compounds5~7 were identified asmalabaricone derivatives,while they have not reported from crudematerial of this plant in China,and processing preparation was supposed to be the reason for the contents increasing of these components.
Myristica fragransHoutt.;Processing;Chemical constituents;Structrual identification
*高慧媛,Tel:(024)23986482,E-mail:gaohuiyuan1997@yahoo.com.cn
2011-09-20)

