退火條件對山梨醇玻璃焓松弛參數的影響
葉 斌 高 才 劉向農 楊 鎖 江 斌
(合肥工業大學機械與汽車工程學院,合肥230009)
退火條件對山梨醇玻璃焓松弛參數的影響
葉 斌 高 才*劉向農 楊 鎖 江 斌
(合肥工業大學機械與汽車工程學院,合肥230009)
采用差示掃描量熱法(DSC)測定山梨醇樣品經歷不同時間(ta)等溫退火后,以10 K·min-1速率進行升溫時玻璃化轉變溫度(Tg)前后的比熱容(Cp(T)).將Gómez Ribelles(GR)提出的一種基于構型熵的現象學模型用于描述山梨醇玻璃的焓松弛行為,考察GR模型能否適用于小分子玻璃體系.結果表明,單組GR模型參數擬合的曲線均能較好重現對應熱歷史條件下的山梨醇體系的實驗所得Cp(T)曲線,盡管并未找到不隨熱歷史而變的一組參數作為材料常數,但與其它現象學模型應用于小分子玻璃時,其模型參數都隨熱歷史變化而變化的特點相比,GR模型的某些參數基本保持不變.且在較長退火時間下擬合得到的模型參數普適性較好.同經歷連續降溫的山梨醇相比,等溫退火過程得到的松弛極限態參數(δ)的平均值與Tg處比熱容增量(ΔCp(Tg))的比值明顯增大,但仍小于聚合物的值,表明GR模型提出的亞穩極限態對小分子玻璃的影響值得商榷.
焓松弛;差示掃描量熱法;構型熵;山梨醇;玻璃化轉變;等溫退火;脆度
1 引言
玻璃化轉變是玻璃態與橡膠態之間的轉變,可看成是較長分子(或鏈段)運動的“凍結”或“解凍”過程,對應溫度稱為玻璃化轉變溫度(Tg).1玻璃態物質多處于熱力學非平衡態,在Tg溫度以下會逐漸向平衡態轉變,體系的熱力學性質(焓、熱膨脹系數)以及力學性質(模量、力學損耗)也隨之發生連續變化,稱之為結構松弛,當采用焓的變化來描述結構松弛時則稱為焓松弛.2有許多實驗方法可研究這一現象,其中以差示掃描量熱法(DSC)應用最為廣泛,它是通過獲取一定升溫速率下跨越玻璃化轉變區域的比熱容,推測體系之前所經歷的復雜熱歷史及微觀位形的演變,為合理使用材料提供科學依據.3,4一些現象學模型可以較好地描述玻璃化體系的轉變和松弛行為,代表性的有Tool-Narayanaswamy-Moynihan (TNM)5-7和Adam-Gibbs-Voegel(AGV)8,9模型,二者均使用假想溫度Tf來表征體系的結構演變,5只是特征松弛時間的表達有所差異.盡管兩個模型能很好地重現玻璃化體系的升溫比熱容,但模型參數有時不是材料常數,而是隨體系熱歷史的不同而變化.此外,這兩個模型都假定只要時間足夠長,玻璃態最終會松弛到對應溫度的平衡態,但迄今未被實驗所證實.5-9Gómez Ribelles(GR)等10,11在Adam-Gibbs(AG)8協同松弛理論基礎上,擯棄了傳統現象學模型中用假想溫度表征結構演變的做法,而是提出用構型熵演變表征體系結構的變化.12-15不僅如此,該模型還假設玻璃態不能最終松弛到對應溫度的平衡態,而只能松弛到某一中間亞穩極限態.由于聚合物是鏈狀大分子的緣故,中間亞穩極限態理論的提出確實使GR模型預測聚合物焓松弛的能力有了明顯提高,13-15近年來該模型在聚合物玻璃的松弛動力學研究中也得到廣泛應用,16-22但迄今為止尚未見到有人將此模型用于研究聚合物玻璃以外的體系,尤其是對于小分子玻璃體系而言是否也存在這樣的一個亞穩極限態還不得而知,也并未有相關文獻來說明.本文正是為研究GR模型中提出的亞穩極限態是否適用于小分子玻璃而展開的.在稍早的工作中,我們已將此模型用于研究無定形山梨醇體系經歷連續降溫的情形,23結果表明GR模型能很好地重現山梨醇不同降溫速率下Cp(T)曲線,且某些模型參數表現出不隨熱歷史的變化而變化的特征,相對于其他模型改進效果明顯.但物質的熱歷史不僅包括經歷不同降溫速率,還應包括退火(物理老化),由于現實中這種現象較連續降溫更為常見,因此考察等溫退火條件下山梨醇玻璃的松弛特性和GR模型參數可能展現的新特征,現實意義更為明確.
GR模型是在Kohlrausch-Williams-Watts(KWW)和AG描述的傳統理論的基礎上,提出用構型熵(Sc)替代TNM和AGV模型中的假想溫度Tf來表征體系的結構演變,并設想玻璃態物質在時間t→∞時并不能松弛到過冷液體線性外推的平衡態,而只能松弛到依溫度而變的另一假想的極限態(如圖1所示).
如用Sclim() T表示此極限態構型熵,并用T(ξ)(其中ξ滿足-∞<ξ≤t)表示溫度歷史,將溫度歷史表示為

h為單位階躍函數,則構型熵Sc(t)可表示:10
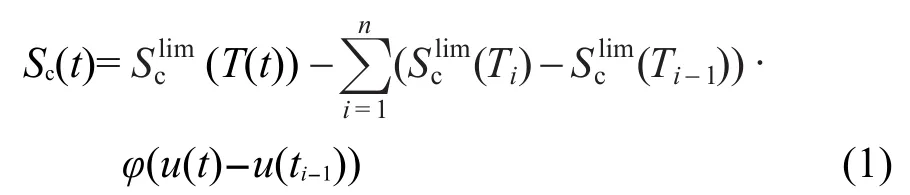
φ(u)是松弛函數(也稱衰減函數),可用KWW延展指數函數得到:

β是表征體系松弛時間譜分布寬度的非指數參數(0≤β≤1),u(t)為約化時間:6

τ(σ)是特征松弛時間,由σ時刻的構型熵(Sc)和溫度(T)共同決定.由AG協同松弛理論:

圖1 基于構型熵的焓松弛模型中松弛極限態示意圖12Fig.1 Scheme of the hypothetical limit state in the enthalpy relaxation model based on the configurational entropy12Sketch of the configurational entropy corresponding to the equilibrium liquid state(eq.)(dashed line),to an experimental cooling scan at a finite cooling rate(solid line),and to the metastable line of the hypothetical limit states of the structural relaxation process(lim.) (dashed-dotted line).Tg:glass transition temperature, Td:Tg+5,Tu:Tg+10
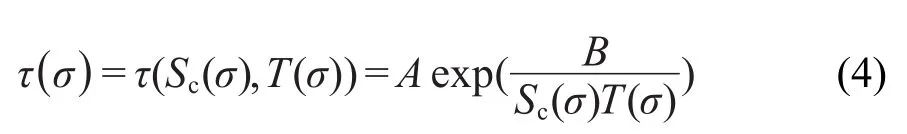
其中A是指前因子,可看成是體系在無限高溫度下的松弛時間;B=Sc*Δμ/k,Sc*表示最小協同重排域的位形熵;Δμ表示阻止單體(鏈段或分子)協同重排的能量勢壘,k是Boltzmann常數.
在Tg以上,極限構型熵與平衡態相同:

其中位形比熱容ΔCp(T)=Cpl(T)?Cpg(T),Cpl(T)和Cpg(T)分別表示過冷液體與玻璃的比熱容;T2是Gibbs-Dimarzio轉變溫度;θ為積分變量.24
在玻璃化轉變區及Tg以下,極限構型熵可表示為:
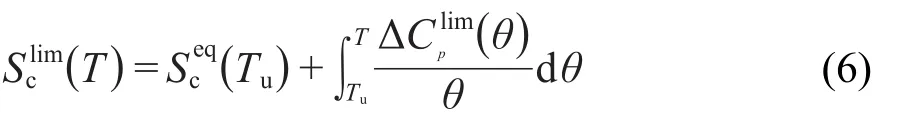
其中Tu是Tg以上的某一溫度(通常取Tu=Tg+10).
借鑒Hodge等25的做法,由以上各式可得經歷等溫退火后的構型熵表達:

其中ta為退火時間,nA(nA≤n≤nA+10)是開始退火子步,當 k=nA+1時,Δta,k=t110a;當k>nA+1時,Δta,k=
Gómez Ribelles12通過定義構型焓(Hc)建立構型熵和比熱容的關聯:
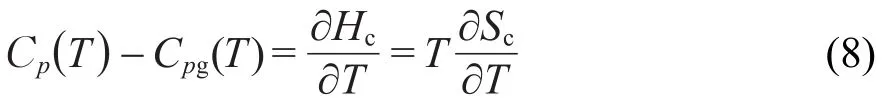
由圖1可知玻璃態斜率dSlimc(T)/dT=(ΔCp(T)-δ)/T,故該模型中共有A,B,β,T2,δ五個待求參數,可用曲線擬合方法確定,并通過最優搜索使模型預測的Cp(T)曲線和DSC測定的結果最接近.
2 實驗部分
2.1 試劑與儀器
結晶態山梨醇(瑞士Fluka,純度99%,合肥森瑞科貿有限公司進口分裝)未經進一步純化,置于常溫、壓力40 Pa的真空干燥箱中干燥24 h后備用.取樣品5-10 mg(精確到±0.01 mg)置于標準液體鋁皿中央并壓蓋密封.采用配備G-M二級制冷系統的DSC儀器(Pyris-Diamond,美國Perkin-Elmer公司),標稱最低溫度193 K,實測DSC內樣品溫度最低可達約200 K.DSC以金屬銦(99.999%,Perkin-Elmer)和純水(自制二次蒸餾去離子水)做兩點溫度標定,標定范圍210-320 K;以冰的融化潛熱(333.88 J·g-1)進行單點焓尺度標定,標定速率10 K·min-1.氮氣(99.999%)氣氛,流量約25 mL·min-1,并保持恒定.
2.2 DSC實驗流程
山梨醇晶體以10 K·min-1的速率升溫至388 K充分熔融后降溫至Tg(267.5 K左右)以下,結果表明,熔融態的山梨醇不再形成結晶體,而是形成完全的玻璃態.
等溫退火實驗流程如圖2所示,先將玻璃態樣品升溫至加樣溫度303.15 K后,以10 K·min-1的降溫速率降至Ta=253.15 K等溫退火(退火時間ta分別為10、30、60、120、240、480 min),再以10 K·min-1繼續降溫至218.15 K,待熱流穩定后按如下溫度程序采集數據:(1)等溫1 min;(2)以10 K·min-1速率升溫到308.15 K;(3)等溫1 min.取和樣品皿質量相同的空皿(±0.01 mg),驟冷至218.15 K,熱流穩定后,按與分析樣品相同的溫度程序獲得基線熱流,用于比熱容計算,為保證熱接觸狀況的一致性,針對一個樣品的所有分析結束后再獲得一條用于計算比熱容的基線.

圖2 測量不同退火時間(ta)的等溫退火焓松弛的實驗程序Fig.2 Schematic representation of the experimental procedure for measuring the isothermal annealing enthalpy relaxation with different annealing time(ta)qc(cooling rate)=10 K·min-1,qh(heating rate)=10 K·min-1, Ta=253.15 K
2.3 曲線擬合及誤差分析
曲線擬合程序以Matlab?語言編制,采用Nedler-Mead搜索方法26尋求最優參數,使模型與實驗數據之間擬合的均方差最小:
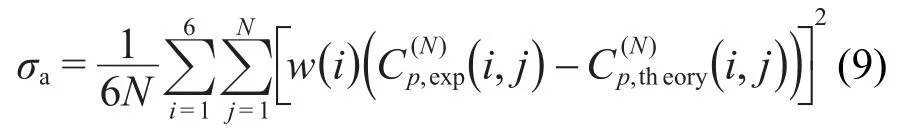
式中i是實驗次數,j是實驗掃描時的溫度點,w(i)為權重因子.最優搜索可以通過固定T2或者B來實現,將B置于循環之外來進行處理.數據誤差主要來自如下3方面:(1)平行樣間誤差;(2)DSC重復性誤差;(3)曲線擬合誤差.分析結果表明,曲線擬合誤差最大.
3 結果和討論
3.1 結 果
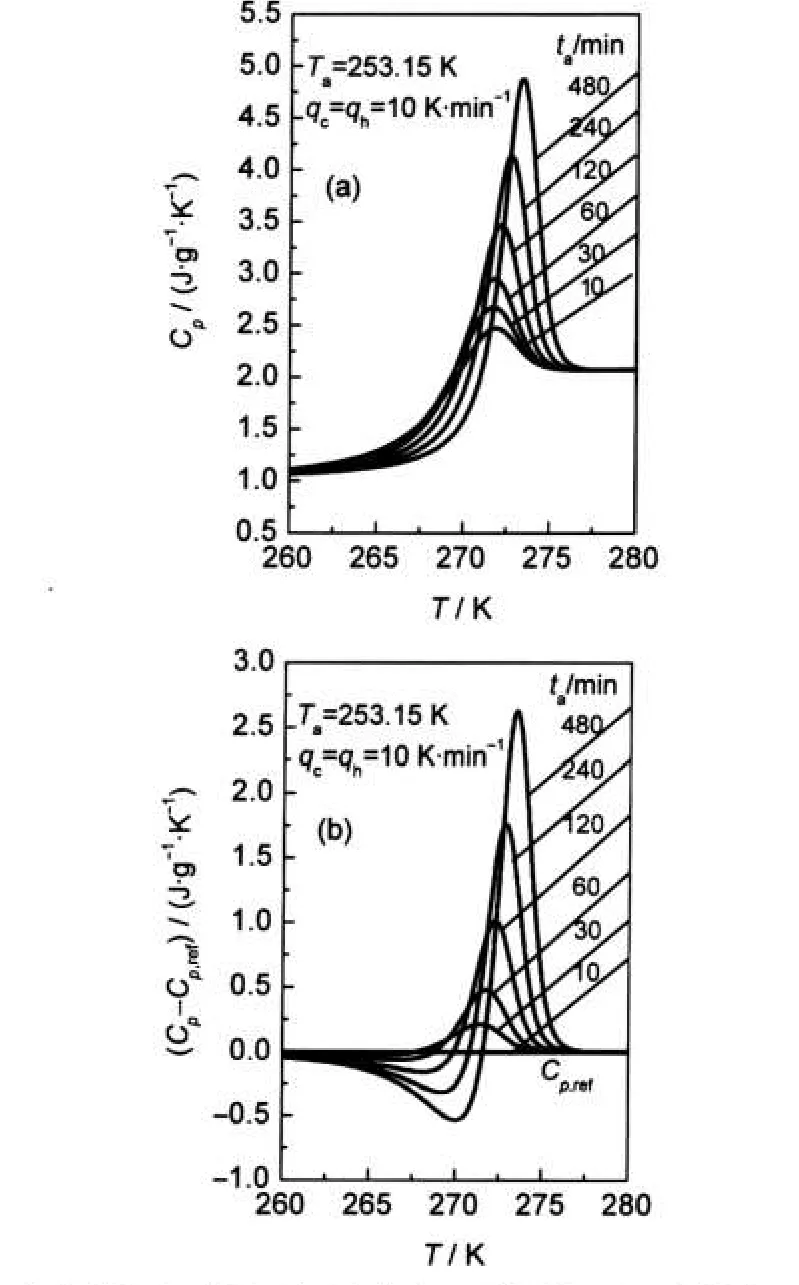
圖3 不同退火時間下山梨醇在Tg附近的比熱容曲線(a)以及與參照比熱容之差(b)Fig.3 Specific heat capacity curves near Tgat different annealing time for D-sorbitol(a)and difference between the Cp(T)curves of the reference scan(b)

圖4 253.15 K時恢復焓ΔH與ta的關系Fig.4 Recovery enthalpy ΔH as a function of the annealing time for D-sorbitol annealing at 253.15 KΔH-ta(☆),ΔH-1/ta(□),ΔH-lgta(○)
采用DSC測定的山梨醇玻璃在Tg前后的比熱容曲線如圖3(a)所示.觀察發現,經歷不同ta的山梨醇在玻璃化轉變區域的高溫側皆呈現α松弛所引起的明顯焓恢復峰,且隨ta的增加,比熱容最大值Cp_max增加明顯,峰的右移效果顯著.在進行恢復焓計算時,需預先獲取一條未發生明顯松弛體系的比熱容曲線作為參照.由于ta越小,其松弛效應越不顯著,故選擇ta=10 min的比熱容曲線作為參考曲線Cp,ref,計算結果如圖3(b)所示,同連續降溫相比,熱流“下沖”現象顯著.圖4表示實驗得到的恢復焓ΔH與ta關系,觀察發現隨ta增加,ΔH起始增加顯著,隨后趨于平緩,說明此時山梨醇玻璃接近亞穩極限態,由ΔH-1/ta關系外推可求得山梨醇玻璃在t→∞時,恢復焓極限值ΔH∞約為3.11 J·g-1,ΔH與lgta基本呈線性關系.
表1列出由DSC實驗讀取的恢復焓,及按不同讀取方法27獲得的Tg.此前針對山梨醇連續降溫的實驗結果23表明,隨降溫速率的增加,極限假想溫度Tf′逐漸增加,而其余讀法則無規律.而由表1可知,隨ta的增加,Tf′逐漸減小,其余讀法的溫度則是單調遞增.比較發現,等溫退火實驗得到的Tf′略低于Duvvuri等28利用介電法的分析結果(267.5 K).盡管退火時間的不同可能會導致體系微觀結構和松弛程度的差異,但表1結果顯示,松弛并未引起比熱容增量ΔCp(Tg)的明顯變化.玻璃化轉變過程中ΔCp(Tg)被稱為熱力學脆度,它的大小表明了玻璃在升溫過程中自由度的釋放程度,值越大,則由玻璃態轉變為過冷態后,松弛單元獲得的活動性越大,29等溫退火實驗得到的ΔCp(Tg)值保持在0.94 J·g-1·K-1,與連續降溫實驗23的ΔCp(Tg)=0.99 J·g-1·K-1相比,稍低.
3.2 討 論
同TNM和AGV模型相比,GR模型引入了新參數δ,進一步增加了曲線擬合的難度.盡管GR模型無需使用無量綱比熱容,減少了無量綱化造成的誤差,但與TNM模型25,30,31和Scherer-Hodge模型9,30,32-34相似,GR模型參數A、B、T2和β之間依然存在相關性,10-12全參數擬合的結果難以找到全局最優解.故需在擬合中人為選定某一參數后求取其他參數.目前除了Théneau等17選擇A及Andreozzi等34-36選擇T2以外,其余均是將B作為可選參數,如Brunacci等37在B=500-3000 J·g-1的范圍內獲取了聚苯乙烯的GR模型參數,Gómez Ribelles等10在B=1000-2000 J·g-1的范圍內獲取了聚碳酸酯的GR模型參數, Meseguer Due?as等13在B=500-1500 J·g-1的范圍內獲取了丙烯腈共聚物的GR模型參數.由于同聚合
物相比,其它模型參數隨B值的變化相對緩慢,因此在曲線擬合程序中將B值選取在一個更寬的范圍(500-5000 J·g-1)內.結果表明,當B在500-5000 J· g-1范圍內,GR模型均能很好地重現DSC實驗測得的升溫比熱容曲線.擬合得到的GR模型參數如表2所示.圖5給出B=3000 J·g-1時不同ta下GR模型預測Cp值與實驗數據的比較結果(其它參數見表2).顯然,針對單條實驗Cp(T)曲線,計算程序始終能找到一組與之對應的GR模型參數,使得模型預測值和實驗值相吻合.
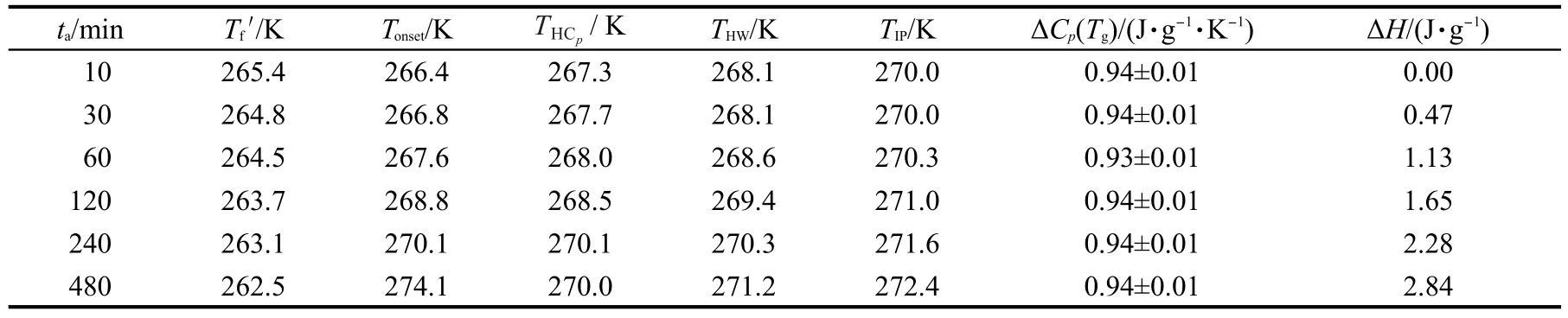
表1 不同ta下山梨醇玻璃化轉變溫度(Tg)和焓恢復參數Table 1 Glass transition temperature(Tg)and enthalpy recovery parameters of D-sorbitol at different annealing time

表2 曲線擬合方法得到的不同退火時間山梨醇玻璃GR模型參數Table 2 GR model parameters of D-sorbitol glass at different annealing time obtained using curve-fitting method
假設液態與玻璃態的比熱容與溫度之間存在線性關系,對ΔCp(T)來說這種線性關系依然存在,在GR模型中常表示為溫度T的線性函數.如取6條實驗曲線的平均值,可得到:
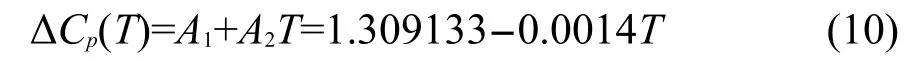
由于A2為負值,因此在Tg之上的某一個溫度(T≈935 K),ΔCp=0.Hodge在AGV模型9中使用雙曲關系ΔCp(T)=ΔCp(Tg)Tg/T計算ΔCp,隨T的增加,ΔCp減小,但它并不會等于零.由表1可知兩種方法計算結果基本相同.
Moynihan等7提出利用極限假想溫度隨降溫速率的依變關系確定松弛活化焓

由連續降溫實驗結果得到Δh*/R=79.258×103K.根據Angell38,39提出的動力學脆度計算公式:

得到m≈128.6,這與介電松弛分析得到的結果(m≈127.0)28非常吻合.根據公式(4)可推知:

由公式(5)、(10)、(11)、(12)及表2數值,計算各種ta下不同B對應動力學脆度m,結果見表2.觀察發現,當B≤4000 J·g-1,隨ta增加,相同B值對應的m逐漸減少,而B=5000 J·g-1時,m的變化則毫無規律.此前文獻40發現采用TNM模型擬合的松弛活化焓要小于變降溫速率實驗計算得到的結果,但是這一現象在應用GR模型描述經歷等溫退火熱歷史的山梨醇玻璃時得到改觀.表2的脆度計算結果表明,多種狀況下m>128.6.B=3000 J·g-1時,脆度平均值mmean約為129.2,和式(11)及介電松弛的分析結果吻合.同時也發現,不同退火時間下,B=3000 J·g-1時,Tg-T2的平均值約為51.1 K,這也與大多數玻璃化物質這一結論41吻合.

圖5 山梨醇實驗(○)與GR模型預測(-)的比熱容(Cp)曲線Fig.5 Curves of specific heat capacities(Cp)of experimental data(○)and GR fits(-)for D-sorbitolB=3000 J·g-1,the remaining parameters of GR model as shown in Table 2.ta/min:(a)480,(b)240,(c)120,(d)60,(e)30,(f)10
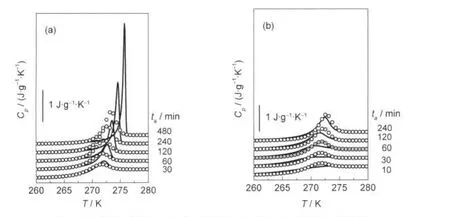
圖6 GR模型預測(-)與山梨醇實驗(○)的比熱容(Cp)曲線對照Fig.6 Comparison between some of the predictions of the GR model(-)and the experimental scans(○)parameters obtained for D-sorbitolthe GR model parameters at(a)ta=10 min,B=3000 J·g-1,-ln(A/s)=46.78,T2=213.6 K,β=0.510,δ=0.281 J·g-1·K-1; (b)ta=480 min,B=3000 J·g-1,-ln(A/s)=42.70,T2=209.7 K,β=0.372,δ=0.0125 J·g-1·K-1
由表2可知,與已報道過的某些聚合物12,13的參數δ基本保持不變(且普遍較大)的特點不同,經歷等溫退火熱歷史后的山梨醇的δ是在一定范圍(0.001-0.464 J·g-1·K-1)內波動.B=3000 J·g-1時山梨醇玻璃δ的平均值為0.107 J·g-1·K-1,約為ΔCp(Tg)的11.4%.連續降溫過程中B=4000 J·g-1時δ的平均值為0.021 J·g-1·K-1,約為ΔCp(Tg)的2.0%,對比發現等溫退火條件下得到的δ明顯偏大,可以推斷對于山梨醇玻璃體系而言,等溫退火條件下的亞穩松弛極限態要更遠離平衡液態外推對應的平衡態,但是仍然要小于某些聚合物的δ值,這也許是因為聚合物是鏈狀大分子的緣故,所以受亞穩態極限參數δ的影響較大,但對小分子山梨醇玻璃體系來說,GR模型所提出的亞穩極限態概念的影響還值得進一步探討.
現象學模型參數須為材料常數,即與體系經歷的熱歷史無關,13圖5顯示單組擬合參數能很好地重現對應熱歷史的實驗Cp(T)曲線,但這組參數是否適用于其它熱歷史尚不清楚.如果其中的某組參數能夠較好地重現所有熱歷史的DSC實驗曲線,則可將其近似看成不依賴于熱歷史的材料常數.但表2中無法找到這樣一組參數,只是B=3000 J·g-1時,-lnA和T2變化不大,可看成是材料常數,而β值則隨ta的增加而逐漸減小,且變化幅度較大.但通過用不同退火時間下的模型參數來預測其它實驗條件下比熱容曲線,可以發現用GR模型對經歷等溫退火熱歷史山梨醇的焓松弛行為進行描述時,哪種實驗條件下得到的模型參數的預測力更好.圖6表示B=3000 J· g-1時(其它B值結果相同,未列出)分別將ta=10 min和ta=480 min的兩組GR參數(其余參數見表2)看成材料常數后用來預測其它退火時間實驗比熱容的結果.觀察發現較短退火時間擬合得到的模型參數普適性較差,用來預測其它熱歷史的效果不能令人滿意,而反之效果稍微好一些,至少峰形和臺階變化不大.總體來說將GR模型應用在山梨醇玻璃焓松弛行為研究過程中也并不能發現一組確定的模型參數可以作為不依賴于熱歷史的材料常數,但是考慮到TNM和AGV模型應用于多元醇玻璃體系時,其模型參數都隨熱歷史的變化而變化,27,42而GR模型中某些參數值基本保持不變,這一點值得肯定.
4 結論
采用DSC技術結合GR模型考察了經歷不同退火時間的山梨醇玻璃的焓松弛行為.由實驗數據可推知,當退火時間無限長時,山梨醇的恢復焓極限值為3.11 J·g-1.擬合結果表明單組GR模型參數能很好地重現對應熱歷史條件下的山梨醇體系的實驗比熱容,但也并未找到一組模型參數能作為材料常數,但B為3000 J·g-1時,-lnA和T2的變化并不明顯,與TNM和AGV模型的四個參數都在變化相比,GR模型已經有了很大的改善.且觀察發現,采用較長退火時間的GR模型參數對較短退火時間的實驗升溫比熱容進行預測時,效果稍好一些.與連續降溫過程相比,松弛極限態參數δ值增加顯著,可判定等溫退火條件下的山梨醇玻璃體系亞穩極限態更加遠離過冷液體外推平衡態,但仍低于某些聚合物的相應值.盡管GR模型提出的亞穩極限態用在小分子玻璃上確實有值得商榷的地方,但采用GR模型擬合得到的山梨醇動力學脆度參數與介電松弛分析得到的結果卻很吻合.
(1) Lebrun,N.;van Miltenburg,J.C.J.Alloy.Compd.2001,320, 320.
(2) Hodge,I.M.J.Non-Cryst.Solids 1994,169,211.
(3) Hutchinson,J.M.;Kumar,P.Thermochim.Acta 2002,391,197.
(4)Cameron,N.R.;Cowie,J.M.G.;Ferguson,R.;McEwan,I. Polymer 2000,41,725.
(5)Tool,A.Q.J.Am.Ceram.Soc.1946,29,240.
(6)Narayanaswamy,O.S.J.Am.Ceram.Soc.1971,54,491.
(7) Moynihan,C.T.;Easteal,A.J.;DeBolt,M.A.;Tucker,J.J.Am. Ceram.Soc.1976,59,12.
(8)Adam,G.;Gibbs,J.H.J.Chem.Phys.1965,43,139.
(9) Hodge,I.M.Macromolecules 1987,20,2897.
(10) Gómez Ribelles,J.L.;Monleón Pradas,M.Macromolecules 1995,28,5867.
(11) Gómez Ribelles,J.L.;Monleón Pradas,M.;Vidaurre Garayo, A.;Romero Colomer,F.;Más Estellés,J.;Mese-guer Due?as,J. M.Macromolecules 1995,28,5878.
(12) Gómez Ribelles,J.L.;Monleón Pradas,M.;Vidaurre Garayo, A.;Romero Colomer,F.;Más Estellés,J.;Meseguer Due?as,J. M.Polymer 1997,38,963.
(13)Meseguer Due?as,J.M.;Vidaurre Garayo,A.;Romero Colomer,F.;Más Estellés,J.;Gómez Ribelles,J.L.;Monleón Pradas,M.J.Polym.Sci.Part B:Polym.Phys.1997,35,2201.
(14) Gómez Ribelles,J.L.;Vidaurre Garayo,A.;Cowie,J.M.G.; Ferguson,R.;Harris,S.;McEwen,I.J.Polymer 1998,40,183.
(15) Cowie,J.M.G.;Harris,S.;Gómez Ribelles,J.L.;Meseguer,J. M.;Romero,F.;Torregrosa,C.Macromolecules 1999,32,4430.
(16) Tanaka,Y.Polym.J.2009,41,125.
(17) Théneau,C.;Salmer?n Sánchez,M.;Rodríguez Hernández,J. C.;Monleón Pradas,M.;Saiter,J.M.;Gómez Ribelles,J.L. Eur.Phys.J.E 2007,24,69.
(18) Mano,J.F.;Gómez Ribelles,J.L.;Alves,N.M.;Salmer?n Sánchez,M.Polymer 2005,46,8258.
(19)Alves,N.M.;Gómez Ribelles,J.L.;Manoa,J.F.Polymer 2005, 46,491.
(20) Salmer?n Sánchez,M.;Touzé,Y.;Saiter,A.;Saiter,J.M.; Gómez Ribelles,J.L.Colloid Polym.Sci.2005,283,711.
(21)Andreozzi,L.;Autiero,C.;Faetti,M.;Galli,G.;Giordano,M.; Zulli,F.Macromol.Rapid Commun.2008,29,928.
(22)Hernández Sánchez,F.;Meseguer Due?as,J.M.;Gómez Ribelles,J.L.J.Therm.Anal.Cal.2003,72,631.
(23) Gao,C.;Chen,K.S.;Ye,B.;Yang,S.;Liu,X.N.;Jiang,B.Acta Chim.Sin.2011,69,37. [高 才,陳開松,葉 斌,楊 鎖,劉向農,江 斌.化學學報,2011,69,37.]
(24) Gibbs,J.H.;DiMarzio,E.A.J.Chem.Phys.1958,28,373.
(25) Hodge,I.M.;Berens,A.R.Macromolecules 1982,15,762.
(26) Nedler,J.A.;Mead,R.Comput.J.1965,7,308.
(27) Gao,C.;Yang,S.;Liu,X.N.;Wang,T.J.;Jiang,B.Acta Phys.-Chim.Sin.2010,26,453. [高 才,楊 鎖,劉向農,王鐵軍,江 斌.物理化學學報,2010,26,453.]
(28) Duvvuri,K.;Richert,R.J.Phys.Chem.B 2004,108,10451.
(29)Huang,D.;MacKenna,G.B.J.Chem.Phys.2001,114,5621.
(30) Gómez Ribelles,J.L.;Ribes Greus,A.;Diaz Calleja,R. Polymer 1990,31,223.
(31) Moynihan,C.T.;Crichton,S.N.;Opalka,S.M.J.Non-Cryst. Solids 1991,131-133,420.
(32) Romero Colomer,F.;G6mez Ribelles,J.L.Polymer 1989,30, 849.
(33) Hodge,I.M.J.Non-Cryst.Solids 1991,131-133,435.
(34)Andreozzi,L.;Faetti,M.;Giordano,M.;Palazzuoli,D.J.Non-Cryst.Solids 2003,332,229.
(35)Andreozzi,L.;Faetti,M.;Zulli,F.;Giordano,M.Eur.Phys.J.B 2004,41,383.
(36)Andreozzi,L.;Faetti,M.;Giordano,M.;Palazzuoli,D. Macromolecules 2002,35,9049.
(37) Brunacci,A.;Cowie,J.M.G.;Ferguson,R.Macromolecules 1996,29,7976.
(38) Angell,C.A.Science 1995,267,1924.
(39) Ediger,M.D.;Angell,C.A.;Nagel,S.R.J.Chem.Phys.1996, 100,13200.
(40) Wungtanagorna,R.;Schmidst,S.J.Thermochim.Acta 2001, 369,95.
(41) Williams,M.L.;Landel,R.F.;Ferry,J.D.J.Am.Chem.Soc. 1955,77,3701.
(42) Gao,C.;Wang,T.J.;Liu,X.N.;Zhou,G.Y.;Hua,T.C.Chin.J. Chem.Phys.2007,20,258.
November 8,2010;Revised:December 29,2010;Published on Web:March 8,2011.
Effect of Annealing Conditions on Enthalpy Relaxation Parameters of D-Sorbitol Glass
YE Bin GAO Cai*LIU Xiang-Nong YANG Suo JIANG Bin
(School of Mechanical and Automotive Engineering,Hefei University of Technology,Hefei 230009,P.R.China)
We studied the enthalpy relaxation dynamics of amorphous D-sorbitol by differential scanning calorimetry(DSC).A series of specific heat capacities(Cp(T))for D-sorbitol were measured upon heating of 10 K·min-1.The samples were subjected to thermal treatment involving isothermal annealing with different annealing time(ta).A new phenomenological model by Gómez Ribelles(the GR model)of enthalpy relaxation based on the evolution of configurational entropy was used to simulate the experimental data to verify the applicability of the GR model to small molecular glass.The results indicated that a single set of GR model parameters only reproduced the corresponding experimental Cp(T)curve of D-sorbitol fairly well. It failed to find a set of GR model parameters as the material constant independent of the thermal history.In contrast with other phenomenological models,some parameters of the GR model remained unchanged. The model parameter sets obtained under longer annealing time show better predictive ability.In contrast to the continuous cooling process for D-sorbitol,the ratio between the mean value of the limit state parameter(δ)and the increment of specific heat capacity at Tg(ΔCp(Tg))apparently increases,but the increase is less than that of polymers.The results brought into question if the metastable limit state introduced by the GR model applied to small molecular glass systems.
Enthalpy relaxation;Differential scanning calorimetry;Configurational entropy; D-sorbitol;Glass transition;Isothermal annealing;Fragility
O642
*Corresponding author.Email:gao_cai@hotmail.com;Tel:+86-13721029540.
The project was supported by the National Natural Science Foundation of China(20803016)and Natural Science Foundation ofAnhui Province, China(070414163).
國家自然科學基金(20803016)和安徽省自然科學基金(070414163)資助項目

