傷寒沙門菌核糖核酸酶G對胞內非編碼RNA T3956水平的影響
王菲,孟彥辰,詹莉芳,張曉磊,張海方,生秀梅,徐順高,黃新祥
近年來,隨著生物信息學和分子生物學技術的不斷發展,細菌中的非編碼RNA(non-coding RNA,ncRNA)作為一類新發現的基因表達調控因子,已受到越來越多的關注[1]。過去長期認為RNA僅是把遺傳信息從DNA帶到蛋白質的一個過渡產物,然而目前大量的研究陸續發現細菌中一些非編碼小RNA,作為應答環境壓力的調節元件[2],在細菌的物質代謝、環境適應、群體感應和細菌毒力等方面發揮著重要的調節作用[3-6]。絕大多數非編碼小RNA通過與靶mRNA配對,在轉錄后水平影響靶基因mRNA的翻譯或(和)穩定性,從而調節目的基因的表達,影響細胞的多種生理功能[2,7]。在細菌體內,這些ncRNA分子的活力主要受控于其胞內的水平。對大腸埃希菌和其他一些菌屬的研究表明,核糖核酸酶 E、G、Ⅲ主要參與對 ncRNA水平的調控[8]。因此,研究ncRNA分子在菌體內的水平是更好了解ncRNA作用的前提。
傷寒沙門菌(Salmonella enterica serovar Typhi,S.Typhi)是一種嚴重的人類腸道致病菌,也是一種重要的研究原核基因表達與調控的模式生物。本室通過對傷寒沙門菌野生株GIFU10007在普通LB、氧應激、高酸、高鹽等不同生長條件下的基因轉錄譜分析、測序、生物信息學預測和實時定量PCR(qRTPCR)驗證,從中挑選出一個位于基因ftsX和t3957之間的非編碼區ncRNA分子,命名為T3956。我們通過實時定量PCR分析初步發現,在傷寒沙門菌RNase E、RNase G、RNaseⅢ三種主要核糖核酸酶的缺陷變異株中,T3956的胞內水平在核糖核酸酶G基因(rng)缺陷株中變化較為明顯。因此,本研究擬通過構建傷寒沙門菌rng缺陷變異株和rng缺陷回補株,并利用qRT-PCR分析RNase G對傷寒沙門菌胞內ncRNA T3956水平的影響。
1 材料與方法
1.1 材料
1.1.1 菌株和質粒 野生型S.Typhi GIFU10007、E.coli SY372λpir和自殺質粒pGMB151由日本岐阜大學醫學院微生物學教研室饋贈;E.coli DH5α由本室保存;pGEM-T載體為Promega公司產品。
1.1.2 主要試劑與材料 DNA聚合酶 ExTaq、rTaq、限制性內切酶 BamH I、Xho I、BglⅡ、T4DNA連接酶、dNTP、DNase I、實時 PCR 均為 TaKaRa(大連)公司產品;DNA聚合酶pfu、RNase G為Fermentas(上海)公司產品,X-Gal、L-阿拉伯糖、氨芐西林為Sigma(美國)公司產品,TA克隆試劑盒為Promega(北京)公司產品;質粒提取試劑盒、膠回收試劑盒為Axygen(美國)公司產品;總RNA提取試劑盒為Qiagen(德國)公司產品;逆轉錄試劑盒為Invitrogen(美國)公司產品。
1.1.3 主要儀器 凝膠成像分析系統(Syngene);PCR擴增儀2720 Thermal Cycler(ABI);核酸檢測儀Speetrophotometer ND-100(NanoDrop);電轉化儀Gene Pulsero II(BIO-RAD9);超速冷凍離心機Centifuge 5417R(Eppendorf);熒光定量PCR儀CFX96TMReal-Time System(Bio-Rad)。
1.2 方法
1.2.1 引物設計 根據本室測定的傷寒沙門菌野生株GIFU10007基因組序列信息(未公布),利用Oligo6軟件設計rng缺陷株引物、rng缺陷回補株引物和t3956 qRT PCR引物。rng缺陷株引物設計:依據GiFU10007基因序列顯示,rng基因全長1 488 bp,在rng基因上游和下游設計兩對特異性PCR引物F1A/F1B和F2A/F2B,以S.Typhi GIFU10007為模板,擴增出340 bp和728 bp的同源性片段(分別用F1,F2表示)。在F1B、F2A的5'端共有20個堿基互補配對通過PCR用以定向連接F1和F2片段,在F1A、F2B的5'端加BamH I酶切位點用以克隆F1和F2連接片段至自殺質粒。rng缺陷回補株引物設計:在rng基因上下游設計引物FA,FB,并在5'端分別加上 Xho I及 BglⅡ酶切位點用以連接pBAD/gⅢ載體。t3956 qRT PCR引物設計:根據本室對傷寒沙門菌野生株GIFU10007基因組中的t3956基因測序信息,在序列中間設計一段特異性引物,通過檢測熒光值來觀察該基因的表達情況。所用引物均由上海生工生物技術服務有限公司合成,序列見表1。

表1 引物序列Tab 1 Sequences of primers
1.2.2 傷寒沙門菌rng缺陷株的制備 傷寒沙門菌rng缺陷變異株的制備過程主要參考文獻[9]。以傷寒沙門菌野生株基因組DNA為模板,用特異性引物F1A/F1B和F2A/F2B分別擴增出rng基因上下游同源性片段F1和F2。由于在F1B、F2A的5'端共有20個堿基互補配對,用酚仿-乙醇法純化后的F1和F2片段共同作為模板通過PCR獲得F1-F2定向連接產物。膠回收F1-F2片段后與pGMET載體連接,熱擊法導入E.coli DH5α,先用BamH I酶切和PCR檢測對疑似陽性克隆質粒作初步鑒定,再用DNA序列分析(測序由上海生工生物技術服務有限公司完成)予以進一步鑒定。用BamH I酶切陽性重組pMD18-T質粒,膠回收酶切片段(F1-F2),通過T4DNA連接酶將其連接至自殺質粒pGMB151的BamH I酶切位點,用熱擊法導入E.coli SY372λpir,篩選疑似陽性克隆并用BamH I酶切和PCR檢測鑒定。通過試劑盒提取帶有目的片段F1-F2的陽性自殺質粒,用電擊法導入傷寒沙門菌野生株,并在5%蔗糖LB平板上進行同源重組。用引物F1A、F2B擴增同源性片段觀察重組現象,將連續4次傳代完全重組的菌株作為S.Typhi rng缺陷株。
1.2.3 傷寒沙門菌rng基因缺陷回補株的制備根據傷寒沙門菌野生株基因組序列信息,在rng基因上下游設計引物FA、FB,并在5'端分別加上Xho I及BglⅡ酶切位點,用高保真的DNA聚合酶pfu擴增出目的片段。純化目的片段后用Xho I及BglⅡ對其進行雙酶切反應,通過T4DNA連接酶將其與經同樣酶切的pBAD/gⅢ質粒4℃過夜連接。用熱擊法將酶切產物轉化至E.coli DH5α,篩選陽性克隆并用酶切和PCR進行初步鑒定,再用DNA測序分析驗證(測序由上海英駿生物技術服務有限公司完成)。試劑盒提取測序正確的陽性克隆質粒和空質粒pBAD/gⅢ(陰性對照),分別電擊導入傷寒沙門菌rng缺陷變異株中,命名為rng缺陷回補株 Δrng(pBAD-rng),空質粒對照株 Δrng(pBAD)。
1.2.4 細菌培養及總 RNA提取 分別挑取S.Typhi野生株、rng缺陷株、rng缺陷回補株和空質粒株單菌落于1 ml等滲LB培養液中,37℃振蕩(250 r/min)培養過夜,然后以1∶100分別轉接于20 ml等滲LB培養液中,37℃振蕩(250 r/min)培養至 D(600 nm)值各為0.2,0.8 和1.2,其中培養回補株和回補空質粒株的LB液體中需加入L-阿拉伯糖和氨芐西林,終濃度分別為0.5 mg/ml和100 μg/ml。將培養管冰上放置 10 min后離心(4 000 r/min,10 min,4℃)收集菌體,再用TE緩沖液洗菌體1次,離心(4 000 r/min,10 min,4℃)收集菌體。用總RNA提取試劑盒分別提取細菌總RNA,并用無RNA酶的DNA酶 I(37℃ 30 min,80℃ 2 min)消化殘余DNA,用核酸檢測儀檢測RNA,確定其濃度,同時進行瓊脂糖凝膠電泳,分析RNA的質量(要求rRNA條帶清晰且無殘余DNA)。
1.2.5 RNA逆轉錄與實時定量PCR(qRT-PCR)采用上述方法提取細菌總RNA后用特異性引物逆轉錄成 cDNA。逆轉錄體系和條件:4 μg總 RNA,4 μl特異性引物 t3965FB,1 μl dNTP 和 4 μl無 RNA 酶的ddH2O混合后65℃作用5 min,冰浴1 min,再加入 5 × Fs 緩沖液 4 μl,0.1 mol/L DTT 1 μl,RNase OUT 1 μl,SuperScript Ⅲ 1 μl,總體積 20 μl,逆轉錄反應條件為25℃10 min,50℃50 min,70℃15 min。然后按照TaKaRa公司的實時定量PCR試劑盒操作說明進行實驗。qRT-PCR的反應體系:逆轉錄產物 1 μl,t3956 上下游引物各 1 μl,混合物(含有 ExTaq DNA聚合酶、dNTP、PCR緩沖液和SYBR Green)17 μl。實驗重復3次,每次設置平行對照組,得到的qRT-PCR結果用One-way ANOVA進行統計分析。
2 結果
2.1 成功制備傷寒沙門菌rng缺陷變異株
以S.Typhi野生株GIFU10007的基因組DNA為模板,用特異性引物F1A/F1B和F2A/F2B進行PCR擴增,獲得了rng基因上、下游同源性片段F1和F2,分別為340 bp和728 bp(圖1a)。通過PCR得到長度約1 068 bp的F1-F2定向連接片段后進行TA克隆,對篩選得到的陽性克隆經酶切和PCR鑒定后,再進行DNA測序分析,結果顯示F1-F2連接產物序列與S.Typhi野生株GIFU10007的rng基因序列一致。將F1-F2片段成功克隆至自殺質粒后(圖1b),提取帶有目的片段的自殺質粒電擊轉入S.Typhi野生株GIFU10007,然后在5%蔗糖LB平板上進行同源重組,得到僅有缺失972 bp的小片段菌株后,在普通LB平板上連續4次傳代均只有小片段出現(圖1c),表明S.Typhi rng缺陷變異株制備成功。
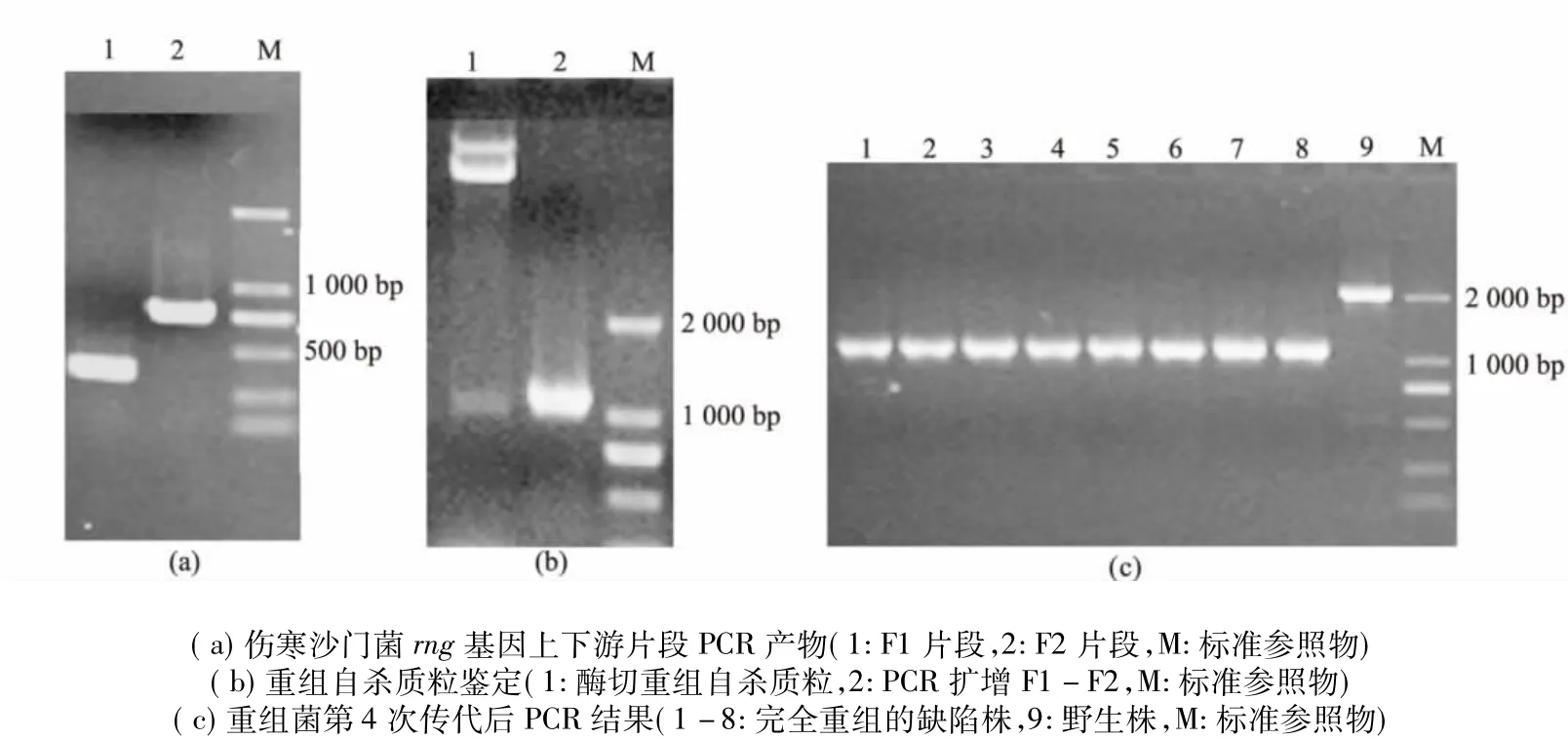
圖1 傷寒沙門菌rng基因缺陷變異株的制備Fig 1 Preparation of the rng deleted mutant of S.Typhi
2.2 成功制備傷寒沙門菌rng缺陷回補株
以野生株基因組DNA為模板,用引物FA/FB進行PCR擴增,獲得rng基因回補片段大約1 588 bp(圖2a)。將擴增的目的片段經雙酶切后與表達載體pBAD/gⅢ進行連接,熱擊導入 E.coli DH5α中,對疑似陽性克隆進行酶切和 PCR鑒定后(圖2b),再經DNA測序分析驗證,測序結果顯示插入的回補片段與目的基因完全一致。試劑盒提取測序正確的陽性克隆質粒和空質粒pBAD/gⅢ(陰性對照),分別電擊導入傷寒沙門菌rng缺陷變異株中,用目的基因特異性引物FA/FB對回補株進行PCR擴增,結果顯示在回補株中獲得了目的基因的特異片段(圖2c),說明含rng基因的載體成功轉入缺陷株中,即S.Typhi rng缺陷回補株制備成功。
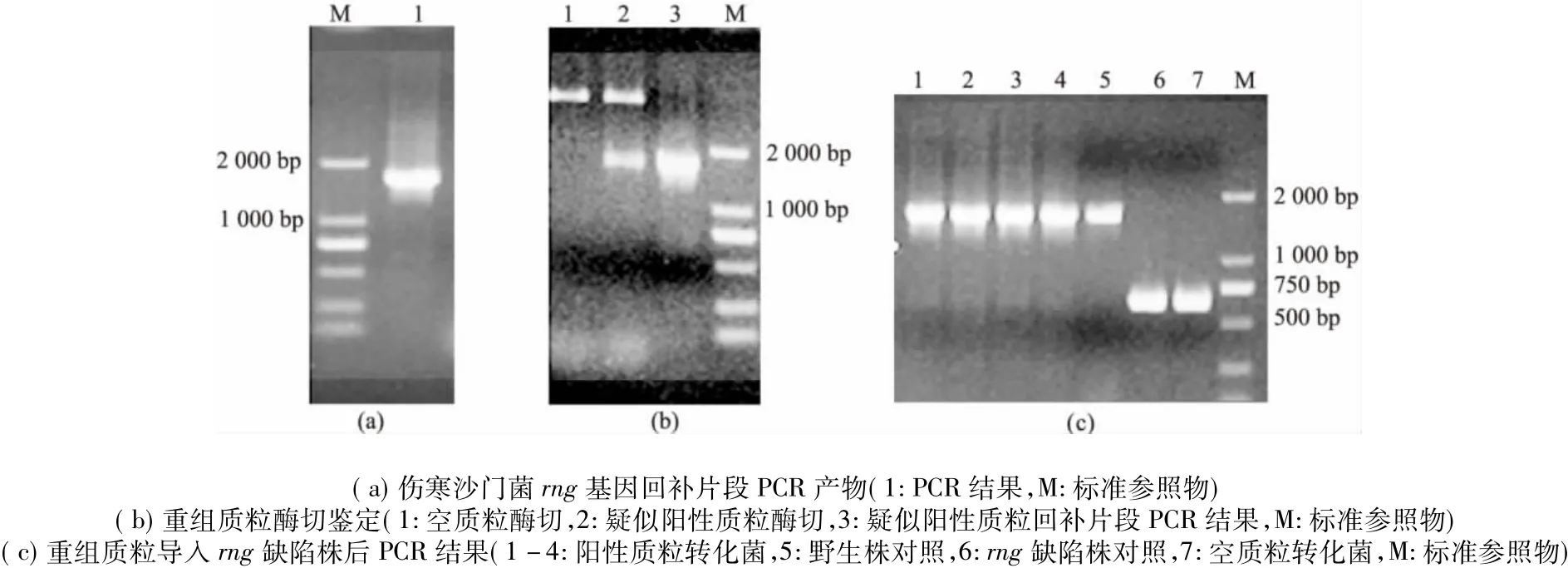
圖2 傷寒沙門菌rng基因缺陷回補株的制備Fig 2 Rescue of rng in the rng deleted mutant of S.Typhi
2.3 qRT-PCR分析RNase G對胞內T3956水平的影響
為探討RNase G對傷寒沙門菌ncRNA T3956表達的影響,我們分別提取傷寒沙門菌D(600 nm)值為0.2,0.8 和1.2 時的總 RNA,并用 qRT-PCR 分析各時相野生株、rng缺陷株、回補株和空質粒株中T3956的水平。結果(圖3)顯示,當細菌處于對數早期即D(600 nm)為0.2時,各菌株的胞內T3956水平并無顯著差異;當D(600 nm)為0.8及1.2即對數生長中后期和穩態期時,rng缺陷株的T3956胞內水平均較野生株明顯增加(P<0.01)。在各時相中,回補株與野生株之間、空質粒菌株與缺陷株之間的T3956胞內水平相似。結果表明,在傷寒沙門菌中RNase G可影響胞內ncRNA T3956的水平,并且在細菌對數生長中后期和穩態期時RNase G對T3956水平的影響更為明顯。
3 討論
核糖核酸酶類對ncRNA的成熟、降解和胞內水平起著重要的調控作用。目前,在大腸埃希菌中已發現的核糖核酸酶類有20多種[10]。在細菌中主要的核糖核酸酶有RNase E、RNase G和RNaseⅢ。RNase E是主要作用于單鏈RNA的核糖核酸內切酶,其羧基末端還可以與其他的酶類連接組裝成降解復合體,參與許多小RNA的降解[11]。RNase G由rng基因編碼,與RNase E起催化作用的氨基末端具有同源性。同RNase E一樣,RNase G主要降解單鏈RNA,并且多水解5'末端含有單磷酸基團的RNA和富含AU堿基的區域[12]。在大腸埃希菌中,RNase G和RNase E共同參與16S rRNA 5'端的成熟加工。盡管RNase G與RNase E的氨基末端具有同源性,但是兩者作用的酶切位點并不完全一致[13]。RNaseⅢ是一種作用于雙鏈RNA的核糖核酸內切酶,對sRNA和靶mRNA配對的雙鏈區進行切割,可以同時降解sRNA和其配對的靶mRNA[14]。另外,參與小RNA調控的核糖核酸外切酶還有聚核甘酸磷酸化酶(PolynucleotidePhosphorylase,PNPase)和聚腺苷酸聚合酶(PolyA polymerase I,PAP I)。PNPase和RNase E一起參與組成降解體,參與小RNA降解[15]。PAP I的多聚腺苷化作用可以影響大腸埃希菌GlmY sRNA的穩定性[16]。

圖3 qRT-PCR分析傷寒沙門菌核糖核酸酶G對非編碼RNA的影響Fig 3 qRT-PCR was performed to analyze the influence of RNaseG on the cellular level of non-coding RNA T3956 in S.Typhi.
在原核生物中,非編碼小RNA的胞內水平和生理作用往往受到多種核糖核酸酶的共同調控,不同核糖核酸酶的作用方式也各不相同[17]。例如,對鼠傷寒沙門菌的一種非編碼小RNA MicA的研究表明,其胞內周轉調控涉及兩種不同的作用機制,當MicA與靶mRNA配對后,RNaseⅢ可以同時降解MicA sRNA和靶mRNA,而對于未配對的MicA sRNA來說,RNase E則是參與游離MicA降解的主要因子,同時RNase E還可以招募其他因子如PNPase來參與游離MicA的周轉,控制MicA sRNA的胞內水平[18]。這些核糖核酸酶共同參與調控MicA sRNA轉錄后的水平,使其達到最適的水平,從而發揮對靶mRNA的調節作用。
本文研究了傷寒沙門菌RNase G對胞內ncRNA T3956水平的影響,實時定量PCR結果表明RNase G可以影響胞內ncRNA T3956的水平,并且在細菌的對數生長中后期和穩態期作用更加明顯,提示傷寒沙門菌中的RNase G對ncRNA T3956的胞內水平和周轉更新發揮著重要的調節作用,這對研究ncRNA T3956的生理功能有著重要的意義。但RNase G對T3956發揮降解作用的具體酶切位點和作用機制尚不清楚,以及有無其它的核糖核酸酶共同參與對胞內ncRNA水平的調控,還有待進一步的研究。
[1]Vogel J,Sharma CM.How to find small non-coding RNAs in bacteria[J].Biol Chem,2005,386(12):1219-1238.
[2]Storz G,Opdyke JA,Zhang A.Controlling mRNA stability and translation with small non-coding RNAs[J].Curr Opin Microbiol,2004,7(2):140-144.
[3]Grke B,Vogel J.Noncoding RNA control of the making and breaking of sugars[J].Genes Dev,2008,22(21):2914-2925.
[4]Mass E,Gottesman S.A small RNA regulates the expression of genes involved in iron metabolism in Escherichia coli[J].Proc Natl Acad Sci USA,2002,99(7):4620-4625.
[5]Lenz DH,Mok KC,Lilley BN,et al.The small RNA chaperone Hfq and multiple small RNAs control quorum sensing in Vibrio harvevi and Vibrio cholerae[J].Cell,2004,118(1):69-82.
[6]Romby P,Vandenesch F,Wagner EG.The role of RNAs in the regulation of virulence-gene expression[J].Curr Opin Microbiol,2006,9(2):229-236.
[7]Guillier M,Gottesman S.Remodelling of the Escherichia coli outer membrane by two small regulatory RNAs[J].Mol Microbiol,2006,59(1):231-247.
[8]Viegas SC,Pfeiffer V,Sittka A,et al.Characterization of the role of ribonucleases in salmonella small RNA decay[J].Nucleic Acids Res,2007,35(22):7651-7664.
[9]茅凌翔,朱超望,黃新祥,等.傷寒沙門菌phoP基因缺陷變異株的制備[J].江蘇大學學報:醫學版,2007,17(2):145-149.
[10]Arraiano CM,Andrade JM,Dominques S,et al.The critical role of RNA processing and degradation in the con-trol of gene expression[J].FEMS Microbiol Rev,2010,34(5):883-923.
[11]Carpousis,AJ,Van Houwe G,Ehretsmann C,et al.Copuri cation of E.coli RNAase E and PNPase:evidence for a specific association between two enzymes important in RNA processing and degradation[J].Cell,1994,76(5):889-900.
[12]Jiang X,Belasco JG.Catalytic activation of multimeric RNase E and RNase G by 5'-monophosphorylated RNA[J].Proc Natl Acad Sci USA,2004,101(25):9211-9216.
[13]Tock MR,Walsh AP,Carroll G,et al.The CafA protein required for the 5'-maturation of 16S rRNA is a 5'-end-dependent ribonuclease that has context-dependent broad sequence specificity[J].J Biol Chem,2000,275(12):8726-8732.
[14]Afonyushkin T,Vecerek B,Moll I,et al.Both RNase E and RNase III control the stability of sodB mRNA upon translational inhibition by the small regulatory RNA RyhB[J].Nucleic Acids Res,2005,33(5):1678-1689.
[15]Andrade JM,Arraiano CM.PNPase is a key player in the regulation of small RNAs that control the expression of outer membrane proteins[J].RNA,2008,14(3):543-551.
[16]Reichenbach B,Maes A,Kalamorz F,et al.The small RNA GlmY acts upstream of the sRNA GlmZ in the activation of glmS expression and is subject to regulation by polyadenylation in Escherichia coli[J].Nucleic Acids Res,2008,36(8):2570-2580.
[17]Viegas SC,Arraiano CM.Regulating the regulators:How ribonucleases dictate the rules in the control of small noncoding RNAs[J].RNA Biol,2008,5(4):230-243.
[18]Viegas SC,Silva IJ,Saramago M,et al.Regulation of the small regulatory RNA MicA by ribonuclease III:a targetdependent pathway[J].Nucleic Acids Res,2011,39(7):2918-2930.

