BuAENA 合成過程中反應熱的測定及動力學關聯
朱 勇,李普瑞,葛忠學,蘭 英,劉建利
(西安近代化學研究所,陜西 西安710065)
引 言
丁基-疊氮乙基硝胺(簡稱BuAENA)是熱安定性好、感度低、相容性優良的含能增塑劑,于發射藥、推進劑及混合炸藥中廣泛應用[1]。BuAENA是由丁基-硝氧乙基硝胺(簡稱BuNENA)經疊氮化反應所制得,研究其反應放熱規律及宏觀動力學數據能夠為工藝放大及生產裝置設計提供理論依據。
熱流法具有精度高、適應范圍廣等優點,已成為合成過程反應熱測定的主流方法。Allian[2]、Osato[3]等利用該方法測定了化學過程的反應熱數據并用以指導工藝優化,陳利平等[4]通過測定甲苯硝化過程的反應熱對工藝的熱危險性進行了理論分析。
本研究采用熱流法測定BuAENA 合成過程的化工熱力學數據,并初步進行其合成過程安全性分析,同時,將宏觀動力學方程與熱生成速率曲線進行關聯,擬合得到動力學參數。
1 實 驗
1.1 合成路線
BuAENA是以BuNENA 為前體,在DMSO 溶劑中經疊氮化反應制備,合成路線如下:
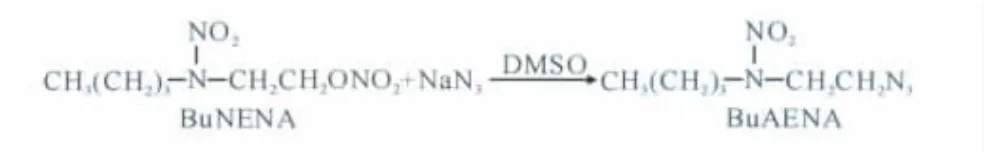
1.2 儀器與材料
反應熱測定裝置,瑞士METTLER-TOLEDO公司的全自動反應量熱器RC1e,配有德國優萊博公司的FP52 型低溫循環器,量熱數據分析采用METTLER-TOLEDO 公司的iControl軟件。
BuNENA,自制,純度不小于98%;疊氮化鈉,西安慶華公司,工業級;二甲基亞砜,分析純,西安化學試劑廠。
1.3 BuAENA 的制備
預先在iControl中設定實驗流程,開啟RC1e,向2L 常壓玻璃反應釜中加入450mL DMSO 和159g BuNENA,攪拌轉速設為200r/min,升溫至70℃,校準量熱完畢后一次性加入50g NaN3,保溫5h,校準量熱后出料。
1.4 傳熱數據的測定結果
采用熱流法測得BuAENA 合成反應體系的傳熱系數為173.2W/(K·m2),由此算出反應物料的比熱容Cpr為2.1J/(K·g),反應焓變△Hr為-13.75kJ,摩爾焓變△Hm為-18.1kJ/mol,最大放熱速率Qrmax為25.4J/s。
2 結果與討論
2.1 測量原理
采用熱流法測定反應熱生成速率與時間的關系,結果如圖1 所示。在一次性加入NaN3后,反應熱生成速率很快達到25.4J/s,隨后迅速下降至9J/s并開始緩慢衰減,表明BuAENA 的合成反應主要受加料控制,最大熱生成速率Qrmax取決于物料的加入量及加料時間,加料完成后熱生成速率平穩下降。
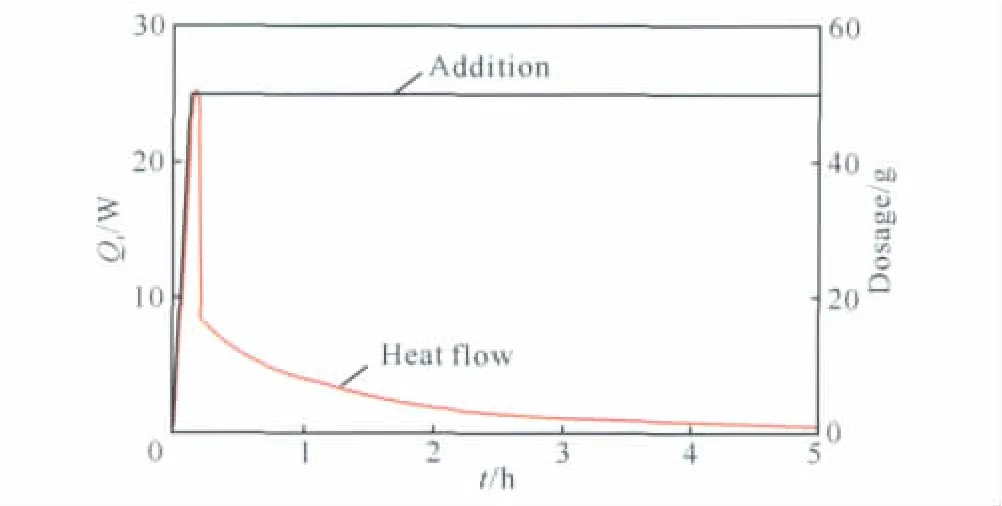
圖1 描述BuAENA 合成過程的熱流曲線Fig.1 Heat flow curves describing synthesis process of BuAENA
反應放大研究中一個很重要的計算依據是:單位體積反應體系的熱生成速率與反應規模無關,為常數。
對于工業反應器來說,其夾套、盤管等設備的綜合冷卻能力必須滿足Qrmax情況下的換熱要求,因此,實驗測得的最大熱生成速率Qrmax將是進行疊氮化反應器設計時的一個重要參考。
反應釜的熱量流動狀況見圖2。依據能量衡算,反應釜遵循如下的熱流平衡:

式中:Qreaction為反應熱;Qflow為通過反應釜壁的熱流;Qaccu為反應累計熱;Qdos為加料產生的熱量。
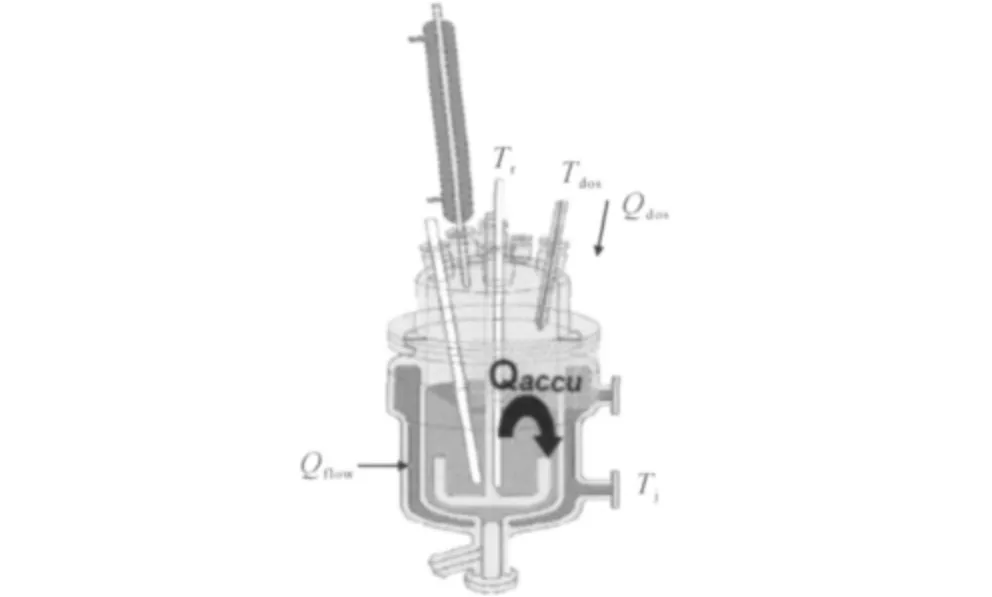
圖2 反應釜熱流狀況Fig.2 The heat flow status of reactor
由于反應體系累計的熱量將被冷卻系統帶走,故
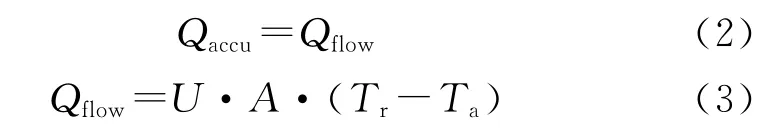
式中:U為傳熱系數;A為傳熱面積;Tr為反應溫度;Ta為夾套壁面溫度。
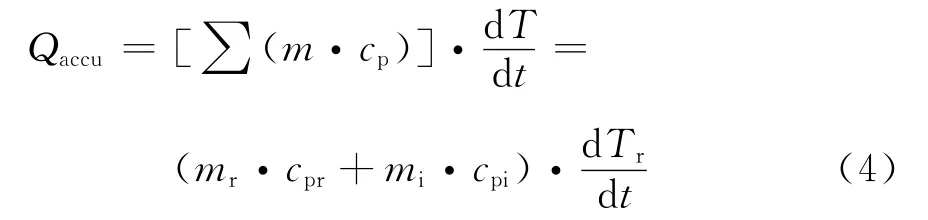
聯立(2)、(3)、(4)式,計算得:
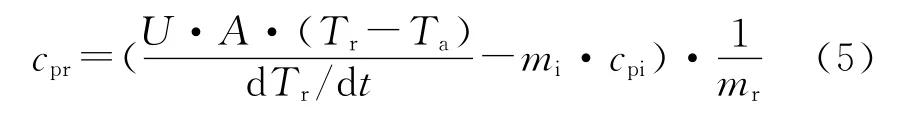
比熱容表示反應體系自身儲熱能力的強弱。由式(5)可計算出BuAENA 合成反應體系的比熱容為2.1J/(K·g),體系自身的儲熱能力較弱,反應放出的熱量能夠及時被移走。
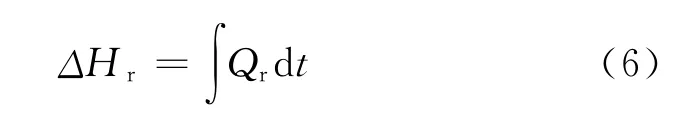
根據式(6),積分圖1中熱生成速率曲線,得到BuNENA 疊氮化過程的反應焓△Hr為-13.75kJ。基于反應量熱儀的測量原理,此處的反應焓是特定工藝條件下反應體系內所發生的所有物理、化學現象的總和。
BuAENA 合成過程的摩爾反應熱為-18.1kJ/mol,該值在工藝條件不變時不隨反應規模而變化,因此是反應冷卻系統的重要設計依據。
2.2 合成過程的熱安全性分析
含能材料合成反應基本為放熱或強放熱反應,對反應熱的準確測定是實現過程安全放大的重要依據。反應失控的主要原因有溫度、壓力、加料速度、攪拌、冷卻等,其本質在于反應放出的熱量沒有及時得到控制,從而引發物料分解等物理、化學連鎖反應。
MTSR(冷卻失效狀況下合成反應理論上可達到的最高溫度)是反應過程安全評估必不可少的因素,MTSR 為反應溫度與絕熱溫升(△Tad)之和,△Tad依據下式計算[4]:
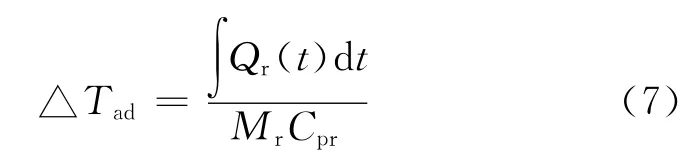
式中:Mr為反應物料總質量。由于NaN3在反應初期一次性加入,可以視為間歇反應,因此Mr恒定,由此計算得到加料完畢后反應體系的絕熱溫升為11.1K,而此時反應物料溫度為70℃,這表明在當前工藝操作條件下 MTSR 為81.1K,遠低于BuAENA 的分解溫度(150℃左右),不會引發分解反應。
2.3 動力學關聯
目前,計算反應熱與反應速率之間的關系有兩種方法:一種是利用BatchCAD 等商業化軟件[5];另一種是從機理模型出發建立數學關系式并解析[6]。本研究采用建模的方式求解疊氮化反應動力學參數。
由于NaN3在反應初期一次性加入,可以假設反應體積不變,故:
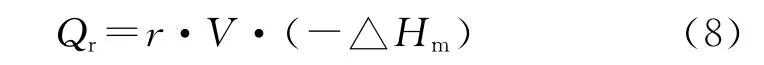
式中:r為反應速率(mol·m3·s);V為反應體積(m3),反應速率r表達式如下:
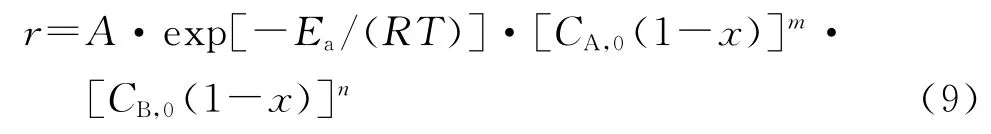
式中:A為指前因子;Ea為活化能(J/mol);CA,0、CB,0分別為BuNENA、NaN3的初始濃度(mol/m3);m、n分別為相應的反應級數;x為反應轉化率,根據文獻[7],認為反應轉化率與熱轉化率相當,x可通過下式計算:
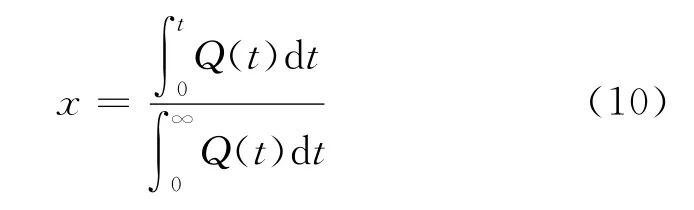
通過式(10)計算轉化率,得到Qr與x的關系,轉化率曲線如圖3所示。
由圖3可以看出,加入NaN3后,反應轉化率曲線斜率較大,加料完畢轉化率達到25%左右,隨后緩慢升高。
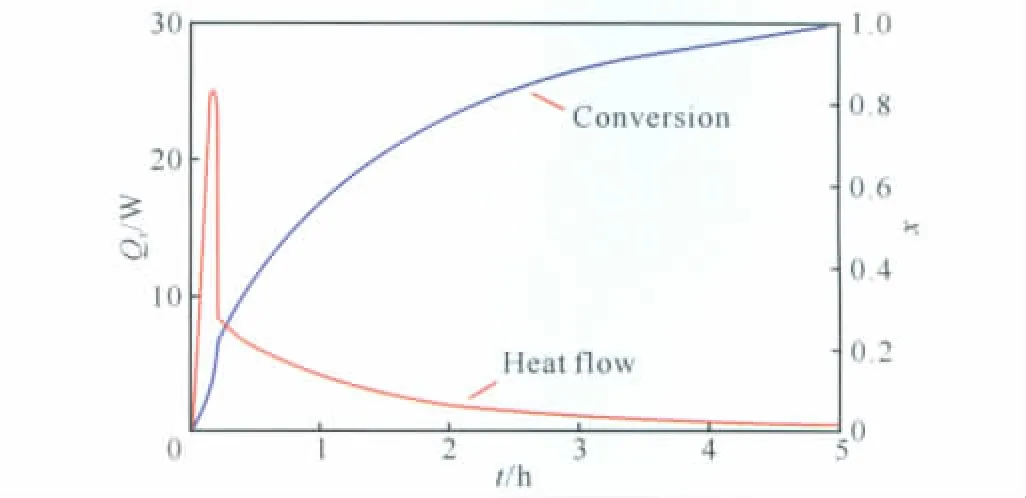
圖3 描述BuAENA 合成過程的熱流和轉化率曲線Fig.3 Heat flow and conversion curves describing the synthesis process of BuAENA
聯立式(8)、(9),獲得反應放熱速率Qr與轉化率x的關聯式。選取加料結束后的Qr-x曲線作為關聯對象,采用Levenberg-Marquardt法進行非線性擬合,動力學參數擬合結果見表1,圖4表明該動力學方程預測所得Qr曲線與實際狀況吻合較好。
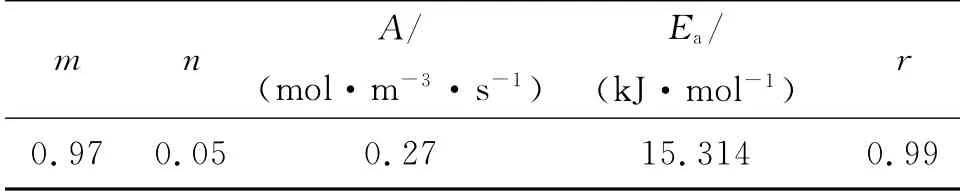
表1 由L-M 法所得的動力學參數Table 1 Kinetic parameters obtained by L-M method
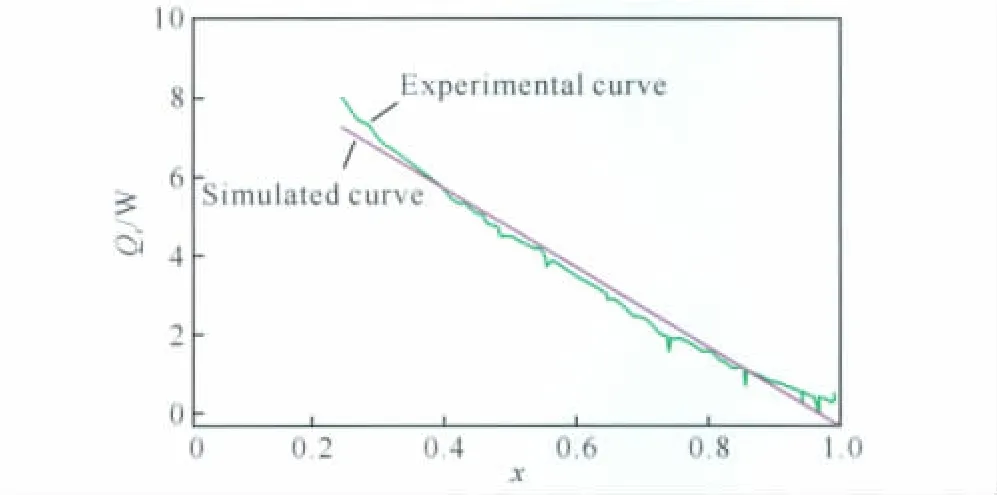
圖4 反應過程Qr的計算值和實驗值Fig.4 Experimental values and calculated ones for Qr
3 結 論
(1)測定了BuNENA 疊氮化過程的反應熱,反應焓變為-18.1kJ/mol,最大放熱速率為25.4W,反應絕熱溫升為11.1K。
(2)關聯放熱速率與反應速率,解析得到疊氮化反應級數分別為0.97、0.05,指前因子為0.27mol/(m3·s),反應活化能為15.314kJ/mol。
[1]陸安舫.新型含能增塑劑-硝基乙基硝胺族化合物發展概況[J].含能材料,1998,6(1):43-47.
LU An-fang.A review on development of nitroxyethylnit-ramine plasticizer[J].Chinese Journal of Energetic Materials,1998,6(1):43-47.
[2]Allian A D,Richter S M,Kallemeyn J M,et al.The development of continuous process for alkene ozonolysis based on combined in situ FTIR,calorimetry,and computational chemistry[J].Organic Process Research and Development,2011,15(1):91-97.
[3]Osato H,Kabaki M,Shimizu S.Development of safe,scalable nitric acid oxidation using a catalytic amount of NaNO2for 3-Bromo-2,2-bis(bromomethyl)propanoic acid:an intermediate of s-013420[J].Organic Process Research and Development,2011,15(3):581-584.
[4]陳利平,陳網樺,李春光,等.一硝基甲苯硝化過程的熱危險性[J].火炸藥學報,2008,31(3):36-40.
CHEN Li-ping,CHEN Wang-hua,LI Chun-guang,et al.Thermal hazard in the process of mononitrotoluene nitration[J].Chinese Journal of Explosives and Propellants,2008,31(3):36-40.
[5]Gigante L,Lunghi A,Martinelli S,et al.Calorimetric approach and simulation for scale-up of a friedel-crafts reaction[J].Organic Process Research and Development,2003,7(6):1079-1082.
[6]Maskow T,Kiesel B,Schubert T,et al.Calorimetric real time monitoring of lambda prophage induction[J].Journal of Virological Methods,2010,168(1/2):126-132.
[7]Balland L,Cosmao J M,Hebert J P,et al.Evaluation of dinitration energetic and kinetic parameters in a calorimetric reactor[J].Journal DE Physique IV,2002,(7):300-305.

