頂空氣相色譜法測定鹽酸伐昔洛韋中的殘留溶劑
寧偉志,吳秀榮,林煥澤,李 桃,莫 劍(茂名市人民醫院藥劑科,廣東茂名 525000)
藥品中的殘留溶劑系指在原料藥或輔料的生產中,以及制備過程中使用的,但在工藝過程中未能完全去除的有機溶劑。由于此類雜質不僅沒有療效,還可能增加藥物的毒副作用,影響藥物的穩定性,故其中的有機溶劑應盡可能除去。因此,有必要對藥品中的殘留溶劑量進行控制。鹽酸伐昔洛韋(Valaciclovir hydrochloride)是阿昔洛韋的前體物,進入體內后立即水解成阿昔洛韋,其抗病毒作用由阿昔洛韋發揮。筆者考察鹽酸伐昔洛韋的制備工藝后,發現其中有可能引入甲醇、乙醇、丙酮和四氫呋喃4種有機溶劑。本試驗采用頂空氣相色譜法對鹽酸伐昔洛韋中的殘留溶劑進行了測定,結果表明,本方法靈敏度高、分離度好、簡單快速,可用于鹽酸伐昔洛韋中的殘留溶劑檢查。
1 儀器與試藥
1.1 儀器
GC-6890N氣相色譜儀、氫火焰離子化檢測器(FID)、色譜柱 DB-5(30 m×0.53 mm,0.25 μm)、G1888頂空爐(美國Agilent公司);色譜柱 CP-Sil 8 CB(30 m×0.53 mm,1.5 μm)(美國瓦里安公司)。
1.2 試藥
鹽酸伐昔洛韋(某公司提供,批號:20100701、20100817、20101104,純度:均大于99.0%);甲醇、乙醇、四氫呋喃(廣州化學試劑廠)、丙酮(天津化學試劑一廠)均為分析純;水為純凈水。
2 方法與結果
2.1 色譜條件
色譜柱:Agilent DB-5(30 m×0.53 mm,0.25 μm);柱溫:35℃;進樣口溫度:200℃;FID溫度:260℃;流速:1.5 mL·min-1;分流比:1∶1;載氣:氮氣;頂空爐溫度:80 ℃(平衡時間:45 min);定量環溫度:85 ℃;轉移線溫度:90 ℃;進樣量:1 mL。
2.2 對照品溶液的制備
分別取甲醇、乙醇、丙酮和四氫呋喃置于同一量瓶中,加水溶解并稀釋至刻度,得4種溶劑濃度分別為0.75、1.25、1.25、0.18 mg·mL-1的溶液,作為對照品貯備液。
2.3 供試品溶液的制備
取供試品約1.0 g,加水20 mL溶解,搖勻,取該溶液5 mL,加入含無水硫酸鈉1 g的頂空瓶中密封,即得。
2.4 系統適用性試驗
將對照品貯備液稀釋5倍后取5 mL,加入無水硫酸鈉1 g,置于頂空瓶中密封,進樣,結果,各峰分離度均大于4.0。另取供試品進樣,色譜結果見圖1。
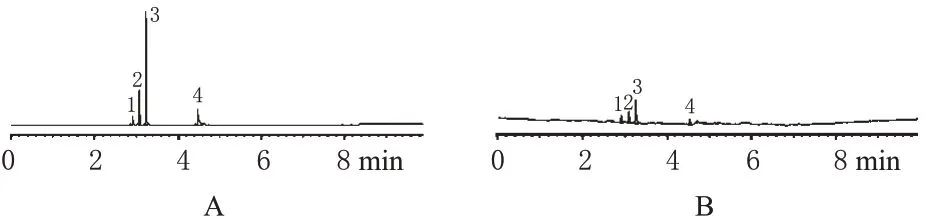
圖1 氣相色譜圖Fig 1 GC chromatograms
2.5 線性關系考察
取對照品貯備液,分別稀釋20倍(甲醇、乙醇、丙酮、四氫呋喃濃度分別為37.5、62.5、62.5、9 μg·mL-1)、10倍(甲醇、乙醇、丙酮、四氫呋喃濃度分別為0.075、0.125、0.125、0.018 mg·mL-1)、5倍(甲醇、乙醇、丙酮、四氫呋喃濃度分別為0.15、0.25、0.25、0.036 mg·mL-1)、2倍(甲醇、乙醇、丙酮、四氫呋喃濃度分別為0.375、0.625、0.625、0.09 mg·mL-1)和不稀釋(甲醇、乙醇、丙酮、四氫呋喃濃度分別為0.75、1.25、1.25、0.18 mg·mL-1),并分別取5 mL和無水硫酸鈉1 g,置于頂空瓶中密封,進樣,記錄色譜圖,并測量各待測溶液峰的峰面積,以峰面積(Y)對濃度(x)作線性回歸,結果見表1。

表1 線性關系結果Tab 1 Result of linear correlations
2.6 精密度試驗
取“2.5”項下試驗溶液(甲醇、乙醇、丙酮、四氫呋喃濃度分別為0.15、0.25、0.25、0.036 mg·mL-1),在同一天內重復進樣5次,記錄色譜圖,并測量各待測溶液的峰面積,計算各組分峰面積的RSD,結果分別為2.1%、0.9%、1.3%、2.8%。
2.7 檢測限和定量限檢測
精密量取對照品貯備液適量,作系列稀釋后進樣測定,以各峰達信噪比3倍和10倍時的量分別為最低檢測限和最低定量限,結果甲醇、乙醇、丙酮、四氫呋喃檢測限分別為0.596、0.38、0.32、1.251 μg·mL-1),定量限分別為0.239、0.117、0.83、5.013 μg·mL-1)。
2.8 回收率試驗
取供試品(批號:20100701)溶液5 mL,以2010年版《中國藥典》二部附錄規定的相應溶劑限度[1]所得相應的對照品溶液(甲醇、乙醇、丙酮、四氫呋喃分別為0.15、0.25、0.25、0.036 mg·mL-1)為基準,制備濃度為該對照品溶液80%、100%、120%的溶液,并分別取各溶液5 mL及無水硫酸鈉1 g,置于頂空瓶中密封,依法測定,每個濃度測定3次,計算回收率,結果見表2。

表2 回收率試驗結果Tab 2 Results of recovery test
2.9 耐用性試驗
取“2.5”項下溶液(甲醇、乙醇、丙酮、四氫呋喃濃度分別為0.075、0.125、0.125、0.018 mg·mL-1),分別用色譜柱Agilent DB-5和Varian CP-Sil 8 CB重復進樣6次,進行耐用性試驗,結果4組分峰面積的RSD分別為1.38%、0.98%、1.34%、2.01%。
2.10 樣品檢測結果
取3批樣品進樣,結果甲醇、乙醇、丙酮、四氫呋喃的含量均小于《中國藥典》2010年版二部附錄[1]中對相應有機溶劑的限度規定(甲醇:0.3%;乙醇:0.5%;丙酮:0.5%;四氫呋喃:0.072%),詳見表3。
3 討論
《中國藥典》2010年版和《歐洲藥典》(EP)7.0都收載有鹽酸伐昔洛韋質量標準[1,2],但均未列有殘留溶劑檢查項,《美國藥典》(USP)32未收載伐昔洛韋的質量標準。國內王文芳等[3]采用直接進樣法測定鹽酸伐昔洛韋中的甲醇、乙醇、醋酸乙酯、四氫呋喃和N,N-二甲基甲酰胺的含量;而本文是根據待測樣品的相關工藝確定檢測的有機溶劑為甲醇、乙醇、丙酮和四氫呋喃,且本文采用頂空氣相色譜法,因此,檢測限和定量限結果更優于直接進樣法,因此本法更能真實地反映鹽酸伐昔洛韋中有機溶劑的殘留量。

表3 樣品中4種溶劑測定結果(%)Tab 3 Results of content determination of 4 solvents in samples(%)
本研究的方法和限度參考人用藥品注冊技術要求國際協調會(ICH)[4]和《中國藥典》2010年版的相關規定,對甲醇、乙醇、丙酮和四氫呋喃4種有機溶劑的量進行檢測,采用頂空氣相色譜法。本試驗樣品進樣處理中加入了無機鹽無水硫酸鈉,其作用是改變有機溶劑在液相和氣相中的分配系數,以促進有機溶劑的揮發[5]。本試驗柱溫采用35℃,因柱溫較低,建議試驗結束后升高柱溫以凈化色譜柱。
本試驗測定結果表明,鹽酸伐昔洛韋中4種有機溶劑的量均符合相關規定,各峰間達到良好的分離。本方法操作簡單、準確、可靠、靈敏度高,能達到殘留溶劑的檢測要求,可用于鹽酸伐昔洛韋中殘留溶劑的檢測。
[1]國家藥典委員會.中華人民共和國藥典(二部)[S].2010年版.北京:中國醫藥科技出版社,2010:686、附錄61-65.
[2]European Director for the Quality of Medicines & Healthcare.European Pharmacopeia(7.0)[S].Germany:Druckerei C.H.Beck Nordlingen,2010:3 185-3 188.
[3]王文芳,楊 敏,賴招連.鹽酸伐昔洛韋中有機溶劑殘留量的測定 [J].醫藥導報,2007,26(9):1 088.
[4]李 眉,馬玉楠.簡介ICH關于藥品中溶劑殘留的指導原則[J].中國藥師,1998,1(3):119.
[5]朱海燕,藍偉松,鄭凝堅.頂空氣相色譜法測定利巴韋林中的殘留溶劑[J].分析試驗室,2002,21(2):33.

