原鹽質量對聯堿生產的影響機理淺析
嚴國慶
(甘肅金昌化學工業集團有限公司,甘肅 金昌 7 3 7 0 0 0)
原鹽質量對聯堿生產的影響機理淺析
嚴國慶
(甘肅金昌化學工業集團有限公司,甘肅 金昌 7 3 7 0 0 0)
我公司采用原鹽直接加入聯堿生產系統的方法,原鹽中雜質對生產影響很大。分析了原鹽雜質中的鈣鎂離子、硫酸根離子對聯堿生產的影響機理,并具體描述了雜質在生產過程中引起的不良影響。
原鹽;鈣鎂離子;硫酸根;聯堿;影響機理
原鹽是聯合制堿法生產的主要原料,經精制去雜質后,以固體小顆粒(平均粒徑≦0.5mm)的形式加入循環母液中,達到國家工業鹽標準(G B/T 5 4 6 2-2 0 0 3)優級品的原鹽可不經精制直接加入。我公司目前所用原鹽全是湖鹽,1#產地的鹽質量相對較好,2#、3#產地的鹽雜質含量高,但這些原鹽質量都不能達到國家優級品的要求。生產中3種產地的原鹽混合參配使用,不經精制直接加到系統中,雜質對生產系統影響很大。

表1 不同產地原鹽質量
1 原鹽中雜質對聯堿生產的影響
原鹽中含有C a2+、M g2+、S O42-和泥沙等雜質,雜質超標會造成堿生產系統出現以下不良后果。
1)母液中水不溶物C a C O3、M g C O3、泥沙等超標,會使純堿產品白度下降,氯化銨產品主含量下降、氮含量不達標,嚴重影響產品的市場競爭力。
2)母液中的C a2+、M g2+、S O42-等雜質多,會使母液濁度增加、比重增大、粘度增大,引起氯化銨及重堿結晶變細,不利于結晶器的稠厚、過濾、干燥或煅燒等工序的操作。
3)部分泥沙等水不溶物和C a2+、M g2+、S O42-易生成結疤,物附著在管道、吸氨器、結晶器、母換列管、碳化塔水箱冷卻列管、外冷器壁上,影響降溫及有效容積,降低設備的生產能力。
4)生產系統向外排出的氨Ⅱ泥量增多,氨、鹽損失加重。
原鹽中不溶性雜質主要是氧化硅、氧化鋁、泥沙等,水溶性雜質以C a S O4、M g S O4、M g C l2等形式存在。水溶性雜質和不溶性雜質對聯堿生產的影響機理完全不同。
2 鈣鎂雜質在鹽析結晶器中沉淀反應
2.1 碳酸鈣鎂沉淀物的形成
未經精制的原鹽夾帶C a S O4、M g S O4、M g C l2加入鹽析結晶器,在母液Ⅱ中溶解并離解成C a2+、M g2+、S O42-、C l-,與母Ⅱ中的(NH4)2C O3、N a2C O3(聯堿生產常規母液Ⅱ中約有(NH4)2C O34.5t t、N a2C O32.5t t左右)發生鈣鎂沉淀反應。
溶液中存在C O2-3時,C a2+必然以C a C O3的形式產生沉淀:
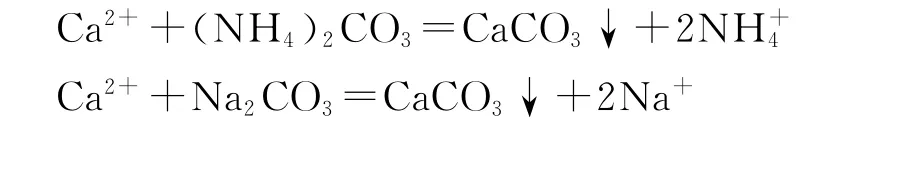
母液Ⅱ中二氧化碳濃度和碳化度較高,鎂離子將產生M g C O3和其他復鹽沉淀:
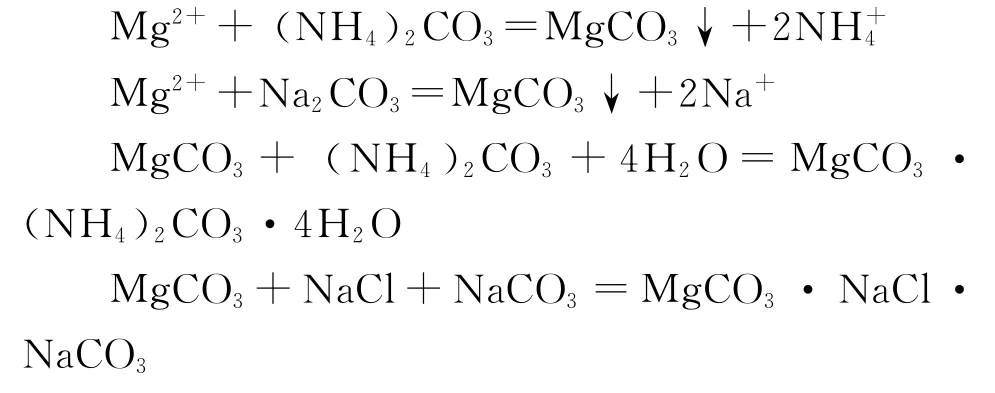
反應生成的C a C O3和M g C O3的溶解度很小。在鹽析結晶器操作溫度1 3~1 7℃下,溶度積K s p如下:C a C O3為2.8×1 0-9;M g C O3為3.5×1 0-8。母液Ⅱ中M g2+含量不同差別較大,一般在(5~1 5)×1 0-3m o l/l,鹽析結晶器母液Ⅱ中:
[C a2+]×[C O2-3]=(2.9~7.2 5)×1 0-4>2.8×1 0-9
[M g2+]×[C O2-3]=(0.4 4~2.1 8)×1 0-3>3.5×1 0-8
鈣鎂離子和碳酸根濃度的乘積遠遠大于碳酸鈣和碳酸鎂的溶度積,沉淀反應幾乎不可逆,鈣鎂沉淀是比較完全的,反應產生的復鹽M g C O3·N a C l· N a2C O3、M g C O3·(NH4)2C O3·4 H2O變為難溶化合物。
2.2 碳酸鈣鎂沉淀物的帶出途徑及對生產的影響
1)鹽析結晶器中生成的C a C O3和M g C O3沉淀,約有3 0%~5 0%沉淀被氯化銨產品夾帶出系統,其余部分留在母液Ⅱ中。結晶逆料生產工藝操作,由于部分母液Ⅱ返混到冷析結晶器半母液Ⅱ中,半母液Ⅱ的濁度上升,氯化銨結晶“介穩區”縮小,使冷析結晶粒度變小。同時半母液Ⅱ在軸流泵的作用下去外冷器,在降溫過程中,C a C O3和M g C O3沉淀隨同氯化銨結晶附著在外冷器列管壁上,使外冷器結疤加快,換熱效果降低,作業周期縮短。
2)在鹽析結晶器生成的C a C O3和M g C O3沉淀中約有5 0%~7 0%隨同母液Ⅱ沉降槽溢流至母Ⅱ桶。再經過母液換熱器和母Ⅱ吸氨后進入氨母液Ⅱ澄清桶沉降分離。在換熱和吸氨過程中,使母液換熱器列管結垢,換熱效率下降,吸氨器堵塞,阻力增大。母液Ⅱ經過與熱AⅠ換熱和吸氨,溫度由1 5℃逐漸上升到4 0℃。C a C O3和M g C O3的溶解度隨溫度升高而增大,特別是M g C O3溶解度增大幅度更為顯著,有關實驗測定,4 0℃碳酸鎂的溶解度約是1 5℃時的3倍。在母液Ⅱ溫度逐漸升高的過程中,M g C O3沉淀被部分溶解,沉淀顆粒變小。在氨Ⅱ桶沉降分離中,母液Ⅱ中夾帶的泥沙澄清效率達到9 5%以上,C a C O3的澄清效率8 0%~9 0%,而M g C O3的澄清效率只有5 0%。由此可見,原鹽中含M g2+可溶性雜質越高,氨母液Ⅱ的濁度越大。
3)在聯堿生產中受氨母液Ⅱ澄清工藝設備的限制,大量的C a2+、M g2+雜質隨氨母液Ⅱ進入碳化塔,在碳化過程中,再次產生碳酸鈣和碳酸鎂沉淀,并與氨母液Ⅱ中原有的細小C a C O3、M g C O3沉淀被進一步碳化,在有氧存在的條件下,被氧化成鈣和鎂的堿式碳酸鹽沉淀,使碳化塔冷卻水箱列管結疤加劇,造成碳化塔作業周期縮短,甚至出現堵塔現象。C a C O3、M g C O3和堿式碳酸鹽的沉淀一起夾雜于重堿結晶之中,并進入純堿產品,使純堿水不溶物增大。經過測定原鹽中帶入雜質流向,進入純堿產品M g2+雜質竟高達3 0%,使用含M g2+高的青海原鹽(特別是柯柯與榮仁鹽),不但使純堿水不溶物上升,而且還會使碳化塔生產條件惡化,重堿結晶變細,濾過洗水量增加,聯堿系統水膨脹,肥堿比倒掛,氨、鹽消耗上升。
3 硫酸根對生產的影響機理
3.1 硫酸根在聯堿生產母液中的存在形式
在原料鹽中S O42-雜質主要以M g S O4、N a2S O4的形式存在。在聯堿生產S O42-雜質隨原鹽進入鹽析結晶器,在母液Ⅱ中溶解并離解成M g2+、N a+、S O42-。由于母液Ⅱ中存在C O32-,M g S O4與C O32-生成M g C O3沉淀,反應式如下:
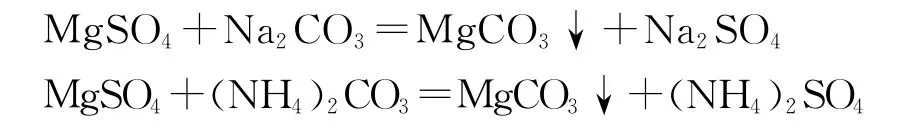
反應生產的N a2S O4和原鹽中的N a2S O4隨母液Ⅱ經吸氨后進入碳化塔,在碳化塔中與C O2、H2O、NH3反應生成N a HC O3結晶和(NH4)2S O4,反應式如下:
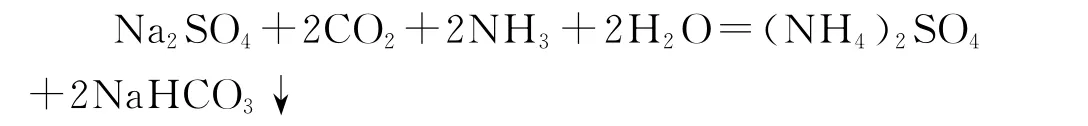
由于聯堿生產過程中母液循環使用,在碳化塔中生產的(NH4)2S O4溶解于母Ⅰ中,隨母Ⅰ再次進入鹽析結晶器和溶解于母液Ⅱ中的N a C l反應生成NH4C l結晶和N a2S O4,反應式如下:
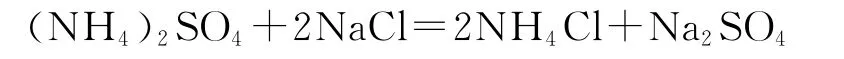
通過上述分析可知S O42-在循環過程中,在母液Ⅱ和氨Ⅱ中主要以N a2S O4的形式存在,在母液Ⅰ和氨Ⅰ中主要以(NH4)2S O4的形式存在。
3.2 硫酸根在聯堿生產系統的積累和平衡濃度
在聯堿生產中母液是封閉循環的,且基本上處于平衡,不論是母液Ⅱ、氨Ⅱ中的N a2S O4,還是母液Ⅰ、氨Ⅰ中的(NH4)2S O4,在制堿和制銨過程中的溶解度相對比較大,不可能形成結晶隨產品取出系統,只能隨重堿和濕銨夾帶的母液排出系統,因此S O42-在母液系統內存在動態平衡:
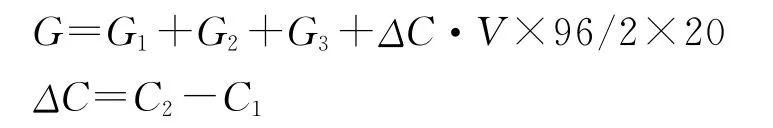
式中,G——原鹽帶入的S O42-,t t;
G1——重堿帶出的S O42-,t t;
G2——濕銨帶出的S O42-,t t;
G3——氨Ⅱ泥帶出的S O42-t t;
C1——母液系統內S O42-變化前的濃度,t t;
C2——母液系統內S O42-變化后的濃度,t t;
Δ C——母液系統內S O42-變化量,t t。
所以,原鹽中S O42-含量變化時,母液系統中S O42-存在3種變化情況:
1)當原鹽中S O42-含量不變時,則G=G1+G2+G3,Δ C=0,C1=C2,此時,母液系統內,S O42-濃度基本不發生變化。
2)當原鹽中S O42-含量下降時,則G<G1+G2+G3,Δ C<0,C1>C2,母液系統內S O42-濃度下降,C2下降到一定值時,G=G1+G2+G3,母液系統內S O42-建立一個新的動態平衡。
3)當原鹽中S O42-含量上升時,則G>G1+G2+G3,Δ C>0,C1<C2,母液系統內S O42-濃度上升,C2上升到一定值時G=G1+G2+G3,母液系統內S O42-又建立一個新的動態平衡。
從上述分析可知,原鹽中S O42-含量越高,母液中S O42-濃度就越高,當S O42-濃度大于1 0t t時,生產工藝會發生很大變化,比如,2 0 1 0年元月至2 0 1 0年9月份的我公司純堿生產惡化的工藝狀況就是一個很好的例證。
3.3 硫酸根對聯堿生產Ⅱ過程的影響
原鹽S O42-含量超過0.6%時,系統母液中S O42-會積累,N a2S O4逐漸達到飽和,母液Ⅱ的比重和粘度隨之增加。按照物質溶解度變化的一般規律(鹽析原理)可知,由于系統中N a2S O4濃度增加,N a C l的溶解度變小,在鹽析結晶器中加鹽無法進行,氯化銨結晶析出量少,既影響氯化銨產品質量又導致母液ⅡC NH3偏高、T C l和N a+濃度偏低、γ值下降,由于母液Ⅱ比重增加,造成鹽析結晶器內大量結晶無法沉降,溢流帶料嚴重;使得聯堿Ⅰ過程碳化反應物濃度下降,生成物濃度上升,碳化反應速度減緩,母液當量增大,碳化率下降。另一方面,因N a2S O4具有逆溶解性,其逆溶解度轉折點為1 7.9℃(N a2S O4在1 7.9℃與水反應生成N a2S O4· 1 0 H2O),當溫度高于1 7.9℃時,N a2S O4的溶解度隨溫度的上升而下降。在母液換熱器中,列管內母液Ⅱ溫度在2 6℃左右,高于N a2S O4的逆溶解度轉折點溫度,在母液Ⅱ中已飽和的N a2S O4容易析出粘附在列管內壁,影響氨Ⅰ和母Ⅱ的傳熱效率,冷氨Ⅰ溫度難以達到工藝指標要求,使母液換熱器作業周期縮短。
3.4 硫酸根對聯堿Ⅰ過程的影響
1)對母液Ⅱ吸氨器的影響
由于溶解度變化一般規律可知,N a2S O4在氨水中的溶解度比在純水中的溶解度要小,并且隨氨濃度的增加,溶解度下降。因此母Ⅱ吸氨時,N a2S O4極易在噴嘴處以結晶形式析出,引起噴嘴堵塞,使母液噴射吸氨器效果變差,生產能力下降。
2)對氨Ⅱ澄清效率的影響

3)對碳化塔反應條件的影響
在碳化塔中,上部溫度一般控制在5 5℃左右,中部溫度控制在6 0℃左右,下部溫度控制在3 4℃左右,都高于N a2S O4的逆溶解轉折點。同時,母液中固體N a2S O4的存在使N a HC O3、NH4HC O3的溶解度減小,結晶區擴大,過飽和度增大,結晶粒度變細。N a HC O3、NH4HC O3和N a2S O4一起在塔壁、冷卻水箱列管的表面析出沉積,導致塔的容積減少,二氧化碳與碳化液的接觸面積減少,降低單塔的生產能力。另外,由于冷卻水管結疤增厚,引起傳熱系數下降,冷卻效果變差,取出溫度高。并且N a2S O4難用氨Ⅱ清洗下來,只能增加水洗的次數。2 0 1 1年我公司碳化塔生產狀況就可證明上述分析。
3.5 對聯堿兩種產品質量的影響
前面已經分析過,原鹽帶入聯堿生產母液系統的S O42-,除小部分由氨Ⅱ泥夾帶出外,大部分由純堿和氯化銨兩種產品帶出。純堿和氯化銨兩種產品中S O42-雜質含量上升,導致主含量下降。
以上論述是本人對原料鹽質量影響聯堿生產的機理淺易分析,如有不妥之處望各位工程技術人員和聯堿操作人員批評指正。
[1] 大連化工研究設計院.純堿工學(第二版)[M].北京:化學工業出版社,2 0 0 4
[2] 王全.純堿制造技術[M].北京:化學工業出版社,2 0 0 9
[3] 韓行治.聯合制堿工藝[M].沈陽:遼寧科技出版社,1 9 8 9
[4] 新旭法制造純堿的技術[J].純堿工業,1 9 7 9(2)
[5] 李正明.芒硝對聯堿生產的影響及其原因[J].純堿工業,1 9 9 2(2)
[6] П.В什謝娃(蘇).硫酸鈉的性質和制造[M].山西運城鹽化局出版
[7] 姚玉英.化工原理(上冊)[M].北京:化學工業出版社,2 0 0 4
T Q 1 1 4.1 6 2
C
1 0 0 5-8 3 7 0(2 0 1 2)0 5-1 1-0 4
2 0 1 2-0 7-0 9

