染料敏化太陽能電池中敏化染料分子合成研究*
鄭州大學 化學系 張高賓 李 明 魯春芝
染料敏化太陽能電池中敏化染料分子合成研究*
鄭州大學 化學系 張高賓 李 明 魯春芝
一、染料敏化太陽能電池簡介
隨著全球對能源需求的增加,發展可再生資源成為人們解決能源問題的重要出路。太陽能在經濟、環保、可持續發展等方面優點顯著,因而對太陽能電池的研究具有重要的顯示意義。染料敏化電池是太陽能電池的一種,其原理為:染料受光照激發,激發態的染料分子將電子注入半導體電極的導帶中,從而使電子被輸運到外電路;同時激發態的染料分子被電解質還原。染料敏化太陽能電池是模仿光合作用的原理而研制出來的新型太陽能電池,生產這種電池的原材料豐富,成本低廉,生產工藝相對簡單,有利于大規模生產,并且其原料和生產工藝污染較小,符合可持續發展的要求,有利于環境保護。
二、敏化染料分子的特征分析
染料敏化太陽能電池主要有染料敏化劑、多孔半導體薄膜、氧化還原電解質、Pt對電極和導電基底等部分組成。其中,敏化染料是染料敏化太陽能電池的核心部分,它擔任著主要的光電轉換功能。并非所有的染料都可以作為這類電池的敏化染料分子,這類電池的敏化染料分子必須滿足以下條件。
1.染料在TiO2的表面吸附性好,達到吸附平衡且不易脫落。染料分子上要有能與納米TiO2表面結合的基團,例如–SO3H, –PO3H2,–COOH等。這些基團可以和TiO2表面的羥基鍵合,使電子轉移更容易。
2.在可見光區域要有較強的、較寬的吸收光譜。
3.染料分子要有足夠高的最高空余軌道能級以保證激發態染料電子注入到TiO2導帶中。
4.染料分子要具有足夠低的最高占有軌道能級以保證氧化態染料被電解質還原再生。
5.染料分子的基態,激發態與氧化態的光穩定性要足夠高。
三、合成過程
在上述理論的基礎上,筆者設計并合成了一種符合要求的純有機染料,其合成過程如圖1所示。
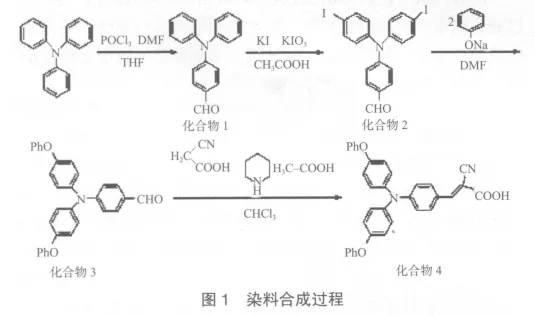
1.制備(4–二苯胺基)苯甲醛(化合物1)。取100 m L的三頸圓底燒瓶,向瓶中加入DMF(氮氮二甲基甲酰胺,一種常見有機溶劑) 40 m L,在冰鹽浴條件下加入三氯氧磷6.0 g,繼續攪拌約45 min,然后加入5.0 g三苯胺的DMF溶液。滴加結束后升溫至90℃,反應8 h(其中,三氯氧磷在使用之前重蒸,DMF要嚴格處理無水)。經TLC檢測,若無原料剩余,則結束反應。靜置至室溫,緩慢倒入冰水中,用NaOH溶液調節pH為7左右,水洗后過濾得到灰色固體,再用少量的乙醇溶劑洗兩次,重結晶后得到淡黃色固體3.2 g,產率60%。
2.制備4–(4′,4′–二碘二苯胺基)苯甲醛(化合物2),取4.96 g制備好的4–二苯胺基)苯甲醛、3.91 g KI、6 m L水置于裝有60 m L乙酸的三口瓶中,加熱至80℃,再加入3.84 g KIO3,在80℃的溫度下攪拌4 h。反應結束后,蒸出乙酸,用稀NaHCO3洗滌,然后用乙酸乙酯萃取,合并有機相濃縮結晶得黃色晶體。
3.制備4–(4′,4′–二苯氧基二苯胺基)苯甲醛(化合物3),先制備苯酚鈉,取1 gNa置于裝有4.6 g苯酚–乙醚溶液的三口瓶中,待反應結束后將乙醚蒸出,再向三口瓶中加入0.1 gCuI和20 m LDMF,A r氣保護,加熱至80℃。向反應液中滴加0.8 g化合物4–(4′,4′–二碘二苯胺基)苯甲醛的DMF溶液,滴加結束后保持溫度恒定的條件下反應20 h,TLC檢測無原料剩余時,停止反應。反應結束后,過濾掉不溶物。然后將反應液倒入大量的水中,接著用乙酸乙酯萃取,收集有機相,減壓蒸餾得粗產品,重結晶得黃色固體。
4.制備化合物4,在50 m L的圓底瓶內加入30 m L氯仿,將0.3 g 4–(4′,4′–二苯氧基二苯胺基)苯甲醛完全溶解,加入0.23 g氰基乙酸,同時分別滴加3~5滴哌啶和冰醋酸,氬氣保護,加熱回流,瓶內有濃烈的白色煙霧,反應液為綠色,之后變為黃綠色,伴隨白煙,最后為紅棕色,回流溫度下反應12 h結束反應。停止反應之后,靜置到室溫,pH調到2,使用旋轉蒸發器減壓濃縮至有大量黃色固體出現時,抽濾得黃色固體,再用稀鹽酸洗滌兩遍,得化合物4,常溫下為紅棕色固體。產率為82%。
四、結論
以常見的化學試劑三苯胺為原料,經過維斯邁爾反應、親電取代反應、親核取代反應、以及腦文格縮合等反應,設計合成了一種簡單的具有D–∏–A結構的敏化太陽能電池染料。在美國化學會的《Chemical Abstract》的在線版數據庫進行查閱,發現尚無此種化合物的報道,此合成工作尚屬首次,此種原料的生產具有廣闊的發展前景。
鄭州大學研究生科學研究基金資助項目(11L10301)。

