應急管理理論在基層藥監執法工作中的應用
北京市藥品監督管理局朝陽分局 段志永 劉建軍 蔚冬紅
“應急管理”一詞在20世紀引入我國,現在普遍認為2003年的“非典”是我國應急管理建設的轉折點[1]。我國及時總結抗擊“非典”的經驗和教訓,提出應對突發公共事件的“一案三制”(法制、體制、機制以及預案)建設,應急管理工作逐步走上了規范化、法制化的軌道[2]。
目前,我國藥品安全突發事件應急管理方面的“一案三制”體系已初步形成。特別表現在預案體系上,以《國家突發公共事件總體應急預案》[3]為總綱,制定了《藥品和醫療器械突發性群體不良事件應急預案》[4]、《國家突發公共衛生事件應急預案》[5]等。省市縣三級藥品安全突發事件應急預案也相繼制定。近年來,我國藥品安全事件呈現比較平穩的態勢。藥監分局處在藥品執法監管一線,處理著大量的群眾投訴舉報及各類威脅藥品安全的違法違規事件。但是,國家、省級應急預案中定義的突然發生、造成嚴重的群體健康損害的藥品安全突發事件極少發生或只占很小的比例。因此,國家、省級應急預案對基層藥監部門的執法實踐并沒有很強的借鑒、指導意義。如何將應急管理理念應用到藥監日常管理的程序和體系中來?能否建立相應的處理程序,以便在一線執法實踐中高效甄別藥品安全風險預警,預防或緩解事故發生?筆者在本文中從基層藥監稽查工作的角度探討這些內容。

▲北京市藥監局朝陽分局工作人員對可疑藥品抽檢
1 藥監稽查工作的應急特質
應急管理的本質在于:消除潛在隱患,阻止或減緩正在發生的危害,減輕事故后果,通過經驗總結和信息反饋為下一步管理提供依據。藥監部門稽查辦公室的工作職責是:負責本行政區域內藥品、醫療器械、保健食品、化妝品方面的執法監督工作,依法查處有關違法案件,受理有關投訴和舉報。可以看出,稽查辦公室工作性質和職責在于保障“三品一械”質量安全,消除隱患,查處違法行為[6]。
1.1 預警,即案件受理階段 應急管理運行機制的“預警”,指的是相關部門針對各種可能發生的突發公共事件,進行信息采集,開展風險分析,并根據預測分析結果,對其危害程度、范圍做出估計,必要時向決策者建議發出危機警報,啟動危機處理程序。藥品安全預警一般定義為:發現、評估、理解和預防藥品研發、生產、流通、使用過程中與藥物有關問題的科學和活動。對藥品安全風險進行預警的目的在于做到“早發現、早報告、早處置[7]”。
在案件受理階段,稽查受理人員依據法律法規對舉報投訴信息進行甄別、判斷,對屬于本部門管轄、主管的舉報投訴予以受理。這些涉及藥品研究、生產、經營、使用環節的個案,存在著引發藥品安全危機的可能性,需要充分重視,采取措施降低危機發生的概率;另一方面,如若危機已經發生,則應努力調查原因,減輕事故造成的負面影響。
1.2 應急響應,即案件辦理階段 應急響應是應急管理運行的核心部分,指的是應急指揮部門及時啟動相關預案,統一指揮或指導有關地區、部門,開展應對突發公共事件的處置工作。
1.2.1 信息報告 受理部門依據《北京市藥品監督管理局受理違法案件舉報暫行規定》,將受理的案件統一編號、登記后,當日報請主管局長。信息報告還包括事中報告和結案報告。
1.2.2 分級響應 稽查辦公室根據《北京市藥品監督管理局受理違法案件舉報暫行規定》、《藥品監督行政處罰程序規定》承辦舉報案件,并于7日內展開調查。
1.2.3 應急升級 現場調查符合立案條件的,報主管領導批準立案。調查發現案件超出藥監分局控制處置職責范圍的,及時請示市藥監局或區(縣)政府,并按照上級批復精神,組織開展處置工作。
1.2.4 應急措施 在藥監稽查執法過程中,采取的應急措施包括:責令暫停問題產品的生產、經營、使用,責令召回產品,對現場涉案產品抽檢,對涉案物品、證據采取查封扣押、先行登記保存等。必要時,通報衛生、公安等相關部門,聯合執法。
1.3 后期處置 應急管理運行的后期處置是指在應急結束后進行的善后處置、調查與評估、恢復重建等工作。稽查辦公室對舉報、案件的后期處置主要包括以下兩方面:①報告和歸檔。即制作相關文書、報告、案卷,報送相關領導或部門;②評估反饋。稽查辦公室及時將查處企業信息通報相關監督科室。
綜上所述,稽查辦公室的工作在內容上、流程上合乎應急處置工作運行程序,同時印證和踐行了應急處置中“減少危害、快速反應、注重預防”的原則。
2 藥監稽查案件分級管理與響應
2.1 案件分級管理與響應 目前北京市藥監系統每年受理舉報投訴案件達數千件。案件信息來源大致有以下幾類:①群眾舉報;②上級機關批轉;③日常監督或專項檢查發現;④其他單位移送或協查;⑤檢驗機構檢驗發現;⑥新聞媒體曝光;⑦其他途徑。藥監分局受理的各類舉報、案件數量大、來源廣、情況雜,因此,監管任務重,監管力量嚴重不足,舉報案件辦理呈現疲于應對的局面。
當前,《北京市藥品監督管理局受理違法案件舉報暫行規定》將案件分為了一般情況和緊急情況兩級。“緊急情況”的標準是“需藥品監督管理部門立即制止違法行為或參與協助其他相關行政部門的”,而未就具體情形進行表述,實踐指導性存在欠缺。本文結合工作實踐,參照各級應急管理預案,提出案件分級管理與響應原則。
2.1.1 按照上述原則將分局稽查辦公室受理的舉報、案件分為四級。
Ⅰ級:①已經或者可能造成藥品安全突發事件的;②衛生部門通報的非法行醫致人死亡或傷殘的案件。
Ⅱ級:①有證據表明涉案藥品造成舉報投訴人人身傷害,舉報投訴人要求趕赴現場的;②涉及藥品生產環節的、證據較為翔實的舉報;③涉及血液制品、疫苗、生物制品等高風險品種或麻醉藥品、精神藥品、毒性藥品、放射性藥品等特殊管理藥品的舉報;④新聞媒體已報道,社會影響較大的;⑤上級要求緊急調查處理的其他舉報投訴事項。
Ⅲ級:①檢驗機構檢驗發現不合格產品的;②未取得藥監部門行政許可,非法從事相關生產經營活動的;③需要及時到現場抽檢取證的。
Ⅳ級:除Ⅰ級、Ⅱ級、Ⅲ級以外的其他舉報投訴事項。
2.1.2 分級響應 對應案件級別,將響應級別分為Ⅰ級、Ⅱ級、Ⅲ級、Ⅳ級。
Ⅰ級:需立即啟動分局應急預案,按分局應急工作領導小組統一部署,開展調查及信息上報工作。Ⅰ級是最為緊急的情況,要求執法人員嚴守時限,接到命令立即趕赴現場,進行調查、產品控制及抽樣,并在時限內上報信息。Ⅱ級、Ⅲ級、Ⅳ級由稽查辦公室分級處理。
Ⅱ級:情況緊急,需稽查執法人員立即趕赴現場展開調查。
例如,2010年6月,北京市藥品監督管理局緊急轉發河北省食品藥品監督管理局通報的假藥“洛汀新”在北京市的流向,各分局稽查辦公室立即行動,對轄區藥品經營企業展開調查,責令召回問題批號藥品,對庫存涉案藥品查封扣押,及時、有效遏制了可能發生的藥害事件。
Ⅲ級:情況比較緊急,需稽查執法人員及時出現場調查。如2010年9月,北京市藥監局朝陽分局接到群眾舉報,反映轄區某藥店銷售的某批次復方丹參滴丸涉嫌存在質量問題。執法人員接到舉報后及時到該藥店,對涉及批號的復方丹參滴丸抽樣送檢,消除可能發生的藥品質量風險。
Ⅳ級:此級案件由稽查執法人員按時限依法調查處理。
主要包括:①情節較輕、危害較小的違法行為和一般違規行為,如零售藥店未憑處方銷售處方藥;②舉報人無法提供問題產品詳細信息、相關票據、證據等情況;③經初步核實,違法主體不存在或違法地址無法查找的情形;④違法行為已被控制,需要進一步調查核實情況的,如北京市藥監局朝陽分局經常接到的外省市藥監局請求協查標示紫竹藥業、雙鶴藥業生產藥品真偽的函,及有關企業資質的核查等。

▲北京市藥監局朝陽分局工作人員查獲假藥窩點
2.2 分級管理與響應中應注意的問題
2.2.1 了解案情,明確需求 充分了解案情是分級管理的基礎和依據。將調查前置,在受理階段充分與舉報人交流,了解案情細節,如涉案產品名稱、批號、廠家、來源、地址信息,能否提供實物,是否有相關票據,舉報訴求等。
2.2.2 了解法律,明確權限 依法行政的前提是知法、懂法。對案情依法做出研判,是案件查處過程中的關鍵環節。在此過程中,對超出管轄或主管權限的情況及時移送,而對于處在法律邊緣的情況要多請示、多匯報,切忌不履行職責或不當履職。
2.2.3 了解事態,洞察發展 各類舉報、案件反映的是群眾快速增長的藥品安全需求與當前依然嚴峻的藥品安全形勢的矛盾。因此,在案件處理過程中,執法人員一定要密切關注事件發展的趨勢和范圍,若發現藥品存在安全隱患,采取措施及時清除;另一方面,如果已經發生藥品使用危害,做好產品控制、抽檢、溯源工作,敦促企業履行責任,減輕危害后果。
2.2.4 判斷形勢,靈活應對 對發生在首都重點地區,以及舉辦全國“兩會”或重大政治活動等特殊時期發生的案件,相應提高響應級別,確保迅速、有效控制事件,維護社會和諧穩定。
3 北京市藥監局朝陽分局的稽查工作模式
北京市藥監局朝陽分局每年受理舉報案件近700件,稽查辦公室在崗執法人員9人,分為3個執法組,不包括每年的各類專項檢查,每年度每組出現場200余次,監管任務重與監管力量不足的矛盾十分突出。當前,該分局稽查辦公室沿襲奧運期間的監管模式,將轄區按地域劃分為北、中、南三片,每個片區由一個執法組負責。稽查辦公室負責人接到主管局長批轉的案件,依據監管區域分配到各執法組辦理,重大、復雜的案件則統籌科室力量,指定人員重點辦理。從主管局長—稽查辦公室負責人—執法組,層級把關,力爭最大限度地控制藥品安全風險,確保監管到位。
筆者依據本文提出的分級管理和響應原則對北京市藥監局朝陽分局稽查辦公室2008~2010年受理的案件進行統計。該分局受理案件的年度總量分別為:2008年660件,2009年702件,2010年694件,統計各級案件所占比例(見附表)。
由附表可以看出,雖然每年受理舉報案件數量、情況不盡相同,但三年來每一級案件所占比例卻基本穩定。從Ⅰ級到Ⅳ級,案件比例成金字塔型分布,Ⅰ~Ⅱ級是需要執法人員立即趕赴現場的情況,占總量的2%~3%,Ⅰ~Ⅲ級比例之和接近30%,這是高風險舉報案件所占的比重,Ⅳ級占到70%以上,說明大部分案件可以按規定時限依法調查處理。
4 延伸的思考
本文從應急管理的角度分析基層藥監稽查執法工作,提出案件分級管理與響應原則,提高執法效率,降低藥品安全風險。研究藥監稽查工作的應急特質,還應考慮完善程序細則、深化案源管理等方面的問題。
4.1 完善程序細則 目前我國已搭建起“一案三制”藥品安全應急管理框架。完善的細則有利于使工作規范化,促進快速反應、科學決策和有條不紊地應對緊急、突發事件的發生。這方面美國FDA完善的應急程序規定值得我國藥品監管部門借鑒。
4.2 深化案源管理 北京市各藥監分局稽查辦公室基本已建立舉報案件臺賬,數字稽查系統的運用也使全市藥品舉報案件有據可查。但目前大家的關注點主要集中于立案查處的案件,而對于大量的未立案案件缺少匯總分析。實際上,對每年度固定時間段的舉報情況及趨勢進行分析,可以發現群眾關注的熱點、監管薄弱點,以及執法難點(未立案案件中包含法律邊緣問題、受執法手段局限無法繼續調查等問題),這是藥品安全預警信息的重要組成部分。完善這些信息的采集分析,有助于發現藥品安全風險點,從而采取相應措施,防止其進一步演化為危機事件。
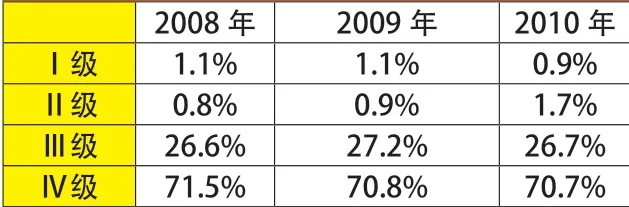
附表 2008~2010年北京市藥監局朝陽分局稽查辦公室受理案件分級情況統計
4.3 重視人的因素 任何先進的系統、程序,最終運行離不開人的操作,人的因素是一個老生常談的問題。本文探討的是應急工作,除了人員素質培養、結構構成等問題外,還需強調兩點:①戰時的執行力,應急情況下一線人員的執行力尤為重要,只有快速、堅決地貫徹上級決策,嚴謹細致,依法履職,才能盡快消除或緩解危機;②培育質疑的精神,執法人員平時要養成思考的習慣,對于可能對藥品安全產生不利后果的現象、活動、決策要提高警惕,鼓勵和重視不同的意見,通過思維的多元化來避免群體思維誤區。

