八角茴香中莽草酸提取工藝的優化
張迎,劉軍海,*,劉燕飛,李燕,柳仁民
(1.聊城大學化學化工學院,山東 聊城 252059;2.聊城大學 農學院,山東 聊城 252059)
莽草酸又稱毒八角酸,學名為3,4,5-三羥基-1-環己烯-1-羧酸(3,4,5-trihydroxy-1-cyclohexene-1-carboxylic acid),結構式相對分子質量為174.15。莽草酸為白色精細粉末,易溶于水,在25℃下100 mL水中可溶解18 g,難溶于苯、氯仿和石油醚。熔點為191℃~192℃,旋光度為-180°。莽草酸主要存在于八角茴香、馬尾松、側柏等天然植物中,尤以八角茴香中含量相對較多[1]。莽草酸具有鎮痛、抗菌、抗血小板凝集、抗腫瘤、抗血栓形成和抗腦缺血等作用[2-5]。因此,提取莽草酸對開發和利用我國豐富的八角茴香資源具有十分重要的意義。
響應面分析法(RSM)是利用合理的試驗設計,采用多元二次回歸方程擬合因素與響應值之間的函數關系,通過對回歸方程的分析來尋求最佳工藝參數,解決多變量問題的一種統計方法[6]。以水為溶劑利用響應面分析法優化八角茴香中的莽草酸提取最佳工藝條件。
1 材料與方法
1.1 儀器與材料
1.1.1 材料
八角茴香:產于廣西,購于本地集貿市場。莽草酸對照品(98%):購于阿拉丁試劑有限公司;高碘酸(AR),高碘酸納(AR),氫氧化鈉(AR),亞硫酸鈉(AR)。
1.1.2 儀器
TU-1810紫外可見分光光度計:北京普析通用儀器有限責任公司;數顯恒溫水浴鍋HH-6:國華電器有限公司;DKB-501A型超級恒溫水槽:上海精密實驗設備有限公司;AR-1104電子天平:奧克斯國際貿易上海有限公司;循環水式多用真空泵:鄭州長城科工貿有限公司;QE-200高速中藥粉碎機:武義縣屹立工具有限公司。
1.2 方法
1.2.1 八角茴香莽草酸提取工藝流程
八角茴香→粉碎(過篩)→八角茴香粉末→提取回流→抽濾→濾液→測定吸光度
1.2.2 八角茴香莽草酸的提取方法
準確稱取八角茴香粉末約2.0 g,置250 mL圓底燒瓶中,加入一定量的蒸餾水,在實驗條件下回流提取,然后抽濾得濾液,濾液用蒸餾水定容于250 mL容量瓶中,精確量取0.2 mL溶液定容于10 mL容量瓶,測定其吸光度。
1.2.3 分析測定方法[7]
1.2.3.1 標準曲線的繪制
精密稱取莽草酸對照品34.80mg,置于1000mL容量瓶,加蒸餾水溶解并稀釋至刻度。準確移取0.2mmol/L的莽草酸標準曲線 0、0.2、0.4、0.6、0.8、1.0、1.2、1.4、1.6 mL于10 mL容量瓶中,分別加入0.5%的HIO4水溶液和0.5%的Na2IO4水溶液各1.25 mL,搖勻,于37℃放置30 min后冷卻,加入0.056 mol/L的Na2SO3和1 mol/L的NaOH(體積比2∶3)混合液定容至刻度。在室溫下,立即讀取該溶液在382 nm處的吸光度值(A)。得到標準曲線的回歸方程為:C=40.9836A-0.0574,R2=0.9995,在 0~55.68μg/mL 的范圍內,濃度(C)與吸光度(A)有良好的線性關系,標準曲線如圖1所示。
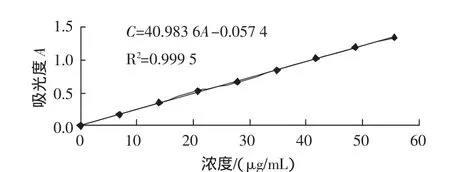
圖1 標準曲線Fig.1 Standard curve
1.2.3.2 莽草酸提取率的測定
取一定體積的八角茴香提取液置于10 mL容量瓶中,分別加入0.5%的HIO4水溶液和0.5%的Na2IO4水溶液各1.25 mL,搖勻,于37℃放置30 min后冷卻,加入0.056 mol/L的Na2SO3和1 mol/L的NaOH(體積比2∶3)混合液定容至刻度。在室溫下,立即讀取該溶液在382 nm時的吸光度值,從回歸方程中計算提取液中莽草酸的含量。提取率用下式計算:

2 結果與討論
2.1 提取時間對提取率的影響
分別稱取20目的八角茴香粉末約2.0 g,6份。固定提取溫度 80 ℃,料液比 1∶20(g/mL),分別提取 0.5、1.0、1.5、2.0、2.5、3.0 h后,提取 1 次,結果如圖 2 所示。
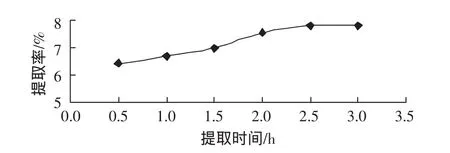
圖2 提取時間對莽草酸提取率的影響Fig.2 Effect of extraction time on extraction rate
從圖2可以看出,隨著提取時間的增加,莽草酸提取率不斷提高,但是當提取時間達到2.5 h后,提取率基本上增加很少。所以在實際的提取過程中要考慮時間效率和成本因素,提取時間取2.5 h左右為宜。
2.2 料液比對提取率的影響
分別稱取20目的八角茴香粉末約2.0 g,5份。固定提取溫度80℃,提取時間1 h,分別在料液比1∶8、1∶14、1∶20、1∶26、1∶32(g/mL)下回流,提取 1 次,結果如圖3所示。

圖3 料液比對莽草酸的影響Fig.3 Effect of the ratio of material to solvent on extraction rate
從圖3可以看出,料液比越大,莽草酸的提取率越大。當料液比達到1∶20(g/mL)時后,提取率增加很少。料液比過小,溶劑不能有效潤濕樣品,影響莽草酸的提取;料液比過高,增加后續蒸發處理的困難,操作成本增加。因此,適宜的料液比取1∶20(g/mL)左右為宜。
2.3 提取溫度對提取率的影響
分別稱取20目的八角茴香粉2.0 g,5份,固定料液比為 1∶20(g/mL),提取時間為 1 h,提取溫度分別在 50、60、70、80、90℃下提取,提取 1次,結果如圖4所示。

圖4 溫度對莽草酸吸提取率影響Fig.4 Effect of extraction temperature on extraction rate
從圖4可以看出,莽草酸的提取率隨提取溫度的升高而增大。但是當提取時間達到70℃后,基本上提取率保持不變。所以在實際的提取過程中要考慮時間效率和操作成本因素,所以在實際的工業生產中采用70℃左右為宜。
2.4 原料粒度對提取率的影響
分別稱取過20目、40目、60目篩的八角茴香粉末約2.0g,各1份,分別在提取溫度80℃,提取時間為1h,料液比為1∶20(g/mL)下,提取1次,結果如圖5所示。

圖5 原料粒度對莽草酸提取率的影響Fig.5 Effect of particle size on extraction rate
從圖5可以看出,原料粉碎得越細,莽草酸的提取率越高,但是,粒數過細,增加處理困難,采用60目左右的八角茴香粉末來提取莽草酸為宜。
2.5 提取次數對提取率的影響
稱取60目的八角茴香粉末約2.0 g,1份。在固定提取溫度 80 ℃,提取時間為 1 h,料液比為 1∶20(g/mL)的情況下,分別提取 1、2、3、4、5 次,結果如表 1 所示。

表1 提取次數比對莽草酸的影響Table 1 Effect of extraction times on extraction rate
從表1可以看出,莽草酸的總提取率隨著提取次數的增加而增大,經過5次提取已基本提取出來,3次提取即可提出總量的95%,考慮生產成本及效率等方面的因素,所以認為提取3次比較合適。
2.6 實驗方案設計與工藝優化
根據Box-Benhnken的中心組合實驗設計原理[6,8],采用響應面實驗設計方法,選取提取時間、料液比、提取溫度等3個影響莽草酸提取率的主要因素,設計三因素三水平的響應面分析。在固定原料粒度為60目,提取次數為1次的情況下,考察3個因素對莽草酸提取率的影響,試驗因子水平編碼表如表2所示。

表2 響應面分析因子及水平表Table 2 Factors and levels of RSM
對提取時間、料液比、提取溫度作如下變換。
式中:Z1、Z2、Z3分別表示提取時間、料液比、提取溫度。在單因素試驗基礎上,以X1、X2、X3為自變量,以莽草酸提取率(Y)為響應值,采用SAS RSREG程序進行響應面分析實驗。實驗設計與結果如表3所示。
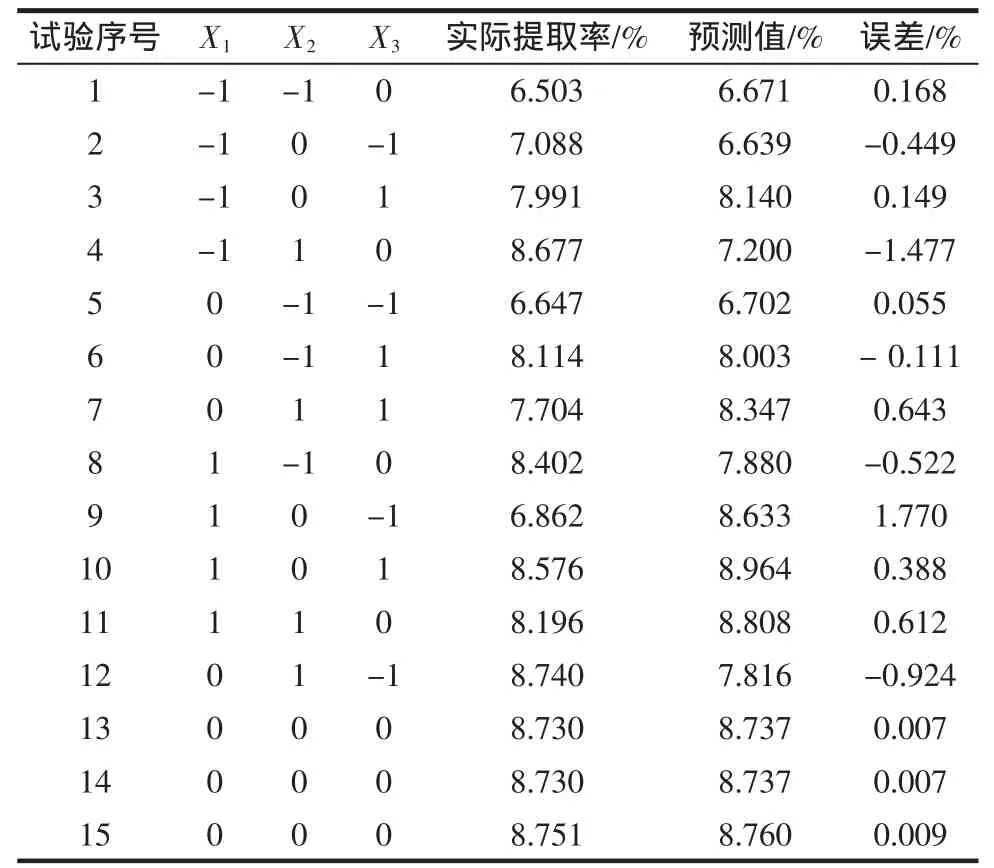
表3 響應面分析方案及試驗結果Table 3 Program and experimental results of RSA
其中1~12是析因試驗,13~15是中心試驗,用來估計試驗誤差。采用SAS 8.0軟件處理上述試驗設計所得響應面與等直線見圖6~圖8。
采用SAS RSREG程序對響應值與各因素進行回歸擬合后,得到回歸方程:

回歸分析結果見表4,回歸方程中各變量對指標(響應值)影響的顯著性,由P檢驗來判定,概率P(Pr>F)的值越小,則相應變量的顯著程度越高。

圖6 提取時間(X1)和料液比(X2)對提取率影響的響應面與等值線Fig.6 Responsive surfaces and contours of Z=f(Xl,X2)

圖7 提取時間(X1)和提取溫度(X3)對提取率影響的響應面與等值線Fig.7 Responsive surfaces and contours of Z=f(Xl,X3)

圖8 料液比(X2)和提取溫度(X3)對提取率影響的響應面與等值線Fig.8 Responsive surfaces and contours of Z=f(X2,X3)
由表4可見,各因素中一次項X1,X2,X3和二次項X2X2都是高度顯著的,二次項X1X1,X3X3和X1X3顯著,因此各具體實驗因子對響應面的影響不是簡單的線性關系。回歸方程也是高度顯著的,相關系數R2=97.80%,說明響應值(提取率)的變化有97.80%來源于提取時間、料液比和提取溫度3個變量。因此,回歸方程可以較好地描述各因素與響應值之間的真實關系,可以利用該回歸方程確定最佳工藝條件。對回歸方程取一階偏導數等于零,整理可得:
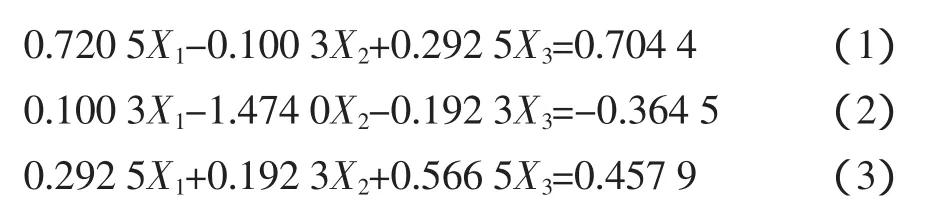
解聯立方程組得:X1=0.9195,X2=0.2783,X3=0.2393。代入前述的變換公式得到最佳提取時間為2.92 h,料液比為 1∶21.67(g/mL),提取溫度為 82.39 ℃,為了操作的方便,將其修正為提取時間3.0 h,料液比1∶22(g/mL),提取時間為 83℃,即八角茴香莽草酸提取工藝最佳工藝條件為:提取時間為3.0 h、料液比為1∶22(g/mL)、溫度為 83 ℃。該模型的 R2=0.9780,此模型與實際試驗擬合較好,試驗失擬項小,因此可用該回歸方程代替實驗真實點對實驗結果進行分析。用此數學模型預測最佳條件下的提取率為8.873%。實驗提取率與理論預測值結果見表3。

表4 莽草酸回歸分析結果Table 4 Results of regression analysis
2.7 最優條件下驗證
準稱3份八角茴香粉末,每份約2.0 g,分別在最佳提取條件:提取時間 3.0 h、料液比為 1∶22(g/mL)、溫度為83℃下提取1次,結果如表5所示。

表5 最佳條件的實驗結果Table 5 The experimental results in the optimum extraction conditions
由表5可見,莽草酸在最佳條件下一次提取率為8.779%,由數學模型得到理論預測值為8.873%,實際提取率比理論預測值僅低了0.094%。因此,建立的二次回歸模型能很好地預測莽草酸的提取率。
3 結論
通過中心組合試驗設計和響應面分析法,能可靠地進行優化試驗以及數據分析。應用這一方法對莽草酸提取的工藝條件進行優化,取得了較好的效果。在單因素試驗基礎上,通過中心組合試驗,設計三因素三水平響應面分析法試驗。最終得到二次回歸方程,確定出八角茴香莽草酸的最佳提取條件為:提取時間為 3.0 h,料液比是 1∶22(g/mL),提取溫度是 83 ℃;單因素實驗確定其最佳提取次數為3次。在最佳提取工藝條件下的一次提取率為8.779%,一次提取理論預測值為8.873%。實際提取率比理論預測值僅低了0.094%,因此該二次回歸數學模型能準確的預測八角茴香中莽草酸的提取率。
[1]陳驍熠,袁利,王敏,等.馬尾松、側柏和八角茴香中的莽草酸含量分析[J].湖北農業科學,2009,48(5):1238-1240
[2]Fang A Q,Demain A L,Wong G K.Enhancement of the antifungal activity of rapamycin by the coproduced elaiophylin and nigericin[J].The journal of antibiotics,2000,53(2):158
[3]林潔,蘭琪欣,韋應芳,等.八角茴香藥用成分的提取及其鎮痛作用的實驗研究[J].右江民族醫學院學報,2008,30(2):195-196
[4]Huang F,Xiu Q.Anti-platelet and anti-thrombotic effects of triacetyl shikimic acid in rats[J].Journal of cardiovascular pharmacology,2002,39(2):262-270
[5]Ma Yi,Xu Qiu-Ping,Sun Jian-Ning.Antagonistic effects of shikimic acid against focal cerebral ischemia injury in rats subjected to middle cerebral artery thrombosis[J].Acta Pharmacologica Sinica,1999,20(8):696-700
[6]高洪霞,劉軍海,于波濤.響應面分析法優化辣椒紅色素提取工藝條件[J].食品研究與開發,2009,30(10):177-181
[7]TH克羅馬蒂,ND波爾格.莽草酸的檢測方法:中國,00806428.8[P].2002-05-29
[8]徐效圣,潘儼,傅力,等.響應面法優化水酶法提取核桃油的工藝條件[J].食品與機械,2010(2):92-96

