臍靜脈內皮細胞來源的微囊泡促進腹膜樣組織血管化的初步研究
程中良 鄒翔宇 吳帥 琚官群 朱英堅
組織血管化是臨床成功應用組織工程技術進行組織修復的重要條件之一。如果沒有快速高水平的組織血管化,移植物中的種子細胞在移植早期不易存活[1]。目前組織血管化的策略主要包括以下幾種:①對支架材料的表面結構進行修飾[2-3];②在材料內復合緩釋的生長因子[4-6];③對種子細胞進行基因修飾[7-8]。雖然這些方法在促進新生血管生成方面具有一定的作用和價值,但是存在支架材料的制備工藝復雜、生長因子降解速度快,以及進行基因修飾的種子細胞存活率低等缺點。研究能夠促進組織血管化的簡單方法是組織工程領域重要研究課題之一[9]。
我們的前期研究發現,腹膜間皮細胞作為種子細胞構建的組織工程腹膜樣組織,可用于尿道缺損的替代修復[10-11]。但是一旦尿道缺損面積太大,滋養血管不能充分供給中心區域時,就會導致治療失敗。
血管內皮細胞生長因子(VEGF)是能夠促進組織工程組織血管化的一種重要的生長因子。已有文獻證實,腹膜間皮細胞在一定條件下也可分泌VEGF[12]。因此,如能尋找到一種促進腹膜間皮細胞分泌VEGF增多并進一步促進腹膜樣組織血管化的方法,就可能明顯提高腹膜樣組織進行組織工程替代的療效。
近年來,越來越多的研究聚焦于細胞的微囊泡。微囊泡被認為是細胞間信號傳遞的重要分子,在細胞通訊和細胞相互作用中具有重要作用。微囊泡是各類細胞遭受一系列應激(激活或凋亡)時,從細胞質膜上脫落而釋放的膜性小囊泡[13]。已有研究發現,內皮細胞來源的微囊泡能夠刺激多種細胞增殖和抑制凋亡[14-15],并能夠促進內皮細胞自分泌VEGF[16]和啟動血管生成。本研究旨在探討人臍靜脈內皮細胞來源的微囊泡能否促進大鼠腹膜間皮細胞增殖,刺激其分泌VEGF,并促進體內腹膜樣組織血管化,為組織工程腹膜樣組織的臨床應用奠定基礎。
1 材料和方法
1.1 材料
SD大鼠、裸鼠(上海第九人民醫院動物實驗中心),新生嬰兒廢棄臍帶(上海市第一人民醫院婦產科無償獲得,均經產婦知情同意),DMEM培養基、EGM-2培養基(Lonze公司),胎牛血清(HyClone公司), 胰蛋白酶(Sigma 公司),CD31、VE-Cad 因子(Abcan 公司),Vimentin、CK-AE1/AE3(Santa Cruz公司),兔抗小鼠二抗(Dako公司),FITC標記的熒光二抗(Dako公司),人VEGF的ELISA試劑盒、大鼠VEGF的試劑盒(R﹠D公司),Ⅰ型膠原酶(Gibco公司),小腸粘膜下層(SIS)。
1.2 實驗方法
1.2.1 大鼠腹膜間皮細胞的分離、培養
取4周齡SD雄性大鼠4只,肌肉注射10%水合氯醛0.5~0.8 mL麻醉,向大鼠腹腔內注射0.25%胰蛋白酶20~30 mL和0.02%EDTA消化液。1 h后脫頸處死大鼠,75%乙醇全身浸泡消毒10min。將大鼠仰面置于超凈工作臺,沿腹白線依次剪開腹壁皮膚及肌肉,吸出腹腔內的消化液,移入15 mL離心管中,加入含20%FBS血清培養基中和胰酶,1500 r/min離心15min,棄上清液,加入含20%FBS的DMEM培養液,輕輕用吹打成細胞混懸液,分裝于25 cm2的細胞培養瓶中,加入培養基,使總體積達到4~5 mL,置于37℃、5%CO2的培養箱中培養。每2 d更換1次完全培養基。常規傳代,取第2代細胞進行實驗和鑒定。
1.2.2 hUVECs原代培養
取胎兒臍帶10~30 cm,PBS沖洗,分離臍帶組織中管腔大、管壁薄的臍靜脈,在臍靜脈一端插入鈍頭灌流玻璃管并固定,PBS沖洗臍靜脈腔,直至流出液澄清無血色;夾閉臍靜脈另一端,臍靜脈內灌注0.1%Ⅰ型膠原酶使其充盈,37℃消化10~12min,收集消化液至50 mL離心管中,并用EGM-2培養液沖洗靜脈,將收集液以1500 r/min離心5min,小心棄上清液,以EGM-2培養液將細胞沉淀重新懸浮,調整細胞密度為(2~3)×105cells/mL,轉移至 25 cm2的培養瓶內,置于37℃、5%CO2培養箱中進行培養,24h后觀察細胞貼壁及生長情況并更換培養液,之后每2天半量換液1次。取第3~5代細胞用于實驗以及鑒定。
1.2.3 hUVECs來源的微囊泡分離、定量和投射電鏡掃描鑒定
hUVECs培養至80%融合時,棄培養液更換為含0.25%BSA的無血清EGM-2,繼續培養24h后,收集上清液,2000 g離心20min,以去除細胞碎片,收集上清放入超高速真空離心機以100000 g、4℃離心1 h,棄上清加入無血清M199洗滌后,再次行超高速真空離心。棄上清,再于2.5%戊二醛溶液固定,4 ℃、2 h以上,PBS(pH7.2)沖洗,1%鋨酸固定后,乙醇梯度脫水,100%丙酮浸透,環氧樹脂包埋、切片,將切片鋪于銅網上,經枸櫞酸鉛及醋酸雙氧鈾染色后,透射電鏡觀察并照相。余微囊泡的重懸于M199培養基中,微囊泡中所含蛋白質用BAD法行蛋白定量,放入-80℃冰箱保存。
1.2.4 微囊泡對rPMC增殖的影響
取對數生長期的rPMC重懸成1×105cells/mL,每孔取100μL種植在96孔板中,待細胞貼壁后試驗組每孔加入30 μg/mL含hUVECs來源微囊泡的蛋白,對照組不加,每組細胞6個副孔,37℃、5%CO2培養箱中孵育, 分別培養 0、24、48、72 h 后,棄上清,每孔加入CCK-8試劑10μL,繼續培養3 h后,用酶標儀進行450 nm處吸光度值的測量。
1.2.5 RT-PCR檢測微囊泡組和對照組rPMC
rPMC以5000個/孔種植在6孔板中,貼壁后MVs組加入30 μg/mL微囊泡,對照組不加,分別在24、48、72 h收集上清液,按ELISA試劑盒說明分別檢測大鼠和人來源VEGF濃度。棄上清后,貼壁細胞采用TRIzol一步法提取總RNA,2 μg總RNA進行逆轉錄合成cDNA,反應體系20μL進行PCR擴增,引物序列包括人VEGF上游引物5'-cccactgaggagtccaacat-3', 下游引物 5'-aaatgctttctccgctctga-3',大鼠 VEGF上游引物5'-gcccatgaagtggtgaagtt-3',下游引物5'-tatgtgctggctttggtgag-3',以β-actin為內參照,擴增后 1.8%瓊脂糖凝膠電泳(90 V,30min)進行PCR產物鑒定,電泳圖像分析儀掃描分析。
1.2.6 rPMC種植在SIS表面移植裸鼠皮下
收集第2代腹膜間皮細胞,以2×106cells/cm2細胞密度,將rPMC均勻接種至小腸黏膜下層(Small intestine submucosa,SIS)支架(第九人民醫院組織工程實驗室提供)表面,實驗組放入含hUVECs來源的微囊泡30 μg/mL的DMEM培養液,對照組為單純DMEM培養液,置于CO2恒溫培養箱中,隔天換液,1周后分別接種于4周齡裸鼠側背部皮下。2周后取出支架移植物,經4%多聚甲醛固定,石蠟包埋切片,脫蠟、脫水、HE染色,鏡下觀察拍照,并對微血管樣結構計數(光學顯微鏡下,10×20倍視野下,每張片隨機選取不重疊的5個視野進行計數)。
1.2.7 統計學處理
運用SPSS 19.0軟件進行t檢驗,P<0.05為差異具有統計學意義。
2 結果
2.1 rPMC和hUVECs鑒定
剛消化下來的腹膜間皮細胞在光鏡下呈分散的小圓型細胞,約24h左右貼壁;融合前相差顯微鏡觀察,細胞呈多樣形(梭形、橢圓形、多角形等)。體外培養1周,細胞生長融合,倒置相差顯微鏡觀察,細胞呈多角形,大小一致,“鋪路石樣”外觀(圖1a)。細胞免疫組織化學染色顯示,抗細胞角蛋白抗原(CKAE1/AE3)和抗波形蛋白抗原(Vimentin)陽性(圖1b、C)。hUVECs原代培養后,相差顯微鏡下可見細胞單層排列,邊界清楚,呈圓形、短梭形或扁平形,3~4 d融合成單層,鋪路石樣排列(圖1d)。細胞免疫熒光示CD31和VE-Cad陽性表達(圖1e、f)。
2.2 透射電鏡觀察微囊泡
透射電鏡下可見有完整膜結構的微囊泡(圖2)。
2.3 微囊泡對腹膜間皮細胞增值的影響
微囊泡組在 24、48、72、96 h 與對照組相比,增殖效應明顯增強(P<0.05)(圖 3)。
2.4 腹膜間皮細胞上清液VEGF蛋白質水平
培養的rPMC經微囊泡干預后與對照組相比,在24、48、72 h分別采取ELISA方法對細胞培養上清液行大鼠VEGF檢測,發現加入hUVECs來源的微囊泡組上清液中,大鼠來源VEGF含量與對照組相比顯著升高(P<0.05)(圖4),未檢測到人來源VEGF表達。
2.5 腹膜間皮細胞VEGF mRNA的表達
培養的rPMC經hUVECs來源的微囊泡干預后與對照組相比,大鼠VEGF的mRNA行RT-PCR檢測,在 24、48、72 h 的表達均明顯高于對照組(圖 5)。兩組均未檢測到人來源的VEGF的mRNA表達。
2.6 微囊泡對SIS支架內新生微血管樣結構的影響
被覆rPMC的SIS支架移植入裸鼠皮下2周后,HE染色可見MVs組移植物中含大量紅細胞的新生微血管樣結構。加入hUVECs來源的微囊泡組中新生血管密度較對照組顯著增多(P<0.05)(圖6)。
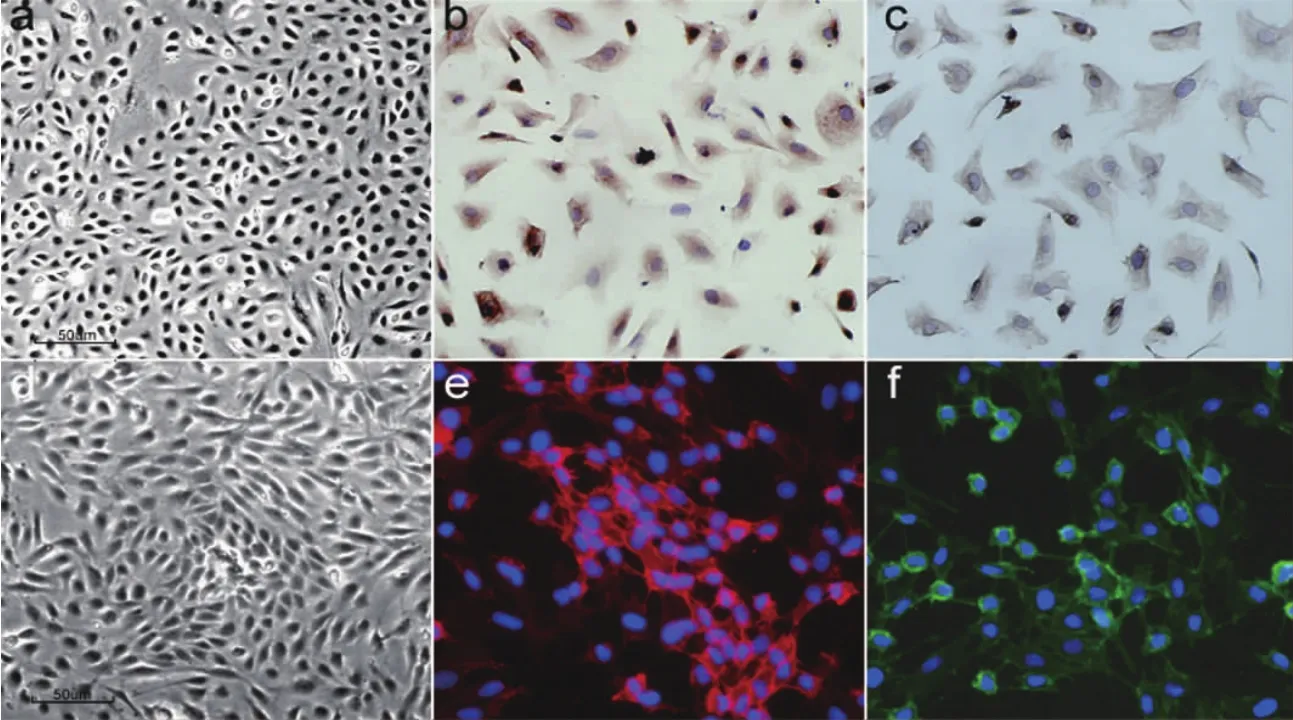
圖1 腹膜間皮細胞與人臍靜脈內皮細胞形態學觀察和鑒定Fig.1 The morphological features and identifications of peritoneal mesothelial cells and human umbilical vein endothelial cells

圖2 人臍靜脈內皮細胞來源的微囊泡透射電鏡觀察(80 KV,30000×)Fig.2 The TEM observations of microvesicles(MVs)derived from human umbilical vein endothelial cells(80 KV,30000×)

圖3 微囊泡對腹膜間皮細胞增殖的影響Fig.3 The effects of MVs on growth ability of rat peritoneal mesothelial cells
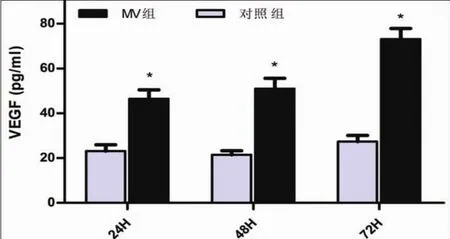
圖4 ELISA檢測24、48、72 h上清液中大鼠VEGF的表達(*:P<0.05)Fig.4 The rat VEGF expression of supernatant in MVs group and control group at 24,48,72 h were tested by ELISA(*:P<0.05)
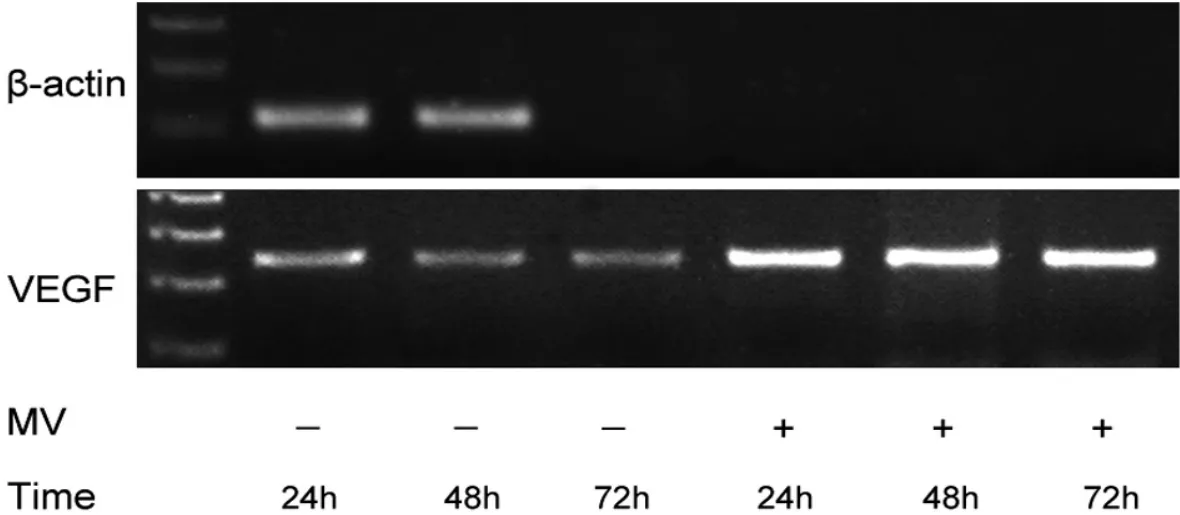
圖5 RT-PCR檢測MVs組和對照組大鼠VEGF表達Fig.5 The rat VEGF expression in MVs group and control group were tested by RT-PCR

圖6 移植裸鼠皮下及取出后HE染色觀察微血管樣結構的數量Fig.6 Transplanted subcutaneously into nude mice,and the number of microvessel-like structures by HE staining
3 討論
先天或后天原因所導致的尿道狹窄和缺損,尤其是大于2 cm的長段尿道缺損和復雜性尿道狹窄的尿道重建,仍然是困擾泌尿外科的難題之一。組織工程學為此提供了全新的思路。在尿道組織工程中,種子細胞的選擇仍然是研究熱點。自體尿路移行上皮細胞是理想的種子細胞來源。但是,尿路上皮細胞的來源有限,體外培養和擴增較為困難。腹膜間皮細胞來源于中胚層,同時表達間葉細胞和上皮細胞的分子標記,易在體外培養和擴增。同時,大網膜和腹膜表面覆蓋間皮細胞,因此具有量多、易取的特點。應用腹膜間皮細胞覆蓋的自體管狀組織修復尿道缺損研究取得了良好的效果[10]。同時,應用腹膜間皮細胞作為尿道組織工程的種子細胞進行尿道修復,也取得了預期的效果[11]。目前的研究中,面臨的瓶頸就是工程化組織的血管化問題。
近年來,血管化問題的研究取得了一些進展,但仍未達到理想的效果。微囊泡,作為一種新發現的細胞間信號傳遞分子,可能在促進細胞自分泌生長因子以及促進血管化方面具有一定的作用。已有研究發現,微囊泡與靶細胞之間的作用方式主要表現為以下幾種:①通過其表面的配體與靶細胞的受體結合繼而激活或者抑制靶細胞內的轉導通路[17]。②傳遞母細胞的蛋白質或mRNA到靶細胞[18]。微囊泡在形成過程中可以將母細胞質中的成分(蛋白質、mRNA或miRNA包裹進去),然后傳遞到靶細胞中,使其具有新的生物學或遺傳特征。③將母細胞膜的受體轉移到靶細胞而呈現相關受體表型[16]。④作為載體轉移完整的細胞器或者致病因子[19]。最新研究顯示,內皮細胞來源的微囊泡被證實能夠刺激內皮細胞的增殖并抑制凋亡,同時能夠促進內皮細胞自分泌VEGF,并啟動血管生成。本實驗中,我們成功地從人臍靜脈內皮細胞的上清液中分離出微囊泡,并初步證實此微囊泡能夠促進腹膜間皮細胞增殖、刺激其釋放VEGF,并使移植的組織工程樣腹膜組織血管化。同時,我們還發現,人臍靜脈內皮細胞來源的微囊泡與大鼠的腹膜間皮細胞共培養后,上清液中的大鼠來源的VEGF表達增高,但未檢測出人VEGF蛋白表達,也沒有檢測到人VEGF的mRNA表達。據此,我們推測,人臍靜脈內皮細胞來源的微囊泡可能是通過其表面的配體與靶細胞的受體結合,繼而激活或者抑制靶細胞內的轉導通路,進而激活腹膜間皮細胞內促進VEGF高表達的信號通路,具體的機制尚需更進一步的研究。
本實驗中,我們首次證實了人臍靜脈內皮細胞來源的微囊泡在體外能促進大鼠腹膜間皮細胞增殖,同時刺激大鼠來源的VEGF釋放。同時,在體內實驗驗中,發現微囊泡可促進組織工程化腹膜樣組織血管化增加,該發現為組織工程組織血管化研究提供了新的實驗依據。
[1]Madeddu P.Therapeutic angiogenesis and vasculogenesis for tissue regeneration[J].Exp Physiol,2005,90(3):315-326.
[2]Sarkar S,Lee GY,Wong JY,et al.Development and characterization of a porous micro-patterned scaffold for vascular tissue engineering applications[J].Biomaterials,2006,27(27):4775-4782.
[3]Kim BS,Baez CE,Atala A.Biomaterials for tissue engineering[J].World J Urol,2000,18(1):2-9.
[4]Zisch AH,Lutolf MP,Ehrbar M,et al.Cell-demanded release of VEGF from synthetic,biointeractive cell ingrowth matrices for vascularized tissue growth[J].FASEB J,2003,17(15):2260-2262.
[5]Bauer SM,Bauer RJ,Liu ZJ,et al.Vascular endothelial growth factor-C promotes vasculogenesis,angiogenesis,and collagen constriction in three-dimensional collagen gels[J].J Vasc Surg,2005,41(4):699-707.
[6]Elcin YM,Dixit V,Gitnick G.Extensive in vivo angiogenesis following controlled release of human vascular endothelial cell growth factor:implications for tissue engineering and wound healing[J].Artif Organs,2001,25(7):558-565.
[7]Wenger A,Kowalewski N,Stahl A,et al.Development and characterization of a spheroidal coculture model of endothelial cells and fibroblasts for improving angiogenesis in tissue engineering[J].Cells Tissues Organs,2005,181(2):80-88.
[8]Unger RE,Sartoris A,Peters K,et al.Tissue-like self-assembly in cocultures of endothelial cells and osteoblasts and the formation of microcapillary-like structures on three-dimensional porous biomaterials[J].Biomaterials,2007,28(27):3965-3976.
[9]Kanematsu A,Yamamoto S,Ogawa O.Changing concepts of bladder regeneration[J].Int J Urol,2007,14(8):673-678.
[10]Gu GL,Zhu YJ,Xia SJ,et al.Peritoneal cavity as bioreactor to grow autologous tubular urethral grafts in a rabbit model[J].World J Urol,2010,28(2):227-232.
[11]Gu GL,Xia SJ,Zhang J,et al.Tubularized urethral replacement using tissue-engineered peritoneum-like tissue in a rabbit model[J].Urol Int,2012,89(3):358-364.
[12]Mutsaers SE.Mesothelial cells:their structure,function and role in serosal repair[J].Respirology,2002,7(3):171-191.
[13]Conde-Vancells J,Rodriguez-Suarez E,Embade N,et al.Characterization and comprehensive proteome profiling of exosomes secreted by hepatocytes[J].J Proteome Res,2008,7(12):5157-5166.
[14]Cantaluppi V,Biancone L,Figliolini F,et al.Microvesicles derived from endothelial progenitor cells enhance neoangiogenesis of human pancreatic islets[J].Cell Transplant,2012,21(6):1305-1320.
[15]Cantaluppi V,Gatti S,Medica D,et al.Microvesicles derived from endothelial progenitor cells protect the kidney from ischemiareperfusion injury by microRNA-dependent reprogramming of resident renal cells[J].Kidney Int,2012,82(4):412-427.
[16]Al-Nedawi K,Meehan B,Kerbel RS,et al.Endothelial expression of autocrine VEGF upon the uptake of tumor-derived microvesicles containing oncogenic EGFR[J].Proc Natl Acad Sci U S A,2009,106(10):3794-3799.
[17]Taraboletti G,D'Ascenzo S,Borsotti P,et al.Shedding of the matrix metalloproteinases MMP-2,MMP-9,and MT1-MMP as membrane vesicle-associated components by endothelial cells[J].Am J Pathol,2002,160(2):673-680.
[18]Deregibus MC,Cantaluppi V,Calogero R,et al.Endothelial progenitor cell derived microvesicles activate an angiogenic program in endothelial cells by a horizontal transfer of mRNA[J].Blood,2007,110(7):2440-2448.
[19]Raymond AD,Campbell-Sims TC,Khan M,et al.HIV Type 1 Nef is released from infected cells in CD45(+)microvesicles and is present in the plasma of HIV-infected individuals[J].AIDS Res Hum Retroviruses,2011,27(2):167-178.

