體外擴散池法評價銀杏酮酯磷脂復合物體外透過性能研究
賴 樂,莫紅纓,賴春麗
(廣州醫學院第一附屬醫院呼吸疾病研究所,廣東 廣州 510120)
銀杏酮酯(GBE50)是從銀杏葉中提取、精制而成,經國家食品藥品監督管理總局批準正式生產的二類中藥新藥,主要成分是黃酮醇苷與萜類內酯,臨床主要用于預防和治療心腦血管疾病,但由于口服吸收差,影響臨床應用,而磷脂復合物中的磷脂分子具有兩親性可作為有效的乳化劑,也是細胞膜的重要組成部分,因此,制備成銀杏酮酯磷脂復合物,通過改善腸透過性能,為提高口服吸收利用度提供可能。體外擴散池法被國外學者譽為胃腸道屏障功能研究的金標準,在研究藥物的腸吸收和代謝方面已有一定的應用,通過高效液相色譜(HPLC)法或分光光度法測定藥物的透過量后,根據藥物的有效滲透系數來評價藥物吸收的動力學的變化,可用于研究藥物在特定腸段的吸收,模擬腸道的生理環境,操作方便簡單。本研究中的體外擴散池法試驗是建立在大鼠腸黏膜基礎上的,是用來預測銀杏酮酯中的黃酮醇苷在人體的吸收,對銀杏酮酯原料和銀杏酮酯磷脂復合物進行體外初步評價,為提高銀杏酮酯磷脂復合物在體內的生物利用度提供有利依據。
1 材料與方法
1.1 儀器與試藥
LC-20A型系列高效液相色譜儀(日本島津公司);7 mL Ussing Chamber裝置(美國 Harvard公司);Model-868型 pH計(Thermo Orion);電子分析天平(sarorius,d=0.1 mg)。戊巴比妥鈉(中國醫藥上海化學試劑廠);銀杏酮酯(GBE50,上海杏靈科技藥業公司,批號為061202);大豆磷脂(上海太偉藥業有限公司,批號為20072101017);四氫呋喃(廣州化學試劑廠,批號為030901-2);甲醇為色譜純;槲皮素對照品(批號為100081-200406)、山柰素對照品(批號為110861-200606)、異鼠李素對照品(批號為110860-20046)均由中國藥品生物制品檢定所提供;磷酸(廣州化學試劑廠,批號為20071003)。SD 大鼠[♂,250~280 g,南方醫科大學實驗動物中心,許可證號SCXK(粵)2006-0015]。
1.2 方法
1.2.1 銀杏酮酯磷脂復合物的制備
按1∶1質量比稱取銀杏酮酯與大豆磷脂適量,溶于四氫呋喃中,反應溫度為30℃,反應物質(銀杏酮酯)的濃度為20 g/L,反應6 h后,40℃真空干燥去掉反應溶劑,用二氯甲烷洗滌未反應的原料,40℃真空干燥去掉二氯甲烷后,即得。
1.2.2 Hepes-Tris緩沖液的制備
精密稱取Hepes 3.0 g,加入400 mL蒸餾水,攪拌使之完全溶解,通入混合氣體(95%O2∶5%CO2)10 min后,加入 0.9 mL KCl(3 mol/L),0.9 mL CaCl2(1 mol/L),0.4 mL MgSO4(1 mol/L)和4.09 g NaCl,充分攪拌完全溶解后,用Tris液(1 mol/L)調節pH至7.4,加入 2.5 mL 葡萄糖(1 mol/L),加入蒸餾水定容至 500 mL。
1.2.3 藥物溶液的制備
由同一名口腔醫生采用精度為0.01 mm的電子數顯游標卡尺(深圳佳林)測量第一前磨牙的全牙長、冠長、根長、冠近遠中徑、冠唇(頰)舌徑、頸近遠中徑和頸唇(頰)舌徑,每個數據測量3次,取平均值。肉眼觀察并記錄各牙根數目,其中雙根型包括根分叉位于根上、根中、根尖1/3處,且有獨立根尖孔。
GBE50原料溶液:稱取0.05 g GBE50溶于1 mL乙醇中,再取 0.5 mL用 Hepes-tris緩沖液定容至 50 mL作為供試液,GBE50的最終質量濃度為0.5 g/L。
GBE50磷脂復合物溶液:稱取0.103 g GBE50磷脂復合物(相當于 GBE50 0.05 g)溶于 1 mL乙醇中,再取 0.5 mL用 Hepes-tris緩沖液定容至50 mL作為供試液,GBE50的最終質量濃度為 0.5 g/L。
杏靈顆粒溶液:稱取0.625 g杏靈顆粒(1 g∶40 mg GBE50,相當GBE50 0.025 g)溶于0.5 mL乙醇,用 Hepes-tris緩沖液定容至50 mL作為供試液,GBE50的最終質量濃度為0.5 g/L。
1.2.4 體外擴散池法
選取SD大鼠禁食16~19 h,3%戊巴比妥鈉(32 mg/kg)腹腔注射麻醉,沿腹中線將腹部切開2.5 cm左右,胃下5 cm處為空腸(約10 cm),在空腸前端插入硅膠管(內徑2 mm)結扎,空腸末端剪開一小口后,輕緩地用0.9%氯化鈉注射液沖洗干凈,分離空腸置HEPES緩沖液中,冰浴培養5 min,剪取3~4 cm長的腸段,迅速分離筋膜層,將腸黏膜固定于擴散池上。黏膜側加入37.5℃試驗用藥物7 mL,漿膜側加入等體積同溫度的HEPES緩沖液;在混合氣體(95%O2∶5%CO2)的作用及37.5℃水浴保溫下,分別于 15,30,45,60,75,90,120 min 時在接收側取樣 0.5 mL,同時補充0.5 mL緩沖液。
1.2.5 銀杏酮酯中黃酮醇苷的測定
標準曲線繪制:分別取在五氧化二磷減壓干燥器中放置過夜的對照品槲皮素、山柰素、異鼠李素對照品適量,用甲醇溶解配制不同質量濃度,槲皮素質量濃度分別為 12.5,25,50,100,200 ng/mL,山柰素質量濃度分別為 8.75,17.5,35,70,140 ng/mL,異鼠李素質量濃度分別為 8.75,17.5,35,70,140 ng/mL。分別繪制標準曲線(X軸為質量濃度,g/L,Y軸為峰面積),得回歸方程,槲皮素為 Y=117.09X +324.94(R2=0.998 3);山柰素為Y=52.528 X +48.783(R2=0.999 9);異 鼠 李 素 為 Y=49.93 X +34.5(R2=0.999 5)。
空白干擾試驗:取不含任何藥液的透過液按2.5.2項下方法處理,由于透過液在368 nm波長處無吸收,因此不會對透過液中黃酮醇苷的測定產生干擾,見圖1。
1.2.6 數據處理
將高效液相色譜法測得的數據用Excel軟件進行處理,根據標準曲線得到的各個時間點的濃度(Ctn),用下列公式計算累計樣體積和加入藥液量,單位為L。根據給藥劑量 D,計算累計透過率:Qtn/D×100%。表觀滲透系數(Papp)是表示藥物經黏膜透過能力的重要指標,其計算公式為:Papp=(dQ/dt)×(1/AC0),其中dQ/dt表示穩態時時間,累計透過量線性回歸所得的斜率,A為有效滲透面積1.78 cm2,C0為加入藥液時初始藥物濃度。
2 結果
2.1 最佳區段腸的選擇
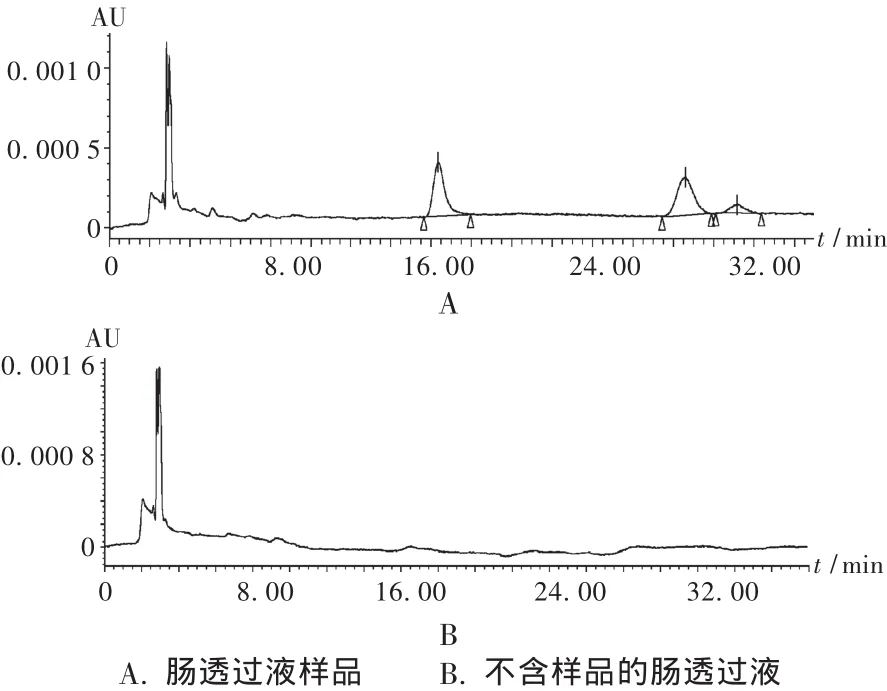
圖1 高效液相色譜圖
分別選擇十二指腸、空腸、回腸、結腸作比較,以各區段腸的累計透過率與時間作圖,詳見圖2,而表觀滲透系數比較見表1。用SPSS 13.0統計軟件對各區段腸間的表觀滲透系數進行組間one-way ANOVA分析,多重比較采用LSD法,各區段腸的表觀滲透系數比較結果,十二指腸的Papp與其他3組相比都有顯著性差異,空腸與回腸和結腸相比也有顯著差異。Papp是評價透過性能的重要指標,說明十二指腸的透過性能最好,空腸次之,但由于藥物在十二指腸的停留時間較短,則選用空腸為最佳區段腸。
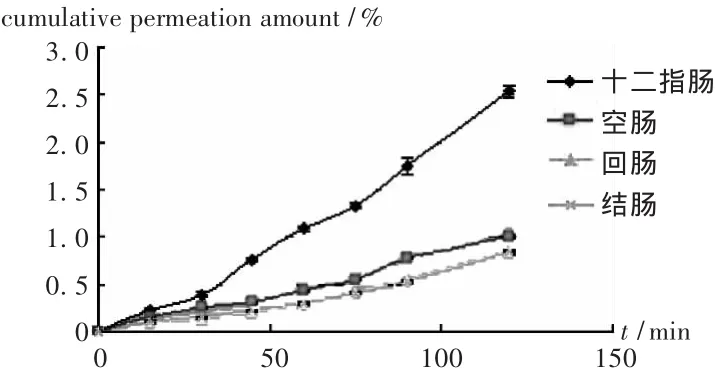
圖2 GBE50體外擴散池法試驗透過圖(n=3,X±s)
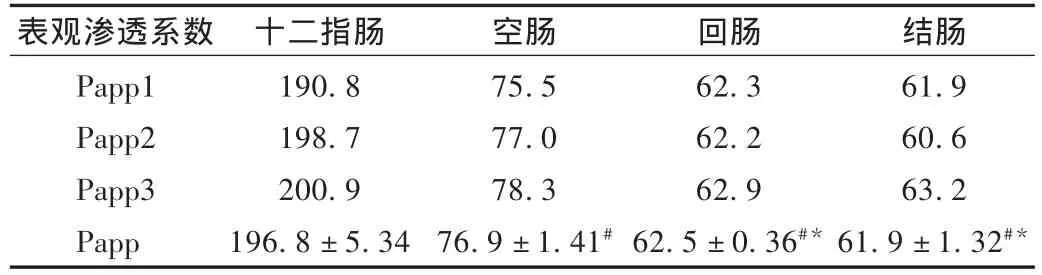
表1 GBE50在各區段腸的表觀滲透系數
2.2 藥物組間比較
分別取藥液銀杏酮酯原料藥、銀杏酮酯磷脂復合物和陽性對照藥(杏靈顆粒)并比較三者在空腸的透過性能,以累計透過率與時間作圖,詳見圖3,表觀滲透系數比較見表2。用SPSS13.0統計軟件對各組間的表觀滲透系數進行組間one-way ANOVA分析,多重比較采用LSD法,各組的表觀滲透系數比較結果,與GBE50原料組比較,GBE50磷脂復合物組與陽性對照組均有顯著差異,且均有提高;陽性對照與GBE50磷脂復合物比較,也有顯著差異,Papp也有提高,透過性能也有所改善。

圖3 GBE50體外擴散池法試驗透過曲線圖(n=3,X±s)

表2 GBE50在空腸的表觀滲透系數
3 討論
體外擴散池法用來評價銀杏酮酯磷脂復合物的透過性能,用高效液相法測定腸黏膜通過的黃酮醇苷的量,該方法靈敏度較高,重現性較好,而且該方法測定黃酮醇苷比較成熟,因此,選擇用高效液相色譜法測定黃酮醇苷的含量作為評價透過性能的指標。
在體外擴散池試驗中要注意控溫和通氣,防止腸變性,氧化,失去正常活性,在選擇溶劑時,用乙醇作為助溶劑能使藥物更好地溶解,但乙醇的濃度不超過1%,以防止破壞腸的活性,且要保證各溶液的乙醇的濃度一致,以減少誤差。
在選擇最佳區段腸時,選取了十二指腸、空腸、回腸、結腸進行透過性能的比較,結果十二指腸較其他區段腸透過性能都好(P<0.01),但由于藥物在十二指腸的停留時間較短,因此選擇此腸段沒有實際意義,而黃酮醇苷在空腸的透過性能僅次于十二指腸,較其他腸段(回腸,結腸)透過性能好(P<0.01),因此最后選擇空腸為最佳評價腸段。
體外擴散池法試驗結果表明,銀杏酮酯磷脂復合物的透過性能較其他兩組都有所改善(P<0.01),可能原因為銀杏酮酯磷脂復合物的脂溶性增加,改善了溶解性能和黏膜透過性能,從而增加了腸透過性能。
至今為止,超過60%的藥物為口服制劑,因此預測藥物經胃腸道黏膜吸收在設計口服給藥劑型非常重要并具有實際價值[3]。Watanabe等[4]通過體外擴散池法試驗對15種水溶性和脂溶性的藥物表觀滲透系數進行測定,并與人體內吸收分數(Fa)比較相關性,結果表明Papp與Fa之間存在良好的相關性。本研究對銀杏酮酯磷脂復合物、銀杏酮酯原料與杏靈顆粒的Papp進行測定,結果相比其他兩組,銀杏酮酯磷脂復合物的Papp有所增加,表明銀杏酮酯制備成磷脂復合物后,有可能提高人體內的吸收度,從而提高生物利用度。
[1]賴 樂,賴春麗,趙建彬,等.銀杏酮酯磷脂復合物的制備與理化性質的研究[J].中藥材,2010,33(10):1 624-1 628.
[2]國家藥典委員會.中華人民共和國藥典(一部)[M].北京:化學工業出版社,2005:220-221.
[3]李國峰,王春霞,晏 媛,等.體外擴散池法評價瑞巴派特經大鼠腸黏膜的透過特性[J].藥學學報,2008,43(3):314-317.
[4]Watanabe E,Takahashi M,Hayashi M.A possibility to predict the absorbability of poorly water-soluble drugs in humans based on rat intestinal permeability assessed by an in vitro chamber method[J].Eur J Pharm Biopharm,2004,58:659-665.

