旋光法研究L-半胱氨酸在食品加工條件下的穩(wěn)定性*
葉麗君,黃雪松
(暨南大學(xué)食品科學(xué)與工程系,廣東廣州,510632)
L-半胱氨酸(L-Cysteine,L-Cys;L-α-氨基-β-巰基丙酸),比旋光度[α]20D=+6.5°(5 mol/L HCl中);L-Cys具有還原性基團(tuán)巰基(—SH),在中性或微堿性水溶液能被空氣氧化成L-胱氨酸(L-Cystine,L-Cys-Cys),酸性溶液較為穩(wěn)定[1]。L-Cys是蛋白質(zhì)、酶等生物活性物質(zhì)的組成成分之一,具有多種生理活性[2-3]。在食品、藥品中有抗氧化和防止非酶褐變作用,常用作抗氧化劑或營養(yǎng)強(qiáng)化劑。由于L-Cys在醫(yī)藥、食品、化妝品等行業(yè)中被廣泛地運(yùn)用,了解L-Cys其加工、貯運(yùn)中穩(wěn)定性或變化規(guī)律,對于發(fā)揮L-Cys的作用和保證有關(guān)產(chǎn)品的質(zhì)量則極為必要。
檢測L-Cys含量的方法主要有電分析化學(xué)法、高效液相色譜法、自動(dòng)分析儀法、化學(xué)滴定法、旋光度法和紫外分光光度法等[4-5]。這些測定方法需要專門儀器,操作繁瑣,難以測定L-Cys在相關(guān)產(chǎn)品、尤其在食品加工條件下的變化過程。本研究根據(jù)多組分旋光物質(zhì)體系的旋光度具有加和性這一特性,測定LCys在常溫下、有氧和無氧溶液、H2O2、NaHSO3存在下和不同溫度下的旋光度變化,探討L-Cys在加工過程中的變化規(guī)律,為加工過程中減少L-Cys的變化提供了理論依據(jù)。
1 材料與方法
1.1 儀器與試劑
WZZ-2B自動(dòng)旋光儀,上海精密科學(xué)儀器有限公司;HH-4恒溫水浴鍋,江蘇金壇市宏華儀器廠。L-半胱氨酸鹽酸鹽(L-Cys·HCl,食品級,含量 >98%),廣東大地食用化工有限公司;L-胱氨酸(優(yōu)級純),上海索萊寶生物科技有限公司;HCl,Na2HPO4,檸檬酸,H2O2,Na2SO3均為分析純,廣州化學(xué)試劑廠。
Mcllvaine緩沖溶液的配制,見參考文獻(xiàn)[6]。
1.2 實(shí)驗(yàn)方法
1.2.1 L-Cys和L-Cys-Cys在不同pH值溶液中比旋光度的測定
稱取5.00 g L-Cys·HCl于具塞試管中,分別加入pH 3.0~8.0的Mcllvaine緩沖溶液,定容至25 mL。以相應(yīng)的pH值緩沖溶液為空白調(diào)零,測定各個(gè)pH值下溶液的旋光度,并計(jì)算各自比旋光度和摩爾旋光度。
稱取2.00 g L-Cys-Cys,用1 mol/L HCl定容至100 mL。取5 mL L-Cys-Cys溶液中,分別加入pH 3.0~8.0的Mcllvaine緩沖溶液,定容至25 mL。以相應(yīng)的pH緩沖溶液為空白調(diào)零,測定各個(gè)pH值下溶液的旋光度,并計(jì)算各自比旋光度和摩爾旋光度。
1.2.2 測定L-Cys在不同pH值下的旋光度
稱取5.00 g L-Cys·HCl于具塞試管中,分別加入pH 3.0~8.0的Mcllvaine緩沖溶液,定容至25 mL。在暴露于空氣的條件下,每隔1 h測定各個(gè)pH值下溶液的旋光度,確定L-Cys最穩(wěn)定時(shí)所對應(yīng)的pH值。
1.2.3 溶液中溶氧對L-Cys旋光度的影響
分別稱取5.00 g L-Cys·HCl于2支具塞試管中,各加入由1.2.2所確定的pH值且經(jīng)過煮沸后冷卻和搖晃5 min以充分溶氧的Mcllvaine緩沖溶液,分別定容至25 mL。在隔絕空氣的條件下,每隔1 h,測定各自旋光度。
1.2.4 配制指定pH值的L-Cys溶液
稱取5.00 g L-Cys·HCl于具塞試管中,加入由1.2.2所確定的pH值的Mcllvaine緩沖溶液,定容至25 mL。
1.2.5 H2O2對L-Cys旋光度的影響
在根據(jù)1.2.4所配制的的L-Cys溶液中加入0.1 mL 30%H2O2后、在隔絕空氣的條件下,立即測定其旋光度,然后每隔5 min測定其旋光度。
1.2.6 NaHSO3對L-Cys旋光度的影響
在根據(jù)1.2.4所配制的的 L-Cys溶液中加入0.10 g NaHSO3,在暴露于空氣的條件下,每隔1 h測定其旋光度。
1.2.7 溫度對L-Cys旋光度的影響
將1.2.4所配制的的L-Cys溶液分別于60℃和100℃的恒溫條件下,每隔15 min測定其旋光度。
1.3 旋光度、反應(yīng)速率常數(shù) k和半衰期 t1/2的計(jì)算[7]
根據(jù)旋光度的加和性,推導(dǎo)L-Cys和L-Cys-Cys兩者的旋光度與各自濃度的計(jì)算公式分別為:
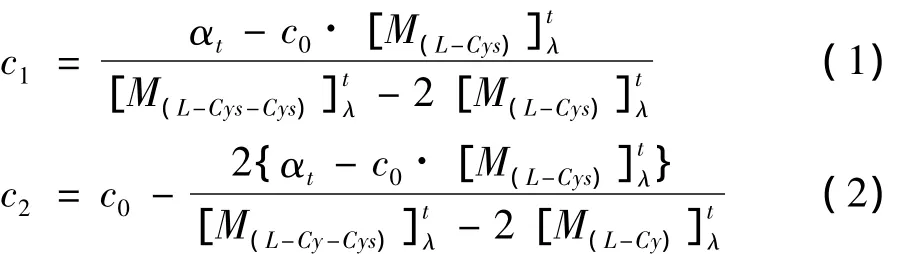
式中c0,c1和 c2分別表示 L-Cys的初始濃度,LCys-Cys和L-Cys-Cys的最終濃度的濃度(mol/L),M摩爾比旋光度(其為比旋光度[α]和摩爾質(zhì)量Mr的乘積)。
以c對t作圖,所得函數(shù)曲線的斜率即為反應(yīng)速率常數(shù) k[mol/(dm3·h)],即:

式中:c是L-Cys的濃度(mo/L);t是反應(yīng)時(shí)間(h);a為所得函數(shù)曲線在縱坐標(biāo)上的截距,為常數(shù);t1/2為半衰期(h)。
2 結(jié)果與討論
2.1 L-Cys和L-Cys-Cys在不同pH值下的比旋光度
L-Cys和L-Cys-Cys在不同pH值下的比旋光度變化結(jié)果分別見圖1。由圖1可知,L-Cys和L-Cys-Cys的比旋光度均隨著pH值升高而降低,且其變化規(guī)律分別符合一次函數(shù):[α]=-0.434(pH)-6.69(R2=0.985)和[α]= -11.73(pH)-192.6(R2=0.942)。t檢驗(yàn)(P=0.01,n=6)表明,這2個(gè)方程可反映 L-Cys和 L-Cys-Cys隨 pH值變化的規(guī)律[8]。因?yàn)長-Cys和L-Cys-Cys是具有酸堿兩性的氨基酸,pH值不同,其電離度、分子構(gòu)象不同,而分子構(gòu)象決定旋光性物質(zhì)的旋光度[9-10],所以pH影響其比旋光度的大小。因此,在研究L-Cys和L-Cys-Cys時(shí),不應(yīng)忽略它們隨pH值而變化的影響。
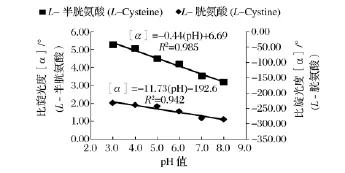
圖1 L-Cys和L-Cys-Cys在不同pH值下的比旋光度變化規(guī)律Fig.1 Specific rotation changes of L-Cys in different pH values
2.2 室溫下L-Cys在不同pH值下的氧化破壞
由圖2可見,pH 3.0~8.0時(shí),隨著時(shí)間的增加,L-Cys的濃度降低;L-Cys的氧化符合零級反應(yīng),即其反應(yīng)速率與反應(yīng)物的濃度無關(guān)[7]。根據(jù)式1和式2式計(jì)算L-Cys在pH 3.0~8.0緩沖溶液中的氧化動(dòng)力學(xué)參數(shù)見表1。L-Cys的氧化屬于非酶化學(xué)反應(yīng),應(yīng)當(dāng)符合質(zhì)量作用定律。以L-Cys濃度c對時(shí)間t作圖,得直線(如圖2)。

圖2 pH 3.0~8.0時(shí)L-Cys的氧化曲線Fig.2 Oxidation curves of L-Cys at pH 3.0~8.0
由表1可知,L-Cys在不同pH值下的氧化符合零級反應(yīng)。其中在pH 3.0時(shí),L-Cys的氧化反應(yīng)速率常數(shù)最小,為 2×10-7mol/(dm3·h),半衰期最長,為2.76×106h;在pH 4.0和pH 8.0時(shí),L-Cys的氧化反應(yīng)速率常數(shù)均達(dá)到最大,為9×10-7mol/(dm3·h),是L-Cys在pH 3.0的緩沖溶液中的氧化反應(yīng)速率常數(shù)的4.5倍,而半衰期分別為6.13×105h和6.23×105h。

表1 常溫下L-Cys在不同pH值的緩沖溶液中的氧化動(dòng)力學(xué)參數(shù)Table 1 Kinetic parameters of oxidation of L-Cys in different pH values at room temperature
2.3 溶液中溶氧對L-Cys氧化破壞的影響
溶液(pH 3.0)是否溶氧對L-Cys氧化的影響如圖3所示。L-Cys在溶液中有氧和無氧時(shí),其氧化破壞均符合零級反應(yīng)。溶液中是否溶氧影響L-Cys濃度,但對L-Cys的氧化速率幾乎無影響,二者氧化速率常數(shù)均為2×10-7mol/(dm3·h),這可能是由于在有氧溶液中,L-Cys一開始便迅速與其中的氧氣反應(yīng)生成L-Cys-Cys,所以在溶液無氧時(shí)較有氧時(shí)的濃度高。同時(shí)有氧溶液中氧氣幾乎被耗盡,其體系近似于無氧溶液體系;而二者均是在隔絕外界氧氣的條件下測定的(見1.2.3),所以L-Cys在有氧和無氧溶液中的氧化速率常數(shù)相等。此外根據(jù)1.2.2和圖2可知,即使L-Cys溶液在暴露于外界空氣時(shí)測定,其氧化速率常數(shù)仍為2×10-7mol/(dm3·h),由此推測L-Cys的氧化可能與溶氧速率有關(guān)。可見,在實(shí)際生產(chǎn)中,在pH 3.0、常溫的體系中存在L-Cys,若避免加快溶氧速率的操作(如避免攪拌、隔氧等措施),體系中的L-Cys可穩(wěn)定存在。

圖3 溶液中有氧無氧時(shí)L-Cys氧化曲線(pH 3.0)Fig.3 Oxidation curves of L-Cys in aerobic and anaerobic solutions(pH 3.0)
2.4 H2O2對L-Cys的氧化破壞
圖4-(a)是pH 3.0、溶液中加入H2O2后L-Cys的氧化情況,即加入H2O2后,L-Cys溶液迅速被氧化成L-Cys-Cys;隨時(shí)間增加、H2O2被逐漸消耗完,LCys濃度降低的速率減小。根據(jù)圖4-(a)的曲線可見,在0~0.42 h時(shí),體系中L-Cys的濃度變化接近一條直線。為便于比較,將0~0.42 h的L-Cys溶液氧化反應(yīng)初期的數(shù)據(jù)按零級反應(yīng)處理(見圖4-(b)),L-Cys的氧化反應(yīng)速率常數(shù)從未添加H2O2時(shí)(見表1)的2 ×10-7mol/(dm3·h)增加至9 ×10-6mol/(dm3·h),反應(yīng)速率是未添加H2O2的45倍,半衰期由2.76×106h減少至6.10×104h。這主要是因?yàn)檫^氧化氫的氧化還原電位Eθ(H2O2/H2O)=+1.77 V,而 O2的氧化還原電位 Eθ(O2/H2O)= +0.816 V,前者比后者大得多[11-12]。所以在本試驗(yàn)中,L-Cys溶液加入H2O2后是隔絕外界空氣進(jìn)行測定的,但是其氧化反應(yīng)速率常數(shù)仍比未添加H2O2、暴露于外界空氣時(shí)的大得多。
2.5 NaHSO3對L-Cys的氧化破壞
圖5是pH 3.0、溶液中存在NaHSO3時(shí)L-Cys的氧化破壞情況。由圖5和 圖2可見,當(dāng)溶液中添加NaHSO3后,L-Cys的氧化反應(yīng)速率常數(shù)是未添時(shí)的10倍,為2×10-6mol/(dm3·h),其半衰期為2.76×105h。可見NaHSO3對L-Cys氧化成L-Cys-Cys的反應(yīng)具有促進(jìn)作用。這主要是由于Eθ(L-Cys-Cys/LCys)=-0.34 V,而在酸性溶液中,HSO3-以H2SO3的形式存在,Eθ(H2SO3/HS2O4-)= -0.08 V,表明L-Cys的還原性大于 H2SO3。根據(jù) Eθ(H2SO3/HS2)- Eθ(L-Cys-Cys/L-Cys)=+0.26 V > +0.2 V,體系中可能發(fā)生反應(yīng):2L-Cys+H2SO3→ L-Cys-Cys+HS2O4-+H2O+H+,從而促使L-Cys氧化成 L-Cys-Cys[11,12]。而在本試驗(yàn)中,加有 NaHSO3的L-Cys溶液在是暴露于外界空氣下測定的,空氣中氧氣加上NaHSO3的雙重氧化作用,使L-Cys的氧化速率常數(shù)增加。NaHSO3和L-Cys在食品生產(chǎn)中都可用作抗氧化劑[13],據(jù)上述結(jié)果與分析可見,NaHSO3會加速L-Cys的氧化,不能作為保護(hù)L-Cys的抗氧化劑使用。

圖4 H2O2存在時(shí)L-Cys氧化破壞曲線(pH 3.0)Fig.4 Oxidation curve of L-Cys in solution containing H2O2(pH 3.0)

圖5 NaHSO3存在時(shí)L-Cys氧化降解曲線(pH 3.0)Fig.5 Oxidation curve of L-Cys in solution containing NaHSO3(pH 3.0)
2.6 溫度對L-Cys的影響
根據(jù)旋光度的加和性可知,L-Cys被氧化生成LCys-Cys,其混合液總旋光度應(yīng)減小。但由圖6可見,pH 3.0、在加熱條件下,L-Cys溶液的總旋光度不隨時(shí)間增加而逐漸減小,而是出現(xiàn)無規(guī)律的變化。這說明在加熱條件下,尤其是加熱至100℃ 時(shí),L-Cys不僅發(fā)生氧化反應(yīng)生成L-Cys-Cys,而可能發(fā)生其他化學(xué)反應(yīng)形成不同的物質(zhì),因而導(dǎo)致其旋光度出現(xiàn)不規(guī)律變化。L-Cys具有熱不穩(wěn)定性,其水溶液加熱至100℃以上會發(fā)生熱降解反應(yīng),根據(jù)溶液pH值不同生成不同物質(zhì),如160℃時(shí),在pH 2.2時(shí)會主要生成噻吩硫醇、三噻環(huán)庚烯等,在pH 5.1和pH 7.1時(shí)則主要生成2-甲基三硫化合物[14-16]。在本實(shí)驗(yàn)條件下,雖然加熱沒超過100℃,但通過L-Cys溶液旋光度變化可知,L-Cys在加熱至60℃時(shí)開始呈現(xiàn)不穩(wěn)定性,不是只氧化生成L-Cys-Cys。當(dāng)加熱至100℃時(shí),溶液總旋光度變化幅度更大,更無規(guī)律,說明L-Cys可能發(fā)生了熱降解,生成了其他復(fù)雜的化合物而非單純的L-Cys-Cys,所生成的其他化合物又有各自的旋光度,導(dǎo)致體系的總旋光度不如預(yù)期般逐漸減小。

圖6 溫度對L-Cys旋光度的影響(pH 3.0)Fig.6 The influence of temperature to optical activity of L-Cys(pH 3.0)
3 結(jié)論
L-Cys和L-Cys-Cys的比旋光度和pH值的關(guān)系呈極顯著正相關(guān),分別符合一次函數(shù):[α]=-0.434(pH)-6.69(R2=0.985)和[α]= -1.73(pH)-192.6(R2=0.942)。在pH值3.0~8.0內(nèi),L-Cys的氧化反應(yīng)符合零級反應(yīng),其氧化反應(yīng)速率常數(shù)在pH 3.0時(shí)最小,在pH 4.0和pH 8.0時(shí)均達(dá)到最大。溶液中是否有氧會影響L-Cys的起始濃度,其濃度在無氧溶液中比在有氧溶液中高,但是不會影響其氧化速率常數(shù)。溶液中存在H2O2時(shí)使L-Cys的氧化速率常數(shù)增大,促進(jìn)其氧化形成L-Cys-Cys。溶液中加入NaHSO3后,在空氣中氧和 NaHSO3的雙重氧化作用下,L-Cys溶液的氧化速率常數(shù)是未加NaHSO3的10倍,因此NaHSO3不能作為保護(hù)L-Cys的抗氧化劑。L-Cys具有熱不穩(wěn)定性,當(dāng)加熱至60℃時(shí)其溶液總旋光度開始出現(xiàn)無規(guī)律變化,其化學(xué)結(jié)構(gòu)被破壞;當(dāng)加熱至100℃時(shí),其溶液總旋光度變化更不規(guī)則,L-Cys可能發(fā)生熱降解產(chǎn)生多種化合物。
[1] 馬貴生.化學(xué)試劑國內(nèi)外標(biāo)準(zhǔn)手冊[M].北京:中國紡織出版社,1994:360-360.
[2] 闞建全.食品化學(xué)(第二版)[M].北京:中國農(nóng)業(yè)大學(xué)出版社,2008:45-53.
[3] 聶劍初,吳國利,張翼伸,等.生物化學(xué)簡明教程(第三版)[M].北京:高等教育出版社,1999:2-13.
[4] 王永華.食品分析[M].北京:中國輕工業(yè)出版社,2010:28-37.
[5] 劉瑞江,左武婷,孫云雷,等.L-半胱氨酸含量測定模型的研究[J].計(jì)算機(jī)與應(yīng)用化學(xué),2011,28(4):429-432.
[6] 杭州大學(xué)化學(xué)系分析化學(xué)教研室編.分析化學(xué)手冊(第二分冊)[M].北京:化學(xué)工業(yè)出版社,1982:27-27.
[7] 印永嘉,奚正楷,張樹永,等.物理化學(xué)(第四版)[M].北京:高等教育出版社,2007:334-339.
[8] 王欽德,楊堅(jiān).食品試驗(yàn)設(shè)計(jì)與統(tǒng)計(jì)分析[M].北京:中國農(nóng)業(yè)大學(xué)出版社,2003:167-168.
[9] 尹玉英,劉春蘊(yùn).有機(jī)化合物分子旋光性的螺旋理論[M].北京:化學(xué)工業(yè)出版社,2000:15-19.
[10] 葉秀林.立體化學(xué)[M].北京:北京大學(xué)出版社,1999:2-7.
[11] Fasman G D.Handbook of Biochemistry and Molecular Biology(3rd Edition)[M].Physical and Chemical Data Volume 1.Cleveland,Ohio:CRC Press,1976:123 -129.
[12] 天津大學(xué)無機(jī)化學(xué)教研室.無機(jī)化學(xué)(第三版)[M].北京:高等教育出版社,2007:107-109.
[13] GB 2760-2011.食品安全國家標(biāo)準(zhǔn)——食品添加劑使用標(biāo)準(zhǔn)[S].
[14] Shu C K,Hagedorn M L,Mookherjee B D,et al.pH Effect on the volatile components in the thermal degradation of cysteine[J].Journal Agriculture& Food Chemistry,1985,33:442-446.
[15] Zhang Y G,Chien M J,Ho CT.Comparison of the volatile compounds obtained from thermal degradation of cysteine and glutathione in water[J].Journal Agriculture&Food Chemistry,1988,36:992-996.
[16] Sohn M G,Ho C T.Ammonia generation during thermal degradation of amino acids[J].Journal Agriculture &Food Chemistry,1995,43(12):3 001-3 003.

