杜仲葉中綠原酸的提取分離及結構鑒定
楊秀芳,汪洋,馬養民
(陜西科技大學教育部輕化工助劑化學與技術重點實驗室,陜西西安 710021)
杜仲(Eucommia ulmoides Olive)為杜仲科杜仲屬植物,僅一屬一種。杜仲在我國研究和利用已有兩千多年的歷史[1]。傳統中醫以皮入藥,但樹皮生長緩慢,種植10年~20年后才能剝皮,每年杜仲皮的增長量僅為0.4 kg左右,緊缺的藥源無法滿足人類的需求[2]。為了保護和擴大藥源,杜仲以葉代皮研究日益活躍,研究發現杜仲葉與皮有著相似的藥理作用和化學成分,杜仲葉在臨床上也具有較好的療效[3]。杜仲屬于落葉喬木,杜仲葉具有廉價、采摘方便、可循環再生等特點。這為杜仲葉的進一步利用奠定了物質基礎,也為緩解緊缺的杜仲資源開辟了途徑[4]。
杜仲葉中富含活性化合物綠原酸,綠原酸又稱3-咖啡酰奎尼酸,是一種廣泛分布于植物體內的苯丙素類物質。經研究發現其具有抗菌、抗炎、保肝、利膽等多種功效,廣泛的應用于醫藥、食品、日用化工等行業,對綠原酸的提取純化為合理開發杜仲資源具有十分重要的意義[5]。本實驗通過對杜仲葉中綠原酸提取工藝和分離純化方法進行了研究,進一步為杜仲綜合利用提供參考。
1 儀器、試劑與材料
1.1 儀器與設備
SENCO電熱恒溫浴鍋:上海申生科技有限公司;RE52CS-1旋轉蒸發器:鄭州南北儀器設備有限公司;Unic-2100型紫外可見光分光光度計:尤尼柯上海儀器有限公司;X-6精密顯微微量熔點測定儀:鞏義市予華儀器有限責任公司;Bruker avanceⅢ-400Hz超導核磁共振儀:瑞士布魯克公司。
1.2 材料與試劑
杜仲葉、皮均采自西北農林科技大學苗圃;綠原酸標準品:中國藥品生物制品檢驗所;D-101大孔吸附樹脂:山東魯抗醫藥股份有限公司;柱層析硅膠:青島海立信精細硅膠化工有限公司;薄層層析硅膠G:青島久隆盛業硅膠干燥劑有限公司;Sephadex LH-20:上海寶曼生物科技有限公司;甲醇、乙酸(色譜純)。
2 方法和結果
2.1 綠原酸水提工藝研究
2.1.1 綠原酸標準曲線的建立
準確稱取綠原酸標準品2.5 mg,甲醇溶解并定容至50 mL,得到綠原酸標準溶液(0.05 g/L)。分別從標準溶液中精確移取 1、2、3、4、5、7 mL 溶液至 10 mL 容量瓶中,甲醇定容,紫外分光光度計于328 nm處測定其吸光度[6]。以綠原酸濃度為橫坐標,吸光度為縱坐標,繪制標準曲線,建立回歸方程。
2.1.2 水提法正交試驗
以水提法作為杜仲葉中綠原酸的提取方法。在單因素實驗的基礎上,選取料液比、提取時間、提取溫度為考察因素進行正交實驗,正交因素設計見表1。
準確稱取陰干粉碎后的杜仲葉2 g,以水為溶劑,按正交水平表的工藝條件提取2次。提取液過濾并減壓蒸干,用甲醇溶解,過濾除去不溶物。將濾液轉移至50 mL容量瓶中,甲醇定容。再從上述容量瓶中精確移取1 mL溶液到100 mL容量瓶中,定容,利用紫外可見光分光光度計測其吸光度,由標準曲線得出綠原酸含量并計算得率。
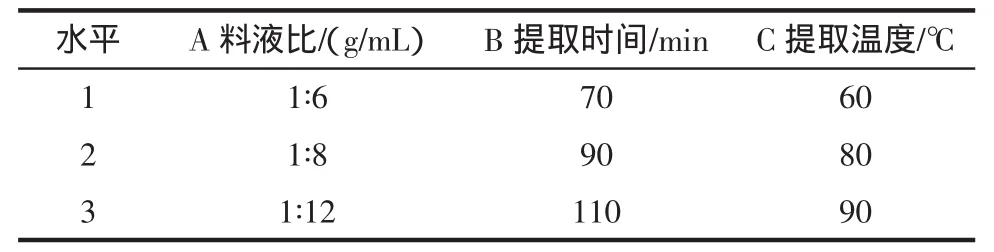
表1 正交因素表Table 1 Factors of orthogonal experiments
2.1.3 實驗結果
依據實驗數據,繪制標準曲線見圖1,建立回歸方程。
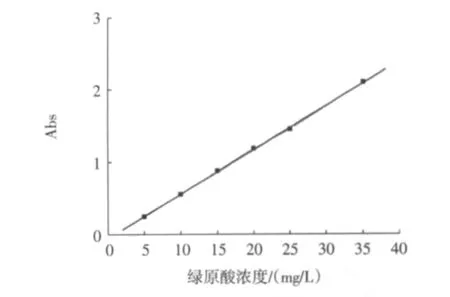
圖1 綠原酸標準曲線Fig.1 Standard curve of chlorogenic acid
由標準曲線可知,綠原酸在5mg/L~35mg/L濃度范圍內線性關系良好,回歸方程為:y=0.061 4x-0.056 39,r=0.999 79,SD=0.015 26。水提法提取綠原酸正交試驗結果見表2。
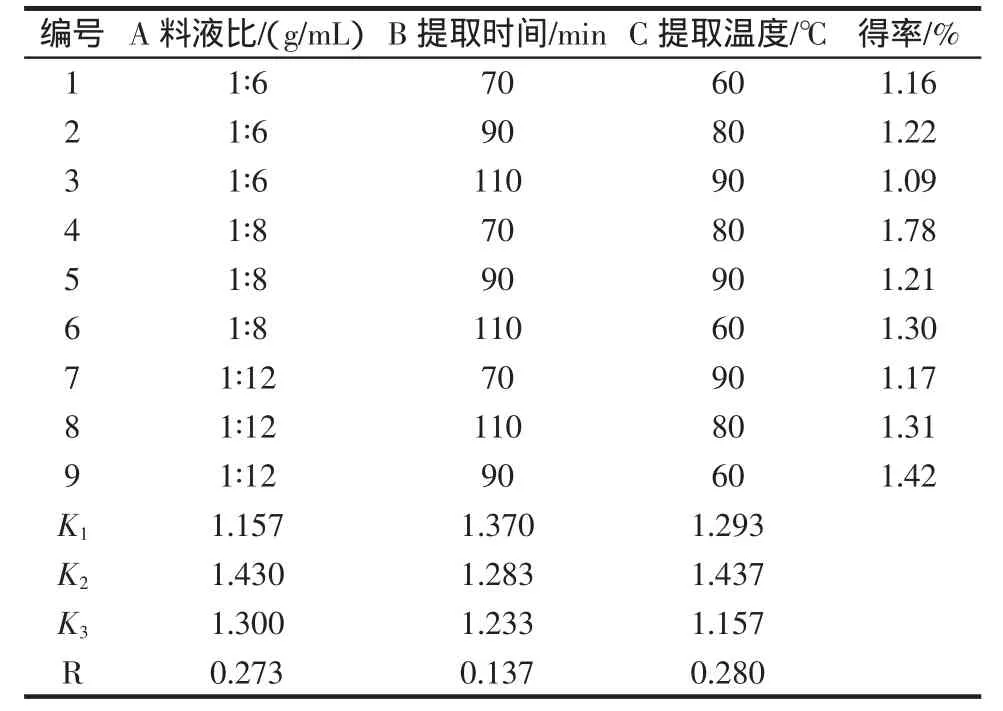
表2 正交試驗結果Table 2 Result of orthogonal experiments
極差分析表明,各因素對綠原酸得率的影響程度為:C>A>B,即提取溫度對綠原酸得率影響最大,其次是料液比,影響最小的因素是提取時間。比較A、B、C等因素的K1、K2和K3數據,3個因素的最優組合是A2B1C2,即綠原酸水提法的最佳工藝條件是:料液比為1∶8,提取時間 70 min,提取溫度 80℃,以熱水作為溶劑提取杜仲葉2次,測得此條件下的綠原酸得率為1.78%。
2.2 綠原酸的純化工藝研究
2.2.1 綠原酸的純化
將杜仲葉陰干并粉碎,按2.1.3確定的最佳工藝進行提取。將提取物減壓濃縮得到粗提物。向粗提物中添加等量的工業酒精,經過多次的攪拌、沉淀,乙醇部分合并,減壓濃縮至無乙醇蒸出。通過此操作除去浸膏中大量的多糖、淀粉、蛋白質等得粗浸膏。利用D-101大孔吸附樹脂純化所得粗浸膏,水-乙醇進行梯度洗脫,收集水相部分,減壓濃縮得到浸膏。利用硅膠柱層析進一步對浸膏進行純化。以乙酸乙酯-甲醇進行梯度洗脫(乙酸乙酯-甲醇體積比分別為 1∶0,20∶1,10∶1,5∶1,10∶3,5∶2,2∶1,5∶3,10∶7,1∶1,0∶1),利用薄層層析,結合標準品對化合物進行比較。經薄層層析后發現5∶2梯度洗脫液含有與綠原酸標準品相同Rf值的斑點。經多次硅膠柱層析后,再以甲醇為洗脫劑,利用Sephadex LH-20凝膠柱層析進行純化。收集、合并與標準品具有相同Rf值斑點的洗脫液,揮干洗脫劑后得到白色固體。
2.2.2 化合物純度檢測與結構鑒定
以不同極性的展開劑將上述白色固體進行薄層層析,顯色后在紫外燈下進行觀察,看是否呈現單一斑點,若始終呈現單一的特征斑點;或利用熔點儀測定熔點,若熔程較短且與文獻值相符,可確定為純品化合物。
同時,利用1H-NMR、13C-NMR等波譜技術進行分析測定,確定化合物的結構。
2.2.3 結果
2.2.3.1 純度的檢測
分離得到的白色固體,易溶于乙醇、丙酮等極性溶劑,難溶于氯仿等低極性溶劑。經檢測其熔點為207℃~208℃,與綠原酸的熔點相同,向白色固體中加入少量綠原酸標準品,其熔點不發生變化。同時薄層色譜呈現出單一斑點,且與標準品有相同的Rf值,由此可初步確定白色固體為綠原酸。
2.2.3.2 結構鑒定
1H-NMR(400 Hz,DMSO-d6)δ:12.45(1H,s,H-7′)為羧基氫的信號峰;9.63(1H,s,H-4),9.19(1H,s,H-3)為苯環上羥基氫的信號峰;7.04(1H,d,J=1.8,H-2),7.00 (1H,dd,J=1.8Hz,8.2Hz,H -5),6.78 (1H,d,J=8.1Hz,H-6)為苯環上未被取代的氫原子信號峰;7.44(1H,d,J=15.9 Hz,H-7),6.17(1H,d,J=15.9 Hz,H-8)為烯基氫的信號峰;5.57,4.98,4.81為與六元環直接相連的羥基氫信號峰;5.08(1H,m,H-3′),3.57(1H,s,H-4′),3.92 (1H,s,H-5′),2.05 (2H,m,H-6′),1.95(2H,m,H-2′)為六元環上的氫原子信號峰。
13C-NMR (100 Hz,DMSO- d6)δ:126.02 (C-1),116.17(C-2),148.79(C-3),145.43(C-4),115.20(C-5),121.84(C-6)為苯環上的六個碳原子的信號峰;146.00(C-7),114.69(C-8)為烯基碳的信號峰;166.17(C-9)為酯基碳的信號峰;73.84(C-1′),37.63(C-2′),68.42(C-3′),71.34(C-4′),70.68(C-5′),36.54(C-6′)為六元環上的碳原子信號峰;175.41(C-7′)為羧基碳的信號峰。
以上核磁數據與文獻[7]中綠原酸的數據基本一致,故鑒定該白色固體為綠原酸。
3 結論
研究表明杜仲葉中綠原酸的含量遠大于其皮中的含量。本文探討了杜仲葉中綠原酸的提取工藝,為開發利用該資源提供了有益的參考。杜仲葉中綠原酸的最佳水提工藝條件為:料液比1∶8,提取時間70 min,提取溫度80℃,以水作為溶劑提取杜仲葉2次,測得此條件下的綠原酸得率為1.78%。粗提物經醇沉工藝除雜后,依次利用D-101大孔吸附樹脂、硅膠柱層析、Sephadex LH-20凝膠柱層析對所得浸膏進行純化,分離得到的化合物經1H-NMR、13C-NMR波譜鑒定和文獻對比為綠原酸。
[1] 艾倫強,李婷婷,何銀生,等.杜仲的應用研究進展[J].亞太傳統醫藥,2010,6(10):163-165
[2] 蘭小艷,張學俊,龔桂珍.杜仲葉中綠原酸的研究進展[J].中國農學通報,2009,25(21):86-89
[3] 盧琪,段家彩,高麗,等.杜仲綠原酸的提取純化及結構鑒定[J].食品科學,2010,31(14):275-279
[4] 張軍民,高振川,張琪,等.杜仲葉及提取物營養價值和藥用成分研究[J].氨基酸和生物資源,2002,24(1):1-2
[5] 張英鋒,張立艷,馬子川,等.植物綠原酸的研究進展[J].中國教育,2011(4):1-2
[6] 向昌國,李文芳,聶琴,等.甘薯莖葉中綠原酸提取方法的研究及含量測定[J].食品科學,2007,28:126-130
[7] 陳立娜,李萍.牽牛子化學成分研究[J].林產化學與工業,2007,27(6):105-108

