辛伐他汀治療慢性阻塞性肺疾病合并代謝綜合征患者的臨床觀察
陳 實,李承紅,葉勝蘭
(江漢大學 附屬醫院呼吸內科,湖北 武漢 430015)
辛伐他汀治療慢性阻塞性肺疾病合并代謝綜合征患者的臨床觀察
陳 實,李承紅*,葉勝蘭
(江漢大學 附屬醫院呼吸內科,湖北 武漢 430015)
目的:探討辛伐他汀對慢性阻塞性肺疾病(COPD)合并代謝綜合征患者的影響及臨床價值。方法:將60例慢性阻塞性肺疾病合并代謝綜合征患者隨機分為辛伐他汀片治療組和對照組,治療組加用辛伐他汀片,治療8周,于治療前、后記錄CAT得分、肺功能及血漿CRP、IL-8、IL-6、SOD的含量。結果:治療后治療組與治療前比較CAT得分、CRP、IL-8、IL-6、SOD及血脂均前明顯降低,差異有統計學意義(P<0.05);治療后治療組比對照組也有明顯下降,差異有統計學意義(P<0.05);對照組治療前后差異無統計學意義;治療前后治療組、對照組及兩組間相比,FEVl、FEVl%差異無統計學意義(P>0.05)。結論:短期辛伐他汀治療能改善COPD合并代謝綜合征患者臨床癥狀及降低CRP及炎癥介質水平,但不能改善肺功能。
慢性阻塞性肺疾病;代謝綜合征;辛伐他汀
慢性阻塞性肺病(Chronic Obstructive Pulmo?nary Disease,COPD)為一種全身性疾病,除了破壞呼吸系統的結構和功能,也同時會影響到全身臟器[1-2]。代謝綜合征(Metabolic Syndrome,MS)通常被認為與肥胖、缺乏運動和遺傳等多種風險因子有關,是一組復雜的代謝紊亂癥候群,中心性肥胖和胰島素抵抗是其重要的致病因素,它也是一種全身性疾病。而COPD患者由于呼吸困難而活動受限,不良的生活方式可能增加了中心性肥胖的發生。另外COPD患者由于全身炎癥反應、組織缺氧和氧化-抗氧化失衡等各種因素導致患MS的風險增高。有研究發現大約有40%的COPD的患者合并有代謝綜合征[3-4]。這兩種疾病都存在炎癥反應的共性。他汀類藥物通常被用來調脂,可以用于代謝綜合征患者,但他汀類藥物除了傳統的降脂作用外,還包括抗炎、抗氧化、抗血栓和血管內皮細胞修復功能等,這些作用同樣可以影響炎性氣道疾病,也有可能用于COPD的治療。本組通過研究辛伐他汀對COPD合并MS的患者臨床癥狀、肺功能和血漿炎癥因子、血脂的影響,探討他汀類藥物在COPD合并MS的患者治療中的作用及其臨床應用價值。
1 資料與方法
1.1 一般資料
選擇江漢大學附屬醫院呼吸科病房2010年5月-2012年5月期間60名COPD合并有代謝綜合征的患者。所有COPD患者的診斷均符合2011年COPD全球策略(Global Initiative for Chronic Ob?structive Lung Disease,GOLD)的診斷標準[5];代謝綜合征符合2005年國際糖尿病聯盟(Interna?tional Diabetes Federation,IDF)制定的標準[6]。需要排除患活動性肺結核、肺纖維化、肺癌、氣胸者、3個月內使用過激素者及女性患者。
1.2 方法
COPD合并MS的每位患者進行身高、體質量、膽固醇、甘油三酯(TG)、高密度脂蛋白(HDL-C)、低密度脂蛋白(LDL-C)、空腹血糖及血壓的測定。患者在采血前空腹12 h,進行血糖、血脂、CRP、IL-8、IL-6、SOD的測定。所有患者都進行肺功能檢查,記錄肺功能參數,并采取標準化的步驟以獲得1 s用力呼氣量(FEV1)、用力肺活量(FVC)、FEV1/FVC和FEV1%。同時記錄患者的年齡、吸煙史,以及詢問是否有高血壓、降脂治療及糖尿病病史。按隨機數字表法隨機將COPD合并MS患者分為兩組:辛伐他汀治療組(治療組)和常規治療組(對照組)各30例,辛伐他汀干預組給予常規治療及辛伐他汀(商品名:舒降之,默沙東公司生產)20 mg,每晚口服,對照組予常規治療(常規使用抗感染、平喘、化痰治療),療程8周,于治療前、后記錄CAT評分、血脂、肺功能及血漿CRP、IL-8、IL-6、SOD及血脂值。
1.3 慢性阻塞性肺疾病評分測試(CAT)
CAT評分[7]是2011年慢性阻塞性肺疾病全球防治策略中提出的COPD分級分期的評價方法。所有入選對象均應用CAT評分表進行評估。由一有經驗的專業醫生用交談法采用CAT中文版對患者的生命質量進行評分。量表內容包括:咳嗽、咳痰、胸悶、爬坡或上一層樓梯的感覺、家務活動、離家外出信心程度、睡眠和精力等8個問題。患者根據自身情況,對每個項目做出相應評分(0~5),CAT分值范圍是0~40。得分為0~10分的患者被評定為COPD“輕微影響”,11~20者為“中等影響”,21~30分者為“嚴重影響”,31~40分者為“非常嚴重影響”。患者CAT評估測試≥2分的差異或改變量即可提示具有臨床意義。
1.4 統計學處理
所有的統計分析采用SPSS13.0統計軟件。計數資料以(均數±標準差)表示,采用t檢驗,計量資料采用卡方檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 兩組一般情況比較
COPD合并MS治療組和對照組在年齡、性別及吸煙狀況等一般臨床資料比較差異無統計學意義,未發現明顯不良反應。
2.2 兩組治療前后CAT評分及肺功能對比
COPD合并MS兩組患者治療前CAT評分表得分差異無統計學意義(P>0.05)。治療后治療組CAT得分較治療前及治療后對照組明顯降低(P<0.05)。而對照組治療前、后比較差異無統計學意義。兩組FEVl及FEVl%組間及組內比較差異無統計學意義(P>0.05),見表1。
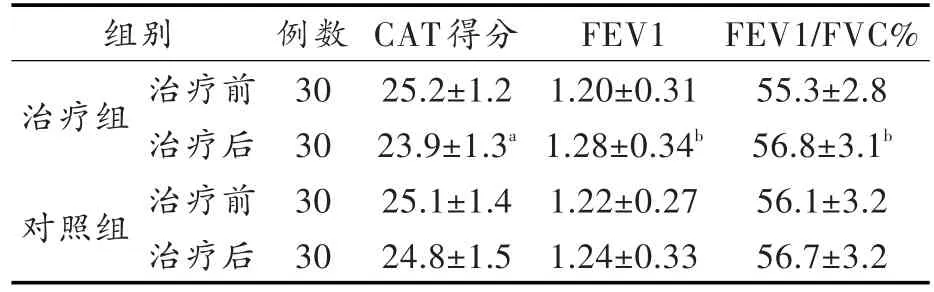
表1 兩組治療前后臨床癥狀評分及肺功能對比
2.3 兩組治療前后TC、TG、HDL-C、LDL-C對比
治療后治療組TC、TG、HDL-C、LDL-C水平較本組治療前均有降低,差異有統計學意義(P<0.05),但對照組治療前后TC、TG、HDL-C、LDL-C水平比較差異無統計學意義(P>0.05),見表2。

表2 兩組治療前后血脂對比
2.4 兩組治療前后CRP、IL-6、IL-8、SOD對比
治療后治療組和對照組CRP、IL-6、IL-8水平較本組治療前均有降低,差異有統計學意義(P<0.05),但治療組與對照組治療后相比CRP、IL-6、IL-8水平明顯降低,差異有統計學意義(P<0.05),見表3。
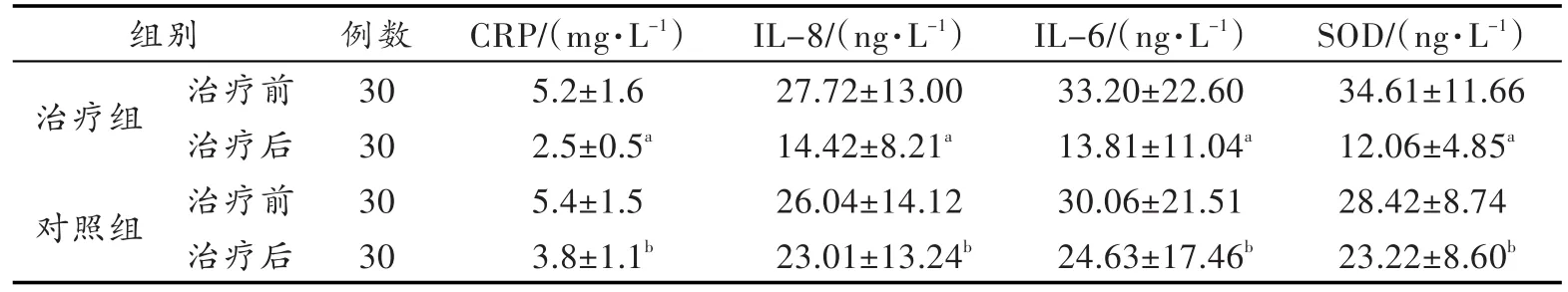
表3 兩組治療前后CRP、IL-6、IL-8、SOD對比
3 討論
3.1 COPD與炎癥的關系
COPD的患者隨著病情的進展,可導致血循環炎癥標志物水平升高,使患者易反復感染,使COPD患者病死率增加。COPD不僅表現為局部慢性炎癥,還表現為系統、全身的炎性反應。COPD可以引起多種炎癥介質的異常,其中CRP、IL-6、IL-8、SOD為反映COPD患者全身性炎癥反應的重要介質。IL-8可以持續介導中性粒細胞的聚集、活化,造成局部炎癥,同時還與中性粒細胞的趨化作用有關。IL-6為重要的致炎細胞因子,可使活化的T細胞和成纖維細胞產生的淋巴因子;可誘導肝細胞表達CRP、肺上皮細胞生成黏蛋白;有研究表明肺功能損害越嚴重,血中IL-6水平越高[8]。血漿IL-6水平是COPD病情監測和療效判斷的較好指標[9]。CRP是一種非特異性的急性期反應蛋白,可以激活補體和加強吞噬細胞的吞噬而起調理作用,CRP可以反應COPD患者急性加重期和穩定期的氣道炎癥程度,且治療效果與CRP下降水平有關[10]。SOD活力高低在一定程度上反映了機體的抗氧化能力。SOD基因多態性可能通過改變SOD活力,導致氧化-抗氧化失衡,參與COPD的發病[11]。本研究也發現COPD患者的CRP、SOD、IL-6、IL-8這些炎癥指標均有明顯增高,與目前國內外研究相符。
3.2 代謝綜合征與炎癥的關系
本觀察中發現代謝綜合征的患者炎癥指標比正常值有升高,反映了代謝綜合征與炎癥反應關系密切。國外有研究者發現糖尿病的患者基礎CRP水平較無糖尿病的患者較高,從而提出“炎癥在糖尿病病因學中發揮作用”的推斷[12]。在胰島素抵抗狀態下,脂肪細胞分泌過量的IL-6和TNF-α可促進肝臟CRP的合成;炎癥本身也可以引起胰島素信號傳導異常,從而引起胰島素抵抗。肥胖是MS的重要臨床表現,而肥胖本身就是一種炎癥狀態-即“肥胖炎”,肥胖者脂肪細胞增生、肥大,過度分泌IL-6、TNF-α等炎癥因子,導致全身CRP水平升高。此外,Mendall等[13]研究中發現CRP與肥胖、高胰島素血癥、血糖、高甘油三酯血癥等各水平有較強的正相關性,與高密度脂蛋白負相關。多項大型臨床研究表明CRP可作為MS的重要預測質變。這些研究與本觀察一致,因此降低炎癥介質水平可能會成為MS的臨床治療新的方法。
3.3 他汀類藥物的作用機制及療效
COPD與MS均為全身性疾病,且都與炎癥介質有關,積極抗炎治療是治療疾病的重點及新方法。他汀類藥物是羥甲基戊二酰輔酶A(HMG-CoA)還原酶抑制劑,通常用于治療與預防高脂血癥和動脈粥樣硬化,目前有研究發現他汀類藥物的藥理性具有多效性,其作用包括抗炎、抗氧化、抗凝血和免疫調節等效應。其中的抗炎效應是治療COPD合并MS患者的新方法。汀類藥物的抗炎機制包括:減少動脈粥樣硬化斑塊內巨噬細胞的數量而發揮抗炎作用;增加一氧化氮合酶的表達,降低內皮素及活性氧中間體的合成;降低炎癥細胞因子、趨化因子、黏附分子的表達,降低CRP水平;抑制巨噬細胞的生長及平滑肌細胞的遷移和增殖等[14-15]。國內外也有一些研究證實。Chello等[16]發現辛伐他汀可降低CRP、TNF、IL-6及其他促炎因子水平可起到抗炎作用。近年來有研究發現在呼吸系統疾病中他汀類藥物可以增強吸入性糖皮質激素抗炎效應,延緩COPD患者肺功能減退[17]。他汀類藥物可以減少COPD患者急性發作的次數[18];Keddissi[19]的研究發現,有超過50%的接受他汀類藥物治療的COPD患者,其肺功能的下降較未服用他汀類藥物有所減緩。而Kaczmarek等[20]研究卻認為辛伐他汀雖能降低總膽固醇、低密度脂蛋白膽固醇水平,卻不能降低重度阻塞性肺通氣功能障礙的COPD患者CRP、IL-6水平。而他汀類藥物本身的降脂、抗炎作用用于代謝綜合征的治療已得到廣泛的認可。有許多研究[21]也表明:建議對如患有心血管疾病、糖尿病、肥胖者以及吸煙等患者,不管他們的膽固醇水平是否超過5.7 mmol/L,都應添加他汀類藥物治療。本觀察發現,經辛伐他汀片治療后COPD合并MS的患者炎癥指標、血脂水平均有下降,治療組患者臨床癥狀有明顯改善,治療有效果。但短期使用他汀類藥物不能改善肺功能。
綜上所述,本研究結果表明,辛伐他汀片可以降低COPD合并MS患者的CAT評分,降低CRP、IL-6、IL-8、SOD及血脂水平。但本研究中發現經辛伐他汀片治療后患者的肺功能無明顯改善,考慮與慢阻肺疾病本身肺功能呈進行性下降有關。辛伐他汀片對COPD合并MS患者的抗炎作用機制以及遠期療效仍需進一步研究。
[1] Agusti A G N,Noguera A,Sauleda J,et al.Systemic ef?fects of chronic obstructive pulmonary disease[J].Eur Respir J,2003,21(2):347-360.
[2] Gan W Q,Man S F P,Senthilselvan A,et al.Associa?tion between chronic obstructive pulmonary disease and systemic inflammation:a systematic review and a me?ta-analysis[J].Thorax,2004,59(7):574-580.
[3] Rogala B,Rymarczyk B,Gluck J,et al.Coexistence of chronic obstructive pulmonary disease-retrospective analysis[J].PneumonolAlergolPol,2007,75:230-235.
[4] Baker E H,Janaway C H,Philips B J,et al.Hypergly?caemia is associated with poor outcomes in patients ad?mitted to hospital with acute exacerbations of chronic obstructive pulmonary disease[J].Thorax,2006,61:284-289.
[5] 柳濤,蔡柏薔.慢性阻塞性肺疾病診斷、處理和預防全球策略(2011年修訂版)介紹[J].中國呼吸與危重監護雜志,2012,11(1):1-12.
[6] International Diabetes Federation.The IDF consensus worldwide definition of the metabolic syndrome[M]. Berlin:IDF,2005.
[7] 柴晶晶,柳濤,蔡柏薔.慢性阻塞性肺疾病評估測試中文版臨床應用意義的評價[J].中華結核和呼吸雜志,2011,34(4):256-258.
[8] Waiter R E,Wilk J B,Larson M G,et al.Systemic ird?lam.mation and COPD:the Framingharn Heart Study[J].Chest,2008,133(1):19-25.
[9] Dentener M A,Creutzberg E C,Schols A M,et al.Sys?temic anti-inflammatory mediators in COPD:increase in soluble interleukin 1 receptor II during treatment of exacerbations[J].Thorax,2001,56(9):721-726.
[10]Weis N,Almdal T.C-reactive protein can be used as a marker of infection in patients with exacerbation of chronic obstructive pulmonary disease[J].Eur J Intern Med,2006,17(2):88-91.
[11]郭鋒,況九龍.超氧化物歧化酶基因多態性及其活力與慢性阻塞性肺疾病的易感性研究[J].中華結核和呼吸雜志,2011,34(6):424-428.
[12]Barzilay J I,Abraham L,Heekbert S R,et al.The rela?tion of markers of inflammation to the development of glucose disorders in the elderly:the cardiovascular health study[J].Diabetes,2001,50:2384-2389.
[13]Mendall M A,Strachan D P,Bufland B K,et al.C-re?active protein:relation to total mortality,cardiovascular mortality and cardiovascular,risk factorsin men[J].Eur Heayt J,2000,21(19):1584-1590.
[14]Chello M,Anselmi A,Spadaccio C,et al.Simvastatin in.creases neutrophil apoptosis and redBcea inflamina?tory reaction after coronary surgery[J].Ann Thorac Surg,2007,83(4):1374-1380.
[15]Morimoto K,Janssen W J,Fessler M B,et al.Lovastatin enhances clearance of apoptotic cells(efferoeytosis)with implications for chronic obstructive pulmonary dis?ease[J].J Immunol,2006,176(12):7657-7665.
[16]Chello M,Anselmi A,Spadaccio C,et al.Simvastatin in.creases neutrophil apoptosis and redBcea inflamina?tory reaction after coronary surgery[J].Ann Thorac Surg,2007,83(4):1374-1380.
[17]Walsh G M.Defective apoptotic cell clearance in asth?ma and COPD:a new drug target for statins?[J].Trends in Pharmacological Sciences,2008,29(1):6-11.
[18]Blamoun A I,Batty G N,DeBari V A,et al.Smtins may reduce episodes of exacerbation and the requirement for intubation in patients with COPD:evidence from a retro?spec.tire cohort study[J].Int J Clin Pract,2008,62(9):1373-1378.
[19]Keddissi J I.The Ilse of statins and lung function in cur?rent and former smokers[J].Chest,2007,132(6):1764-1771.
[20]Kaczmarek P,Stadek K,Skucha W,et al.The influence of simvastatin on selected inflammatory markers in pa? tients with chronic obstructive pulmonary disease[J]. Pol Arch Med Wewn,2010,120(1/2):11-17.
[21]Ong H T.The statin studies:from targetinghyperehole?stemlaemia to targeting thehigh.risk patient[J].QJM,2005,98(8):599-614.
Simvastatin Therapy to Patients with Chronic Obstructive Pulmonary Disease Complicated with Metabolic Syndrome
CHEN Shi,LI Cheng-hong,YE Sheng-lan
(Department of Respiratory Disease,Affiliated Hospital,Jianghan University,Wuhan 430015,Hubei,China)
Objective:To investigate the functional mechanism and impact of simvastatin inter?vention in patients with chronic obstructive pulmonary disease complicated with metabolic syndrome. Methods:60 patients with chronic obstructive pulmonary disease with metabolic syndrome in sta?tionary phase were randomly divided into intervention group and control group.The intervention group was given additional oral simvastatin 8 weeks for a cycle.CAT scores,pulmonary function and the levels of plasma C-reactive protein(CRP),interleukin-6(IL-6),interleukin-8(IL-8),SOD,blood lipids were recorded before and after treatment.Results:The CAT scores and CRP levels,inter?leukin-6(IL-6),interleukin-8(IL-8),SOD,blood lipids decreased in interventiong group after treatment;compared the intervention group before and after treatment,and compared intervention group after treatment to control group after treatment,there was statisticat difference(P<0.05);in control group,compared before treatment to after treatment,there was no statistical difference.In comparison of FEV1,FEVl%,in intervention group and in control group before and after treatment,between the two groups also,there were no statistical differences(P>0.05).Conclusion:Short term simvastatin treatment can improve the clinical symptoms and reduce the CRP and inflammatory mediators levels in patients with COPD,improve the quality of life,reduce the level of lipids.but can not improve lung function.
chronic obstructive pulmonary disease;metabolic syndrome;simvastatin
R563.05
:A
:1673-0143(2013)01-0083-05
(責任編輯:范建鳳)
2012-12-19
武漢市青年科技晨光計劃項目(201150431109)
陳 實(1983—),男,住院醫師,碩士,研究方向:呼吸內科臨床。
*通信作者:李承紅(1960—),女,主任醫師,研究方向:呼吸內科臨床。E-mail:15827636399@163.com

