VI-型慢消化淀粉的制備與鑒定
沙晨希 田耀旗 金征宇
(1.江南大學食品科學與技術國家重點實驗室,江蘇 無錫 214122;2.江南大學食品學院,江蘇 無錫 214122)
慢消化淀粉(SDS)作為一種新型的功能性碳水化合物,受到國內外學者的廣泛關注。相關的研究領域主要集中在普渡大學Whistler碳水化合物研究中心、美國農業部南方地區研究中心、韓國首爾國立大學、華南理工大學、中國農業大學、江南大學等國內外研究機構。目前SDS形成的主流途徑局限于淀粉結晶,此類途徑制備形成的慢消化淀粉多為A-型晶體的原淀粉和B-型晶體的回生淀粉,此類SDS熱穩定性差(55~70℃),產率低(<55%),加工性能差[1]。
直鏈淀粉與乳化劑等客體分子可以形成絡合物,該絡合物具有3種晶體類型:VⅠ-型,VIIa-型和 VIIb-型。VⅠ-型為客體進入淀粉螺旋內部形成的松散型晶體,熱穩定性較VII-型差(95~100℃),但適用于制備SDS;VIIa-型和 VIIb-型為客體分子夾雜于淀粉螺旋之間形成的,熱穩定性較高(105~120℃),但由于具備較完美結晶,通常用于制備抗性淀粉[2,3]。綜上,VⅠ-型淀粉絡合物為制備新型慢消化淀粉提供了重要思路。
本試驗采用高直鏈玉米淀粉為原料,添加一定量的乳化劑(單硬脂酸甘油酯、月桂酸單甘酯、硬脂酰乳酸鈣),分別采用蒸煮糊化法、HCl/KOH沉淀法和酒精堿法制備V-型淀粉-脂質絡合物,采用DSC對產品進行晶型分析,同時測定樣品的絡合率、慢消化淀粉含量、預測血糖指數(pGI),研究制備VⅠ-型慢消化淀粉的最佳制備方法。
1 材料與方法
1.1 材料與儀器
1.1.1 材料與試劑
高直鏈玉米淀粉:國民淀粉工業上海有限公司;
單硬脂酸甘油酯(GMS)、月桂酸單甘酯(GML)、硬脂酰乳酸鈣(CSL):杭州富春食品添加劑有限公司;
豬胰α淀粉酶:50U/mg,西格瑪奧德里奇貿易有限公司。
1.1.2 主要儀器設備
差示掃描量熱儀(DSC):Pyris-1型,美國 Perkin-Elmer公司;
雙束紫外可見分光光度計:TU1900型,北京普析通用儀器責任有限公司;
臺式離心機:TDL-5型,上海安亭科學儀器廠。
1.2 方法
1.2.1 V-型絡合物制備
(1)蒸煮糊化法:準確稱取5g高直鏈玉米淀粉和0.5g乳化劑(單硬脂酸甘油酯、月桂酸單甘酯、硬脂酰乳酸鈣),置于具塞比色管中,均勻混合后加入100mL蒸餾水,攪拌均勻后置于沸水浴中加熱30min,冷卻一下,于105℃下烘烤24h。粉碎,過100目篩,密封備用。
(2)HCl/KOH 沉淀法:以0.01mol/L KOH 為溶劑,分別準確配置10mg/mL的乳化劑溶液50mL、100mg/mL的高直鏈玉米淀粉溶液50mL。將高直鏈玉米淀粉溶液置于磁力攪拌器上保持高速攪拌,緩慢加入已經預熱到90℃的乳化劑溶液。加入完畢后冷卻至60℃,逐滴加入12mL 0.1mol/L的HCl溶液,滴加完畢后體系在60℃下保溫30min,離心(2 000r/min,15min)后去除上清液,用蒸餾水洗滌沉淀物,再次離心,反復3次,去除多余的乳化劑,真空干燥后研磨、過篩,密封備用[4]。
(3)酒精堿法:參考文獻[5]的方法,并稍作改變。準確稱取5g高直鏈玉米淀粉和0.5g乳化劑(單硬脂酸甘油酯、月桂酸單甘酯、硬脂酰乳酸鈣),加入35mL 40%乙醇的溶液,調成一定濃度的淀粉乳后置于35℃恒溫振蕩水浴鍋中保溫,并向上述淀粉乳中逐滴加入KOH(3M)25mL,使最終淀粉乳體系組成比為淀粉∶KOH∶乙醇=1∶0.6∶2.8(m∶m∶V)。上述反應體系充分反應15min,待冷卻至25℃,倒掉上清液,將沉淀分散到50mL 67%乙醇溶液中,用3M的檸檬酸溶液調節體系pH至中性,棄去上清液,用50mL 95%的乙醇重復洗滌2次,蒸餾水洗滌2次,于75℃中干燥,粉碎,研磨,過100目篩,密封備用。
1.2.2 V-型淀粉脂質絡合物晶型分析 采用差示掃描量熱儀對絡合物進行晶型分析。準確稱量絡合物2~3mg于鋁坩堝中,在25℃下平衡4h后,以空皿為參比,以10℃/min的速率升溫,溫度范圍為30~160℃,分別測定起始溫度(To),峰值溫度(Tp),終止溫度(Tc)及焓值(ΔH)的變化情況。
1.2.3 V-型淀粉絡合物絡合率測定 淀粉-脂質絡合物的絡合率以絡合物對脂質的利用率來表示。絡合物中脂質含量的測定采用酸水解法進行測定[6]。淀粉-脂質絡合物的絡合率根據式(1)計算:
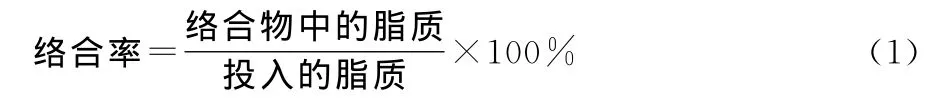
1.2.4 慢消化性評價 采用改進的Englyst法對樣品進行體外消化性評價[1]。慢消化淀粉含量、預測血糖指數(pGI)的計算依據式(2)~(4)進行:
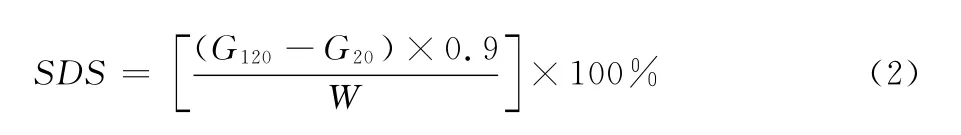
式中:
SDS——慢消化淀粉含量,%;
G20——淀粉被酶水解20min后產生的葡萄糖量,mg;
G120——淀粉被酶水解120min后產生的葡萄糖量,mg;
W—— 淀粉總量,mg。

式中:
pGI——預測血糖指數;
HI——水解指數。
2 結果與分析
2.1 制備方法對V-型淀粉絡合物晶型的影響
DSC可以鑒定淀粉-脂質絡合物的結構形態[7]。通過測定樣品的融化溫度(To,Tp,Tc)和焓變(ΔH),即可鑒定淀粉-脂質絡合物的結構及種類。通常,融化溫度(To,Tp,Tc)越高,且融化溫度范圍(Tc-To)越小,則表明形成淀粉晶體同質性程度越高[8]。由表1可知,以 GMS、GML、CSL為配體制備的樣品的Tp均大于95℃,表明3種乳化劑均可以與高直鏈玉米淀粉形成V-型淀粉-乳化劑絡合物。酒精堿法制備的3種樣品的Tp均為98℃左右,(Tc-To)范圍最大,說明該方法制備的絡合物主要為VⅠ-型絡合物。糊化法制備的3種樣品Tp為100℃左右,(Tc-To)范圍最小,說明該方法制備的絡合物主要為VⅡ-型絡合物。HCl/KOH沉淀法制備的3種樣品Tp均大于110℃,(Tc-To)范圍小于酒精堿法制備的樣品大于糊化法制備的樣品,說明此方法制備的絡合物可能為VⅠ-型絡合物和VⅡ-型絡合物的混合物。由此可知,可以選擇酒精堿法和HCl/KOH沉淀法作為制備VⅠ-型慢消化淀粉的方法。
2.2 制備方法對V型淀粉絡合物絡合率的影響
由圖1可知,采用GMS制備的樣品的絡合率均最高,CSL制備的樣品其次,GML制備的樣品絡合率最低。對比糊化法、酒精堿法和HCl/KOH沉淀法3種方法,HCl/KOH法制備的樣品絡合率最高,酒精堿法其次,糊化法最低。綜上,以GMS為配體,可以選擇酒精堿法和HCl/KOH沉淀法作為VⅠ-型慢消化淀粉制備方法。
2.3 制備方法對V-型淀粉絡合物慢消化淀粉含量的影響
由圖2可知,3種方法中,以GMS為配體制備的樣品中SDS含量均最高,CSL制備的樣品其次,GML制備的樣品SDS含量最低。對比不同方法制備的樣品發現,酒精堿法制備的樣品中SDS含量最高,HCl/KOH沉淀和糊化法制備的樣品中的慢消化淀粉含量均較低。由此可見,選用GMS為配體,酒精堿法為制備VⅠ-型慢消化淀粉的最佳方法。這主要是因為酒精堿法制備VⅠ-型絡合物過程中,堿性環境會使淀粉上羥基上的質子被解離,導致淀粉分子上帶負電而相互排斥,隨著堿濃度的增大,淀粉分子間斥力不斷增強,最終導致雙螺旋區的展開變成單螺旋,結晶結構被打破,結晶序列發生變化。同時,淀粉顆粒周圍由于乙醇的存在,抑制顆粒溶脹,維持了淀粉單螺旋的打開狀態,使乳化劑可以進入淀粉分子螺旋內部。酸堿中和作用后,淀粉分子重新形成螺旋,與乳化劑發生絡合,形成VⅠ-型慢消化淀粉[9]。
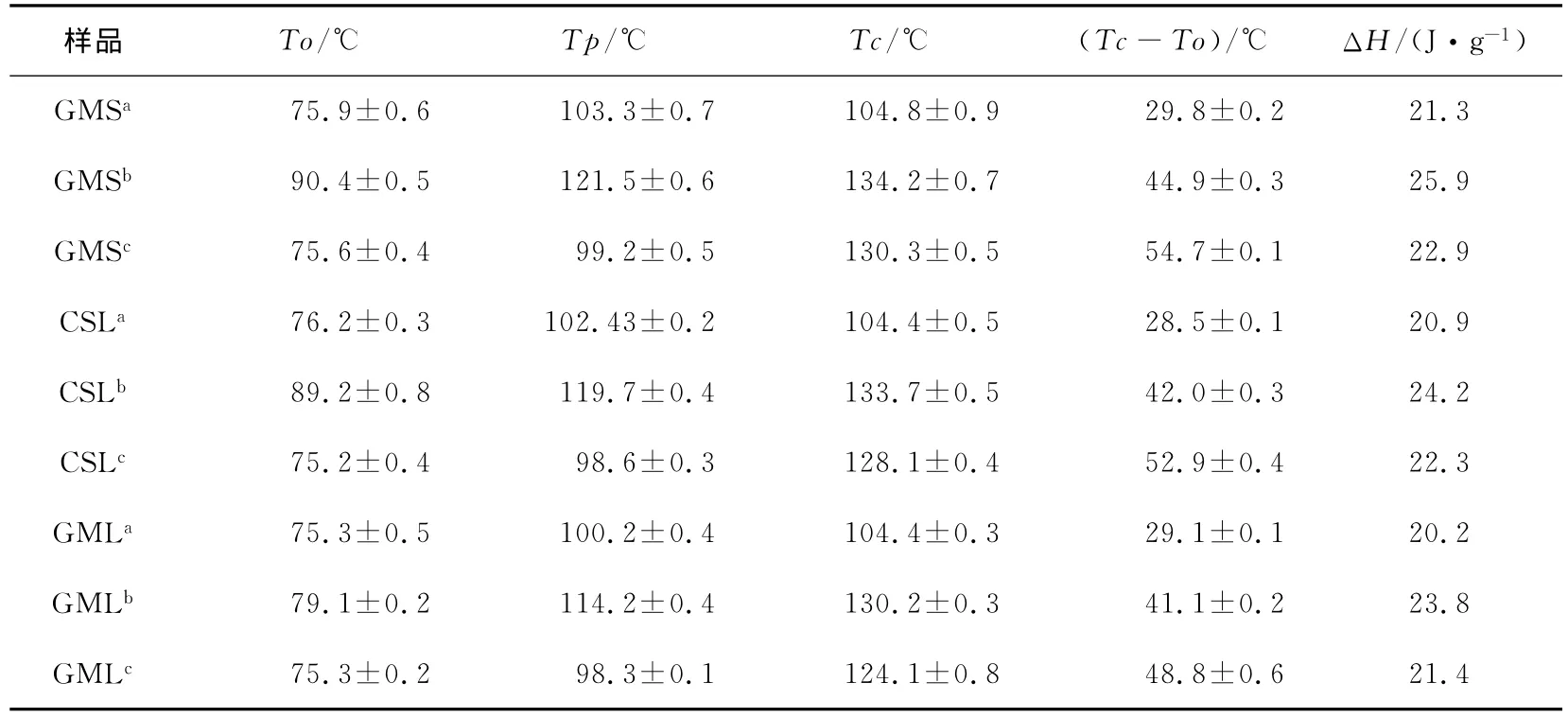
表1 不同方式制備的淀粉-脂質絡合物的熱力學參數?Table 1 Thermodynamic parameter of V-amylose inclusion complexes prepared by different methods
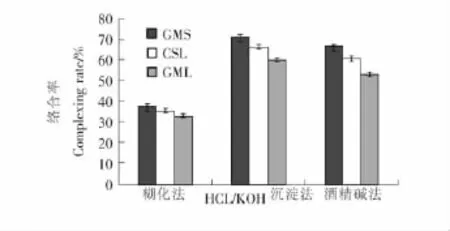
圖1 制備方法對V-型淀粉-脂質絡合物絡合率的影響Figure 1 Complexing rate of V-amylose inclusion complexes prepared by different methods
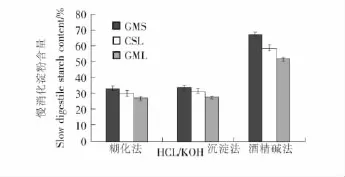
圖2 制備方法對V-型淀粉-脂質絡合物慢消化淀粉含量(SDS%)的影響Figure 2 SDS content of V-amylose inclusion complexes prepared by different methods
2.4 制備方法對V型淀粉絡合物預測血糖指數的影響
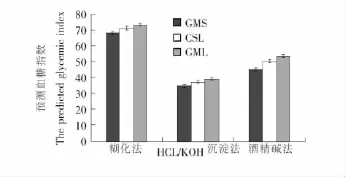
圖3 制備方法對V-型淀粉-脂質絡合物預測血糖指數的影響Figure 3 Predicted glycemic index of V-amylose inclusion complexes prepared by different methods
由圖3可見,3種方法中,以GMS為配體制備的樣品pGI值均最低,CSL制備的樣品pGI值次之,GML制備的樣品pGI值最高,這與圖1和圖2中的結果相對應。對比不同方法制備的樣品發現,HCl/KOH沉淀法制備的樣品pGI值最低,為35~39;糊化法制備的樣品pGI值最高,為68~73;酒精堿法制備的樣品pGI值為45~53。由此可見,除蒸煮糊化法外,酒精堿法和HCl/KOH兩種方法制備的絡合物均屬于低GI值健康食品范疇[10]。
3 結論
以GMS為配體,酒精堿法為制備VⅠ-型慢消化淀粉的最佳方法。DSC分析結果顯示,該方法制備的樣品熱分解溫度 (Tp)為99.2℃,(Tc-To)范圍最寬(54.7±0.1)℃,產物絡合率達到66.7%,SDS最高含量達到67.4%,預測血糖指數pGI=45<55,屬于低GI食品范疇[10]。
1 Zhang Lulu,Hu Xiuting,Xu Xueming,et al.Slowly digestible starch prepared from rice starches by temperature-cycled retrogradation[J].Carbohydrate Polymers,2011,84(3):970~974.
2 Putseys J A,Lamberts L,Delcour J A.Amylose-inclusion complexes:Formation,identity and physico-chemical properties[J].Journal of Cereal Science,2010,51(3):238~247.
3 黃志強,唐健,白永亮,等.抗性淀粉及其防治肥胖癥的研究進展[J].食品與機械,2012,28(4):250~253.
4 林若慧,柴向華,吳克剛,等.硬脂酸-直鏈淀粉復合物的制備工藝的研究[J].食品科技,2011(4):207~210.
5 Chen J,Jane J.Preparation of granular cold-water-soluble star-ches prepared by alcoholic-alkaline treatments[J].Cereal Chemistry,1994,71(6):618~622.
6 中華人民共和國衛生部.GB 5009.3——2003食品中脂肪的測定[S].北京:中國標準出版社,2003.
7 Tian Yaoqi,Li Yin,Frank A,et al.Influence ofβ-cyclodextrin on the short-term retrogradation of rice starch[J].Food Chemistry,2009,116(1):54~58.
8 田耀旗.淀粉回生及其控制研究[D].無錫:江南大學,2011.
9 秦海麗,顧正彪.酒精堿法制備顆粒狀冷水可溶淀粉的研究進展[J].糧食與飼料工業,2005(1):18~19.
10 楊月欣.我國常見食物的血糖生成指數及其健康意義[C].食物血糖生成指數與人體健康研討會.北京:[出版者不詳],2002.

