LC-MS/MS法測定比格犬血漿中的阿那曲唑
陳 真趙瀛蘭晏菊芳
(1.四川大學生物治療國家重點實驗室,四川 成都 610041;2.四川海思科制藥有限公司,四川 成都 611130)
LC-MS/MS法測定比格犬血漿中的阿那曲唑
陳 真1,2,趙瀛蘭1,晏菊芳2
(1.四川大學生物治療國家重點實驗室,四川 成都 610041;2.四川海思科制藥有限公司,四川 成都 611130)
用高效液相色譜-串聯質譜法(LC-MS/MS)測定比格犬血漿中阿那曲唑的濃度。以苯磺酸氨氯地平為內標,加入50μL血漿,用甲基叔丁基醚萃取后取上清液以氮氣吹干,用50%甲醇水溶液復溶,進樣5μL,在電噴霧離子源下進行正離子檢測。色譜柱為Agilent XDB C18(50mm×2.1mm×3.5μm),流動相為0.1%甲酸水-0.1%甲酸乙腈(60∶40)。阿那曲唑和內標的質荷比(m/z)分別為294.4和409,阿那曲唑和內標生成的主要碎片離子的質荷比(m/z)分別為255.3和238。阿那曲唑在0.5~500ng·mL-1內線性良好,檢出限為0.5ng·mL-1,提取回收率均大于80%,日內、日間準確度為101%~104%,日內、日間精密度分別小于7.04%和8.69%,已成功檢測比格犬血漿中阿那曲唑的血藥濃度。所用方法穩定、靈敏度好、分析時間短、提取回收率高,適用于比格犬血漿中阿那曲唑的血藥濃度測定。
阿那曲唑;液質聯用;血藥濃度;液液萃取
0 引言
阿那曲唑是一種強效、高選擇性的非甾體類芳香化酶抑制劑,臨床上廣泛應用于絕經后婦女晚期乳腺癌的治療。絕經后婦女雌激素主要由外周組織中腎上腺雄激素經芳香酶作用轉化而來,芳香酶是一種CYP45O復合酶,可氧化脫去C19類固醇(雄烯二酮和睪酮)的19-甲基,使A環芳香化,從而轉變成C19雌激素(雌酮和雌二醇)。絕大多數乳腺癌病人體內雌激素受體呈陽性,腫瘤在雌激素刺激下生
長。阿那曲唑具有高度選擇性,能有效抑制此酶的活性,充分阻斷絕經后婦女內源性雌激素的合成,降低體循環內雌激素水平,有效阻滯腫瘤生長,甚至導致癌細胞死亡[1]。由于該藥口服劑量小,血漿中藥物濃度很低且干擾物質多,所以對其血藥濃度分析方法的檢測靈敏度和選擇性要求較高。文獻報道的有關阿那曲唑的血藥濃度檢測方法有HPLC-RIA法[2]、氣相色譜-電子捕獲法[3]和高效液相色譜串聯質譜法[4-5],皆為以人血漿或組織為基質建立的分析方法,且基質用量大,不適用于比格犬藥代動力學實驗血漿樣品的高通量分析。本研究建立了快速、靈敏、特異的LC-MS/MS法,用于測定比格犬血漿中的阿那曲唑,達到“化學藥物非臨床藥代動力學研究技術指導原則”中對于生物樣品分析方法的要求,為研究該藥在比格犬體內的藥代動力學特點提供可靠的分析方法。
1 實驗部分
1.1 儀器、試藥與動物
LC-20AD高效液相色譜儀(日本島津);API3200三重四極桿質譜儀(美國AB SCIEX);5804R低溫高速離心機(德國艾本德);XS105分析天平(梅特勒托利多);D11931純水儀(美國熱電);MTN-2800W氮吹儀(天津奧特賽恩斯)。瑞寧德阿那曲唑片(阿斯利康制藥有限公司,批號:WB0130,每片含1mg阿那曲唑);阿那曲唑對照品(上海宇亨醫藥科技,批號:F0H034,純度99.9%,USP);內標苯磺酸氨氯地平(中國食品藥品檢定研究院,批號:100825-200501);乙腈、甲醇、甲酸為色譜純;水為超純水;甲基叔丁基醚為分析純;空白比格犬血漿為肝素鈉抗凝。雄性比格犬(四川省醫學科學院實驗動物研究所,合格證號:SCXK(Chuan)2006-024)6只,體重5~8kg。
1.2 方法與結果
(1)溶液的配制。精密稱取10mg阿那曲唑,加入10mL甲醇,配成1mg·mL-1的貯備液。臨用時以甲醇將貯備液稀釋至以下濃度:5,10,50,100,200,500,1000,2000,5000ng·mL-1,即為所需標準品溶液。精密稱取10mg苯磺酸氨氯地平,加入10mL甲醇,配成1mg·mL-1的內標貯備液,精密吸取300μL 1mg·mL-1內標貯備液,以甲醇定容至10mL,配成30μg·mL-1的內標中間溶液,再吸取1mL 30μg·mL-1中間溶液,加入9mL甲醇,即為3μg·mL-1的內標溶液。標準儲備液及內標溶液均置4℃下保存。
(2)色譜條件。采用Agilent Zorbax,XDB C18色譜柱(50mm×2.1mm×3.5μm),流動相為0.1%甲酸水-0.1%甲酸乙腈(60∶40,v/v),流速0.4 mL·min-1,柱溫35℃,進樣量5 μL。采用電噴霧離子源,以多反應監測(MRM)模式進行正離子檢測,阿那曲唑m/z294.4→225.3,去簇電壓(DP)45V,射入電壓(EP)5V,碰撞能量(CE)29 V,碰撞室出口電壓(CXP)5 V;內標m/z409→238,去簇電壓(DP)30V,射入電壓(EP)3.1V,碰撞能量(CE)23V,碰撞室出口電壓(CXP)4V,阿那曲唑的出峰時間約1.1 min,內標的出峰時間約0.8min,色譜運行時間3min。
(3)血漿樣品前處理。吸取50 μL空白血漿或樣本至1.5mL離心管中,加入5μL“(1)”項標準品溶液(標準曲線樣品)或甲醇(待測血樣),加入5 μL 3 μg·mL-1的內標溶液,充分混勻,再加入500μL甲基叔丁基醚,漩渦混勻2min,于4℃、2250g·min-1離心10 min,吸取上清液400 μL,氮氣吹干,殘留物用100μL 50%甲醇復溶,于4℃、2250g·min-1離心10min后,取5μL上清液進樣。
(4)方法專屬性。分別取6只比格犬的空白血漿,不加內標溶液(以等體積甲醇補足),其余按“(3)”項方法處理后進樣檢測;取對照品溶液按“(3)”項方法處理,阿那曲唑和內標的保留時間約為1.1min、0.8min;取給藥后2h收集的血漿樣品同法操作。結果表明,樣品中內源性物質不干擾阿那曲唑和內標的測定。色譜圖見圖1。
(5)標準曲線、線性范圍及檢出限。取50μL空白血漿,加5 μL“(1)”項標準品溶液,分別配成相當于含阿那曲唑0.5,1,5,10,20,50,100,200,500ng·mL-1的血漿樣品。按“(3)”項方法處理,進樣5 μL,記錄色譜圖。以阿那曲唑的濃度為橫坐標、阿那曲唑與內標的峰面積比值為縱坐標繪制標準曲線,用加權(W=1/x2)最小二乘法進行回歸運算,得到回歸方程:Y=0.040 8X+0.0041(r=0.998 1)。阿那曲唑的線性范圍為0.5~500 ng·mL-1,檢出限為0.5ng·mL-1。
(6)基質效應。取50μL空白血漿,按“(3)”項操作制備18份提取后的空白樣品,取400 μL上清液,分別加入低、中、高濃度質控溶液(15,400,4 000 ng·mL-1)和內標溶液各5 μL,氮氣吹干后,以50%甲醇復溶至100μL,進樣并記錄色譜峰面積。與相應同濃度的6份標準溶液結果比較,以二者的峰面積比值計算其基質效應。低、中、高濃度及內標的基質效應分別為89.2%±3.18%、92.3%±5.79%、90.8%±3.93%、91.6%± 4.17%,比值均在85%~115%,RSD<15%,基質效應對檢測結果影響較小。
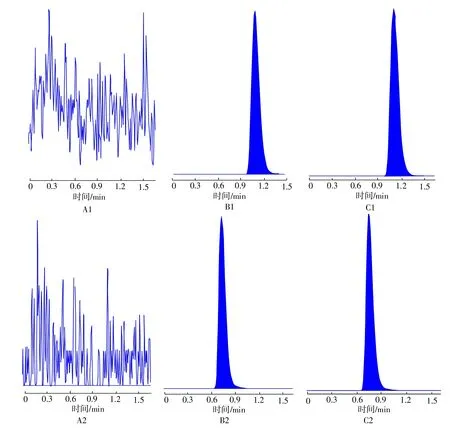
圖1 空白血漿(A)、空白血漿+對照品+內標(B)、血樣(C)溶液中阿那曲唑(1)及內標(2)的專屬性色譜圖
(7)提取回收率。取50μL空白血漿,分別加入低、中、高濃度質控溶液和內標溶液各5 μL,得到1.5,40,400ng·mL-1的質控樣本,每個濃度質控樣本制備6份,按“(3)”項處理,進樣并記錄色譜峰面積。與“(6)”項相應同濃度的6份空白血漿提取后加入質控溶液的樣本相比較,以二者的峰面積比值計算提取回收率。結果低、中、高濃度及內標的提取回收率分別為83.0%±2.38%、81.9%±4.96%、83.7%±4.23%、85.4%±4.52%,RSD<15%。將18份低、中、高濃度質控樣品的阿那曲唑/內標峰面積比代入當日的工作標準曲線計算,得低、中、高濃度的方法回收率分別為104%±6.78%、101%±7.14%、102%±2.25%。
(8)精密度和準確度。取50μL空白血漿,按“(3)”項方法配制低、中、高濃度的質控樣品,每個濃度質控樣本各6份,連續測定3 d,計算日內及日間精密度和準確度,見表1。
(9)穩定性試驗。標準品儲備液在2~8℃避光條件下穩定,至少可儲存35d。阿那曲唑低、中、高濃度樣品在室溫下放置6.5 h,提取后在4℃放置4 d,反復凍融3個循環,在-80℃保存34d的穩定性皆較好,變化均<15%,該化合物及分析方法的穩定性較好,能滿足實驗要求。
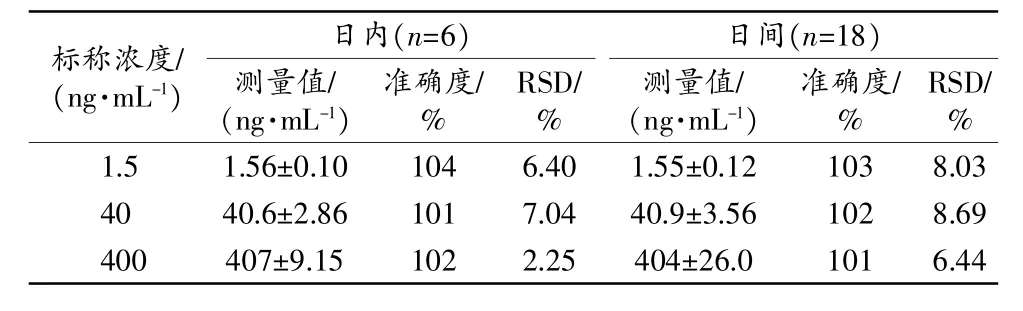
表1 LC-MS/MS測定比格犬血漿中阿那曲唑的準確度和精密度
(10)藥動學參數。6只雄性成年比格犬,禁食過夜,經口給藥,給藥劑量為1mg/只,于給藥前(0h)和給藥后1,2,4,8,12,24h由前肢頭靜脈取血,每次取血2mL,置肝素鈉真空采血管中,離心后分離血漿,于-80℃保存。待測血漿樣品按“(3)”項方法進行前處理,以當天工作標準曲線進行計算,同時分析低、中、高濃度的質控樣品(各濃度不少于兩個),記錄樣本的阿那曲唑/內標峰面積比,根據回歸方程計算每個血漿樣本的藥物濃度。比格犬體內阿那曲唑的血藥濃度-時間曲線見圖2。以DAS(V 2.0)軟件分析藥代動力學參數,得到 Cmax為37.27±8.21μg·L-1、AUC0-t為454.19±55.21 μg·h·L-1、 MRT0-t為 8.42±0.58為 8.58±1.95 h、Tmax為 1.17±0.41 h、CLz/F為1.91±0.32 L·h-1、Vz/F為23.15± 3.30L。
Determination of anastrozole in beagle dog plasma by LC-MS/MS
CHEN Zhen1,2,ZHAO Ying-lan1,YAN Ju-fang2
(1.State Key Laboratory of Biotherapy,Sichuan University,Chengdu 610041,China;2.Sichuan Haisco Pharmaceutical CO.,Ltd,Chengdu 611130,China)
The HPLC-tandem mass spectrometry method(LC-MS/MS)was developed for the determination of anastrozole concentration in beagle dog plasma.50μL plasma samples were mixed with MTBE followed by extraction,the supernatant was dried under N2and re-dissolved by 50% methanol,and 5 μL of which was injected onto LC-MS/MS.The analysis was carried out under the positive mode of electronic-spray ionization(ESI).Chromatographic column was Agilent XDB C18(50mm×2.1mm×3.5μm),mobile phase was 0.1%formic acid in water-0.1%formic acid in acetonitrile(60∶40).The mass-to-charge ratio(m/z)of anastrozole and internal standard were 294.4-225.3 and 409-238, respectively.The linear range ofanastrozole was within the concentration of 0.5-500 ng·mL-1.The LOD was 0.5 ng·mL-1.The extraction recoveries were all higher than 80%.The intra-and inter-day accuracy were 101%-104%,the intra-and inter-day precisions(RSD)were less than 7.04%and 8.69%,respectively.The anastrozole concentration in beagle dog plasma was detected successfully.The method was stable,sensitive,speedy and highly recovered.It was suitable for determining the anastrozole concentration in beagle dog plasma.
anastrozole;LC-MS/MS;plasma concentration;LLE
R917;S829.2;R331.1;O657.7+2
:A
:1674-5124(2014)01-0059-03
10.11857/j.issn.1674-5124.2014.01.016
2013-02-16;
:2013-04-07
陳 真(1981-),女,四川成都市人,助理工程師,碩士,研究方向為制藥工程。

