γ-氨基丁酸受體同源模建及與黃酮類化合物的分子對接
巨修練,錢 程
1.武漢工程大學化工與制藥學院,湖北 武漢 430074;2.綠色化工過程教育部重點實驗室(武漢工程大學),湖北 武漢 430074
黃酮類化合物(如圖1)具有突出的抗焦慮效果,且不引起肌肉松弛、健忘等副作用.這些重大發現推動了對選擇抗焦慮,親和力高的配體研究.6-溴黃酮相對于黃酮對GABAA受體的苯二氮唑結合位點的親和力增加了近10倍[1].6-溴黃酮和GABAA的競爭結合參數是1.6~2.0(通過加入或不加入GABA時測量而得的6-溴黃酮和苯二氮唑結合位點的作用值比),與地西泮很類似,具有完全激動劑的藥理學特征[2].當引入硝基時甚至會得到更有效的配體,6,3’ -二硝基黃酮與苯二氮唑位點結合力更強,其Ki值取值范圍為17~50 nmol/L,它具有極有效的抗焦慮和肌肉松弛作用.6-溴-3’-硝基黃酮相對于雙硝基類似物,對GABAA受體苯二氮唑結合位點的親和力稍有增加,對苯二氮唑位點同樣具有選擇性[3].這類化合物的抗焦慮作用盡管比6,3’-二硝基黃酮稍差,但仍比地西泮的抗焦慮作用強.由于黃酮類化合物藥理學選擇性及其自身對GABAA受體苯二氮唑結合位點的活性低,使得對其衍生物的研究有了一個很大的飛躍,同時也對GABAA受體苯二氮唑結合位點選擇性有了新的認識,促進了黃酮類化合物的發展.
本研究采用海兔乙酰膽堿結合蛋白(2XYS)作為模板,對人α1β2γ2 GABAA受體進行模建并能量優化,利用分子對接進一步指導研究.此外,從對接結果進行分析,發現黃酮類化合物的3’位對活性影響很大,且增多取代基團也會提高活性,進而為更好的設計黃酮類化合物提供了理論依據.
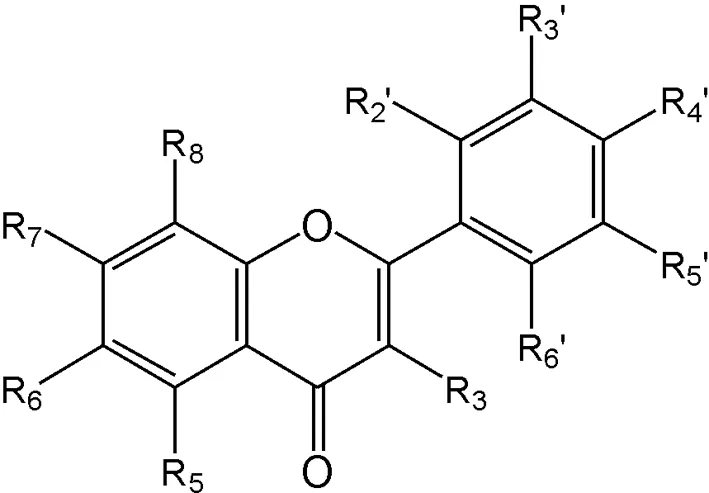
圖1 黃酮類化合物的基本結構Fig.1 Structure of flavonoid
1 實驗部分
本研究的所有計算實驗都是通過SYBYL-X1.2軟件(Tripos Inc.)完成,若無特別介紹,參數均采用缺省值.
1.1 人α1β2γ2GABAA受體同源模建
1.1.1 同源模建簡介 大多數受體蛋白的三級結構尚未解析,并且同源蛋白在進化過程中保持著結構保守性,利用同源蛋白作為模板來構建受體蛋白是一種有效的方法[4].常用的軟件有兩類:一是利用蛋白質分析軟件來預測,例如SWISS-MODEL主要用于預測蛋白質的高級結構,它通過同源建模的方法可對未知序列的三級結構進行預測;另一類是對蛋白的結晶進行X-衍射、核磁共振技術及冷凍電鏡等方法獲得結構信息,將已知的蛋白質立體結構為模板,利用相關軟件構建已知序列的蛋白高級結構,例如SYBYL, Discovery Studio,Modeller都是比較常用的軟件 .
1.1.2 同源模建a.序列選擇 為了模建目標受體人α1β2γ2GABAA受體,首先通過Swiss-Prot/TrEMBL數據庫篩選出合適的亞基序列:人α1亞基(蛋白質序列號:P14867),β2亞基(蛋白質序列號:P47870),γ2亞基 (蛋白質序列號:P18507),然后對以上3種亞基進行編輯.考慮到所構建的受體在跨膜區,所以刪去膜內環區與膜外結合區域的氨基酸序列.
b.模板選擇 模板在同源模建中起關鍵作用,它直接影響靶結構的質量,并對結果起決定性作用[5].由于膜介蛋白晶體結構較難獲得,且當前結構解析技術直接決定了膜介蛋白結構的分辨率,因此已解析的三維結構膜蛋白數目十分有限.本實驗中,采用海兔乙酰膽堿結合蛋白作為模板(PDB登記號2XYS,0.194 nm)[6].
c.構建亞基 首先采用SYBYL-X1.2中的Biopolymer模塊中的compare sequences將靶標序列與模板序列進行比對(sequence alignment),從而生成MSF (multiple sequence format)文件[7].然后再將Model Proteins中的ORCHESTRAR模塊中導入MSF文件,將模板結構與靶序列的三維結構進行結構比對.最后構建靶肽鏈的結構,包括搜索環區,識別結構保守區域(structure conserved regions,SCR)和添加側鏈.
d.模型組合 將人α1β2γ2受體與模板2XYS進行比對,需要將前者的α1亞基β2亞基γ2亞基分別疊合到2XYS為模板的各個亞基上,以順時針方向(β2)(γ2)(α1)(β2)(γ2)構建人α1β2γ2GABAA受體,如圖2所示.
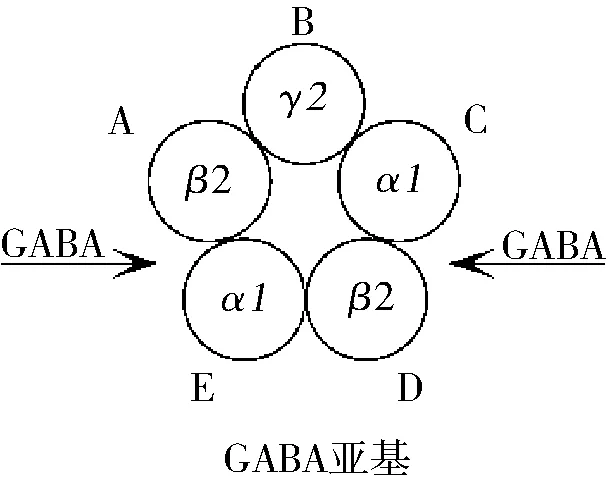
圖2 人α1β2γ2 GABAA亞基對應示意圖Fig.2 Subunit of human α1β2γ2 GABAA
e.模型的優化與修正 因為只有運用分子動力學與分子力學的方法對受體進行修正,才能驗證受體的可靠性.因此,本實驗選取立體場AMBER7 FF99[8],運用共軛梯度法優化體系能量梯度的RMS小于5 kcal/mol/nm,并通過分子動力學(molecular dynamic, MD)優化模型,以檢驗模型的穩定性.計算條件設置為300 K恒溫,每2.5 ps采樣一次軌跡數據,步長1 fs,計算總長為500 ps.
1.2 分子對接
1.2.1 對接方法 本實驗首先利用分子對接法將前面討論的黃酮類配體化合物與人α1β2γ2 GABAA受體蛋白對接.并結合打分函數,研究配體化合物與受體蛋白之間的相互作用,探究結合自由能與實測生物活性的線性關系,同時驗證模型的可靠性.
Surflex-docking[9]是SYBYL-X1.2中的一個模塊,可用于計算配體與受體之間的相互作用能,也可用于復合物的結構優化.本研究利用Surflex-docking進行分子對接實驗. 因為受體的結合口袋直接影響分子對接結果,所以定義結合口袋具有十分重要的意義[10].前文中同源模建人的α1β2γ2GABAA亞型,選用共晶的6-氟-3’-硝基黃酮作為活性區域,利用殘基模式定義活性結合位點. Surflex-docking模塊中,原型分子(protomol)即我們所稱的活性位點.此外,bloat與threshold這兩個參數直接影響原型分子的大小與形狀. 其中,Bloat影響原型分子滲入蛋白空隙的程度,Threshold影響原型分子的大小[11].
1.2.2 對接配體分子 通過SYBYL-X1.2軟件中的dock ligand模塊,41種黃酮類化合物(如圖7)對接到模建的α1β2γ2GABAA受體中.
Surflex-docking進行對接實驗后,分子配體的對接結果可通過Csorce模塊顯示.打分函數基于受體-配體復合物的結合親和力,將會考慮熵作用,極性作用,疏水作用,排斥作用,溶劑化作用.最后給出的總分即-lg10Kd,Kd為配體的解離常數.可通過以下函數計算配體與受體的結合自由能(Free Energy of Binding, kcal/mol):
Free Energy of Binding=RTlnK[12-13]
2 結果和討論
2.1 同源模建
將海兔乙酰膽堿結合蛋白與α1β2γ2進行序列比對,得到其同源性(Identity)分別為19.3%,19.6%和16.0%,由此可知:選取的2XYS作為人α1β2γ2亞基模型是比較合理的.將人α1β2γ2 GABAA受體與海兔乙酰膽堿結合蛋白進行序列比對,如圖3所示.

圖3 人α1β2γ2GABAA受體與海兔乙酰膽堿結合蛋白序列比對圖Fig.3 Result of sequence alignment between human α1β2γ2GABAA and aplysia californica nAChR
經過比對分子序列,搜索保守區域、構建疏水環區、添加分子側鏈、分子動力學優化后,得到人α1β2γ2 GABAA的二級結構,如圖4所示.

圖4 人α1β2γ2GABAA受體二級示意圖Fig.4 Secondary structure of human α1β2γ2GABAA
人α1β2γ2GABAA受體需要進行結構修正和能量優化.通過ProTable驗證受體模型的立體化學性質.人α1β2γ2GABAA的受體模型拉氏構象圖如圖5所示.
從以上拉氏圖可知,大量的氨基酸殘基聚集在值為-150度與-40度處,人α1β2γ2 GABA A受體模型中有96.76%的氨基酸殘基處于允許區域,驗證了模型的合理性.因此,實驗中模建的人α1β2γ2 GABAA受體模型是可靠的,可用作分子對接實驗.
利用SYBYL-X1.2的Dynamics模塊進行分子動力學模擬,人α1β2γ2 GABA A受體模型的動力學模擬能量-時間圖如圖6.經過分子動力學能量優化后,能量-時間圖里可知,α1β2γ2 GABA A受體模型在前300 ps能量變化較大,而后200 ps能量比較穩定,通過分子動力學實驗,也說明了該模型是可靠的[14-15].
2.2 分子對接
本實驗利用分子對接法將黃酮類化合物與人α1β2γ2 GABAA受體進行對接.通過上文軟件打分函數評價對接結果.
利用SYBY-X1.2軟件包中Surflex-docking模塊進行分子對接以及氫鍵,通過分子對接和打分函數的方法對打分函數進行評價,得到黃酮類化合物與人α1β2γ2 GABAA受體的對接得分,如表1所示.
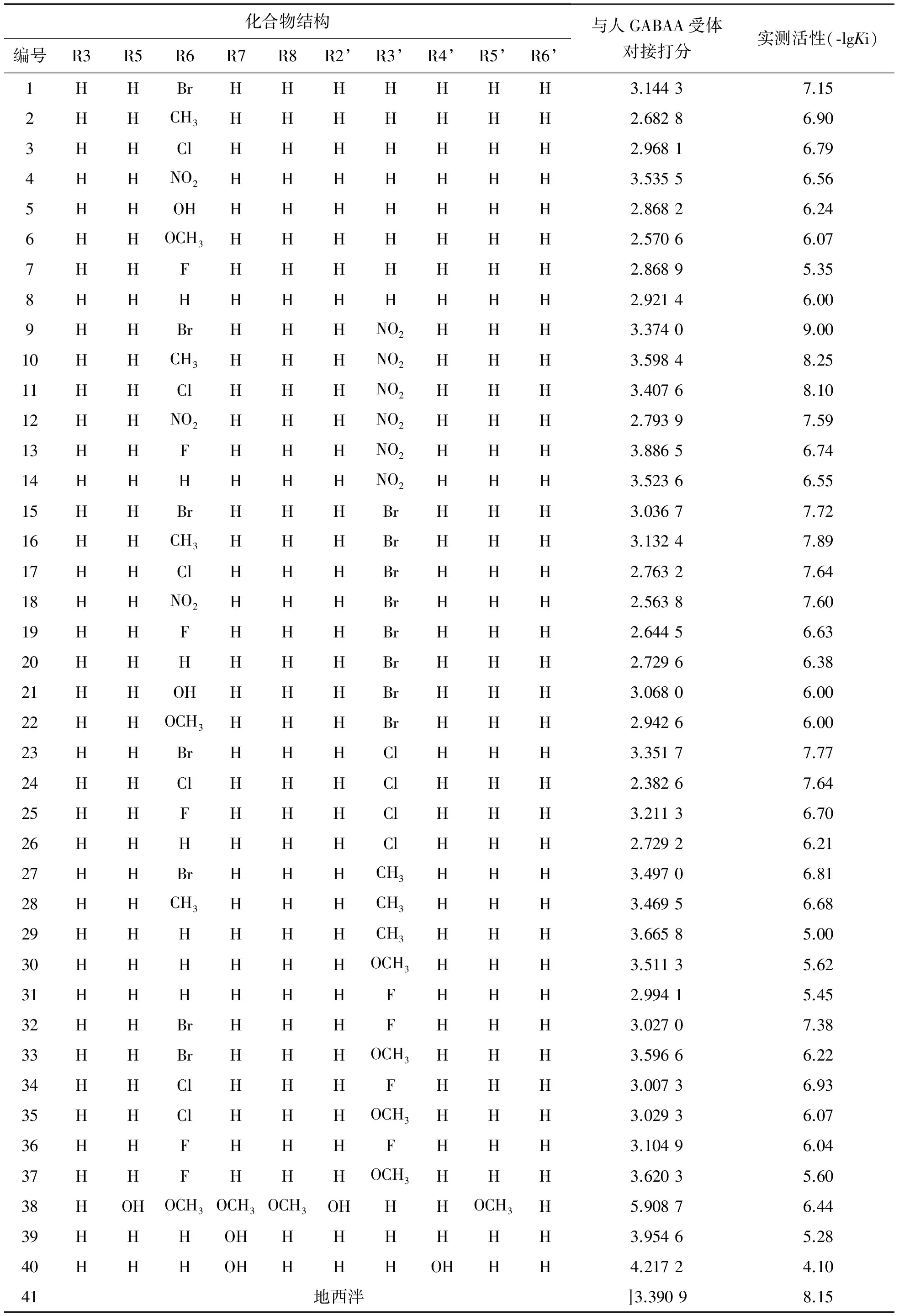
表1 黃酮類化合物的對接得分Tabel 1 Docking result of Flavonoids
由于13號分子打分較高,且結構相似性較高具有代表性,故對其與人α1β2γ2 GABAA受體對接圖(圖7),進行分析.

圖7 人α1β2γ2 GABAA受體與6-氟-3’-硝基黃酮對接圖Fig.7 Human α1β2γ2 GABAA docking with 6-fluoro-3’-nitro flavonoid
從上圖可知,13號分子3’位硝基的一個氧原子和氮原子作為氫鍵受體,與Arg97(精氨酸)側鏈上的亞胺上的氫原子形成氫鍵,為配體分子與受體結合提供了條件,同時也驗證了3’位對黃酮類化合物活性影響的重要性.而且從空間構象來看,13號分子的母環與Tyr190(酪氨酸)和Tyr140(酪氨酸)的苯環形成共軛,這樣能使體系的能量降低,分子穩定,也說明了所建模型的合理性.同時,從表1中可以發現,對比1號分子與9號分子,2號分子與10號分子,3號分子與11號分子,7號分子與13號分子可發現,當6位所連基團相同時,將3’位的氫原子替換成硝基時,對接打分明顯提高.同理可看出,將3’位替換為其他大分子基團時,對接打分也有所提高.且大部分化合物的對接打分與實測活性一致,也驗證了模型的可靠性.綜上所述,黃酮類化合物3’位對活性影響很重要.同時,38號化合物的高得分,可能與較多的取代基提高了與結合口袋的結合能力有關.
3 結 語
本研究通過同源模建人α1β2γ2 GABAA受體跨膜區的三維結構,并結合分子動力學優化和能量優化,驗證了所建模型的穩定性與可靠性.進而將41個黃酮類衍生物與該模型進行分子對接實驗,通過對接結果的分析,得知當母環3’位被取代時,分子活性有所增加,其中被硝基取代時,活性提高較大.并從38號化合物中得到提示,相應的增加取代基的個數,可能會提高活性,為設計黃酮類化合物提供了理論依據.
致 謝
本實驗基于武漢工程大學化工與制藥學院提供的計算平臺,在此表示感謝!
[1] ARGYROPOULOS S V, NUTT D. The use of benzodiazepines in,anxiety and other disorders [J]. The journal of the European College of Neuropsychopharmacology, 1999, 9 (6): 407-412.
[2] VIOLA H, MARDER M, WOLFMAN C, et al. 6-Bromo-3’-nitroflavone, a new high affinity benzodiazepine receptor agonist recognizes two populations ofcentral cortical binding sites [J]. Bioorganic and Medicinal Chemistry Letters, 1997, 7 (3): 373-378.
[3] CRISTINA W, MARIEL M. Flavonoids as GABAA receptor ligands:the whole story[J]. Journal of Experimental Pharmacology, 2012, 4: 9-24.
[4] MARSHALL G R, MAYER D, NAYLOR C B, et al. Mechanism-based analysis of enzyme inhibitors of amide bond hydrolysis [J]. Progress in Clinical and biological research, 1989, 291: 287-295.
[5] ZHU Z Y, SALI A, BLUNDELL T L. A variable gap penalty function and feature weights for protein 3-D structure comparisons [J]. Protein Engineering, 1992, 5 (1): 43-51.
[6] BRAMS M, PANDYA A, KUZMIN D, et al. A structural and mutagenic blueprint for molecular recognition of strychnine and d-tubocurarine by different cys-loop receptors [J]. PloS Biology, 2011, 9 (3): 1100-1034.
[7] NEEDLEMAN S B,WUNSCH C D. A general method applicable to the search for similarities in the amino acid sequence of two proteins [J]. Journal of Molecular Biology, 1970, 48 (3): 443-453.
[8] WANG J M, WOLF R M, CALDWELL J W, et al. Development and testing of a general amber force field [J]. Journal of Computational Chemistry, 2004, 25 (9): 1157-1174.
[9] RUPPERT J, WELCH W, JAIN AN. Automatic identification and representation of protein binding sites for molecular docking [J]. Protein Science, 1997, 6 (3): 524-533.
[10] 巨修練,王黎麗,李科.斑馬魚A型γ-氨基丁酸受體同源模建及分子對接[J].武漢工程大學學報,2013(6):20-29.
JU Xiu-lian, WANG Li-li, LI Ke. Homology modeling and docking of zebrafish γ-aminobutyric acid receptor [J]. Journal of Wuhan Institute of Technology, 2013 (6):20-29.(in Chinese)
[11] CRAMER R D, PATTERSON D E, BUNCE J D. Recent advances in comparative molecular field analysis (CoMFA) [J]. Progress in Clinical and Biological, 1989, 291: 161-165.
[12] CORRINGER P J, BAADEN M, BOCQUET N, et al. Atomic structure and dynamics of pentameric ligand-gated ion channels: new insight from bacterial homologues [J]. The Journal of Physiology, 2001, 588 (4): 565-572
[13] CHEN L G, DURKIN K A, CASIDA J E. Structure model for gamma-aminobutyric acid receptor noncompetitive antagonist binding: widely diverse structure fit the same site [J]. Proceedings of the National Academy of Science of the United Stated of America, 2006, 103 (13): 5185-5190.
[14] MITEVA M A, LEE W H, MONTES M O, et al. Fast structure-based virtual ligand screening combining FRED, DOCK, and Surflex [J]. Journal of Medicinal Chemistry, 2005, 48 (19): 6012-6022.
[15] CHENG Jin, JU Xiu-lian, CHEN Xiang-yang, et al. Homology modeling of human α1β2γ2 and house fly β3 GABA receptor channels and Surflex-docking of fipronil [J]. Journal of Molecular Modeling, 2009, 15: 1145-1153.

