我院藥物臨床試驗(yàn)知情同意書設(shè)計(jì)及簽署情況分析
郭晉敏 張 莉 舒 鶴 趙穩(wěn)華 康長清
濟(jì)南軍區(qū)總醫(yī)院藥劑科,山東濟(jì)南250031
我院藥物臨床試驗(yàn)知情同意書設(shè)計(jì)及簽署情況分析
郭晉敏 張 莉 舒 鶴 趙穩(wěn)華 康長清
濟(jì)南軍區(qū)總醫(yī)院藥劑科,山東濟(jì)南250031
目的分析濟(jì)南軍區(qū)總醫(yī)院(以下簡稱“我院”)藥物臨床試驗(yàn)知情同意書的設(shè)計(jì)及簽署情況。方法制訂知情同意書設(shè)計(jì)及簽署要素標(biāo)準(zhǔn),調(diào)查我院58項(xiàng)藥物臨床試驗(yàn)知情同意書的設(shè)計(jì)及2042份知情同意書的簽署中各要素的出現(xiàn)率,并對出現(xiàn)率低的要素進(jìn)行深入分析。結(jié)果知情同意書的設(shè)計(jì)及簽署基本符合《藥物臨床試驗(yàn)質(zhì)量管理規(guī)范》的要求,但仍存在要素缺失及簽署或修改不規(guī)范問題。國內(nèi)項(xiàng)目的設(shè)計(jì)要素中,各缺失要素的出現(xiàn)率均低于國際多中心,出現(xiàn)率較低的有入選/排除標(biāo)準(zhǔn)(13.7%比71.4%)、試驗(yàn)保險及賠償(7.8%比57.1%)、倫理委員會的聯(lián)系人及聯(lián)系方式(3.9%比85.7%)、知情同意書版本號及版本日期(41.2%比100.0%)。簽署要素中以下容易被忽視:受試者聯(lián)系方式、研究者聯(lián)系方式未填寫或填寫固定電話、法定代理人代簽時未注明受試者姓名及與受試者的關(guān)系,進(jìn)一步分析發(fā)現(xiàn),部分簽署的缺失源于簽字頁項(xiàng)目設(shè)計(jì)不完整。結(jié)論針對發(fā)現(xiàn)問題提出對策,規(guī)范知情同意書的管理,促進(jìn)我院藥物臨床試驗(yàn)的規(guī)范開展。
藥物臨床試驗(yàn);知情同意書;設(shè)計(jì);簽署
藥物臨床試驗(yàn)是確證新藥在人體內(nèi)有效性和安全性必不可少的步驟。為了規(guī)范臨床試驗(yàn)過程,確保其科學(xué)可靠,保護(hù)受試者的權(quán)益并保障其安全,原國家食品藥品監(jiān)督管理局(SFDA)在2003年發(fā)布了《藥物臨床試驗(yàn)質(zhì)量管理規(guī)范》[1],在其中第三章第14、15條中對知情同意做出了明確的規(guī)定。知情同意是臨床試驗(yàn)中保障受試者權(quán)益的主要措施,在開始試驗(yàn)之前,研究者必須向受試者知情告知,并簽署知情同意書(特殊情況下可由法定代理人簽署)。
盡管藥物臨床試驗(yàn)研究者均按規(guī)定執(zhí)行了知情同意,倫理委員會和機(jī)構(gòu)辦公室對其也進(jìn)行了監(jiān)管,但在實(shí)踐中仍存在很多問題[2-4]。為了解濟(jì)南軍區(qū)總醫(yī)院(以下簡稱“我院”)知情同意的現(xiàn)況,本研究回顧性調(diào)查2006年1月~2012年6月已完成的58個藥物臨床試驗(yàn)中的知情同意書,從知情同意書的設(shè)計(jì)及簽署情況方面進(jìn)行分析,旨在發(fā)現(xiàn)我院知情同意工作中存在的問題,制訂相應(yīng)對策,加強(qiáng)管理,保障高水平新藥臨床研究工作的順利開展。
1 資料與方法
1.1 一般資料
我院2006年1月~2012年6月期間已完成的Ⅱ、Ⅲ期藥物臨床試驗(yàn)58項(xiàng),知情同意書共2042份。
1.2 方法
參考國內(nèi)外指南[5-6],制定知情同意書的設(shè)計(jì)及簽署要素標(biāo)準(zhǔn)。對照設(shè)計(jì)要點(diǎn),調(diào)研各項(xiàng)目知情同意書中每條要素的出現(xiàn)率;對照簽署要點(diǎn),調(diào)研每份知情同意書中簽署要素的出現(xiàn)率。根據(jù)調(diào)查結(jié)果,分析知情同意工作的現(xiàn)狀及存在的問題。
2 結(jié)果
2.1 知情同意書設(shè)計(jì)要素標(biāo)準(zhǔn)
結(jié)合國內(nèi)外相關(guān)指南和原則制訂[5-6],具體如下:①研究背景;②項(xiàng)目目的;③試驗(yàn)流程;④試驗(yàn)期限;⑤入選/排除標(biāo)準(zhǔn);⑥試驗(yàn)可能的受益;⑦試驗(yàn)分組情況;⑧試驗(yàn)可能的風(fēng)險;⑨試驗(yàn)藥物及檢查免費(fèi);⑩替代治療方法;試驗(yàn)保密及保護(hù)受試者隱私;試驗(yàn)保險及賠償;受試者的權(quán)利告知(自愿、自由參加及退出);重新獲得知情同意;受試者簽名及日期;受試者聯(lián)系方式;研究者簽名及日期;研究者聯(lián)系方式;法定代理人簽名及日期;法定代理人與受試者的關(guān)系;倫理委員會的聯(lián)系人及聯(lián)系方式;知情同意書的版本號及版本日期。其中,1~4、6~8、 11~13項(xiàng)為我國《藥物臨床試驗(yàn)質(zhì)量管理規(guī)范》規(guī)定知情同意書需告知的要素。
2.2 知情同意書的設(shè)計(jì)完整性
將項(xiàng)目按照申辦者性質(zhì)分為國內(nèi)(51項(xiàng))和國際(7項(xiàng)),分別對知情同意書設(shè)計(jì)要素進(jìn)行綜合分析,國內(nèi)與國際知情同意書基本涵蓋1、2、4、6~11、13~15、17項(xiàng)(出現(xiàn)率>95%),除12項(xiàng)(試驗(yàn)保險及賠償),知情同意書的設(shè)計(jì)基本符合藥品臨床試驗(yàn)管理規(guī)范的要求。
對缺失要素的情況進(jìn)行分析,結(jié)果詳見表1。由表1可見,國內(nèi)知情同意書要素中3、16、18項(xiàng)出現(xiàn)率較高,為82.3%、64.7%、74.5%,國際的出現(xiàn)率分別為100.0%、57.1%、100.0%。國內(nèi)要素5(13.7%)、12(7.8%)、19(49.0%)、20(23.5%)、21(3.9%)、22項(xiàng)(41.2%)出現(xiàn)率較低,而國際出現(xiàn)率分別為71.4%、57.1%、85.7%、57.1%、85.7%、100.0%。國內(nèi)各缺失要素的出現(xiàn)率均低于國際多中心。
2.3 知情同意書簽署要素標(biāo)準(zhǔn)
結(jié)合實(shí)踐與經(jīng)驗(yàn)制訂如下:①受試者簽名及日期;②受試者聯(lián)系方式;③研究者簽名及日期;④研究者聯(lián)系方式;⑤法定代理人簽名及日期;⑥注明法定代理人與受試者的關(guān)系;⑦簽署早于試驗(yàn);⑧受試者與研究者簽署日期相同。備注:2項(xiàng)只適用于受試者本人簽署的知情同意書,5、6項(xiàng)只適用于法定代理人代簽的知情同意書。其中,1、3、5、7、8項(xiàng)為我國《藥物臨床試驗(yàn)質(zhì)量管理規(guī)范》規(guī)定的簽署要素標(biāo)準(zhǔn)。
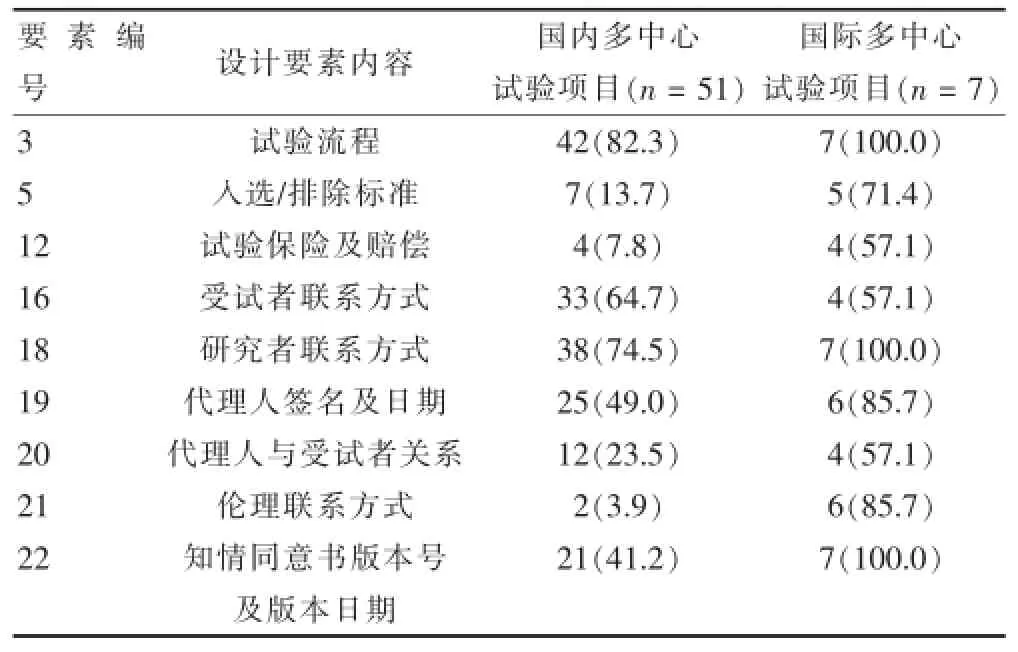
表1 知情同意書缺失要素分析[n(%)]
2.4 知情同意書的簽署完整性
對8項(xiàng)簽署標(biāo)準(zhǔn)進(jìn)行統(tǒng)計(jì),見表2。其中,1、3、5、7、8項(xiàng)基本簽署完整規(guī)范,符合《藥物臨床試驗(yàn)質(zhì)量管理規(guī)范》的要求,但以下要素容易被忽視,包括2項(xiàng)(受試者聯(lián)系方式)、4項(xiàng)(研究者聯(lián)系方式)和法定代理人代簽時的1項(xiàng)(受試者姓名)、6項(xiàng)(注明法定代理人與受試者的關(guān)系)。對以上4項(xiàng)聯(lián)合設(shè)計(jì)和簽署角度進(jìn)行分析發(fā)現(xiàn),設(shè)計(jì)第2項(xiàng)并簽署的占47.41%,未設(shè)計(jì)但簽署的占8.89%,設(shè)計(jì)但未簽署的占24.50%,未設(shè)計(jì)且未簽署的占43.70%(圖1);法定代理人代簽時,均設(shè)計(jì)了第1項(xiàng),簽署的占65.43%(圖2);法定代理人代簽時,設(shè)計(jì)第6項(xiàng)并注明的占29.63%,未設(shè)計(jì)但注明占21.60%,設(shè)計(jì)但未注明的占0.62%,未設(shè)計(jì)且未注明的占48.15%(圖3);設(shè)計(jì)第4項(xiàng)且簽署手機(jī)號碼的占53.57%,設(shè)計(jì)且簽署固定電話的占24.58%,設(shè)計(jì)但未簽署的占4.55%,未設(shè)計(jì)且未簽署的占17.29%(圖4)。
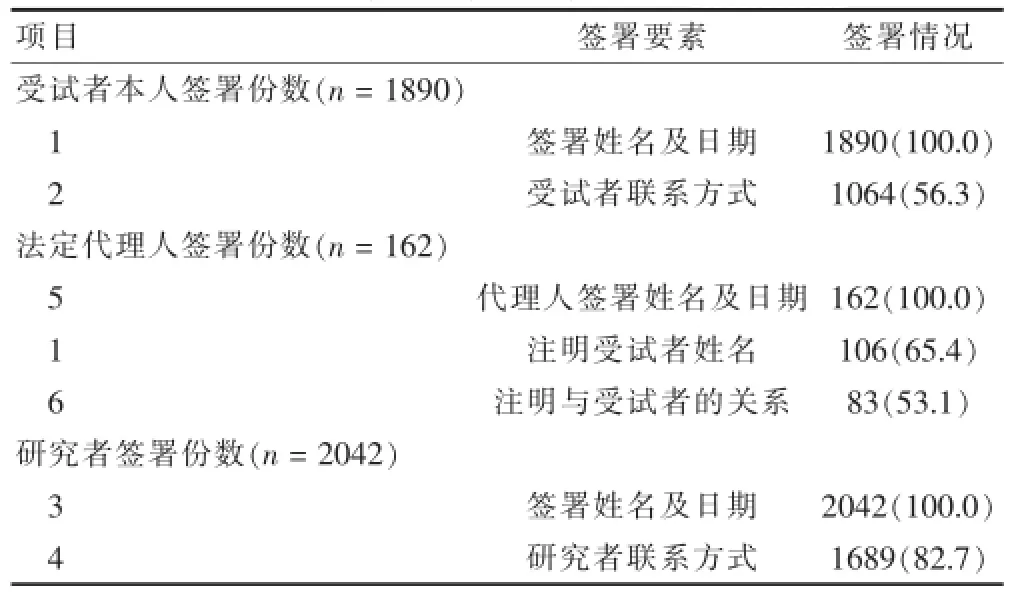
表2 知情同意書簽署情況分析[n(%)]
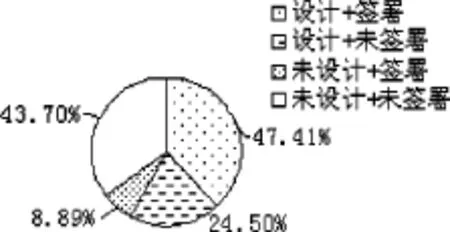
圖1 受試者聯(lián)系方式簽署情況分析
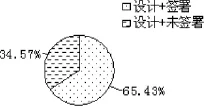
圖2 代理人代簽時受試者姓名注明情況分析
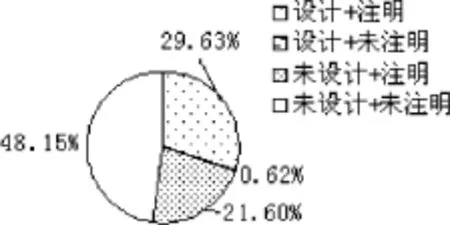
圖3 代理人與受試者關(guān)系注明情況分析
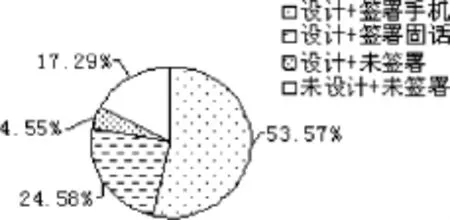
圖4 研究者聯(lián)系方式簽署情況分析
2.5 知情同意書的簽署修改規(guī)范性
知情同意書規(guī)范性修改應(yīng)使用杠改,保持原記錄可見,在旁邊填寫正確記錄,并簽署修改人的姓名(或拼音縮寫)及修改日期。本次調(diào)研中知情同意書簽署修改的規(guī)范率較低,受試者及研究者分別為10.6%和29.4%(圖5)。
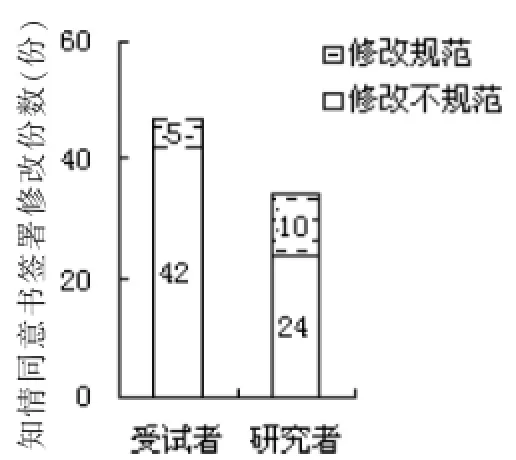
圖5 知情同意書中簽署修改情況分析
3 討論
3.1 國際多中心知情同意書設(shè)計(jì)完整性及質(zhì)量高于國內(nèi)本次調(diào)研中,知情同意書設(shè)計(jì)缺失要素國際有6項(xiàng),國內(nèi)有9項(xiàng),且國內(nèi)缺失要素的出現(xiàn)率均低于國際,總體上國際知情同意書設(shè)計(jì)完整性高于國內(nèi)。國內(nèi)外知情同意書設(shè)計(jì)質(zhì)量存在顯著差異的要素有:①國際多中心臨床試驗(yàn)更重視受試者的權(quán)益保護(hù),知情同意書中多設(shè)計(jì)倫理委員會的聯(lián)系人及電話,而國內(nèi)多中心臨床試驗(yàn)該部分意識則較薄弱。②規(guī)范的知情同意書應(yīng)注明版本號及日期,這一信息有助于確認(rèn)所簽署的知情同意書是獲得倫理委員會批準(zhǔn)的正確版本的知情同意書[4]。國際知情同意書均注明版本號及版本日期,而國內(nèi)該項(xiàng)出現(xiàn)率不足50%。③約57%國際多中心項(xiàng)目提供保險,而國內(nèi)申辦者普遍不為受試者購買保險,知情同意書上關(guān)于保險及賠償問題,尤其對受試者如發(fā)生與試驗(yàn)相關(guān)的損害時,受試者可獲得治療和保險賠償、經(jīng)濟(jì)賠償?shù)染唧w細(xì)節(jié)均未能詳細(xì)列明。這些差異主要由于國外倫理審查較為完善,且對知情同意書有明確的監(jiān)督管理機(jī)制和操作規(guī)程,而國內(nèi)倫理審查仍處于逐步發(fā)展完善階段,且國內(nèi)藥品臨床試驗(yàn)管理規(guī)范沒有明確規(guī)定統(tǒng)一的設(shè)計(jì)格式和標(biāo)準(zhǔn),知情同意書各式各樣。我院甚至有一項(xiàng)目的知情同意書分為兩份,一份為受試者告知單,一份為受試者知情同意聲明及雙方簽署部分,在歸檔資料中僅保留后者。這種做法是不規(guī)范的,知情同意書應(yīng)是一份完整的文件。
在全球性的協(xié)作研究中,應(yīng)學(xué)習(xí)國際科學(xué)的管理方法及研究設(shè)計(jì)等,逐步完善規(guī)范知情同意書的內(nèi)容和格式,縮短與國際臨床試驗(yàn)間的差距,切實(shí)保護(hù)受試者的權(quán)益。
3.2 知情同意書簽字頁設(shè)計(jì)可影響簽署的完整性
本次調(diào)研發(fā)現(xiàn),受試者的聯(lián)系方式有43.70%因未設(shè)計(jì)而未簽署,研究者的聯(lián)系方式有17.29%因未設(shè)計(jì)而未簽署。法定代理人代簽時,有48.15%因未設(shè)計(jì)法定代理人與受試者的關(guān)系一欄而未簽署。這就提示,可能部分未簽署的現(xiàn)象源于簽署設(shè)計(jì)項(xiàng)的缺失。因此,知情同意書的簽字頁設(shè)計(jì)全面,在一定程度上能規(guī)范受試者及研究者的簽署行為。
3.3 知情同意書的簽署存在不規(guī)范現(xiàn)象
本次調(diào)研中,知情同意書的簽署存在不規(guī)范之處,主要表現(xiàn)為:①法定代理人代簽時往往只填寫代理人姓名,是不完整的,應(yīng)同時填寫受試者姓名及注明與受試者關(guān)系,以判斷代理人是否符合代理人的條件[7]。②知情同意書中研究者的聯(lián)系方式不填寫或填寫固定電話。在知情同意書中必須留下研究者的聯(lián)系方式,且應(yīng)填寫手機(jī)號碼,而非固定電話,否則受試者在試驗(yàn)期間出現(xiàn)不良事件時,就不能及時與研究者取得聯(lián)系,給受試者的安全帶來隱患。③知情同意書簽署修改不規(guī)范。研究者自身應(yīng)做到規(guī)范性修改,并能指導(dǎo)受試者進(jìn)行規(guī)范性修改,且不得代受試者進(jìn)行。
3.4 針對發(fā)現(xiàn)問題的對策
上述問題的發(fā)生,反映出我院對知情同意書的設(shè)計(jì)及審查體系需重視并改進(jìn),同時,也暴露出研究人員的職業(yè)素質(zhì)需要強(qiáng)化。為了避免問題的重復(fù)發(fā)生,保證藥物臨床試驗(yàn)知情同意書的規(guī)范性,提出以下對策:①設(shè)計(jì)規(guī)范及標(biāo)準(zhǔn)操作規(guī)程的修訂:機(jī)構(gòu)辦公室及專業(yè)科室對《知情同意書設(shè)計(jì)規(guī)范》和《知情同意的SOP》進(jìn)行修訂,進(jìn)一步規(guī)范和統(tǒng)一知情同意書設(shè)計(jì)及簽署的內(nèi)容及流程。②加強(qiáng)教育與培訓(xùn):加強(qiáng)對研究人員的職業(yè)道德教育,強(qiáng)化“以人為本”的服務(wù)理念。機(jī)構(gòu)辦公室及專業(yè)負(fù)責(zé)人組織研究者進(jìn)行《藥物臨床試驗(yàn)質(zhì)量管理規(guī)范》及知情同意專題的培訓(xùn),要求其嚴(yán)格遵循“完全告知、充分理解、自主選擇”的原則,規(guī)范性簽署知情同意書。③提高倫理審查質(zhì)量:倫理委員會應(yīng)提高對知情同意書的審查標(biāo)準(zhǔn)及審查力度,切實(shí)保護(hù)受試者的權(quán)益,杜絕不規(guī)范的知情同意書。④健全機(jī)構(gòu)內(nèi)部檢查制度,實(shí)施三級質(zhì)控:本機(jī)構(gòu)成立質(zhì)量管理小組,實(shí)施機(jī)構(gòu)辦公室質(zhì)控員、專業(yè)負(fù)責(zé)人、科室質(zhì)控員的三級質(zhì)量控制。提高對知情同意書的審查標(biāo)準(zhǔn),定期對知情同意書的簽署情況進(jìn)行審查。發(fā)現(xiàn)問題及時反饋,提出改進(jìn)措施,限期整改。本次調(diào)研中,未涉及知情同意的過程,以后的質(zhì)控工作中,還應(yīng)對知情同意的執(zhí)行情況進(jìn)行現(xiàn)場檢查或向受試者進(jìn)行電話咨詢。
3.5 結(jié)語
知情同意書是臨床試驗(yàn)成功與否的首要條件。在臨床試驗(yàn)規(guī)范化、科學(xué)化建設(shè)的同時,做好知情同意真正體現(xiàn)以受試者為本的醫(yī)學(xué)倫理、人道精神和行為[8]。通過本次調(diào)研,針對發(fā)現(xiàn)的問題提出對策,加以改進(jìn),實(shí)現(xiàn)對知情同意的規(guī)范化管理,只有這樣才能使更多的患者從臨床試驗(yàn)中受益,使我院的藥物臨床試驗(yàn)水平得到提高。
[1]國家食品藥品監(jiān)督管理局.藥物臨床試驗(yàn)質(zhì)量管理規(guī)范[S]. 2003-09-01.
[2]王曉霞,李育民.我院藥物臨床試驗(yàn)實(shí)施知情同意工作的幾點(diǎn)體會[J].中國藥物與臨床,2009,9(8):772-773.
[3]歐陽櫻君.藥物臨床試驗(yàn)受試者知情同意的現(xiàn)狀及改進(jìn)措施[J].現(xiàn)代醫(yī)院,2008,8(6):116-117.
[4]鐘旋,劉秋生,劉大鉞,等.藥物臨床試驗(yàn)知情同意書常見的倫理問題與對策[J].中國醫(yī)學(xué)倫理學(xué),2008,21(6):128-130.
[5]黃瑾,沈娜,劉厚佳,等.知情同意書信息要素完整性研究[J].藥學(xué)服務(wù)與研究,2011,11(2):123-126.
[6]Mcguire DC,Chadwick GL.Protecting study volunteers in research[M].New York:Center Watch Inc/Thomson,2004:100.
[7]張蓉.知情同意現(xiàn)場檢查中應(yīng)關(guān)注的問題[J].中國醫(yī)藥導(dǎo)刊,2012,14(3):551-552.
[8]杜彥萍,楊忠奇,汪朝暉.對藥物臨床試驗(yàn)知情同意的解析[J].中醫(yī)藥管理雜志,2011,19(7):623-624.
Design and signature of informed consent form from clinical trial drugs of our hospital
GUO JinminZHANG LiSHU HeZHAO WenhuaKANG Changqing
Department of Pharmacy,Ji′nan Military General Hospital,Shandong Province,Ji′nan250031,China
ObjectiveTo discuss the design and signature of informed consent form(ICF)from clinical trial drugs of Ji′nan Military General Hospital(“our hospital”for short).MethodsItems of design and signature from clinical trial drugs were made,the occurrence ratio of every item in 2042 ICF from 58 clinical trial drugs in our hospital were analyzed, and items with lower occurrence ratio were explored.ResultsGenerally,the design and signature of ICF met the requirement of GCP.However,there were some defects of ICF and antonym of signature/revisions.In the domestic trail, the occurrence ratios of missing elements for design were lower than those in international trail,and the elements with low occurrence ratio were shown as follows:criteria of inclusion/exclusion(13.7%vs 71.4%),pay and compensation (7.8%vs 57.1%),the contact person and method of the Institutional Review Board(3.9%vs 85.7%),ICF version numbers and date(41.2%vs 100.0%).The elements for signature frequently missed were the contact information of subjects,contact information of investigators which fill in landlines or nothing,the name of subject and the relationship with subject which legal representative did not write.The absence of signature elements was further analyzed and found that it was partly due to the design defects.ConclusionStudies the causes and puts forward countermeasures to standardize informed consent,which promotes development of clinical trial in our hospital.
Clinical trial drugs;Informed consent form(ICF);Design;Signature
R197.3
B
1673-7210(2014)04(c)-0151-04
2013-11-19本文編輯:程銘)
郭晉敏(1983.2-),女,博士研究生;研究方向:心血管藥理學(xué)和藥物臨床試驗(yàn)。
張莉(1972.12-),女,碩士研究生,副主任藥師;研究方向:生化藥學(xué)、藥品質(zhì)量控制、臨床藥學(xué)和藥物臨床試驗(yàn)。

