煙臺市套子灣污水處理廠排污混合區(qū)水質(zhì)綜合評價與分析
張東華
中國海洋大學 山東青島 266100
利用海洋處置城市污水是一種合理利用海洋水體的環(huán)境容量和自凈能力,改善城市環(huán)境質(zhì)量的可行方法。煙臺市臨近大海,為了發(fā)揮區(qū)位優(yōu)勢,污水經(jīng)過深度處理通過排海管道以浮射流形式排入海洋。套子灣污水處理廠1998年建成投入運轉(zhuǎn),并于2008年進行了升級改造,目前日處理城市污水25×104t,采用二級生物處理AAO工藝,處理后的污水經(jīng)排海泵站及轉(zhuǎn)輸管道送達芝罘島山后海域,經(jīng)水下排海管道進行深海排放[1]。
本研究選取排污混合區(qū)及周圍的海水水質(zhì)進行評價和分析,探討污水處理工程對其接納水域的影響;同時研究結(jié)果可作為芝罘島近海規(guī)劃與整治的參考依據(jù),為將來套子灣污水處理廠進一步升級改造時排污混合區(qū)的規(guī)劃提供科學依據(jù)。
1 材料與方法
1.1 點位布設
套子灣污水處理廠經(jīng)污水改良AAO工藝二級生物處理后排入項目北側(cè)芝罘島外深海區(qū)。排水監(jiān)測站于2016年5月進行了排污混合區(qū)監(jiān)測,布設監(jiān)測點18個,具體監(jiān)測點位見圖1。
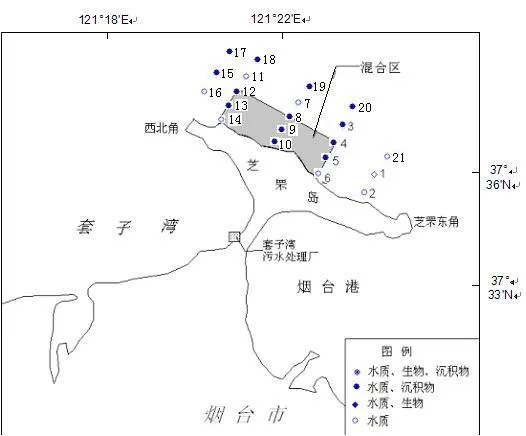
圖1 監(jiān)測點位示意圖
1.2 監(jiān)測項目
高錳酸鹽指數(shù)、溶解氧、無機氮、無機磷、揮發(fā)酚、氰化物、硫化物、石油類、銅、鋅、鉛、汞、鎘、六價鉻、砷、鹽度共16項。水質(zhì)調(diào)查和分析方法按GB/T17378.4-2007《海洋監(jiān)測規(guī)范》執(zhí)行。
1.3 海水水質(zhì)評價
1.3.1 水質(zhì)評價方法
式中:Si,j——第i種污染物在點的標準指數(shù);
Ci,j——第i種污染物在j點的實測濃度;
1.3.2 參數(shù)的選定
根據(jù)套子灣污水處理廠排放污染物的特點,選取COD、無機氮、無機磷、石油類4個參數(shù)進行評價。
1.3.3 評價標準
在2016年以前該海域混合區(qū)邊界以外的海洋功能區(qū)劃為漁業(yè)用海,水質(zhì)執(zhí)行《海水水質(zhì)標準》(GB3079-1997)中的第二類標準。后經(jīng)《山東省近岸海域環(huán)境功能區(qū)劃(2016-2020年)》變更,該海域混合區(qū)邊界以外的海洋功能區(qū)劃為一類功能區(qū),水質(zhì)執(zhí)行《海水水質(zhì)標準》(GB3079-1997)中的第一類標準。為了解變更后海域水質(zhì)能否達到一類標準,此次排污混合區(qū)海域使用后評估按照一類標準計算污染指數(shù)。混合區(qū)內(nèi)無執(zhí)行標準。
2 評價結(jié)果與分析
2.1 海水水質(zhì)評價結(jié)果
各項評價因子的單項污染指數(shù)統(tǒng)計結(jié)果,見表1。
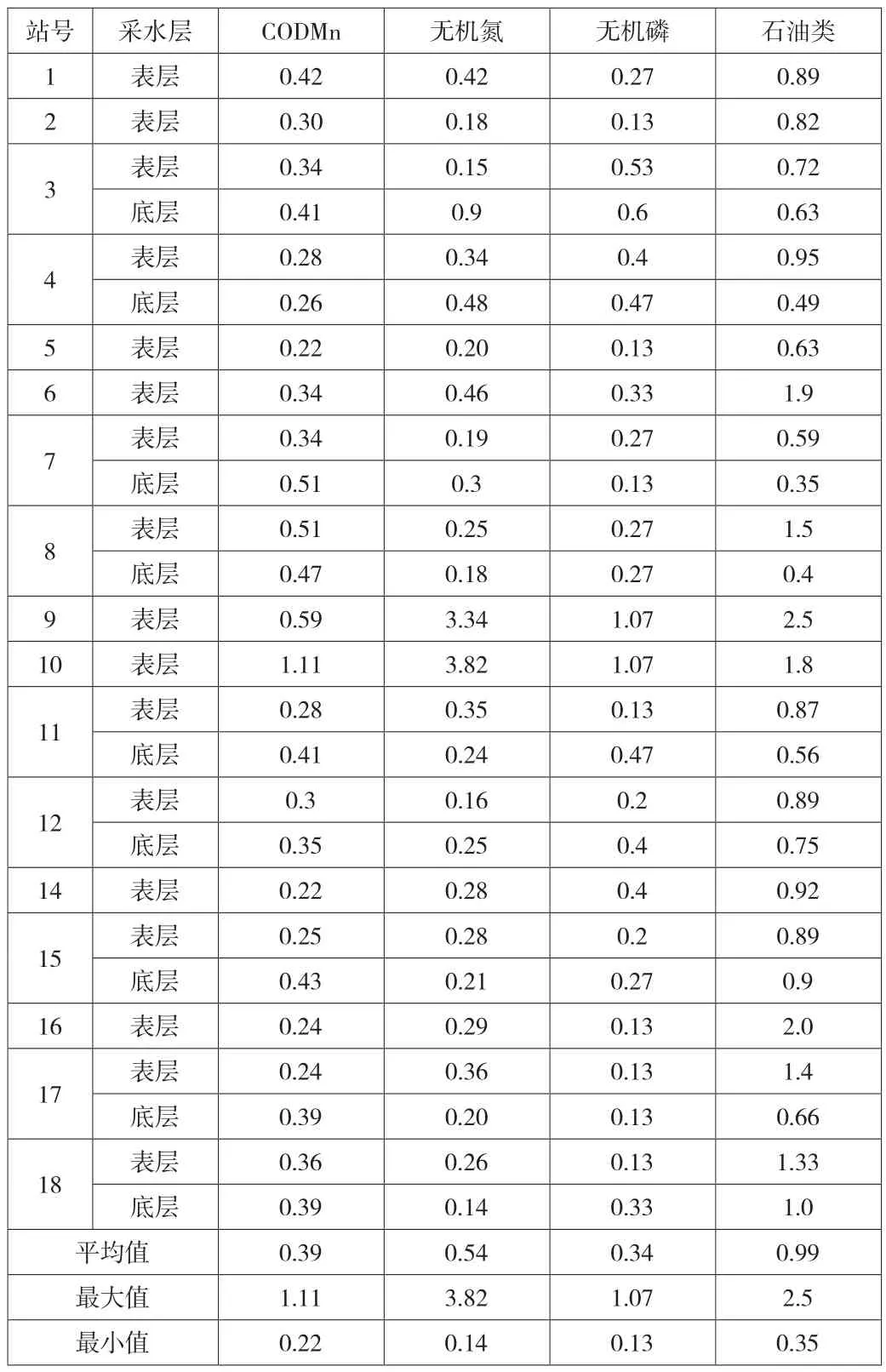
表1 套子灣污水處理廠排污海域海水水質(zhì)評價標準指數(shù)統(tǒng)計
從表1可以看出,排污海域無機氮嚴重超標,9#、10#監(jiān)測站無機氮污染指數(shù)變化范圍為3.31-3.82,全部超過一類水質(zhì)標準。這兩個站都在排污混合區(qū)內(nèi),其他站均符合《海水水質(zhì)標準》(GB3097-1997)中的一類標準。
油類6#、8#、9#、10#、15#、16#、17#、18#監(jiān)測站超過二類水質(zhì)標準,6#、8#、9#、10#監(jiān)測站在排污混合區(qū)內(nèi),15#、16#、17#、18#監(jiān)測站在排污混合區(qū)外。
除油類15#、16#、17#、18#監(jiān)測站超標外,其他所有檢測項目都符合《海水水質(zhì)標準》(GB3097-1997)中的一類標準。
2.2 評價結(jié)果分析
自2008年起,套子灣污水處理廠進行了升級改造工程,其污水處理工藝為二級生物處理(改良AAO工藝),大大降低了陸域排海污染負荷,有效改善了海洋環(huán)境。
從整體來看,排污海域水質(zhì)基本達標(個別站位的無機氮和石油類除外)。
3 結(jié)語
污水處理廠的運行一方面會造成排放海域局部超一類水質(zhì),排放海域會有一定海洋生物資源的損失;另一方面污水處理廠大幅度地減少本市向沿海排入的污染負荷量,有效減輕了近海水質(zhì)環(huán)境的污染,從而大大減少了海洋生物資源的損失[2]。
套子灣污水處理廠排污混合區(qū)位于芝罘島外海,此處水深環(huán)境容量大,污水稀釋擴散條件優(yōu)越,水深和海水交換能力及環(huán)境容量符合《污水海洋處置工程污染控制標準》(GB18486-2001),也符合海洋功能區(qū)劃,根據(jù)海域跟蹤監(jiān)測得出,該排污混合區(qū)工程用海面積合理、科學[3]。

