藥物及個人護理品在水中光解的研究進展
趙 群
(山東省環境保護科學研究設計院, 山東 濟南 250013)
1 PPCPs的直接光解
許多PPCPs具有萘環、雜環、硝基等結構,能吸收自然光發生化學鍵斷裂、電子重排以及異構化等轉變成另外一種物質.有些PPCPs雖能吸收自然光,但將能量傳遞出去不發生光化學轉化或轉化較慢.如卡馬西平吸收的光最多,但降解常數最小.氯貝酸雖吸收的光最小,但能迅速降解生成4-氯酚、對羥基苯酚、苯酚和對位苯醌[9].一般來說,PPCPs的直接光解取決于三方面:PPCPs分子結構、溶液pH值和PPCPs自敏化.
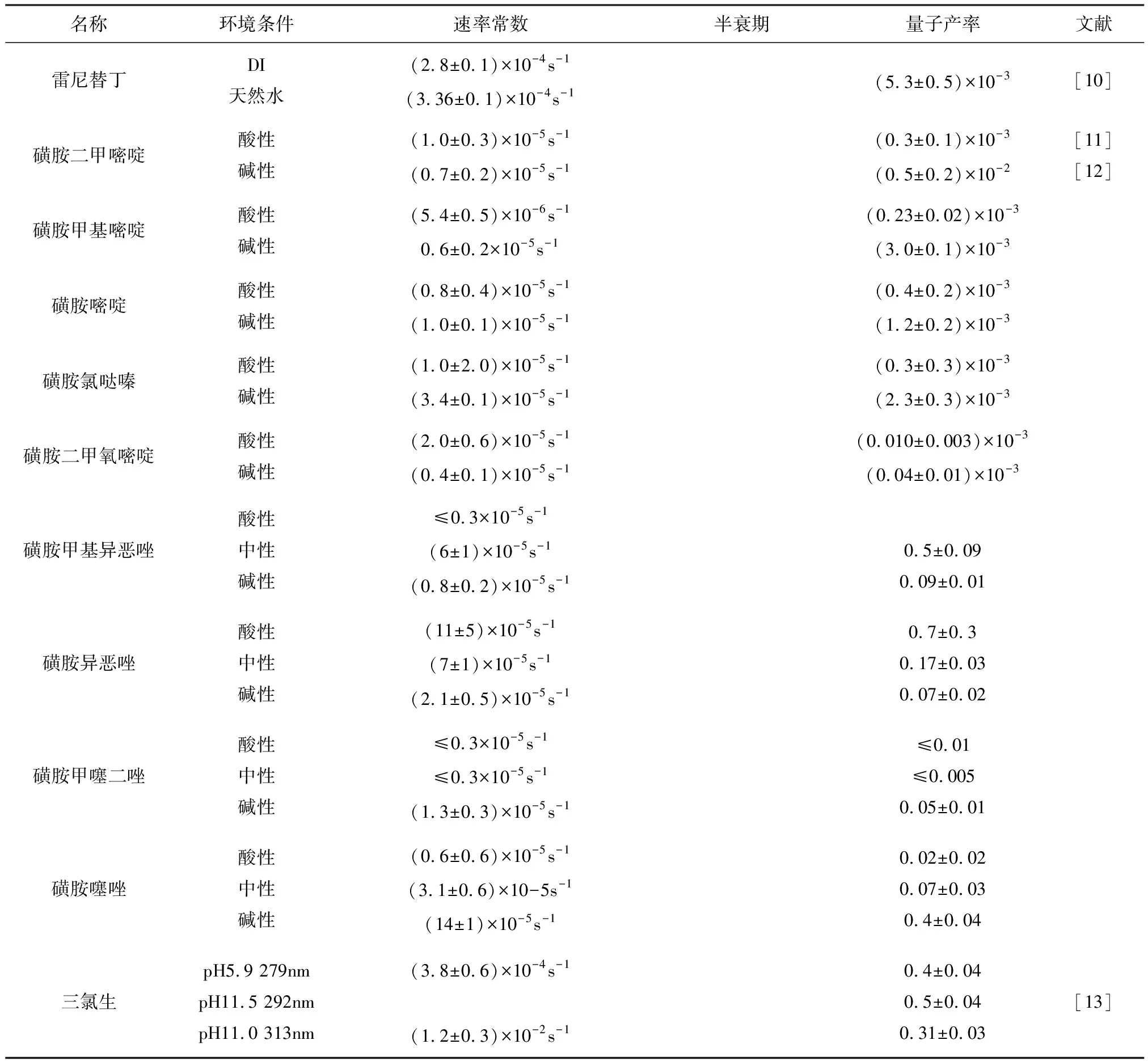
表1 一些PPCPs的直接光降解速率常數、半衰期和量子產率
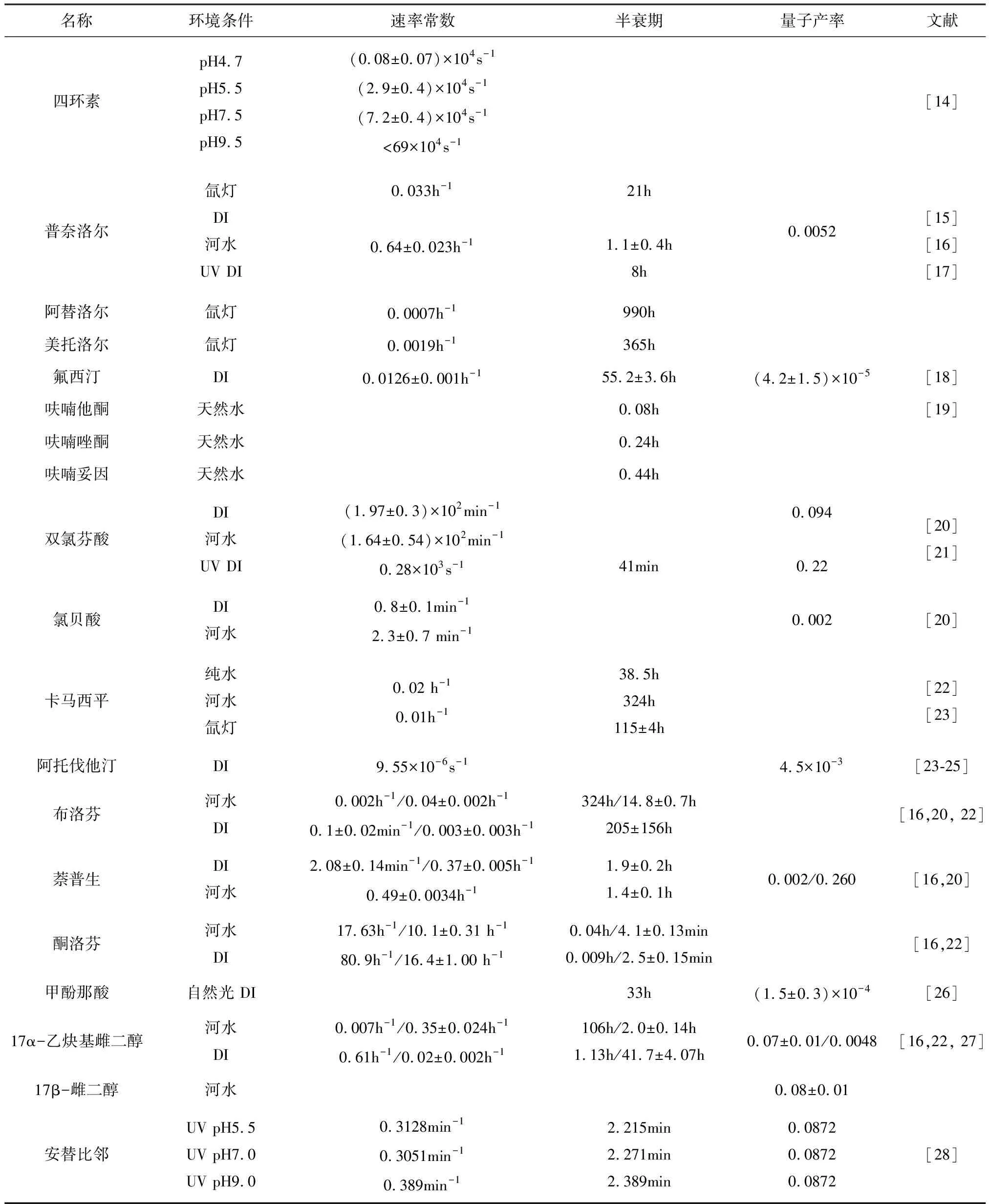
續表
注:表中DI為去離子水,UV為紫外光
1.1 分子結構
PPCPs對光的吸收與去定域化π電子體系有關,這類體系最可能發生π→π*躍遷.如果π電子體系存在帶有雜原子,還可發生n→π*躍遷.通常一個分子的共軛效應越明顯,其吸收峰向長波方向偏移越多,與太陽光譜重疊越多[29].普奈洛爾具有萘結構,吸收光譜與太陽光譜重疊最多,光解最快.而阿替洛爾和美托洛爾只有苯環結構,無論在低濃度(1mg/L)還是高濃度(10mg/L)二者光解速率均遠遠低于普奈洛爾[15].酮洛芬直接光解很快是由于其中羰基與兩個苯環共軛,使n→π*躍遷能很低,易產生活性三重態.雌二醇和炔雌二醇的量子產率非常接近,分別為0.067和0.062,這與具有酚結構的物質很接近[27].
1.2 pH值
許多PPCPs陰離子形態傾向于紅移,吸收光譜與自然光譜重疊的部分增加,利于光降解.在pH為5.9、8.0、9.1、11.0下,三氯生光解速率常數分別為(3.8±0.6)×10-4s-1、(6.9±0.5)×10-3s-1、(1.1±0.2)×10-2s-1、(1.2±0.3)×10-2s-1[13,30].雷尼替丁在pH為6時量子產率為(5.3±0.5)×10-3,pH為10時量子產率為(5.5±0.5)×10-3[10].pH升高使撲熱息痛中酚羥基失去質子發生紅移吸收更多自然光[31].
但有些PPCPs的光降解機理比較復雜,酸催化可使PPCPs在酸性下的降解速率大于堿性和中性.呋喃類抗生素(呋喃他酮、呋喃唑酮和呋喃妥因)的光解受pH的影響,光解速率在酸性條件下達到最大,pKa影響較小[19].也存在堿催化現象.自然光照下氟西汀在pH為9時的速率常數為pH為4和7時的二倍,在堿性條件下未觀察到紅移現象[18].
1.3 自敏化
PPCPs能自敏化產生活性氧(ROS)降解自身.四環素在水中光解并不滿足一級動力學,這是因為降解產物發生自敏化產生ROS使其具有直接光解和ROS氧化兩個途徑,另外一個解釋是四環素之間發生自敏化,這種自敏化在其帶有兩個負電荷時達到最大,甚至遠大于直接光解,甚至加入金屬離子后,這種自敏化仍能夠發生[14].
一些磺胺類藥物直接光解機理較為復雜,磺胺甲基異惡唑的光解速率隨著吸收光量的增加而增加,在中性時光解速率常數最大,陰離子態光解速率則慢得多.磺胺異惡唑在中性時吸收光量最多,但陽離子態時光解速率最快.磺胺甲噻二唑和磺胺噻唑在中性時吸收光量最多,但是它們在陰離子態時光解速率最快,這些磺胺類物質結構相似,僅有雜環中雜原子及其取代基不同,但是光解特點卻有很大差別[12].
2 PPCPs的間接光解
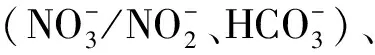
2.1 PPCPs與和體系的光反應
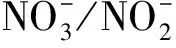
2.2 PPCPs與DOM體系的光反應
DOM與PPCPs的光反應機制較為復雜,一方面DOM通過能量轉移、電子轉移和氫轉移或產生活性氧(HO·、1O2、H2O2等)促進PPCPs的光降解,另一方面DOM具有內濾作用,與PPCPs競爭吸收重要譜段的光抑制PPCPs的光降解,而且作為羥基自由基的淬滅劑DOM也會抑制PPCPs的光化學轉化[36-37].DOM與三氯生競爭光減少三氯生的光降解[13].低濃度的DOM促進卡馬西平的光解,濃度升高時,這種促進作用會減弱[9,22].阿托伐他汀與富里酸的光反應速率大于加入疊氮化鈉的反應速率,阿托伐他汀與富里酸在D2O(重水(氧化氘)是由氘和氧組成的化合物)的反應速率也大于在水中光反應速率,單重態氧能被疊氮化鈉淬滅,單重態氧在D2O中的存留時間比H2O中長,這說明阿托伐他汀與富里酸在光照下有單重態氧參與反應[24].DOM能夠促進甲酚那酸的光降解,經過研究發現是DOM吸收光后向甲酚那酸傳遞能量或傳遞電子使其發生降解[26].撲熱息痛與兩種富里酸的光解反應速率均隨著富里酸濃度的增加而加快,這是由于形成一系列活性中間體[38-39].
2.3 PPCPs與Fe3+的光反應
Fe3+主要通過兩種途徑參與PPCPs光降解:(1)Fe3+與有機物結合,使不吸收太陽光譜的有機物吸收太陽光譜發生光降解;(2)Fe3+通過光化學氧化還原循環產生羥基自由基參與PPCPs的氧化[40].卡馬西平和Fe3+的光解速率隨著pH的增加而減小,溶解態FeOH2+能在光照下產生羥基自由基降解卡馬西平,隨著pH增加,FeOH2+減少,自由基減少.但將Cl-加入卡馬西平和Fe3+后,光解速率隨pH的增加而增大.酸性條件下,Cl-是羥基自由基的淬滅劑,所以反應速率低,堿性條件下,Cl-對羥基自由基的淬滅減弱,Fe3+將Cl-氧化成Cl·/Cl2·參與卡馬西平的氧化[41].雌酮水溶液幾乎不發生光解,加入三價鐵后,降解效率隨光照時間延長而增加,但降解效率(55.1%)不高.pH為3~4時,雌酮與鐵-草酸鹽配合物有較高光解效率,pH降低或升高光解效率都有所下降[42].
2.4 PPCPs與生物體系的光反應
國外對PPCPs與生物體系的光反應研究較少,國內劉先利和葛利云研究了乙炔基雌二醇和雌二醇與藻類體系的光降解,發現魚腥藻使乙炔基雌二醇光降解率增加.藻液中增多了活性氧H2O2、單重態氧和腐殖質,反應途徑增加.在紫外光下,藻在107cells/L和109cells/L時具有催化作用,而在108cells/L則不理想,因為隨著藻濃度增加,水體中光強受到部分削減,濃度繼續增大,藻或腐殖質增大的綜合催化補償了光削減的影響[43].普通小球藻也能誘發雌二醇光降解,小球藻與17β-雌二醇結合吸收波長較長的光,藻液在光照下產生了活性氧以及藻類的死亡產生了具有催化作用的腐殖質[44].
3 展望
PPCPs種類繁多,不同種類PPCPs的化學結構不同,在水環境中的光解途徑會有很大差別.同時,水環境介質是一個非常復雜的混合體系,即使是同種PPCPs,在不同水環境中光解途徑也可能會有很大差別.目前已經有許多科研工作者對環境中出現的典型PPCPs進行了光化學降解研究,這些研究主要集中在:PPCPs在純水中的直接光解和光解產物的鑒定以及根據光解產物推斷直接光解機理;羥基自由基、單重態氧對PPCPs的光化學轉化和產物鑒定以及根據產物推斷機理;PPCPs在模擬水環境體系如硝酸根體系、碳酸根體系、DOM體系和金屬絡合物體系中的光解動力學及影響因素、產物鑒定及相關機理.也有人研究PPCPs在天然水包括海水環境中的光降解狀況,并推斷降解的機理.隨著對PPCPs在水環境光降解研究的不斷深入,人們發現有些PPCPs的光降解產物的毒性遠大于母體化合物,如三氯生光解后能產生毒性極大的二噁英,所以很有必要對PPCPs的光降解產物進行毒性實驗.一些PPCPs的光降解機理非常復雜,如磺胺類藥物的降解無法用常規的直接光解、活性氧氧化進行解釋,這就需要一些新的手段檢測可能未被認識的物質如自由基或反應機理.隨著QSAR技術的不斷成熟,可對PPCPs的化學結構及空間構型通過合適的參數進行量化,建立光解速率模型來消減實驗次數,減少人力、物力和財力的投入.
[1] EPA. Pharmaceuticals & personal care products in the environment: an emerging concern?[EB/OL]. (1999-12-24)[2005-3-20]. http://www.epa.gov/nerl/research/1999/html/g8-14.html.
[2] Carballa M, Omil F, Lema J M,etal. Behavior of pharmaceuticals, cosmetics and hormones in a sewage treatment plant[J]. Water Research, 2004. 38(12): 2 918-2 926.
[3] Heberer T. Occurrence, fate, and removal of pharmaceutical residues in the aquatic environment: a review of recent research data[J]. Toxicology Letters, 2002,131(1-2): 5-17.
[4] Daughton C G, Ternes T A. Pharmaceuticals and personal care products in the environment: Agents of subtle change? [J]. Environmental Health Perspectives, 1999,107: 907-938.
[5] Jorgensen S E, Halling-Sorensen B. Drugs in the environment[J]. Chemosphere, 2000,40(7): 691-699.
[6] Kummerer K. Drugs in the environment: emission of drugs, diagnostic aids and disinfectants into wastewater by hospitals in relation to other sources - a review[J]. Chemosphere, 2001,45(6-7): 957-969.
[7] Arnold W A, McNeill K. Transformation of pharmaceuticals in the environment: photolysis and other abiotic processes[J]. Comprehensive Analytical Chemistry, 2007,50: 361-385.
[8] Boreen A L, Arnold W A, McNeill K. Photodegradation of pharmaceuticals in the aquatic environment: a review[J]. Aquatic Sciences, 2003,65(4): 320-341.
[9] Doll T E, Frimmel F H. Fate of pharmaceuticals-photodegradation by simulated solar UV-light[J]. Chemosphere, 2003,52(10): 175 7-176 9.
[10] Latch D E, Stender B L, Packer J L,etal. Photochemical fate of pharmaceuticals in the environment: cimetidine and ranitidine[J]. Environmental Science & Technology, 2003,37(15): 3 342-3 350.
[11] Boreen A L, Arnold W A, McNeill K. Triplet-sensitized photodegradation of sulfa drugs containing six-membered heterocyclic groups: Identification of an SO2extrusion photoproduct[J]. Environmental Science & Technology, 2005, 39(10): 3 630-3 638.
[12] Boreen A L, Arnold W A, McNeill K. Photochemical fate of sulfa drugs in the aquatic environment: Sulfa drugs containing five-membered heterocyclic groups[J]. Environmental Science & Technology, 2004,38(14): 3 933-3 940.
[13] Tixier C, Singer H P, Canonica S,etal. Phototransformation of triclosan in surface waters: a relevant elimination process for this widely used biocide - laboratory studies, field measurements, and modeling[J]. Environmental Science & Technology, 2002,36(16): 3 482-3 489.
[14] Werner J J, Arnold W A, McNeill K. Water hardness as a photochemical parameter: tetracycline photolysis as a function of calcium concentration, magnesium concentration, and pH[J]. Environmental Science & Technology, 2006,40(23): 7 236-7 241.
[15] Liu Q T, Williams H E. Kinetics and degradation products for direct photolysis of beta-blockers in water[J]. Environmental Science & Technology, 2007,41(3): 803-810.
[16] Lin A Y C, Reinhard M. Photodegradation of common environmental pharmaceuticals and estrogens in river water[J]. Environmental Toxicology and Chemistry, 2005,24(6): 1 303-1 309.
[17] Piram A, Salvador A, Verne C,etal. Photolysis of beta-blockers in environmental waters[J]. Chemosphere, 2008,73(8): 1 265-1 271.
[18] Lam M W, Young C J, Mabury S A. Aqueous photochemical reaction kinetics and transformations of fluoxetine[J]. Environmental Science & Technology, 2005,39(2): 513-522.
[19] Edhlund B L, Arnold W A, McNeill K. Aquatic photochemistry of nitrofuran antibiotics[J]. Environmental Science & Technology, 2006, 40(17): 5 422-5 427.
[20] Packer J L, Werner J J, Latch D E,etal. Photochemical fate of pharmaceuticals in the environment: aproxen, diclofenac, clofibric acid, and ibuprofen[J]. Aquatic Sciences, 2003,65(4): 342-351.
[21] Eriksson J J, Svanfelt L K. A photochemical study of diclofenac and its major transformation products[J]. Photochemistry and Photobiology, 2010,86(3): 528-532.
[22] Matamoros V, Duhec A, Albaiges J,etal. Photodegradation of carbamazepine, ibuprofen, ketoprofen and 17 alpha-ethinylestradiol in fresh and seawater[J]. Water Air and Soil Pollution, 2009,196(1-4): 161-168.
[23] Lam M W, Mabury S A. Photodegradation of the pharmaceuticals atorvastatin, carbamazepine, levofloxacin, and sulfamethoxazole in natural waters[J]. Aquatic Sciences, 2005,67(2): 177-188.
[24] Razavi B, Ben Abdelmelek S, Song W,etal. Photochemical fate of atorvastatin (lipitor) in simulated natural waters[J]. Water Research, 2011,45(2):625-631.
[25] Cermola F, DellaGreca M, Lesce M R,etal. Photochemical behavior of the drug atorvastatin in water[J]. Tetrahedron, 2006,62(31): 7 390-7 395.
[26] Werner J J, McNeill K, Arnold W A . Environmental photodegradation of mefenamic acid[J]. Chemosphere, 2005,58(10): 1 339-1 346.
[27] Mazellier P, Meite L, De Laat J. Photodegradation of the steroid hormones 17 beta-estradiol (E2) and 17 alpha-ethinylestradiol (EE2) in dilute aqueous solution[J]. Chemosphere, 2008,73(8): 1 216-1 223.
[28] 鐘明潔, 陳勇, 胡春. 水中安替比林的紫外光降解研究[J]. 環境工程學報, 2009(6): 1 049-1 053.
[29] 瑞恩 P. 施瓦茨巴赫,菲利普 M. 施格文, 迪特爾 M. 英博登.環境有機化學[M]. 王連生,譯. 北京:化學工業出版社,2003.
[30] Latch D E, Packer J L, Stender B L,etal. Aqueous photochemistry of triclosan: formation of 2,4-dichlorophenol, 2,8-dichlorodibenzo-p-dioxin, and oligomerization products[J]. Environmental Toxicology and Chemistry, 2005,24(3): 517-525.
[31] 劉鈺, 楊曦, 高穎. 撲熱息痛在硝酸根溶液中的光解研究[J]. 環境科學, 2007,28(6): 1 274-1 279.
[32] Zafiriou O C, True M B. Nitrite photolysis in seawater by sunlight[J]. Marine Chemistry, 1979,8(1): 9-32.
[33] Zepp R G, Hoigne J, Bader H. Nitrate-induced photooxidation of trace organic-chemicals in water[J]. Environmental Science & Technology, 1987,21(5): 443-450.
[34] Brezonik P L, Fulkerson-Brekken J. Nitrate-induced photolysis in natural waters: controls on concentrations of hydroxyl radical photo-intermediates by natural scavenging agents[J]. Environmental Science & Technology, 1998, 32(19): 3 004-3 010.
[35] Vione D, Khanra S, Man S C,etal. Inhibition vs. enhancement of the nitrate-induced phototransformation of organic substrates by the (OH)-O-center dot scavengers bicarbonate and carbonate[J]. Water Research, 2009, 43(18): 4 718-4 728.
[36] Canonica S, Jans U, Stemmler K,etal. Transformation kinetics of phenols in water - photosensitization by dissolved natural organic material and aromatic ketones[J]. Environmental Science & Technology, 1995, 29(7): 1 822-1 831.
[37] Richard C, Vialaton D, Aguer J P,etal. Transformation of monuron photosensitized by soil extracted humic substances: energy or hydrogen transfer mechanism? [J]. Journal of Photochemistry and Photobiology a-Chemistry, 1997, 111(1-3): 265-271.
[38] 高穎, 楊曦, 劉鈺. 在Suwannee河富里酸溶液中撲熱息痛的光解行為[J]. 環境化學, 2008, 27(4): 432-435.
[39] 高穎, 楊曦, 張金鳳. 腐殖質NAFA溶液中的撲熱息痛光解研究[J]. 環境保護科學, 2008, 34(3): 26-29.
[40] 鄧南圣, 吳峰. 環境光化學[M]. 北京:化學工業出版社,2003.
[41] Chiron S, Minero C, Vione D. Photodegradation processes of the Antiepileptic drug carbamazepine, relevant to estuarine waters[J]. Environmental Science & Technology, 2006, 40(19): 5 977-5 983.
[42] 陳勇, 張長波, 吳峰,等. 雌酮在鐵(Ⅲ)-草酸鹽配合物體系中的光降解[J]. 環境污染治理技術與設備, 2006, 7(3): 45-47.
[43] 劉先利, 鄧南圣, 徐棟,等. 含魚腥藻水溶液中17α-乙炔雌二醇光降解[J]. 重慶環境科學, 2003, 25(8): 21-24.
[44] 葛利云, 鄧歡歡, 吳峰, 等, 普通小球藻引發水中17β-雌二醇的降解[J]. 應用生態學報, 2004, 15(7): 1 257-1 260.

