吉西他濱脂質衍生物聚合物膠束的制備及其理化性質和抗腫瘤活性
左 靖,楊 明,李 淼,杜麗娜,金義光
(1.安徽醫科大學研究生學院,安徽合肥 230032;2.軍事醫學科學院放射與輻射醫學研究所藥物化學研究室,北京 100850;3.北京化工大學生命科學與技術學院,北京 100029)
吉西他濱脂質衍生物聚合物膠束的制備及其理化性質和抗腫瘤活性
左 靖1,2,楊 明3,李 淼2,杜麗娜2,金義光1,2
(1.安徽醫科大學研究生學院,安徽合肥 230032;2.軍事醫學科學院放射與輻射醫學研究所藥物化學研究室,北京 100850;3.北京化工大學生命科學與技術學院,北京 100029)
目的制備吉西他濱(Gem)脂質衍生物及其聚合物膠束,克服Gem體內易失活、不能口服和無靶向性的缺陷。方法合成N-苯甲酰-3′-乙酰吉西他濱(BAG)。用注入法制備載BAG的泊洛沙姆188膠束(BAG∶泊洛沙姆188=10∶1,mol/mol);用激光粒度和電位儀測定膠束的粒度和Zeta電位;膠束用負染法透射電鏡法觀察膠束微觀形態。Gem或BAG聚合物膠束5,10,20,30,50,70和90μmol·L-1與人乳腺癌細胞MCF-7培養24,48和72 h,用MTT法測定對MCF-7細胞生長的抑制率。肝癌細胞H22移植瘤小鼠分別iv或ig給予Gem 40 m g·kg-1或BAG聚合物膠束62 m g·kg-1,間隔2 d給藥1次,共3次,末次給藥后第2天處死小鼠,測定抑瘤率。結果經薄層色譜法、核磁共振氫譜和碳譜、紅外光譜和質譜驗證,BAG的結構正確。BAG聚合物膠束外觀為淡藍色乳光的透明溶液,粒徑為62.82 nm,Zeta電位為-18.8 m V,電鏡下呈現球狀均勻分布。MTT法實驗結果表明,Gem和BAG聚合物膠束分別與MCF-7細胞培養24,48和72 h,其抑制MCF-7細胞生長的IC50分別為40.6和90.0,5.0和14.9,5.0和13.6μm o l·L-1。體內實驗結果表明,Gem口服和注射組與模型對照組比較(P<0.01)、BAG聚合物膠束口服和注射組與泊洛爾姆188空白膠束組比較(P<0.05,P<0.01)均具有明顯的抑瘤作用;作用強度,BAG聚合物膠束口服優于Gem口服(P<0.05),BAG聚合物膠束注射優于其口服(P<0.05),BAG聚合物膠束注射與Gem注射作用相當。結論Gem脂質衍生物能載入泊洛沙姆188聚合物膠束內。BAG聚合物膠束體外對MCF-7細胞生長有抑制作用,iv和ig給藥對小鼠H22移植瘤均具有抑瘤作用。BAG聚合物膠束口服優于Gem口服,提示BAG聚合物膠束有望開發成為新型的抗腫瘤口服制劑。
吉西他濱;脂質衍生物;聚合物膠束;抗腫瘤藥
DO l:10.3867/j.issn.1000-3002.2014.03.017
目前,抗腫瘤藥物由于缺乏體內分布的特異性,在正常組織分布較多,致使毒性作用顯著。腫瘤組織血管內皮細胞間隙大,對生物大分子和納米顆粒的滲透性增強,同時腫瘤組織淋巴循環差,使滲透進入腫瘤的生物大分子及納米顆粒滯留增強,稱為增強滲透和滯留效應,成為腫瘤靶向納米系統設計的基礎[1-2],如脂質體[3-4]、納米粒[5-6]、納米脂質載體[7]和聚合物膠束[8-9]等。上市藥物如注射用紫杉醇脂質體(力樸素?)、鹽酸多柔比星脂質體注射液(格萊?)和注射用紫杉醇白蛋白納米粒(Abraxane?)均具有良好腫瘤靶向治療作用,減小了毒性作用。
核苷類藥物被細胞攝取后干擾DNA和RNA復制,使細胞代謝和增殖周期中斷,廣泛用于抗腫瘤治療。吉西他濱(gem citabine,Gem)是一線核苷類抗腫瘤藥,臨床上用于治療胰腺癌和乳腺癌等多種惡性腫瘤[10]。Gem進入細胞后經脫氧胞嘧啶核苷激酶磷酸化,轉化成具有活性的二磷酸核苷及三磷酸核苷發揮抗腫瘤作用。體內普遍存在的胞嘧啶核苷脫氨酶能將Gem迅速脫氨基化而失活。因此,減少或避免脫氨基化成為Gem衍生化研究的熱點[11]。本研究合成了Gem 脂質衍生物 N-苯甲酰-3′-乙酰吉西他濱(N-benzoy-3′-acetylgem citabine,BAG),制備載BAG的泊洛沙姆188(P188)膠束,測定其粒徑、表面電位及載藥量,評價其體內外抗腫瘤作用。
1 材料與方法
1.1 藥物、試劑和儀器
Gem,C9H11F2N3O4,純度99.6%,北京凱萊森醫藥科技有限公司,批號20110203,臨用前用生理鹽水溶解;苯甲酸酐、叔丁基二甲基氯硅烷、咪唑和三水合四丁基氟化銨(TBAF·3H2O)均購自北京偶合科技有限公司;乙酸酐,國藥集團化學試劑有限公司;乙酸(含量≥99.5%),國藥集團化學試劑有限公司;P188,德國巴斯夫公司;除HPLC分析所用試劑為色譜純外,其余試劑均為分析純;反應溶劑均經脫水處理。JNM-ECA-400型超導核磁共振儀,日本電子株式會社;LCQ Max型質譜儀,美國Finnigan公司;H-7650型透射電鏡,AMT cam era system,80 kV,日本Hitachi公司;Zetasizer Nano ZS型激光粒度和電位儀,英國Malvern公司;MinitroughⅡ型Langmuir膜天平,芬蘭KSV公司;L-2310型高效液相色譜儀,日本Hitachi公司;VenusilMP C18柱(5μm,250 mm×4.6 mm),天津博納艾杰爾科技有限公司。
1.2 細胞和動物
人乳腺癌MCF-7細胞來自北京化工大學。SPF級昆明小鼠45只,20~24 g,雄性,購自北京維通利華實驗動物技術有限公司,動物合格證號:SCXK(京)2012-0001。
1.3 吉西他濱脂質衍生化
Gem脂質衍生化主要在酰胺鍵和糖環上4位羥基進行脂質化,合成步驟參考阿糖胞苷衍生化路線[12]。具體反應過程如下:稱取Gem 0.2638 g(1 mmol)溶于50 m L乙醇,80℃攪拌回流5 m in,加苯甲酸酐0.2728 g(1.2 mm o l)繼續反應1 h,以后每小時加入苯甲酸酐1.2 mm ol,共加3次,最后1次加入后,繼續回流反應1 h。旋蒸除去溶劑后得粗產物。用二氯甲烷溶解粗產物后在硅膠柱上分離,收集帶有產物點的洗脫液,除溶劑,得N-苯甲酰-吉西他濱(N-benzoyl gemcitabine,BG)白色粉末,產率71%。取BG 0.1835 g(0.5 mmol)、咪唑0.1126 g(1.6 mm ol)溶于6 m L N,N-二甲基甲酰胺,加入叔丁基二甲基氯硅烷0.1388 g(0.9 mm ol),加干燥管后室溫攪拌72 h,加入6 m L甲苯共沸,除溶劑,得透明油狀物。用體積分數2%甲醇氯仿溶液溶解油狀物后,在硅膠柱上分離,收集帶有產物點的洗脫液,除溶劑,得N-苯甲酰-4-叔丁基二甲基硅烷吉西他濱(N-benzoyl-4-tert-butyl dimethyl silyl gem citabine,BTG)白色顆粒。BTG 0.2112 g(0.4 mm o l)溶于12 m L無水吡啶,加乙酸酐(5.3 m L)室溫攪拌24 h,除溶劑,殘渣用體積分數2%甲醇氯仿溶液溶解后柱層析純化,得N-苯甲酰-3′-乙酰-4-叔丁基二甲基硅烷吉西他濱(N-benzoyl-3′-acetyl-4-tert-butyl dimethyl silyl gem citabine,BATG)白色糊狀物。取TBAF·3H2O 1.5575 g(5 mmo l)溶于5 m L四氫呋喃。另取BATG 0.1511 g(0.28 mm o l)溶于上述TBAF溶液中,室溫反應10 m in后,加入乙酸0.1 m L,繼續攪拌2 h,除溶劑,得淡黃色油狀物,在硅膠柱上分離,得終產物N-苯甲酰-3′-乙酰吉西他濱(N-benzoy-3′-acetylgem citabine,BAG)白色粉末(圖1)。
1.4 吉西他濱脂質衍生物結構鑒定
1.4.1 色譜法
參照《中國藥典》第二部(2010版)附錄V B薄層色譜法,吸取BAG甲醇溶液和Gem水溶液10μL,點于硅膠G薄層板上,以氯仿∶甲醇(9∶1,V/V)為展開劑,展開至接近薄層板上緣處取出,晾干,在254 nm紫外燈下觀察物質斑點,計算比移值(Rf)。Rf=點樣原點至斑點中心距離/點樣原點至溶劑前沿距離。
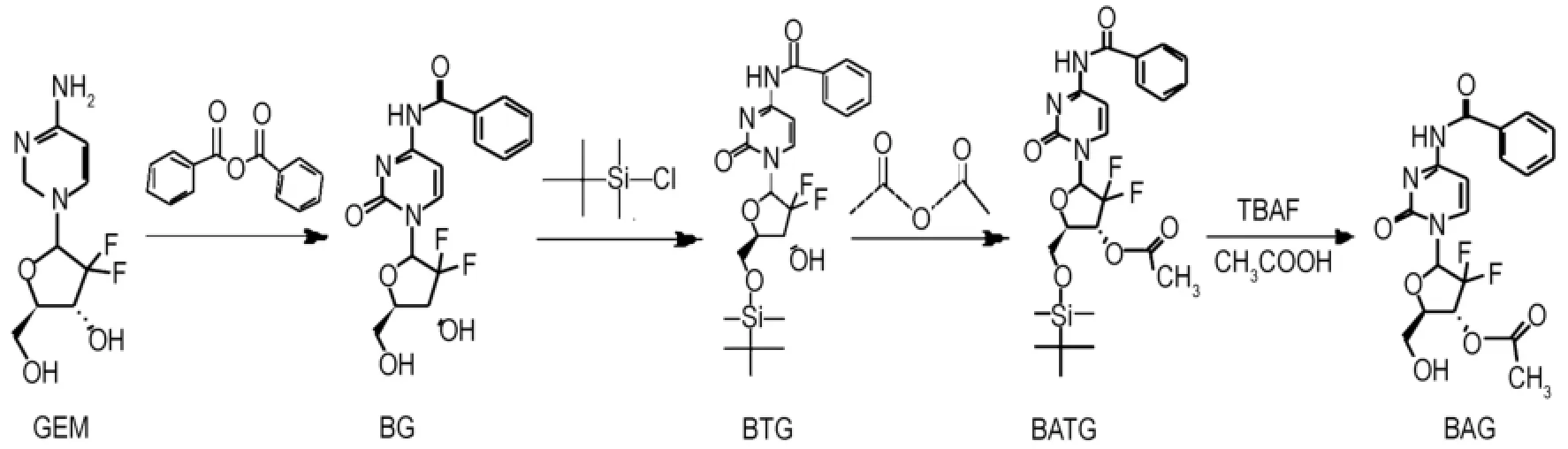
Fig.1 Synthetic route o f N-benzoy-3′-acetyl-gem citabine(BAG).Gem:gem citabine;BG:N-benzoyl gem citabine;BTG:N-benzoyl-4-tert-butyl dimethyl silylgem citabine;BATG:N-benzoyl-3′-acetyl-4-tert-butyldimethyl silylgem citabine;BAG:N-benzoy-3′-acetyl-gem citabine.
1.4.2 光譜法
取BAG 20 mg·L-1甲醇溶液和Gem 20 mg·L-1水溶液,依《中國藥典》第二部(2010版)附錄ⅣA紫外可見分光光度法檢測最大吸收波長。按照常規光譜檢測方法,對BAG進行核磁共振氫譜、核磁共振碳譜、紅外光譜和質譜的檢測。
1.5 BAG聚合物膠束制備和理化性質測定
取BAG 0.025 g和P188 0.050 g(BAG∶P188=10∶1,m o l/m o l)溶于5 m L四氫呋喃中,得到5 g·L-1的BAG四氫呋喃溶液,取2 m L用100μL的微量注射器分次注入到渦旋振蕩的2 m L水中,37℃水浴加熱除去溶劑和部分水分。用2%磷鎢酸溶液對膠束進行負染,透射電鏡觀察聚合物膠束微觀形態。用激光粒度儀測定聚合物膠束粒徑分布和Zeta電位。空白聚合物膠束制備同上,只注入含P188的乙醇/四氫呋喃(5∶1,V/V)溶液到水中,水浴加熱除溶劑。
1.6 測定BAG聚合物膠束載藥量
建立HPLC法測定BAG。色譜條件如下:VenusilMP C18柱(5μm,250 mm×4.6 mm);柱溫:30℃;流動相:甲醇∶水(90∶10,V/V);流速:1 m L·m in-1;進樣量:20μL;檢測波長:261 nm。BAG的保留時間為4 m in。取5 mg BAG溶于5 m L THF,得1 g·L-1BAG標準貯備液,用甲醇稀釋至0.5,1,10,20,50,70和100 mg·L-1。以峰面積(A)對濃度(c)作圖,標準曲線方程為A=74337c-37047(R2=0.999)。將BAG聚合物膠束用甲醇稀釋100倍,過0.22μm濾膜,取續濾液,測定聚合物膠束中BAG含量。BAG聚合物膠束的載藥量(%)=〔BAG(m g)/BAG(m g)+P188(mg)〕×100%。
1.7 BAG聚合物膠束體外抑瘤活性評價
將人乳腺癌細胞MCF-7用DMEM培養液稀釋至1×107L-1,接種于3塊96孔板,每孔200μL,于5%CO2,37℃飽和濕度培養箱培養24 h后,加入不同濃度Gem水溶液和BAG膠束溶液,兩者分別以水和空白聚合物膠束溶液作為對照。Gem和BAG聚合物膠束的終濃度分別為5,10,20,30,50,70和90μmol·L-1。培養24,48和72 h后,除去培養液,每孔加MTT溶液20μL,4 h后加150μL二甲亞砜溶液溶解,于酶標儀590 nm處測各孔A590nm,計算細胞生長抑制率[13]。抑制率(%)=(對照組A590nm-實驗組A590nm)/對照組A590nm×100%。
1.8 BAG聚合物膠束體內抑瘤活性評價
無菌條件下抽取荷肝癌細胞H22小鼠腹水,生理鹽水稀釋至2×1010L-1。小鼠皮下接種0.2 m L H22細胞于右前側腋下,7 d后腋下有隆起腫瘤硬塊即為建模成功。取腫瘤大小均勻的小鼠,隨機分為6組,模型組(iv給予等體積生理鹽水)、模型+P188空白膠束組(尾靜脈iv,40 m g·kg-1)、模型+Gem注射組(尾靜脈iv,40 m g·kg-1)、模型+Gem口服組(ig,40 mg·kg-1)、模型+BAG聚合物膠束注射組(尾靜脈iv,62 mg·kg-1,與Gem 40 mg·kg-1等量)和模型+BAG聚合物膠束口服組(ig,62 mg·kg-1),每組6只。間隔2 d給藥1次,共3次。末次給藥后第2天處死,取出腫瘤,稱瘤濕重,計算抑瘤率。抑瘤率(%)=(正常對照組平均瘤重-給藥組平均瘤重)/正常對照組平均瘤重×100%。
1.9 統計學分析
2 結果
2.1 BAG結構確認
BAG的氫譜、碳譜、紅外光譜和質譜結果如下:1H NMR(400 MHz,DMSO-d6)δ(ppm):2.100(s,3H,O-CO-CH3),4.356(s,1H,OH),5.768(t,1H),7.510-7.548,8.005-8.026(m,6H,5-CH,苯基),8.001(s,1H,NH),11.448(t,1H);13C NMR(100 MHz,DMSO-d6)δ(ppm):21.0(CH3),59.0(-CH2OH),121.5(-CF2-),128.5-133.0(苯基),167.3,169.1(-CO-);FT-IR(KBr,cm-1):3489.4(-CH2OH),3387.7(C-NH);3143.4-3077.2,840.7,710.5(=CH),2964.2-2941.8(CH2,CH3),1749.9(-COO-),1712.6(-CO-),1656.9(-CO-NH-);ESI-MS(+)m/z:410.11(M+H)+,432.15(M+Na)+;ESI-MS(-)m/z:408.10(M-H)+。BAG是在Gem氨基基團和糖環4-OH上分別連接苯甲酰和乙酰基。因為BAG的1H NMR,13C NMR及紅外光譜均顯示有甲基基團、-CO-NH-基團和苯環特征峰,表明BAG合成成功。
薄層色譜法驗證BAG的Rf為0.8,而Gem的Rf為0,前者呈較強非極性,與其結構相對應。BAG的最大吸收波長為261 nm,而Gem為258 nm。兩者相近又不同,表明它們的母核相同,但具體結構不同。
2.2 BAG聚合物膠束的理化性質
BAG是脂溶性分子,可插入P188膠束的疏水性內核中。透射電鏡顯示,BAG聚合物膠束呈球狀,分布均勻(圖2)。BAG聚合物膠束粒徑為62.82 nm,分布較均勻(圖3A);Zeta電位為-18.8 m V(圖3B)。雖然BAG聚合物膠束的表面電位較小,但聚合物膠束外層為長鏈的聚氧乙烯,阻止了膠束聚集和融合,保證了穩定性。BAG聚合物膠束載藥量為(32.83±1.15)%,可滿足給藥需求。
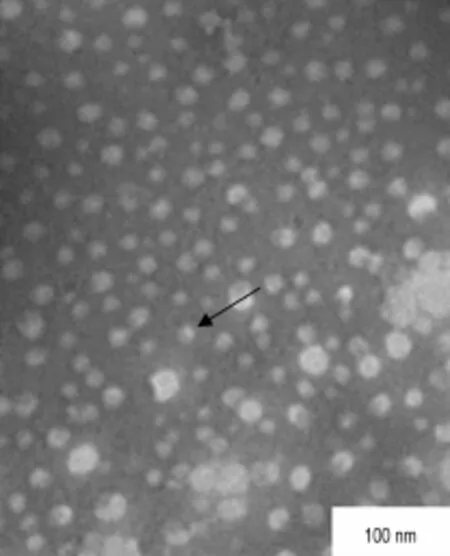
Fig.2 Negatively-stained transm ission elec tron m icroscope image o f BAG po lymeric m icelles.The arrow shows BAG polymeric m icelles.The morphology of BAG polym eric m icelles was spheres and m icelles distributed evenly.
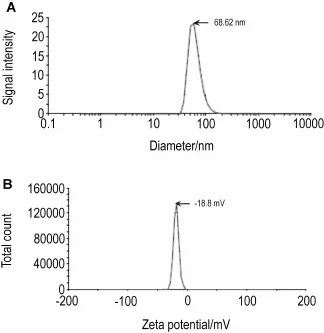
Fig.3 Size d istribu tion(A)and zeta po ten tia l(B)o f BAG po lym eric m icelles.The measurement was performed on Malvern Zetasizer Nano ZS using the laser dynam ic light scattering m ethod.The peak of num ber m ode size distribution was 68.62 nm.The zeta potentialwas 18.8 m V.
2.3 BAG聚合物膠束體外對人乳腺癌MCF-7細胞的抑制作用
MTT實驗結果(圖4)表明,Gem或BAG聚合物膠束0~90μmol·L-1(0濃度的BAG聚合物膠束表示空白聚合物膠束)與人乳腺癌細胞MCF-7培養24,48和72 h,抑制細胞生長的IC50分別為40.6和90.0,5.0和14.9,5.0和13.6μmol·L-1,表明Gem體外對MCF-7細胞生長的抑制作用強于BAG聚合物膠束。另外,空白聚合物膠束在72 h內的細胞抑制率均<10%,表明空白膠束的細胞毒性很小,BAG聚合物膠束對MCF-7細胞抑制作用主要來源于BAG分子。

Fig.4 lnhibition o f BAG po lymeric m icelles and Gem so lu tion on MCF-7 cells in cubated fo r 24(A),48(B)and 72 h(C).,n=3.*P<0.05,**P<0.01,compared with BAG polym eric m icelles group of the same concentration.
2.4 BAG聚合物膠束體內對肝癌細胞H22移植瘤小鼠的抗腫瘤作用
由表1可見,① 與模型對照組比較,模型+P188空白膠束(iv)、模型+Gem口服和模型+Gem注射組瘤重明顯減輕(P<0.01);與模型+P188空白膠束(iv)組比較,BAG聚合物膠束口服和注射組瘤重亦明顯減輕(P<0.05,P<0.01);表明P188空白膠束、Gem口服和注射及BAG聚合物膠束口服和注射對H22移植瘤均具有明顯的抑瘤作用。②與模型+Gem口服組比較,模型+BAG聚合物膠束口服組瘤重減輕(P<0.05),抑瘤率達47.1%,表明BAG聚合物膠束口服抑瘤作用強于Gem口服給藥。③與模型+BAG聚合物膠束口服組比較,BAG聚合物膠束注射給藥抑瘤作用更明顯(P<0.05)。④與模型+Gem注射組比較,模型+BAG聚合物膠束注射組瘤重無顯著性差異,兩組抑瘤率均達到80%以上,表明BAG聚合物膠束靜脈給藥其抑瘤作用與Gem相當。
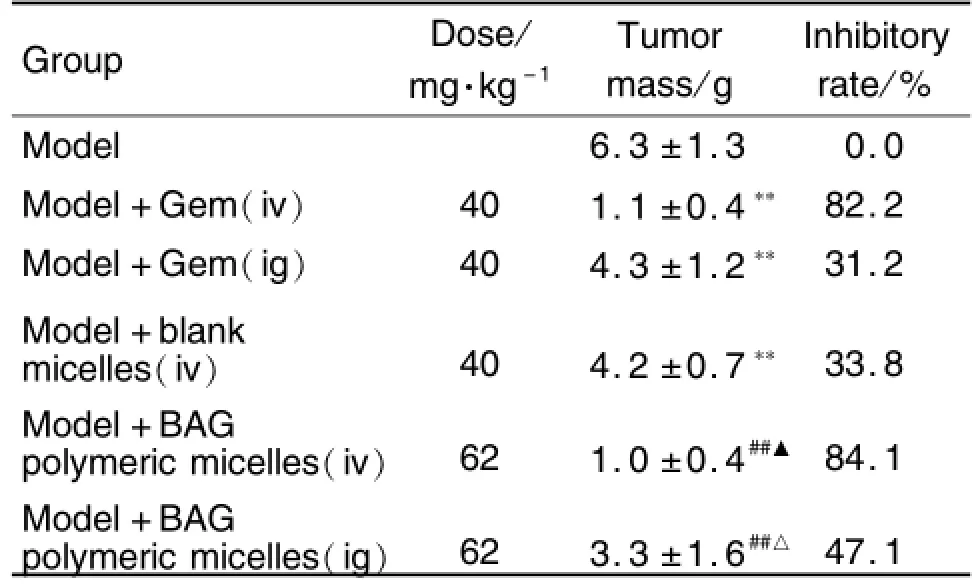
Tab.1 Tum o r inhib ition o f BAG po lym eric m ice lles and Gem on hepatoma cells H22xenograft in m ice
3 討論
本研究設計并合成了Gem脂質衍生物BAG,用注入法制備得到高度分散、均勻的含P188的BAG聚合物膠束。聚合物膠束常采用透析法[14-15]、薄膜分散法[16]和固體分散法[17]等方法制備。透析法制備時間長,換液頻繁,藥物易泄漏;因脂質衍生物形成的膜親水性差,不易分散于水,所以用薄膜分散法制備也比較困難;固體分散法對藥物和載體要求較高,不易實現。本研究采用本實驗室經典的渦旋注入法[18-19],能有效分散藥物,可得到均勻混懸液,且耗時短,工藝簡單。一般認為粒子的zeta電位絕對值大于30 m V時,由于靜電相斥作用使體系較穩定。雖然載BAG的P188膠束zeta電位為-18.8 m V,但泊洛沙姆結構中親水性聚氧乙烯長鏈有利于膠束穩定,減少了聚集和融合。
體外實驗結果表明,Gem和BAG聚合物膠束與MCF-7細胞作用48和72 h,在濃度<30μmol·L-1時,BAG聚合物膠束對MCF-7細胞的抑制作用明顯小于Gem;但當濃度>30μmo l·L-1時,BAG聚合物膠束對MCF-7細胞的抑制作用與Gem相當。因此推測,BAG聚合物膠束發揮細胞毒性作用必須達到一定時間和濃度。一定時間是指有足夠時間BAG可解離成Gem,一定濃度指有足夠量Gem的產生。該結果也證明了BAG必須生成Gem后才能發揮對MCF-7細胞生長的抑制作用。同時表明,BAG可能會產生緩釋效應。由于細胞培養液中酶很少,使BAG的降解緩慢。BAG進入體內后,酶活性較強,可能較快釋放出活性分子。同一濃度BAG聚合物膠束在48和72 h藥效均明顯高于24 h,說明BAG聚合物膠束有緩釋作用,這是其優勢之一。
據報道,H22荷瘤雌性小鼠腫瘤重量和體積均明顯大于雄性小鼠[20],為充分體現藥效,避免腫瘤體積過大,本研究體內抑瘤實驗選用雄性小鼠。研究結果表明,P188空白膠束靜脈注射后也具有一定抑瘤作用,這主要是由于泊洛沙姆作為非離子型表面活性劑,能增加細胞膜流動性、消耗ATP并抑制藥物外排有關[21]。載藥后,抑瘤作用進一步增強。靜脈注射給藥時,BAG聚合物膠束抑瘤作用與等劑量Gem相當,口服給藥時抑瘤作用明顯優于Gem口服給藥。目前臨床上Gem不能口服,原因是藥物很容易在胃腸道中失活。而Gem脂質衍生化后,不存在脫氨基反應,因此可能增加了藥物的胃腸道吸收。BAG聚合物膠束口服給藥時,藥效雖不及注射給藥,但仍有一定抑瘤作用,這為Gem脂質衍生物口服給藥應用提供了實驗依據。給藥前隨機分組,給藥后小鼠體質量均有所增加,但無統計學差異(數據略),表明BAG聚合物膠束毒性較小。
目前Gem上市制劑為其鹽酸鹽注射劑,無法口服。Gem注射劑在體內降解快,毒性大,患者依從性差。口服BAG聚合物膠束有較明顯抑瘤作用,為基于Gem的藥物治療提供了口服給藥可能。下一步將改進Gem衍生化路線,以增強口服給藥效果且達到緩釋目的,同時研究其體內藥動學特征。本研究為Gem的腫瘤靶向治療和制備口服制劑提供了一種新思路,有較好的臨床應用前景。
[1] Maeda H.The enhanced perm eability and reten-tion(EPR)effect in tumor vasculature:the key role of tumor-selectivemacromolecular drug targeting[J].Adv Enzyme Regul,2001,41:189-207.
[2] Mitra S,Gaur U,Ghosh PC,Maitra AN.Tum our targeted de livery o fencapsulated dextran-doxorubicin con jugate using chitosan nanoparticles as carrier[J].J Control Release,2001,74(1-3):317-323.
[3] Paolino D,Cosco D,Racanicchi L,Trapasso E,Celia C,Iannone M,et al.Gem citabine-loaded PEGylated unilamellar liposomes vs GEMZAR:biodistribution,pharmacokinetic features and in vivo antitumor activity[J].J Control Release,2010,144(2):144-150.
[4] Du B,LiY,Li X,A Y,Chen C,Zhang Z.Preparation,characterization and in vivo evaluation of 2-methoxyestradiol-loaded liposom es[J].Int J Pharm,2010,384(1-2):140-147.
[5] She W,Li N,Luo K,Guo C,Wang G,Geng Y,et al.Dendronized heparin-doxorubicin con jugate based nanoparticle as pH-responsive drug delivery system for cancer therapy[J].Biomate ria ls,2013,34(9):2252-2264.
[6] Fadel M,Kassab K,Fadeel DA.Zinc phthalocyanine-loaded PLGA biodegradab le nanoparticles for photodynam ic therapy in tumor-bea ring m ice[J].Lasers Med Sci,2010,25(2):283-292.
[7] Liu L,Tang Y,Gao C,LiY,Chen S,Xiong T,et al.Charac terization and biodistribution in vivo of quercetin-loaded cationic nanostructured lipid carriers[J].Colloids Surf B Biointerfaces,2014,115:125-131.
[8] Mu CF,Balakrishnan P,Cui FD,Yin YM,Lee YB,ChoiHG,et al.The effects ofm ixed MPEGPLA/Pluronic copolymer m icelles on the bioavailability and multidrug resistance of docetaxel[J].Biomaterials,2010,31(8):2371-2379.
[9] Coimbra M,Rijcken CJ,Stigter M,Hennink WE,Storm G,Schiffelers RM.An titumor efficacy of dexamethasone-loaded core-crosslinked polymeric m icelles[J].J Control Release,2012,163(3):361-367.
[10] W ang XJ.Progerss on clinical research of cem citabine[J].J Oncol(腫瘤學雜志),2005,11(1):69-71.
[11] Moysan E,Bastiat G,Benoit JP.Gem citabine versus Modified Gem citabine:a review of several prom ising chem icalmodifications[J].Mol Pharm, 2013,10(2):430-444.
[12] Alexander RL,Morris-Natschke SL,Ishaq KS,Flem ing RA,Kucera GL.Synthesis and cytotoxic ac tivity of two novel 1-dodecylthio-2-decyloxypropyl-3-phosphatidic acid conjugates with gemcitabine and cytosine arabinoside[J].JMed Chem,2003,46(19):4205-4208.
[13] Wei M,Xiao Y.Nephrotoxicity o f gem citabine on human breast cancer cell MCF-7 and human ermbryonic kidney cell 293 in vitro[J].Chin Hosp Pharm J(中國醫院藥學雜志),2011,31(8):632-635.
[14] Sezgin Z,Yüksel N,Baykara T.Preparation and characterization of polymeric m icelles for solubilization of poorly soluble anticancer drugs[J].Eur J Pharm Biopharm,2006,64(3):261-268.
[15] Shiraishi K,Kawano K,Minowa T,Maitani Y,Yokoyama M.Preparation and in vivo imaging o f PEG-poly(L-lysine)-based polymeric m icelle MRI contrastagents[J].JContro lRelease,2009,136(1):14-20.
[16] Wei Z,Hao J,Yuan S,Li Y,Juan W,Sha X,e t al.Paclitaxel-loaded Pluronic P123/F127 m ixed po lymeric m icelles:formulation,optim ization and in vitro cha racterization[J].Int J Pharm,2009,376(1-2):176-185.
[17] Song L,Shen YY,Hou JW,Lei L,Guo SR,Qian CY.Polymeric m ice lles for parente ral delivery o f cu rcum in:Preparation,cha racterization and in vitro evaluation[J].Colloid Surf A:Physicochem Engin Asp,2011,390(1-3):25-32.
[18] Jin Y,Xin R,Tong L,Du L,Li M.Combina tion an ti-HIV therapy w ith the self-assemblies of an asymmetric bolaamphiphilic zidovudine/didanosine prodrug[J].Mol Pharm,2011,8(3):867-876.
[19] Jin Y,Yang F,Du L.Nanoassemblies containing a fluorouracil/zidovudine glyceryl p rodrug w ith phospholipase A2-triggered drug release for cancer treatment[J].Colloids Surf B Biointerfaces,2013,112:421-428.
[20] Chen RT,Chen B,Xia Y,Yue F,Wang Q.Effects of gender on the grow th of tum or in m ice loaded w ith H22liver cance r[J].Chin Occup Med(中國職業醫學),2008,35(4):283-285.
[21] Dumortier G,Grossiord JL,Agnely F,Chaumeil JC.A review of poloxamer 407 pharmaceuticaland pharmacological characteristics[J].Pharm Res,2006,23(12):2709-2728.
Preparation,physicochem ical p roperties and an ti-tum or activity o f po lym eric m icelles o f one gem citabine lip id derivative
ZUO Jing1,2,YANG M ing3,LIM iao2,DU Li-na2,JIN Yi-guang1,2
(1.Graduate Schoo l,AnhuiMedical University,He fei 230032,China;2.Departm ent o f Pharm aceutica l Sciences,Institute o f Radiation Medicine,Academ y o f M ilitary Medical Sciences,Beijing 100850,China;3.Co llege o f Life Science and Technology,Beijing University o f Chem ica l Techno logy,Beijing 100029,China)
OBJECTlVE To prepare a lipid derivative of gem citabine(Gem)and its polymeric m icelles to overcome the disadvantages of Gem.METHODS N-benzyl-3′-acetyl-gemcitabine(BAG)was synthesized.A BAG-loaded poloxamer polymeric m icelle(BAG∶poloxamer 188=10∶1,mol/mol)was p repared using an in jection method.The m icelles were characterized w ith a laser partic le size and e lectric charge instrum ent and negative ly-stained transm ission e lectron m icroscopy.Human breast cancer ce lls MCF-7 were cu ltured w ith Gem or BAG po lym eric m ice lles o f 5,10,20,30,50,70,90μmo l·L-1for 24,48 and 72 h,respective ly.The inhibitory rate o f ce lls was m easured w ith an MTT m ethod.The MCF-7 cytotoxicity of BAG po lym eric m ice lles was investigated.A pharmacodynam ic study was performed on the m ice bearing mouse hepatocellular cancer cells H22.Intravenous(iv)and oral(ig)adm inistration was used at the dose ofGem 40 mg·kg-1or BAG polymericm icelles 62 mg·kg-1.The m ice were adm inistered on the 1st,4th and 7th day and sacrificed on the 8th day.Tumor inhibitory rates were m easured.RESULTS The BAG structure was identified by thin layer chrom atograph,1H and13C NMR,in frared ray chromatograph and mass spectrum.The appearance of BAG m ice lles was a slightly b lue suspension.The m ice lles were spheres according to the electron m icroscopic observation.Their size was 62.82 nm and the zeta potentia l was-18.8 m V.The half inhibition concentration(IC50)o f Gem and BAG po lymeric m icelles was 40.6 and 90.0μm o l·L-1,5.0 and 14.9μm ol·L-1,5.0 and 13.6μmol·L-1at24,48 and 72 h,respectively according to the MTT results.According to the in vivo results,compared w ith the tumormodel group,Gem(ig),Gem(iv)and BAG polymeric m icelles(iv and ig)had significanteffecton the tumorweightofH22cellxenograftm ice(P<0.01).As foranti-tumor efficiency,BAG polymericm icelles(ig)were better than Gem(ig)(P<0.05);BAG polymeric m icelles(iv)were better than BAG po lym eric m ice lles(ig)(P<0.05),and BAG po lym eric m ice lles(iv)were a lm ost equal to Gem(iv).CONCLUSlON The lipid derivative o f Gem can be loaded in the po loxam er 188 po lym eric m ice lles.BAG po lym eric m ice lles show in vitro MCF-7 ce ll inhibition and in vivo inhibition o fmouse H22xerogra fts;iv or ig.BAG polym eric m ice lles(ig)show better anti-tum or effect than Gem(ig),indicating that BAG polym eric m ice lles are a p rom ising nove l anti-tum or ora l p reparation.
gem citabine;lipid derivatives;po lym eric m ice lles;antineop lastic agents
s:DU Li-na,Tel:(010)66930216,E-mail:dulina@188.com;JIN Yi-guang,Tel:(010)66931220,E-mail:jinyg@139.com
R979.1,R943
A
1000-3002(2014)03-0408-07
Foundation item:The pro jec t suppo rted by National Key Technologies R&D Program fo r New Drugs(2012ZX09301003-001-009);and Nationa l Natura l Science Foundation of China(81072598)
2014-01-28 接受日期:2014-05-19)
(本文編輯:齊春會)
國家科技重大專項(2012ZX09301003-001-009);國家自然科學基金(81072598)
左 靖(1988-),女,碩士研究生,主要從事靶向給藥新劑型研究;杜麗娜(1977-),女,博士,副研究員,主要從事納米靶向制劑和經皮給藥制劑研究;金義光(1973-),男,博士,研究員,博士生導師,主要從事分子藥劑學研究。
杜麗娜,E-mail:dulina@188.com,Tel:(010)66930216;金義光,E-mail:jinyg@139.com,Tel:(010)66931220

