垂盆草片提取工藝及制劑處方的研究
包汝潑, 梁 偉
(寧波天衡藥業股份有限公司, 浙江 寧波 315201)
垂盆草片提取工藝及制劑處方的研究
包汝潑, 梁 偉
(寧波天衡藥業股份有限公司, 浙江 寧波 315201)
目的 優化垂盆草片提取工藝及制劑處方。方法 采用正交設計法,以提取物中的槲皮素、山柰素和異鼠李素總量作指標,考察加水量、煎煮次數、煎煮時間對提取效果的影響;通過垂盆草中間體顆粒的引濕性和片劑的質量差異及崩解限度等質量指標選擇制劑處方。 結果 優選的提取工藝為加 10 倍量水煎煮 3 次, 每次 60 min; 處方組成為浸膏粉、微晶纖維素、聚維酮、微粉硅膠和硬脂酸鎂。結論 所選提取工藝及制劑處方科學合理,質量穩定。
垂盆草片;正交試驗;槲皮素;引濕性
垂盆草片收載在 《中國藥典》 1977 年版一部, 以景天科垂盆草經提取制備而成,具有清熱解毒、活血利濕之功效[1]。 本公司生產該品 種多年, 但因 原有標準要求比較低,中間浸膏粉無有效成分的控制,生產處方和參數設置也以經驗為主,沒有具體的量化,為了更好保證質量,使工藝流程更趨科學合理,本實驗對藥材提取和處方工藝進行優化,獲取最佳工藝條件。
1 儀器與試藥
1.1 儀器 Agilent1260 高效液相色譜系統 ( 美國安捷倫科技有限公司), RE-85Z旋轉蒸發儀 ( 上海醫械專 機廠),SHL-3 型高速攪拌濕法造粒機 ( 上海美陽機械發展有限公司); ZPS008 旋轉壓片機 (上海天祥健臺制藥機械有限公司); AE240 型電子天平 (中國梅特勒-托利多儀器廠)。
1.2 試藥 槲皮素對照品 (100081-200406)、 山柰素對照品 (0861-200002) 、 異 鼠 李 素 對 照 品 (110860-200205 ) 均為中國食品藥品檢定研究院提供,供含量測定用;垂盆草購自寧波市藥材股份有限公司,經檢驗符合 《中國藥典》2010 年版一部有關標準, 輔料購自正規醫藥企業, 乙腈等試劑符合色譜要求。
2 實驗方法和結果
2.1 垂盆草浸膏和藥材中成分測定[2]
2.1.1 色 譜條 件 diamonsil ODS 色 譜 柱 ( 250 mm×4.6 mm, 5 μm); 流動相為甲醇-0.4%磷酸 (48 ∶52); 檢測波長 360 nm; 體積流量 1.0 mL/min; 柱溫 30 ℃; 進樣量 10 μL。 此條件下, 垂盆草片中3 種指標性成分達到較好的分離效果, 分離度大于 1.5, 理論板數按槲皮素峰計算不低于3 000, 典型圖譜如圖 1。
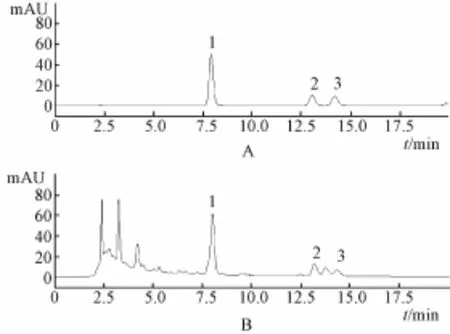
圖1 混合對照品溶液 (A) 和樣品溶液(B) 的 HPLC色譜圖
2.1.2 對照品溶液的制備 取槲皮素、 山柰素、 異鼠李素對照品適量, 精密稱定, 加甲醇制成每 1 mL各含 20 μg、 5 μg、 5 μg的混合溶液, 即得。
2.1.3 供試品溶液的制備 取浸膏或藥材約 0.5 g, 精密稱定, 加入甲醇-25%鹽酸溶液 (4 ∶1) 混合溶液 25 mL,稱定質量, 加熱回流 1 h, 放冷, 再稱定質量, 用甲醇-25%鹽酸溶液 (4 ∶1) 混合溶液補足減失的質量, 搖勻,濾過,取續濾液,即得。
2.1.4 線性關系考察 分別取 18.22 μg/mL的槲皮素、4.805 μg/mL的山柰素和 4.628 μg/mL的異鼠李素對照品溶液各 2.0、 5.0、 10.0、 20.0、 50.0 μL注入液相色譜儀測定, 以峰面積 A為縱坐標, 進樣量 C(μg) 為橫坐標,求得槲皮素、山柰素和異鼠李素回歸線性方程分別為:A槲皮素=4 250.4C-22.656 (r2=0.999 9), A山柰素=4 337.5 C-8.388 ( r2=0.999 5), A異鼠李素=4 156.5C-13.146(r2=0.997 1), 結 果表明槲 皮 素在進樣量 為0.036 44 ~0.911 1 μg范 圍 內 線 性 良 好、 山 柰 素 在 進 樣 量 為0.009 610 ~0.240 2 μg范圍內線性良好、 異鼠李素在進樣量為0.009 256 ~0.462 8 μg范圍內線性良好。
2.1.5 重復性試驗 稱取浸膏 (批號為 20120501) 樣品 6份, 按 “2.1.3” 項下制備供試品, 分別測定, 計算 RSD,結果槲皮素質量分數為 1.47 mg/g(RSD=0.9%), 山柰素質量分數為 0.19 mg/g(RSD=1.3%), 槲皮素質量分數為0.090mg/g(RSD=2.9%), 說明方法重復性良好。
2.1.6 加樣回收率試驗 以浸膏粉為例, 取 6 份 0.25 g左右的浸膏 (批號為 20120501), 精密稱定, 各加入槲皮素對照 品 (0.070 23 mg/mL)、 山 柰 素 對 照 品 (0.010 01 mg/mL) 和異鼠李素對照品 (0.004 628mg/mL) 混合液 5 mL, 混勻, 依法測定, 計算回收率和 RSD, 結果顯示槲皮素的平均回收率為 97.7% (RSD=0.8%), 山柰素平均回收率為 101.87% (RSD=2.2%), 異鼠李素的平均回收率為98.8% (RSD=2.3%), 表明本法符合定量測定的要求。
2.1.7 樣品的測定 按上述供試品制備方法制備后, 精密吸取溶液 10 μL, 注入液相色譜儀測定, 即得。
2.2 片重差異的測定 取藥片 20 片, 精密稱定, 求得平均片重后,再分別精密稱定每片的質量,每片重與平均片重相比較,計算超出質量的最大限度。
2.3 崩解時限和引濕性試驗的測定 參考 《中國藥典》2010 年版一部附錄崩解時限檢查法 (附錄 XIIA), 取素片6 片置吊籃玻璃管中, 于 (37 ±1)℃的恒溫水中, 按每 1 min 作 30 ~32 次上下移動, 記錄各片崩解成碎粒全部通過篩網的時間。
參考 《中國藥典》 2010 年版二部附錄引濕性試驗指導原則 (附錄 XIX J), 將混合好的粉末干燥至恒重后, 在已恒重的稱量瓶底部放入厚約1 mm的粉末,放置在溫度為(25 ±1)℃, 相對濕度為 64% ±2%的恒溫培養箱中保持 24 h后取出稱量,按該指導原則公式計算增重百分率。
2.4 提取工藝條件的篩選[3]
2.4.1 提取工藝的正交設計 根據大部分有效成分具有水溶性特點[4]及藥品注冊法規要求, 確定以水為提取溶媒,采用煎煮法提取, 并用 L9(34) 正交表安排試驗, 因素水平見表1。
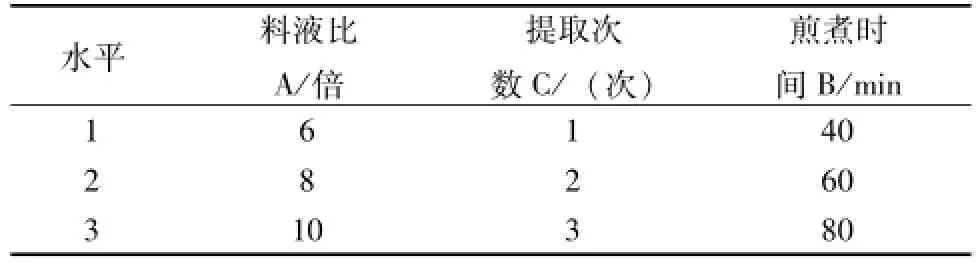
表1 因素水平
2.4.2 實驗安排及結果 根據實驗方案, 稱取處方量藥材, 先浸泡 30 m in, 然后按正交試驗表項下設計的試驗條件進行提取, 合并溶液, 減壓濃縮至浸膏相對密度 1.08 g/mL, 靜置 24 h, 離心, 取上清液濃縮至浸膏相對密度1.12 g/mL, 減壓干燥, 再按 “2.1” 項方法測定槲皮素、山柰素、 異鼠李素量,計算得率 (得率為浸膏中總量占投料藥材中總量的比例,按百分比計算),相同條件重復兩次實驗, 取平均值。 結果見表 2, 方差分析見表 3。
由方差分析表可知, 主次因素為 B>A>C,提取次數對成分提取有顯著性影響, 提取效果 B3>B3>B1, 由直觀分析得出最佳工藝為 A3B3C3, 考慮煎煮時間每次 80min 與每次 60min 相差不大, 煎煮時間太長一方面消耗能源, 一方面易破壞其他不穩定成分,所以最終確定提取工藝為A3B3C2, 即 加 10 倍量 水 , 提取 3 次, 每次煎煮 60 min。
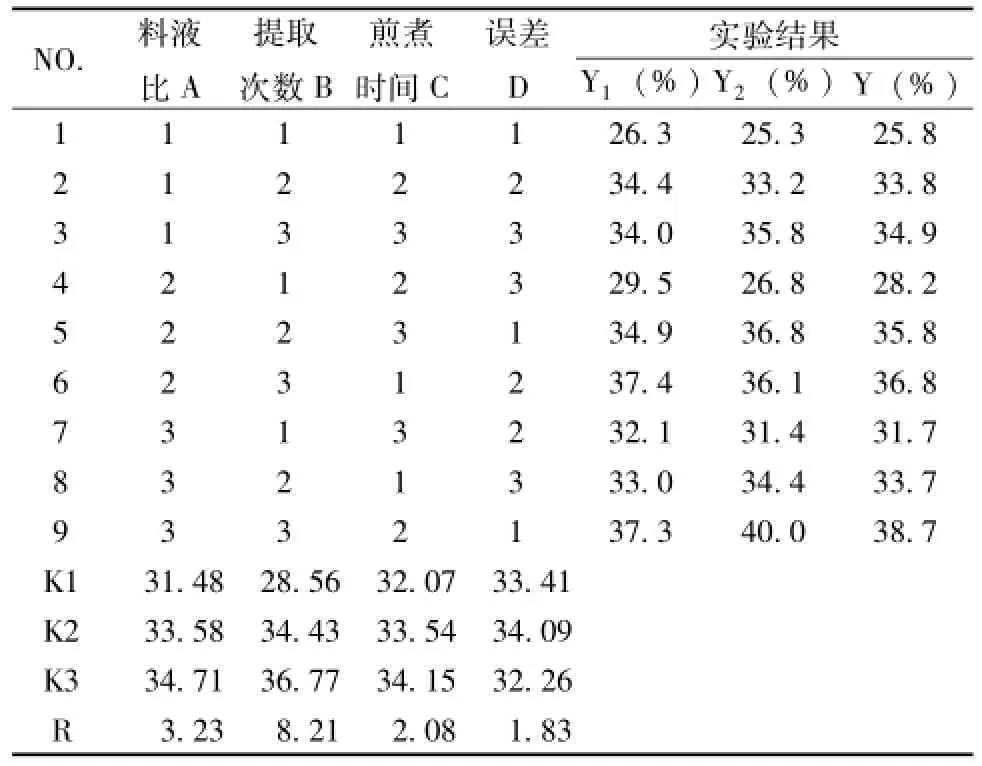
表2 提取工藝正交試驗方案及結果

表3 結果的方差分析
2.5 設備的改造[5]垂盆草浸膏粉制粒時黏合劑加入過度集中易致局部過濕,會產生大量團塊不能整粒過篩,如果通過加高乙醇體積分數,既提高了生產成本又降低了生產安全性,非最佳方法,本實驗采用噴霧法造粒,將噴嘴安裝到造粒鍋頂部,用壓力罐將黏合劑以噴霧形式噴入造粒鍋中,溶液被霧化分散到物料上,制粒過程沒有成團現象,顆粒的均勻性和流動性都有很大的改善。
2.6 處方的篩選[6]按表 4 處方比例稱取浸膏粉與輔料共2 kg左 右 , 倒入 高 速攪拌濕 法 造 粒 機 中 混 勻, 加 入 80%乙醇的 PVP黏合劑, 按規定時間攪拌制軟材, 20 目篩濕整,60 ℃烘箱干燥后整粒, 外加硬脂酸鎂混合 (取一部分做引濕性實驗) , 壓片 ( 以 浸 膏 粉 計 算 為 0.32 g/片) , 檢 查 素片的重量差異和崩解度, 記錄數據, 統計結果見表5。
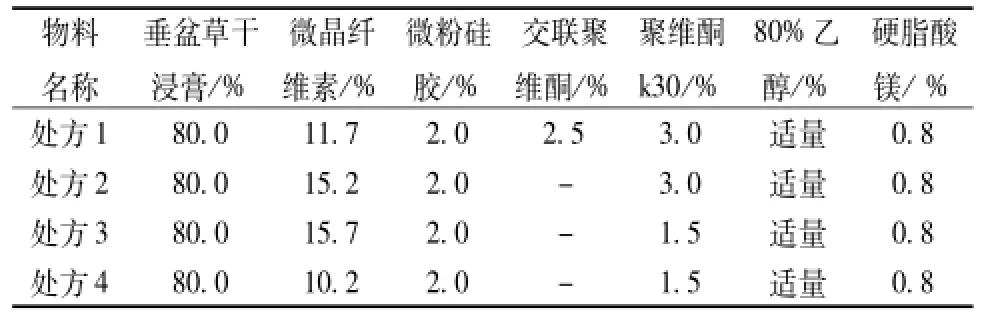
表4 不同處方組成
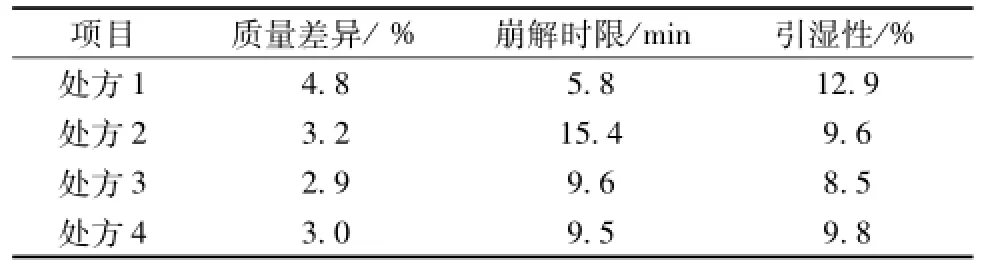
表5 不同處方的樣品質量數據比較
從表5各組試驗數據可見,處方1加了交聯聚維酮增加了引濕性,并且在壓片中出現了粘沖現象,不利于大規模生產, 處方2崩解時限最長, 易致崩解不合格, 處方3、4都符合質量要求,考慮到中藥糖衣片服用量比較多,處方4在保證質量的前提下,相對片重比較輕,服用量小,生產成本也降低,因此確定處方4為最終處方。
2.7 工藝驗證 根據試驗篩選結果, 進行 3 批 40 萬片規模的生產驗證生產,結果3批浸膏的黃酮提取率分別為38.9%、 40.2%和 38.2%, 片劑生產過程中各項指標符合要求,沒有出現粘沖和崩解不合格等現象,表明優化所得工藝穩定、可靠。
3 討論
3.1 垂盆草苷具有明顯的保肝作用, 常作為垂盆草質量指標成分[7], 本實驗也曾以垂盆草苷作為含量測定成分, 但實踐中發現其作為水溶性氰苷類化合物,極不穩定,受熱易分解, 各批提取物中含量相差達10倍, 很難客觀反映制劑的質量。 后據文獻報道[8]垂盆草中黃酮類成分也有保肝作用,性質相對穩定,檢測方法也被藥典收錄,所以采用黃酮成分作為質量控制指標。
3.2 在進行提取工藝優化時, 為了減少各種不明原因及儀器操作引起的誤差,提高實驗結果的精度和可信度,在盡量平衡的操作基礎上各試驗做兩次,數據取兩者均值。同時在實驗中發現浸膏粉對片劑崩解影響也較大,主要是提取液濃縮時,表面產生的藥液膜一定要過濾去除,否則易造成片劑崩解不合格。
3.3 制粒工序是中藥片劑工藝的關鍵步驟, 粘沖、 崩解時限超標和壓片頂裂等現象往往與制備的顆粒好壞有關[9],本實驗對制粒的關鍵因素如黏合劑的種類、用量和攪拌時間等因素也進行了優化。
3.4 本品目前還是糖漿包衣, 生產工藝復雜, 操作過程中大多依賴操作者憑手感控制包衣質量, 與 GMP精神不符,糖衣中的蔗糖成分同時限制了一部分患者的服用[10], 本部門正在做相關研究擬用薄膜包衣來取代糖衣,以解決上述問題。
[ 1 ] 宋玉華, 李春雨, 鄭 艷.垂盆草的研究進展[J].中藥材, 2010, 33(12): 1973-1975.
[ 2 ] 國家藥典委員會.中華人民共和國藥典: 2010 年版一部[S].北京: 中國醫藥科技出版社, 2010: 198-199.
[3] 玄 律,倪 健.多指標優選醒目顆粒水提醇沉制備工藝[J].中成藥, 2010, 32(7): 1238-1240.
[ 4] 邵成雷.垂盆草化學成分及其藥理臨床研究[D].濟南:山東大學, 2006.
[5] 胡功允,彭俊清,余 慧.鹽酸非索非那定鹽酸偽麻黃堿緩釋片處方工藝研究[J].中國現代應用藥學, 2011, 28(9): 846-849.
[6] 孫淑萍,吳少云,李勝利,等.婦科復方抗菌消炎泡騰片的成型工藝研究[J].中成藥, 2013, 35(2): 423-426.
[7] 潘金火,何滿堂,羅 蘭.垂盆草藥材質量控制方法研究[J].成都中醫藥大學學報.2002, 25(1): 44-55.
[8] 潘金火, 潘 萍.垂盆草總黃酮中8種單體成分對肝細胞的保護作用[J].中國醫院藥學雜志, 2010, 30 (19):1621-1623.
[ 9 ] 高愛國.淺談片劑制粒工藝控制[J].齊魯藥事, 2009,28(3): 187-188.
[10] 劉利清, 胡佳文.復方丹參片薄膜包衣工藝研究[J].中國藥業, 2010, 19(5): 37.
R284.2
: B
: 1001-1528(2014)03-0646-04
10.3969/j.issn.1001-1528.2014.03.048
2013-04-12
包汝潑 (1976—) , 男, 碩士, 高級工程師, 從事新藥研究。 E-mail: brp168@163.com

