MicroRNA調控腫瘤耐藥的研究進展
林高陽 綜述 徐克 審校
1 腫瘤細胞的耐藥性
惡性腫瘤是嚴重威脅人類健康的常見病及多發病,1943年,耶魯大學的Gilman等[1]首先將氮芥應用于淋巴瘤的治療,揭開了現代腫瘤化療的序幕。隨后新的抗腫瘤藥物不斷出現,化療成為腫瘤主要的治療方法之一,但是如同細菌易對抗生素產生耐藥性一樣,腫瘤細胞也常對化療藥物產生耐藥性,而且更為普遍,成為導致化學治療失敗的主要原因之一。因此腫瘤耐藥是腫瘤治療急需解決的關鍵問題之一。
腫瘤細胞群體具有內在的、高度有序發展的抗藥能力,無論是細胞毒類藥物還是靶向藥物,均未能克服耐藥問題。腫瘤的耐藥性是影響化療療效和腫瘤根治的主要原因,至今僅有少數組織來源的晚期腫瘤,可以通過藥物治愈,而且即使是這些腫瘤,也可能復發并發生耐藥。腫瘤細胞的耐藥性包括原發性耐藥(intrinsic resistance)和獲得性耐藥(acquired resistance)[2]。原發性耐藥亦稱天然性耐藥、內在性耐藥,指腫瘤的耐藥性是天然的,在腫瘤細胞用藥之前就已經存在,化學治療對這些腫瘤的療效較差;多數腫瘤細胞的耐藥性屬于獲得性耐藥亦稱繼發性耐藥,是在化學治療過程中化療藥物誘導逐漸產生的。腫瘤細胞一旦產生耐藥性,化療藥物就不能發揮完全的抗癌作用殺死癌細胞,即使大多數的腫瘤被殺死,而這一小部分具有抗藥性的癌細胞依然會繼續生長,造成癌癥復發。進而,化學治療療效越來越差,這是導致惡性腫瘤最終無藥可用的重要原因之一。此外,根據腫瘤的耐藥譜還可以分為原藥耐藥(primary drug resistance)和多藥耐藥(multidrug resistance, MDR)。前者是指腫瘤細胞只對開始接觸的原藥不敏感,而后者則除了對開始誘導的藥物有抗性之外,對其他未接觸過而且結構不同、作用機制各異的藥物也產生交叉耐藥性。這個概念是1970年最先由Biedler和Riehm提出的[3]。腫瘤的耐藥機制非常復雜,腫瘤的MDR與多藥耐藥基因(multi-drug resistant genes)過表達密切相關,最近的研究[4]發現,化療藥物以外的損傷因素也可以使多藥耐藥基因表達增強,而這些損傷因素所引起的多藥耐藥基因的高表達均可以使細胞對后來的其他損傷因素產生耐受,因此,多藥耐藥基因應改稱耐多種損傷基因似乎更能體現其內涵。迄今為止,腫瘤的多藥耐藥是腫瘤治療尚未解決的難題之一。
2 microRNA的命名、生物合成和功能
微小RNA(microRNA, miRNA)是長度約22個核苷酸(nucleotide, nt)的單鏈小RNA分子,其中21 nt-23 nt長度的miRNA占大多數,約為84%(圖1)[5]。屬于非編碼RNA(non-protein-coding RNAs, ncRNAs)的一種。非編碼RNA是基因組轉錄產物中非蛋白編碼的部分,曾被認為是轉錄“噪聲”,主要包括miRNA、小干擾RNA(small interfering RNAs, siRNAs)、piwi蛋白相互作用RNA(PIWI-interacting RNAs, piRNAs)和長鏈非編碼RNA(long ncRNAs,lncRNAs)。目前,這些最初被認為是轉錄副產物的物質被發現在生物信息流由DNA模板向蛋白效應分子轉化過程的多個層面發揮著不同形式的調節作用。最近的研究表明,miRNA對多基因表達的調控具有高效性和特異性,對靶基因的異常調控可能構成腫瘤耐藥機制,是腫瘤耐藥復雜性調控的重要構成部分。這些發現改變了“RNA僅僅是DNA和蛋白之間媒介”的傳統觀念。
2.1 MiRNA的命名 miRNA是目前ncRNA中被研究的最多的成員,到目前為止,人們已在植物、線蟲、果蠅,動物中發現了一萬五千多個miRNA,其中人類細胞中已發現的有1,048個[6]。miRNA的命名原則:miRNA可簡寫成miR,再根據其被克隆的先后順序加上阿拉伯數字,如miR-22。一般而言,數字越小,發現越早;高度同源的miRNA在數字后加上英文小寫字母(a、b、c······),如miR-181a、miR-181b、miR-181c;位于基因組不同位點但具有相同成熟體序列的miRNA,應在序列后添加短線和阿拉伯數字以示區別,如miRNA-34a-1、miRNA-34a-2;miRNA前體經過一個發夾環結構,具備兩個臂,但通常只有一個會被選擇成為最終的miRNA,那么被降解掉的另外一條臂則以“*”表示;物種縮寫應置于miRNA之前,如has、mmu和rno分別代表人、小鼠和大鼠;確定命名規則之前發現的miRNA應保留原來名字,如lin-4[7]。
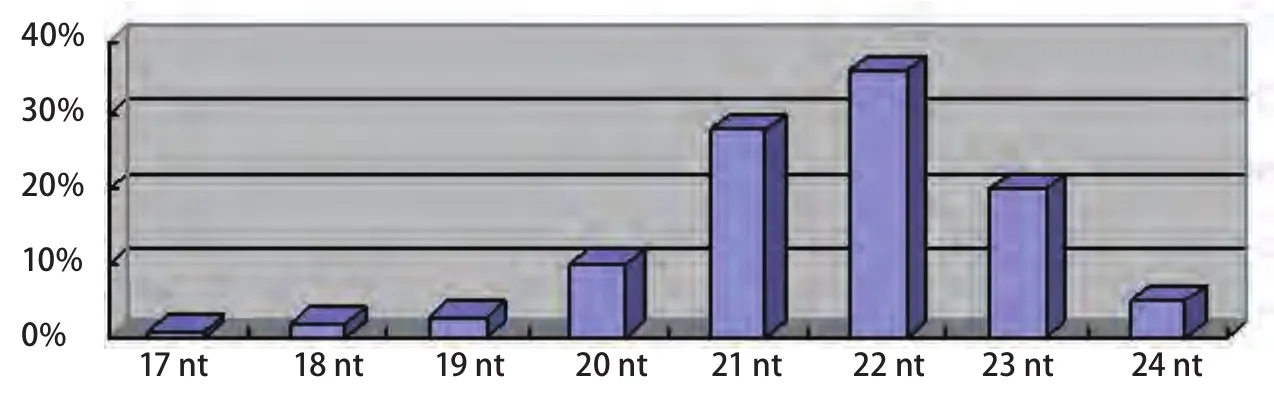
圖1 已知的microRNA核苷酸長度的分布情況Fig 1 The distribution of the length of known microRNA nucleotides
2.2 MiRNA的生物合成 MiRNA可能來自于基因組的基因間隔區或者pre-mRNA的內含子中,但是不論其來自何處,其加工成熟機制都是相同的。首先,在細胞核中,RNA酶III Drosha-DGCR復合體在miRNA原初轉錄物(primRNA)基部切割雙鏈形成60 nt-70 nt的5’末端具有磷酸基,3’末端具有二核苷酸突出(over hang)的莖環中間體---前體miRNA(pre-miRNA)。然后,轉運蛋白Exportin-5通過識別pre-miRNA的3’端的二核苷酸突出信號而與premiRNA結合,依賴Ran-GTP將pre-miRNA輸出到細胞質。植物中是由Exportin-5的同源物HASTY負責miRNA前體的輸出[8]。最后,Dicer識別pre-miRNA雙鏈的5’末端磷酸及3’末端突出,在距莖環大約兩個螺旋轉角處切斷螺旋體的雙鏈,產生一個結構類似于siRNA的二聚體,其中成熟的miRNA來自于pre-miRNA的一條臂,pre-miRNA的另外一條臂產生一個長度與miRNA相同的片段,即miRNA*[9]。在經過切割和核質轉運后,RNA解旋酶作用于miRNA:miRNA*二聚體,其中miRNA進入RNA誘導的沉默復合物(RNA-induced silencing complex, RISC)中發揮作用,miRNA*則被降解[10,11]。
2.3 MiRNA的生物學功能 MicroRNA是通過與靶mRNA的3’-UTR堿基配對的方式來執行對靶mRNA的轉錄翻譯抑制的功能。在動物中,microRNA與靶mRNA進行不完全配對執行轉錄后翻譯抑制的作用。但是如果動物miRNA與靶序列完全互補,則進入RNA干擾路徑指導靶序列降解。在篩選果蠅生長缺陷突變株的過程中發現了Bantam基因座。該基因座編碼了果蠅幼蟲抑制程序性死亡和促進細胞增殖的miRNA。Bantam miRNA大量表達并抑制Hid mRNA的翻譯。Hid是程序性死亡的主要激活因子。Bantam類似于線蟲的miR-80/82,這表明miR-80家族能控制線蟲的細胞死亡和增殖[12]。動物中的miRNA還能影響細胞分化。miR-23與Hes1基因具有較完全的互補性(大約77%)。Hes1是一種基本的螺旋-環-螺旋結構,它只在未分化細胞中表達。將人工合成的miR-23加到未分化的NT2神經細胞中,可以發現細胞內的Hes1水平大幅下降。但是將人工合成的miR-23突變體加入到未分化NT2細胞中,Hes1水平保持不變,且其含量與將野生型miR-23加入到已分化的NT2細胞中是一樣的。這表明miR-23在翻譯水平上抑制Hes1基因的表達,影響細胞分化[13]。在植物中,由于miRNA與mRNA互補程度高,故可用來預測植物microRNA的靶位點。實驗證據[14]表明,miRNA能直接指導靶mRNA的剪切。植物miRNA大多是調控發育與細胞分化的基因。miR-165/166的靶基因PHB與PHV中的序列發生突變后則造成功能獲得性突變,PHB mRNA表達的組織范圍相對于野生型PHB mRNA擴大了[15]。近來的研究發現,植物中的miRNA不僅可以調控細胞周期及細胞分化,還對環境應答和激素應答有一定作用。miR-167和miR-160調節編碼植物激素應答因子基因的表達。在擬南芥中,TIR1蛋白因子通過與E3泛蛋白連接酶SCF復合物的吲哚乙酸結合而參與胚軸分化、橫向根系形成等生理過程,而miR-393調控該蛋白的表達[16]。
3 MiRNA與腫瘤耐藥
腫瘤的耐藥機制復雜,目前,已知化療耐藥的分子機制包括:藥物靶點的改變、藥物的改變或失活、DNA損傷修復增強、細胞凋亡減少、藥物代謝改變以及藥物誘導的細胞核型改變等(圖2)[17,18]。同時,細胞修復和細胞死亡通路等亦與之密切相關。目前研究較多的包括與藥物外排相關的能量依賴型轉運體,如ABC家族的P170、MRP、BCRP、DNA修復系統如錯配修復、細胞凋亡相關分子及谷胱甘肽S轉移酶等。這些關鍵基因發生的一系列遺傳或表觀遺傳上的改變是導致耐藥性的主要機制之一。此類改變包括基因的突變(mutation)、缺失(deletion)、擴增(amplification)、轉置(translocation)、DNA的異常甲基化以及microRNA的轉錄后調節等多種方式。其中,有研究揭示miRNA與腫瘤細胞對化療藥物的敏感程度密切相關,miRNA成為腫瘤耐藥研究領域一個熱點。miR-214可靶向PTEN導致PTEN蛋白低表達,Akt通路過度激活從而促進細胞增殖,致使過表達miR-214的卵巢癌病人對順鉑不敏感[19]。SIRT蛋白是依賴于NAD的蛋白去乙酰化酶,通過對P53蛋白去乙酰化起到抗凋亡作用,在PC3細胞中過表達miR-34a可下調SIRT1的mRNA,導致細胞周期停滯、細胞生長受到抑制并增強了PC3對喜樹堿的敏感度[20]。
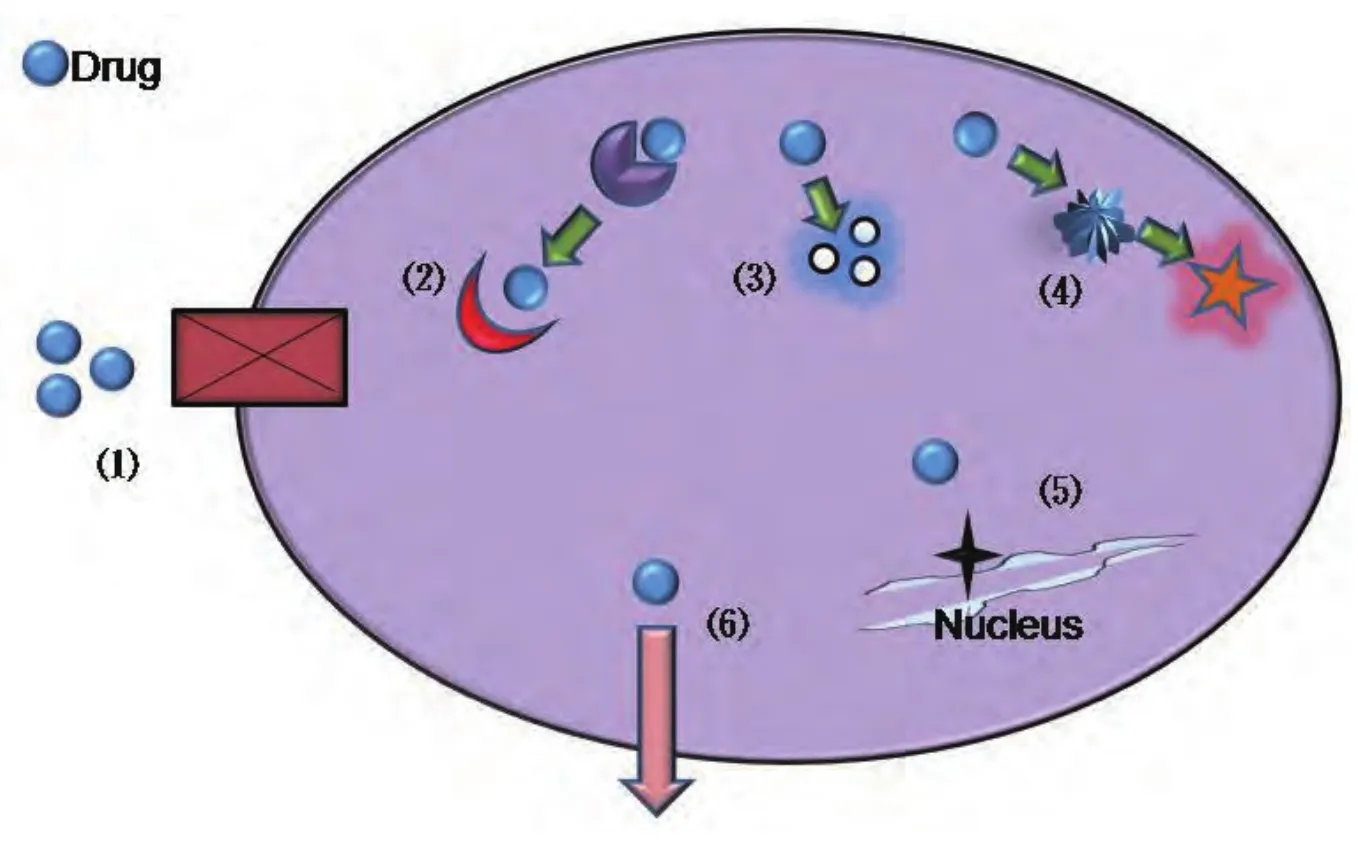
圖2 腫瘤細胞耐藥的典型分子機制。常見耐藥的主要途徑有:(1)由于細胞表面受體或轉運體缺失導致藥物不能進入細胞內;(2)藥物靶點改變;(3)藥物的改變或失活;(4)藥物代謝途徑改變;(5)損傷DNA修復增加;(6)藥物被主動運輸到細胞外。Fig 2 The molecular mechanisms of drug resistance in tumor cells. The main pathways of drug resistance: (1) The drug can not get into the cell due to lost of cell surface receptors or transporters; (2) Mutations in drug target; (3)Changes or inactivation of the drug; (4) Changes in the drug metabolism pathway; (5) Increased repair of damaged DNA; (6) Drug is exported by active transportation.
miRNA的突變(mutation)、異常表達(misexpression)和異常加工均會影響miRNA的正常功能,導致靶基因的蛋白表達水平異常。如果此類靶基因與腫瘤細胞對藥物的敏感程度相關,將改變腫瘤細胞的藥物敏感程度(圖3和表1)。miR-482-3P靶向抑制NF-Yb轉錄水平,上調Top2a表達,提高淋巴細胞型白血病CEM細胞對替尼泊苷的敏感性,而下調其表達則促使了CEM/VM-1-5的藥物耐受[21]。Lu等[22]報道胸甘酸合成酶3’UTR區6個堿基的缺失突變與胃癌患者對5-FU的化療敏感性有關,但具體機制尚不清楚。Tsang的研究[23]表明,let-7a通過下調細胞凋亡中的啟動酶CASP3抑制了細胞凋亡,在A431和HepG2細胞中過表達let-7a可增強它們對阿霉素、紫杉醇及干擾素的耐藥性,抑制let-7a則增加化療藥物引發的細胞凋亡。
4 MiRNA在逆轉腫瘤耐藥中的作用研究
MiRNA究竟通過何種機制對腫瘤細胞的藥物敏感程度產生影響尚待研究。2007年,Bertino等[52]提出了“miRNA的藥物基因組學”(miRNA pharmacogenomics)概念,指出通過研究miRNA及miRNA的突變如何干擾miRNA的正常功能進而改變患者藥物反應程度,最終可找出某些特定的miRNA用以指導患者的個性化用藥。美國國立癌癥研究所對60種癌細胞系(NCI-60)進行了10萬多種化學藥物的敏感性實驗,得到所有細胞系對各種藥物的藥敏數值GI50、LC50和IC50,同時對這60個細胞系做了DNA、RNA、蛋白質水平的多種分析,包括染色體畸變、DNA拷貝數變化、mRNA及miRNA的表達譜分析,所有數據被整合在CellMiner中,為在分子水平系統性研究腫瘤細胞的藥物敏感性提供了數據支持[53]。
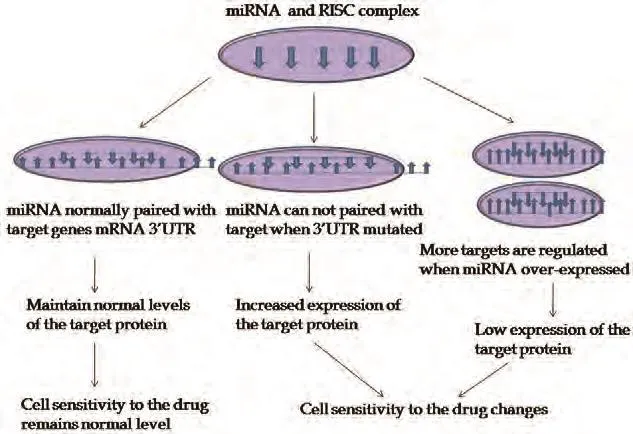
圖3 MicroRNA影響藥物敏感程度的作用機制。正常情況下,microRNA及靶蛋白的水平維持正常狀態;microRNA的基因發生突變時無法與靶mRNA正常配對,靶蛋白高水平表達;microRNA過表達時靶基因低表達。如果此靶蛋白參與細胞對藥物的反應,如藥物轉運體、藥物靶點、細胞凋亡及修復等相關蛋白,則導致藥物敏感度的改變。Fig 3 The mechanism of microRNA effect on the sensitivity to drugs. Normally, microRNAs and target proteins are maintain on the normal levels; when microRNA gene mutated, microRNA can not paired with target mRNA, cause the increased expression of target protein; when microRNA overexpressed, the expression of target gene reduced. If the target involves in cell responses to drugs such as drug transporter protein,drug targets, apoptosis or DNA repair related proteins,the sensitivity to drugs will be changed. RISC: RNA-induced silencing complex.
MiRNA藥物基因組學的最終目標是通過分析患者的miRNA及mRNA特征譜,再結合其他分子標志,可以預測患者對某種藥物的反應程度,從而因人而異的給予最有效的化學治療。通過研究miRNA調控腫瘤細胞耐藥性,探索miRNA在人類腫瘤治療中的潛能具有現實意義。p53是眾所周知的抑癌基因,然而P53相關的轉錄因子P63/P73在鱗癌中均過表達。一項研究發現化療可以引發P63/P73依賴性miR-193a-5p的誘導,從而通過miRNA介導的P73的反饋性抑制以限制化療敏感性。抑制miR-193a可中斷該反饋,抑制離體和在體腫瘤細胞的生存并增強化療敏感性。因此在P53缺失腫瘤中,miR-193a的抑制或可提供新的治療機會[54]。RNAi技術的發展為miRNA調控腫瘤細胞耐藥起到了重要意義,如應用反義核酸技術下調miR-21,使miR-21表達減少可以增強乳腺癌MCF-7細胞對拓撲替康的敏感性[55]。研究發現miR-200c抑制-微管蛋白3(class III-tubulin,TUBB3)表達,過表達miR-200c可恢復子宮內膜癌細胞對化療藥物的敏感性[56]。MiR-203過表達通過抑制靶基因AKT2的活性,下調其下游耐藥相關蛋白MTDH/HSP90的表達,從而增加結腸癌細胞對紫杉醇的敏感性[57]。在MDR大腸癌中miR-222與ADAM-17的表達成負相關,提高HCT116/L-OHP和HCT-8/VCR細胞中miR-222的表達量可降低ADAM-17蛋白表達,使細胞凋亡增加,進而改善大腸癌HCT116/L-OHP和HCT-8/VCR細胞對L-OHP/VCR的敏感性[58]。腫瘤干細胞(cancer stem cells, CSCs)具有廣泛的增殖和自我更新潛能以促進癌癥的發展。研究顯示let-7和miR-181在肝細胞CSCs中表達上調。還表明let-7靶向作用于SOCS-1和CASP3,而miR-181則靶向作用于せSSF1A、TIMP3及NLK。Let-7的抑制可增加肝細胞CSCs對多柔比星和索拉非尼的化療敏感性,而miR-181沉默可減弱肝細胞CSCs的活躍性和侵襲性[59]。最新研究[60]發現,miR-503可能通過抑制藥物外排,負調控腫瘤耐藥相關蛋白表達,促進細胞凋亡進而逆轉肺腺癌A549/DDP細胞對順鉑的耐藥性。
5 展望
目前miRNA在腫瘤耐藥性中的研究尚處于起步階段,許多具體作用機制還需深入的研究證實,有的研究之間甚至存在矛盾之處。Zhu等[61]報道了miRNA-451和miRNA-27a在多藥耐藥的癌細胞系A2780DX5和KB-V1中表達上調,抑制miR-451或miR-27a的表達可導致MDR1的mRNA和蛋白水平的下降,從而增強細胞系對長春堿、阿霉素的敏感程度。但Kovalchuk等[62]研究結果顯示,在多藥耐藥細胞系MCF-7/DOX中過表達miR-451可增強細胞對阿霉素的敏感性。兩個研究結果的矛盾說明了miRNA調節機制的復雜性,也表明該領域的不成熟,同樣也提醒在研究miRNA時一定要謹慎驗證研究結論的可靠性。miRNA表達譜不僅是腫瘤診斷的重要標志物,同時也在腫瘤分期中具有重要作用,近來的研究表明,通過分析藥物敏感性及非敏感性細胞的miRNA的表達譜,可以找到影響藥物敏感性的相關miRNA,這不僅有利于深入認識腫瘤耐藥機制,而且有助于尋找新的藥物靶標及為個體化用藥提供新的依據。在細胞水平上揭示耐藥相關性miRNA及其作用靶點和作用機制只是第一步,這些研究結果最終都要在臨床樣本中進行驗證。
綜上所述,miRNA在調節不同腫瘤耐藥方面起著重要作用。一個miRNA可調節多個靶基因,一個靶基因也可受多個miRNA的調節,因此miRNA的調節機制是一個復雜的網絡結構。正常情況下miRNA通過其精細復雜的調節網絡使細胞內各種蛋白的水平維持在平衡狀態,miRNA的多態性及表達異常可導致腫瘤耐藥相關通路的基因表達水平發生改變、耐藥基因和癌基因的高表達、腫瘤細胞周期改變等,從而打破原有的平衡進而改變腫瘤細胞對藥物的敏感性,導致耐藥現象。MiRNA調控腫瘤細胞耐藥是一個龐大而復雜的miRNA-mRNA基因調控網絡,因此miRNA完全有潛力成為逆轉多因素、多基因導致的腫瘤耐藥的高效靶點,從而極大地改善臨床腫瘤治療耐藥現狀,具有一定的現實意義。 相信基于miRNA的分子靶向治療必將成為臨床攻克腫瘤耐藥的一種高度特異性的,潛在高效的個體化治療手段,開啟逆轉腫瘤耐藥的miRNA基因療法新篇章。

