血小板源生長因子家族在非小細胞肺癌中的研究進展
田逸俊 褚倩 陳元
非小細胞肺癌(non-small cell lung cancer, NSCLC)作為全球癌癥相關死亡率最高的惡性腫瘤之一,其療效預測指標和預后因子尚未明確。以各種腫瘤信號通路為靶點的靶向治療在NSCLC的綜合治療中發揮了越來越重要的作用,其中抗腫瘤血管生成藥物(貝伐珠單抗、血管內皮抑素)在臨床應用中所展現出來的作用有目共睹。血小板源生長因子(platelet derived grow factor, PDGF)作為重要的促血管生成通路,其作用也越來越多地被人們了解。本文將對PDGF通路在NSCLC的診斷、治療以及預后等方面的研究進展進行綜述。
1 PDGF與腫瘤信號轉導通路
1.1 PDGF及其受體 PDGF由四種多肽鏈A、B、C、D以二硫鍵形成二聚體結構,即可形成PDGF-AA、PDGF-BB、PDGF-CC、PDGF-DD,此外,A鏈和B鏈還可形成異源的二聚體,即PDGF-AB,因此目前發現的PDGF有五種二聚體形式[1]編碼以上四條肽鏈的基因分別位于染色體7q22、22q13、4q31和11q22[2]。血小板源生長因子受體(PDGFR)包括亞單位α和β,每個亞單位由胞外配體結合區,跨胞膜區和胞內酪氨酸激酶活性結構區組成。正常狀態下PDGFR亞單位以單體或疏松結合二聚化形式存在于胞膜表面,PDGF與PDGFR結合時,兩種亞單位連結為穩定二聚化形式(αα、αβ、ββ),進而發生磷酸化反應,產生生理效應,α亞單位和PDGF的A、B、C鏈親和力較高,β亞單位和PDGF的B、D鏈親和力較高[3]。
1.2 PDGF涉及多種細胞內信號轉導通路 分泌形式的PDGF與靶細胞表面PDGFR結合以后,使PDGFR發生二聚化,進而激活受體的胞內酪氨酸位點磷酸化,磷酸化的酪氨酸位點又與胞內某些信號分子通路的SH2結構域相互作用,使這些通路被激活。上述胞內信號分子包括:酪氨酸激酶Src亞族、磷脂酶C(PLC-γ)、磷脂酰肌醇-3激酶(PI3-K)、GTP酶活化蛋白(RAS-GAP)、生長因子結合蛋白(Grb2)、酪氨酸特異磷酸酶(Syp)、Src同源物與交聯蛋白(Shc)、適應蛋白(Crk)以及非受體酪氨酸激酶家族(Src)等[2]。這些信號分子介導胞質內復雜的信號網絡,進而作用于細胞核膜上絲蘇氨酸殘基位點,導致多種基因調節蛋白磷酸化,影響轉錄水平的基因表達,最終發揮促細胞生長、遷移、自我修復[3]以及上皮間葉轉化[4]等生物效應。PDGF和PDGFR結合方式及其下游通路見圖1。
2 PDGF與NSCLC
2.1 PDGF及其受體在NSCLC中的表達 PDGF通路在神經膠質瘤中的自分泌和旁分泌環途徑最早被Hermanson等[5]發現。此后Vignaud等[6]對64例病理確診為NSCLC患者肺癌組織與8例非腫瘤病變患者的肺組織進行了病理分析對比:發現約1/3的NSCLC患者肺癌細胞PDGF表達增高,1/2的NSCLC患者肺癌細胞PDGFR表達增高,僅有1/6的NSCLC患者肺癌細胞同時有PDGF及其受體的共同增高;大部分NSCLC患者的腫瘤相關巨噬細胞(tumorassociated macrophage, TAM)都有PDGF的表達增高,且TAM多分布于瘤體的外圍區域;間葉細胞和內皮細胞在病例組和對照組中都有PDGFR的表達,但無因子的表達;腫瘤細胞和間葉細胞的DNA復制速度加快。由此Jean等認為NSCLC中由腫瘤相關巨噬細胞分泌的PDGF雖然直接刺激腫瘤細胞生長的作用有限,但對腫瘤間質的旁分泌刺激作用更有力。另外,Tsao等[7]在肉瘤樣NSCLC與對照組NSCLC的免疫組化對比中發現,肉瘤樣NSCLC具有更高的PDGFR-β的拷貝數和免疫組化計分。由上述病理結果我們可認為,肉瘤樣NSCLC中PDGFR的高表達與PDGF主要調節間質細胞增殖的功能是一致的。腫瘤間質是腫瘤細胞穩定存活于宿主的直接物質基礎,由非腫瘤組織,如腫瘤血管、炎性細胞、成纖維細胞、胞外基質等構成,為腫瘤細胞提供血液供應、基質骨架,同時也是機體和腫瘤發生免疫反應的場所[8]。PDGF通路通過上述多種胞內促增殖信號促進腫瘤間質,尤其是腫瘤周圍血管和淋巴管的生長,從而對腫瘤細胞的生長起促進作用[9,10]。

圖 1 PDGF及其受體結合方式,以及下游主要信號通路示意圖Fig 1 Binding pattern of PDGF, PDGFR and the main signal pathway in the downstream. PDGF: platelet derived grow factor.
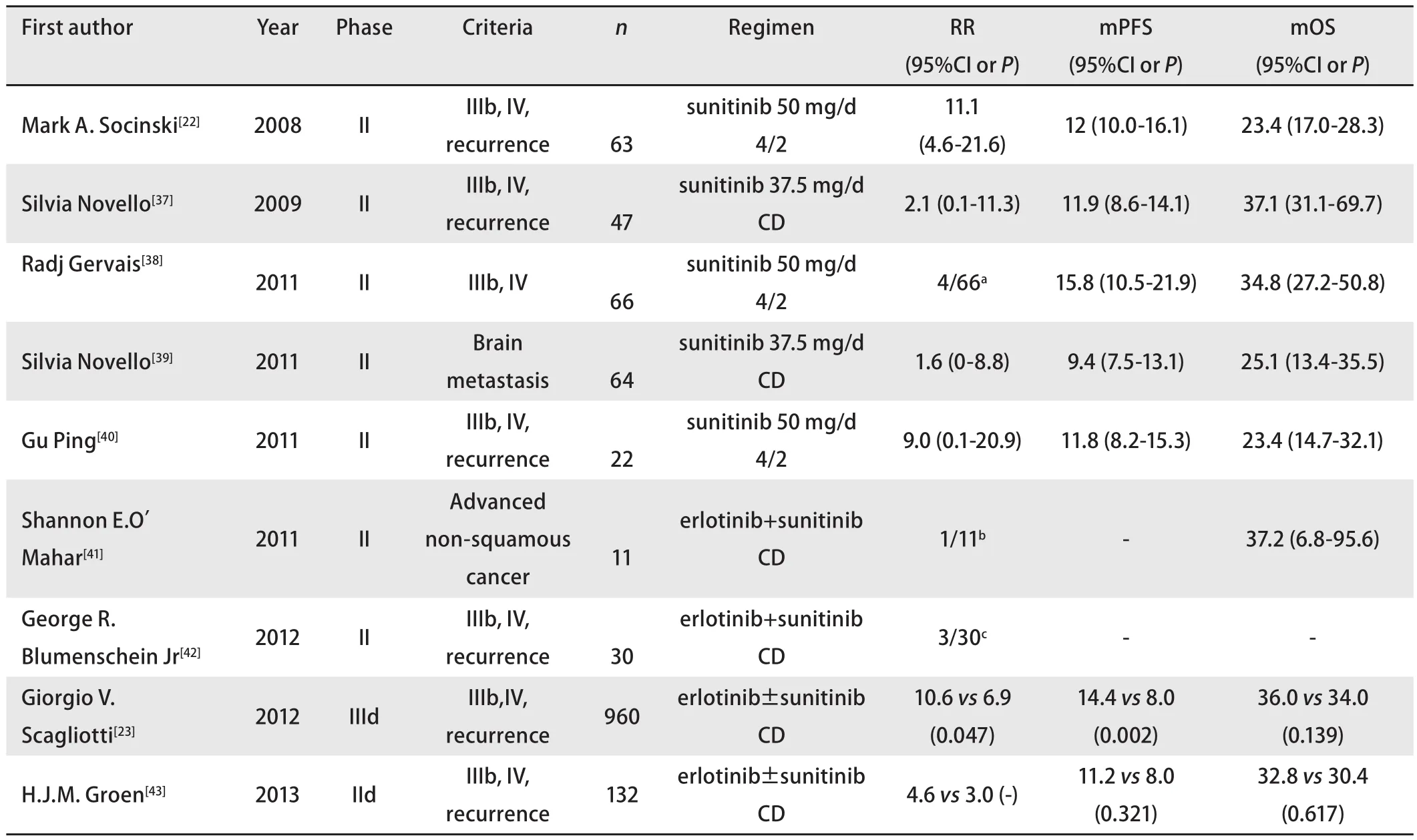
表 1 Sunitinib單藥以及聯合靶向藥物治療NSCLC臨床試驗匯總Tab 1 The clinical trials of sunitinib administrated alone or in combined with TKIs in NSCLC
2.2 PDGF及其受體對NSCLC預后的影響 影響肺癌預后的因素多種多樣,Andersen等[11]對于接受術后放療的患者腫瘤組織促血管標志物和預后的關系進行了研究,發現在多因素分析中,腫瘤細胞表達PDGF是獨立的不良預后因素。Donnem等[12]對NSCLC腫瘤細胞和間質細胞(包括內皮細胞、免疫細胞、成纖維細胞等)中PDGF及其受體和疾病相關生存率進行分析發現,NSCLC腫瘤細胞中PDGF-B和PDGFR-β的高表達和不良預后相關,而腫瘤間質中PDGF-A的高表達則和良好預后相關,提示間質細胞中的這種現象可能與高水平PDGF-A能在某種程度上激活適應性免疫有關。Donnem等[13]也發現不同的促血管生成通路在不同分期腫瘤的進展和轉移中所起的作用并不相同,即腫瘤細胞中VEGF-A/VEGFR-2和VEGFR-3跟T2a期(3 cm<Φ≤5 cm)NSCLC患者預后有關,PDGF-B跟T2b期(5 cm<Φ≤7 cm)NSCLC患者預后有關。在淋巴結轉移方面,腫瘤細胞PDGF-B的表達和淋巴轉移的關系尚存在爭議:Cao等[14]發現PDGF-BB在體內能有效促進腫瘤淋巴管的生成,使表達PDGF-BB的鼠類纖維肉瘤淋巴管生成增加,且淋巴結轉移增多,張楠[15]、林文俐[16]等的研究也支持了Cao的結論。而Donnem等[17]則發現腫瘤細胞PDGF-AA的表達和淋巴結轉移相關,和預后關系不明確,PDGF-B(PDGF-BB或PDGF-AB)和VEGFR-3的共表達和不良預后有關,和淋巴轉移的關系不明確。鄭慶峰等[18]通過對205例NSCLC患者手術標本進行免疫組化檢測,認為PDGFR與VEGFR-3可能存在某種內在聯系。吳麗娜等[19]則發現PDGF-B/PDGFR-α自分泌刺激環可能在NSCLC的發生中起重要作用,且陽性表達與疾病的分期呈正相關。
2.3 PDGF通路與肺癌治療
2.3.1 靶向治療 在對733例NSCLC腫瘤樣本的染色體分析中,Ramos等[20]發現其中31例樣本的染色體4q12有頻繁的擴增,且4q12片段中一個長約600 kb的區域明顯地增加,此區域基因負責編碼PDGFRA及與其緊密相關的受體酪氨酸激酶Kit;體外實驗[21]對六種肺癌細胞系進行了研究,發現NCI-H1703肺鱗癌細胞系高表達PDGFRA,并且對sunitinib和imatinib兩種藥物的單藥治療敏感,而sunitinib和imatinib兩種靶向藥物都對PDGF通路有抑制作用。這些結果表明,NSCLC中存在PDGF通路活化的現象,雖然NSCLC表達PDGF通路的比率并不高,但鱗癌細胞系NCI-H1703對于PDGF通路的依賴性提示其在鱗癌中可能存在的驅動作用。在臨床方面,以PDGF通路為靶點之一的小分子酪氨酸激酶抑制劑sunitinib單藥在晚期NSCLC中的抗瘤活性已得到證實,Socinski等[22]在一項多中心II期臨床試驗中,使用sunitinib單藥(4/2 50 mg qd)治療63例鉑類治療失敗的晚期NSCLC患者,部分緩解率為11.1%,中位無進展生存時間為12.0周,中位總生存時間為23.4周。Scagliotti等[23]主持的一項III期臨床試驗則比較了sunitinib聯合厄洛替尼的方案和厄洛替尼單藥在960例復發的晚期NSCLC患者中的療效差別,證明雖然聯合方案沒有提高總生存時間,但卻能延長無進展生存時間和提高反應率。結合Ramos的研究和上述單藥治療晚期NSCLC患者的臨床試驗數據,雖然PDGF通路在NSCLC中的突變發生率較低,但在臨床研究中,以PDGF為靶點的分子靶向治療仍在NSCLC的治療中占有一席之地;同時也必須認識到sunitinib的抗腫瘤血管生成活性并非完全由抑制PDGF通路產生,即VEGF仍然是目前抗血管治療的重要靶點(表1)。
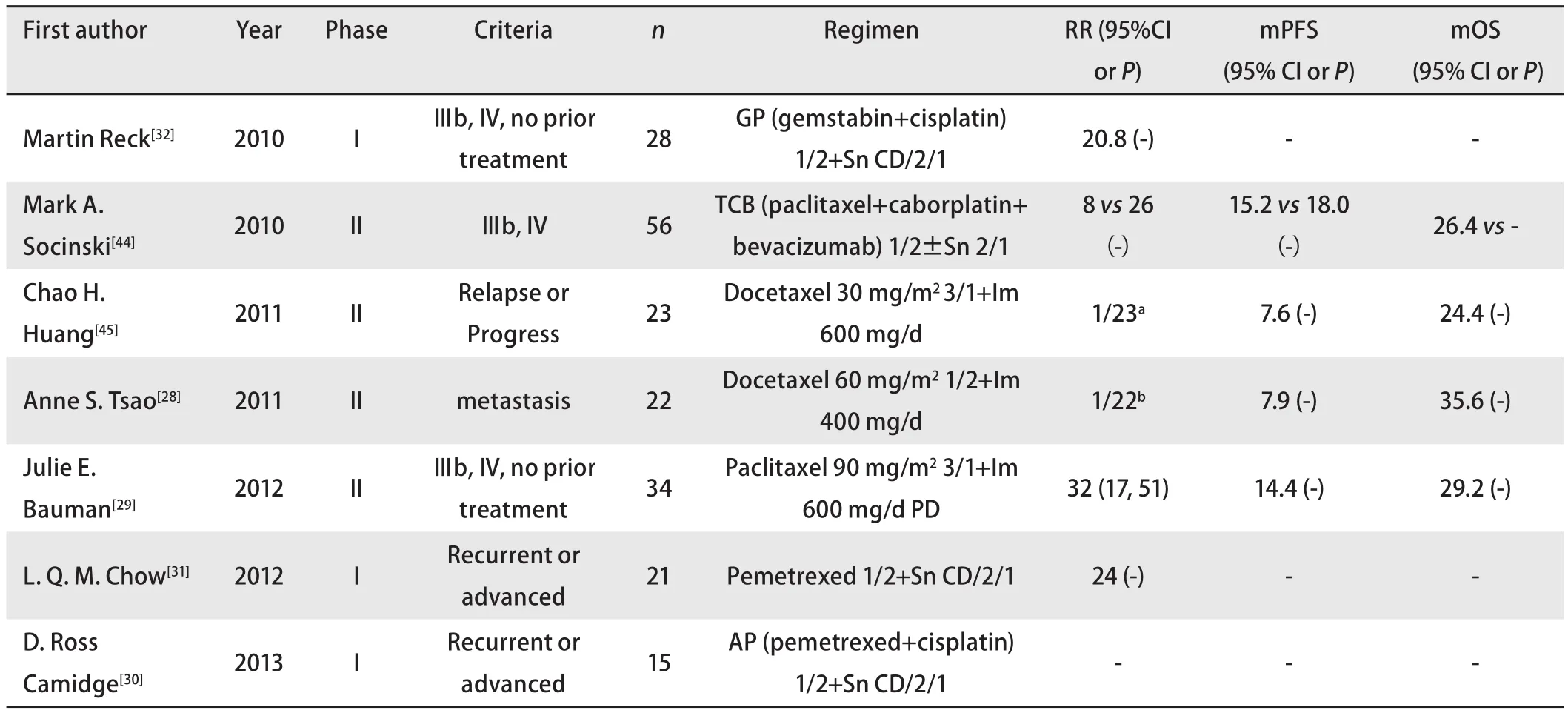
表 2 Imatinib及sunitinib聯合化療治療NSCLC臨床試驗匯總表Tab 2 The clinical trials of sunitinib or imatinib administrated in combined with chemotherapy in NSCLC
2.3.2 化療 腫瘤間質內液壓(interstitial fluid pressure, IFP)指實體腫瘤內部組織和液體共同產生的通常高于正常組織的壓強。升高的IFP影響化療藥物向腫瘤內部的運輸過程。PDGF通路在調控IFP過程中起著重要作用。Kristian Pietras等[24]發現imatinib在鼠類腫瘤模型中增強了泰素和5-Fu的抗腫瘤作用。Bertino等[25]在鼠類移植物的實驗中證明imatinib在體外以及體內均能增加吉西他濱對于惡性間皮瘤的作用,聯合治療較單藥能明顯抑制腫瘤生長、延長荷瘤鼠的生存時間。Vlahovic等[26]在NSCLC的移植瘤實驗中,發現imatinib能增加腫瘤中脂質體阿霉素的濃度,并且能增強多西他賽的抑瘤作用。Zhang等[27]的研究則發現在體外對肺腺癌細胞系A549使用imatinib單藥處理可以產生劑量依賴的細胞生長抑制,且imatinib可通過抑制PDGFR-α的磷酸化增強順鉑對A549細胞的殺傷作用。雖然基礎研究中觀察到抑制PDGF通路對化療所產生的獲益,但是PDGF抑制劑在為數不多的臨床試驗中的表現卻不令人滿意。Tsao等[28]的一項II期臨床試驗,入選了22例有轉移的NSCLC患者和7例化療耐藥的頭頸鱗狀細胞癌患者,均給予多西他賽(每3周1次,60 mg/m2)和imatinib(每天400 mg)的治療,兩部分試驗均在早期因療效差或明顯的毒副作用而提前關閉,Tsao認為泰素類藥物和imatinib之間可能存在潛在的拮抗關系,認為今后對于聯合紫杉醇類藥物和imatinib的方案(尤其是同時給藥方案)的研究應該更加謹慎。Bauman等[29]對34例70歲以上晚期NSCLC患者給予泰素(90 mg/m2d3, 10, 17 Q28d)和脈沖劑量imatinib(圍繞每次泰素注射前后,即600 mg/d d1-4, 8-11, 14-18)的治療,達到了32%的總有效率,但中位無進展生存時間和中位總生存時間無改善。Camidge等[30]在sunitinib聯合培美曲塞加順鉑方案治療晚期惡性實體瘤的I期試驗中,發現給予兩周sunitinib(37.5 mg, qd),間歇1周(2/1組),并每3周行培美曲塞(500 mg/m2)加順鉑(75 mg/m2)化療的方案達到了最大耐受劑量,且使用中因累積的骨髓毒性仍需減少劑量,試驗中NSCLC患者所能達到的最好的療效為穩定。Chow等[31]也進行了一項sunitinib聯合培美曲塞治療晚期實體瘤的臨床試驗,由于去掉了順鉑這種藥物,每日持續37.5 mg sunitinib可被患者耐受。在21例NSCLC患者中,有4人獲得了部分有效的結果。Reck等[32]則在GP(吉西他濱1,000 mg/m2,順鉑 80 mg/m2)方案中聯合sunitinib治療28例NSCLC患者,可評估的20例患者中共有5例達到部分有效的治療效果。這些試驗提示我們,要從兩方面認識PDGF通路在抗腫瘤治療的作用:一方面要承認抑制PDGF通路所產生的明顯減低IFP的作用,改善了化療藥物分布,從而提高對腫瘤細胞的殺傷,另一方面也要注意到正常組織也會因此接受到更大劑量的化療藥物,導致毒性的累積。只有充分了解患者腫瘤細胞及其間質PDGF及其受體的表達,探索更合理的給藥方法,才可能使治療效應提升,毒副作用降低(表2)。
2.3.3 PDGF通路與肺癌的放療 Holdhoff等[33]在體外實驗中發現放療前給予imatinib處理能增強射線對膠質瘤細胞(RS-1)的殺傷作用,且這種作用主要是由于PDGFR的抑制介導的。D'Amico等[34]使用sunitinib處理鼠移植膠質瘤模型后再給予低劑量照射的聯合方法,較單獨使用兩種治療手段,能更有效抑制腫瘤生長;高劑量照射下加用sunitinib產生嚴重的毒副反應。盡管這種聯合治療能明顯抑制腫瘤的生長,但動物的生存時間并沒有改善。Sennino等[10]認為在腫瘤細胞中VEGF通路主要控制腫瘤血管密度而不影響周細胞密度,而PDGF通路則涉及募集周細胞而不影響血管密度。周細胞(pericyte)是一類與毛細血管具有密切關系的血管外平滑肌樣細胞,參與維持血管密度,血管生成和血管重塑等過程,其募集和分化需要PDGF的調控和參與[35]。抑制PDGF通路則會減少周細胞的募集,從而抑制腫瘤血管的自我修復,增強電離輻射對腫瘤的殺傷作用。另一方面,抑制PDGF通路在新奇的放射免疫療法中也表現出神奇的增效作用。其原理在于拮抗PDGF致腫瘤組織間質液壓下降而導致免疫放療藥物更多地被攝入至實體腫瘤細胞,從而增強療效。Baranowska-Kortylewicz等[36]以結腸腺癌細胞系LS174T的裸鼠移植物為對象,發現同時使用免疫放療藥物和STI571較單獨使用兩者能更有效抑制腫瘤生長,同樣的結論在胰腺癌和前列腺癌中重復。由此可見,體外條件下PDGF通路因其獨特的修復血管作用及降低腫瘤間質液壓作用而使腫瘤細胞對放療和免疫放療過程抵抗,抑制這一通路也取得了一定的放療增效的結果。然而,在動物實驗甚至人體試驗中,抑制這一通路所產生的副作用,以及在肺癌細胞中的增效作用具體如何,仍需要更多的實驗來證實。
3 展望
隨著抗血管生成類藥物(貝伐珠單抗、恩度等)越來越廣泛地應用于臨床,耐藥現象的發生也越來越頻繁。抑制VEGF通路這一處于中心地位的血管生成通路,勢必導致人體中其它血管生成通路的激活,削弱抑制VEGF所產生的抗血管生成作用。PDGF通路在肺癌發生發展中直接促腫瘤生長、促進腫瘤血管生成的作用,以及PDGF靶向藥物單藥或聯合常規肺癌治療手段中可能發揮的治療效應,都需要更多的基礎研究和臨床試驗來闡明,從而為設計新型的抗腫瘤藥物提供理論基礎。

