冠狀動脈旁路移植術后延長輔助通氣與遠期心原性死亡的相關性研究
吳慧,胡盛壽,鄭哲,袁昕,侯劍峰,陳祖君,姚垚
冠狀動脈旁路移植術后延長輔助通氣與遠期心原性死亡的相關性研究
吳慧,胡盛壽,鄭哲,袁昕,侯劍峰,陳祖君,姚垚
目的:分析冠狀動脈旁路移植術(CABG)后患者延長機械通氣(PMV)與遠期心原性死亡的相關性研究。
方法:回顧性分析我院2006-01-01至2008-12-31行單純CABG術的4 022例患者,按機械通氣時間分為常規輔助通氣時間≤12 h組(常規組, n=1 764),助輔通氣時間>12 h組(PMV組, n=2 205),遠期隨訪終點事件:全因死亡、心原性死亡、主要心腦血管不良事件(MACCE)、心絞痛發作、因心臟病再次入院,多因素Cox回歸分析PMV與終點事件發生之間的關系。
結果: PMV組較常規組比較,PMV與遠期隨訪心原性死亡(HR=2.54, 95% CI 1.14~5.66)、因心臟病再次入院(HR=1.36,95% CI 1.10~1.69)的風險升高,差異有統計學意義(P<0.05);PMV與遠期隨訪心絞痛發作(HR=1.29, 95% CI 0.99~1.68)的風險臨界相關(P=0.05);PMV與遠期隨訪全因死亡(HR=1.38, 95% CI 0.83~2.29)和MACCE事件(HR=1.20, 95% CI 0.93~1.55)的風險,差異無統計學意義(P>0.05)。
結論: PMV顯著增加了患者遠期心原性死亡及因心臟病再次入院的風險。
冠狀動脈旁路移植術;機械通氣;遠期隨訪;死亡率;主要心腦血管不良事件
(Chinese Circulation Journal, 2014,29:216.)
延長機械通氣(PMV)是冠狀動脈旁路移植術(CABG)術后常見的并發癥[1],可以直接導致患者住院時間、重癥監護病房(ICU)停留時間延長,住院費用增加[2-5],出院后生活質量下降[6,7],我們的前期研究也進一步證實了PMV與患者術后相關或其它并發癥及主、次要事件的顯著相關性[8]。國外相關研究指出PMV增加CABG患者的近、遠期死亡率及相關并發癥的發生率,而國內目前其他機構對于CABG患者PMV的研究僅止于危險因素,且樣本量小、非單一術式,更未與臨床終點事件相結合進行分析。本研究就輔助通氣時間對4 022例單純CABG患者遠期隨訪進行回顧性分析CABG患者PMV與遠期心原性死亡的相關性。
1 資料和方法
研究對象: 收集我院2006-01-01至2008-12-31行單純CABG術的4 022例患者,其中男性3 258例(81.0%),女性764例(19.0%),年齡20~93歲,平均年齡(61.1±9.2)歲。常溫非體外循環2 429例(60.4%),體外循環1 593例(39.6%)。排除標準:同期行瓣膜置換術、先心病矯治術、左心室室壁瘤手術、室間隔穿孔修補、心臟損傷修復、心臟腫瘤切除術、心房顫動(房顫)治療手術、起搏器植入術、主動脈瘤及其他大血管手術、聯合冠狀動脈(冠脈)介入手術、細胞移植、血栓清除、胸腺切除、冠脈內膜剝脫術、冠脈介入治療意外急診CABG。術前、術中、術后的變量參照以往的文獻[6,9,10]作為研究參數。
麻醉方案及手術方法: 依托咪酯、芬太尼、維庫溴銨麻醉誘導,術中丙泊酚維持,常溫加用異氟醚吸入,必要時追加芬太尼及維庫溴銨。正中切口,選擇左乳內動脈、大隱靜脈、橈動脈為橋血管。患者術后均進入心外科監護室,早期使用丙泊酚鎮靜、呼吸機輔助呼吸、血流動力學監測、及必要時水、電解質、酸堿平衡調整、止血、循環支持治療。
拔管流程:分別采用PB-840(Puritan-Bennett Corporation,美國 )、Maquet Servo-i(邁柯唯,上海 )、Drager Saving(Drager Medical AG & Co.KG,德國)三種呼吸機,常規同步間歇指令通氣模式為機械通氣,初始設置:潮氣量8 ml/kg (體重<80 kg),8 ml×(身高-105)cm (體重≥80 kg),呼吸頻率12次/min,吸入氧濃度0.8,吸呼比(I:E)=1:2,壓力支持(PS) 10 mm Hg(1 mmHg=0.133 kPa),呼吸末正壓(PEEP) 2 mm Hg,隨后根據患者的血氣監測調整。拔管指征:清醒、有指令應答,肌力及血氣良好,自主呼吸好、氣道分泌物少,血流動力學穩定、無惡性心律失常及影響血流動力學穩定的心律失常發生,無過多胸液引流。
延長機械通氣的定義及分組:PMV時間:根據既往文獻[11-13]及本研究數據中輔助通氣時間的中位數為13h,定義PMV時間為>12 h,因此本文PMV即為單純CABG后機械輔助通氣時間大于12h的輔助通氣治療。據此將4 022例患者分為兩組: 機械輔助通氣時間≤12 h者為常規輔助通氣時間組(常規組,n=1 764),輔助通氣時間>12 h者為PMV組 (PMV組,n=2 205)。
隨訪時間及方法:隨訪時間2008-01-07至2010-08-05,隨訪時間 0.6~3.6年,平均(1.8±0.5)年。患者遠期隨訪通過電話、信件或門診復查的方式進行,通過患者或家屬敘述及醫學資料記載證實死亡、主要心腦血管不良事件(MACCE)。全因死亡:指患者出院后隨訪期間內任何原因引起的死亡,包括神經系統、循環系統、腫瘤、感染等原因及原因不明死亡。MACCE:指出現心原性死亡、心肌梗死、再血管化、卒中其中一項或多項心腦血管并發癥的綜合評價指標。心原性死亡:指心臟性猝死、致死性心肌梗死、心力衰竭或其他心臟原因導致的死亡。心絞痛發作:術后患者再次發生胸骨后疼痛,硝酸甘油可緩解,心電圖有典型缺血性改變。因心臟病再次入院:患者術后因心臟原因再次住院治療,包括心律失常、心力衰竭、心肌梗死、心絞痛等。
統計學方法:采用SAS軟件 9.1.3進行統計學處理。計量資料用均數±標準差(±s)表示,計數資料用百分構成比表示。多因素Cox 回歸生存分析PMV與遠期隨訪全因死亡、心原性死亡、主要心腦血管不良事件、心絞痛、因心臟原因再次入院的關系,協變量除近期臨床結果分析的各變量還包括術后藥物預防治療,P< 0.05為差異有統計學意義。
2 結果
兩組患者基本臨床資料的比較: PMV組與常規組比較,男女比例、體質指數、左心室射血分數均較低;病史除冠心病家族史、糖尿病史以及高脂血癥病史的構成比較低外,其余均較高;術中體外循環比例較高,體外循環時間較長;術后院內并發癥發生率較高。差異均有統計學意義(P<0.05),見表1。橋血管的選擇:左乳內動脈3 773例 (93.8%),大隱靜脈和橈動脈249例(6.2%),平均搭橋(3.35±1.37)支。
表1 兩組患者基本臨床資料的比較(±s)
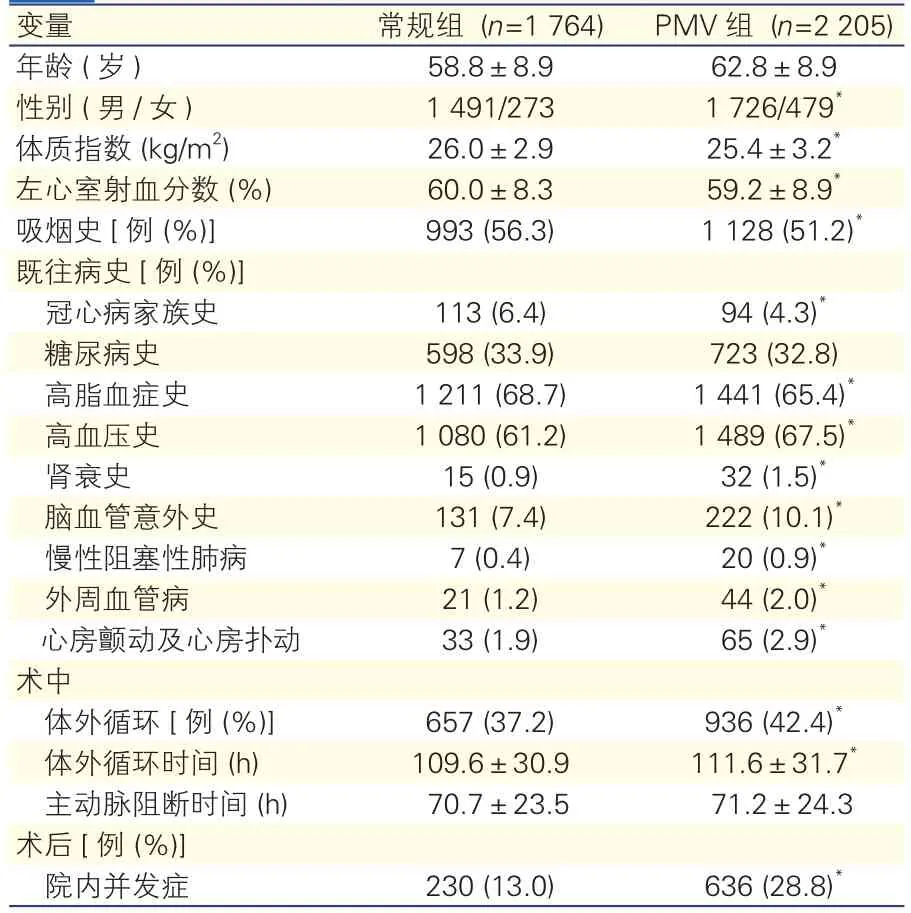
表1 兩組患者基本臨床資料的比較(±s)
注:與常規組比較*P<0.01。PMV:延長機械通氣
變量 常規組 (n=1 764) PMV組 (n=2 205)年齡 (歲) 58.8±8.9 62.8±8.9性別 (男/女) 1 491/273 1 726/479*體質指數 (kg/m2) 26.0±2.9 25.4±3.2*左心室射血分數 (%) 60.0±8.3 59.2±8.9*吸煙史[例 (%)]993 (56.3) 1 128 (51.2)*既往病史[例 (%)]冠心病家族史 113 (6.4) 94 (4.3)*糖尿病史 598 (33.9) 723 (32.8)高脂血癥史 1 211 (68.7) 1 441 (65.4)*高血壓史 1 080 (61.2) 1 489 (67.5)*腎衰史 15 (0.9) 32 (1.5)*腦血管意外史 131 (7.4) 222 (10.1)*慢性阻塞性肺病 7 (0.4) 20 (0.9)*外周血管病 21 (1.2) 44 (2.0)*心房顫動及心房撲動 33 (1.9) 65 (2.9)*術中體外循環 [例 (%)]657 (37.2) 936 (42.4)*體外循環時間 (h) 109.6±30.9 111.6±31.7*主動脈阻斷時間 (h) 70.7±23.5 71.2±24.3術后[例 (%)]院內并發癥 230 (13.0) 636 (28.8)*
隨訪結果:隨訪時間0.6~3.6年,平均(1.8±0.5)年。出院患者3 996例,失訪27例,成功隨訪3969例(99.32%)。隨訪期間全因死亡67例, 其中30天全因死亡15例,180天全因死亡29例,>180至隨訪結束死亡23例;心原性死亡34例,其中30天心原性死亡10例,180天心原性死亡19例, >180至隨訪結束死亡5例。PMV組較常規組全因死亡、180天全因死亡和心原性死亡及180天心原性死亡的發生率較高,差異有統計學意義(P< 0.05 )。隨訪期間共發生MACCE事件257例。PMV組較常規組的心絞痛和因心臟病再次入院的發生率均較高,差異有統計學意義(P<0.05 )。(表 2)
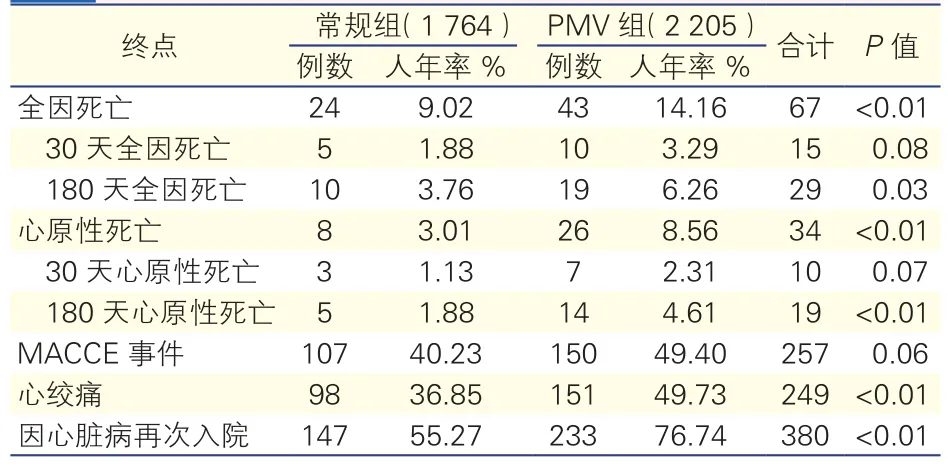
表2 兩組患者遠期隨訪資料對比
多因素Cox回歸分析結果: PMV組與常規組比較,PMV與遠期隨訪心原性死亡(HR=2.54, 95%CI 1.14~5.66)、因心臟病再次入院(HR=1.36, 95% CI 1.10~1.69)的風險升高,差異有統計學意義(P<0.05);PMV與遠期隨訪心絞痛發作(HR=1.29, 95% CI 0.99~1.68)的風險臨界相關(P=0.05);PMV與遠期隨訪全因死亡(HR=1.38, 95% CI 0.83~2.29)、MACCE事件(HR=1.20, 95% CI 0.93~1.55)的風險,差異無統計學意義(P>0.05)。(表 3 )
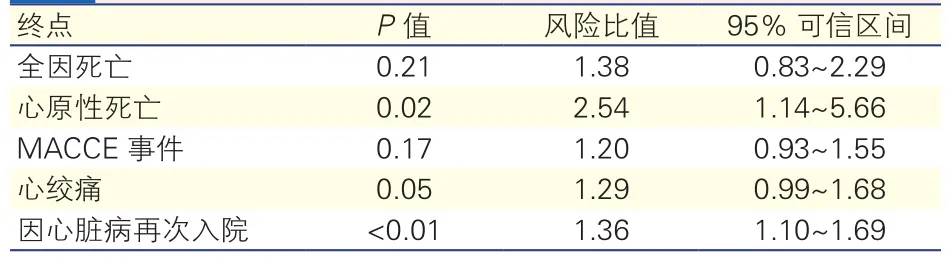
表3 兩組患者遠期隨訪多因素Cox回歸分析
兩組間心原性死亡、因心臟病再次入院及心絞痛發作的Kaplan-Meier曲線結果:經Log-Rank檢驗,PMV組與常規組比較,心原性死亡、因心臟病再次入院、心絞痛發作事件發生率均較高,差異有統計學意義(P<0.05)。(圖 1-3)
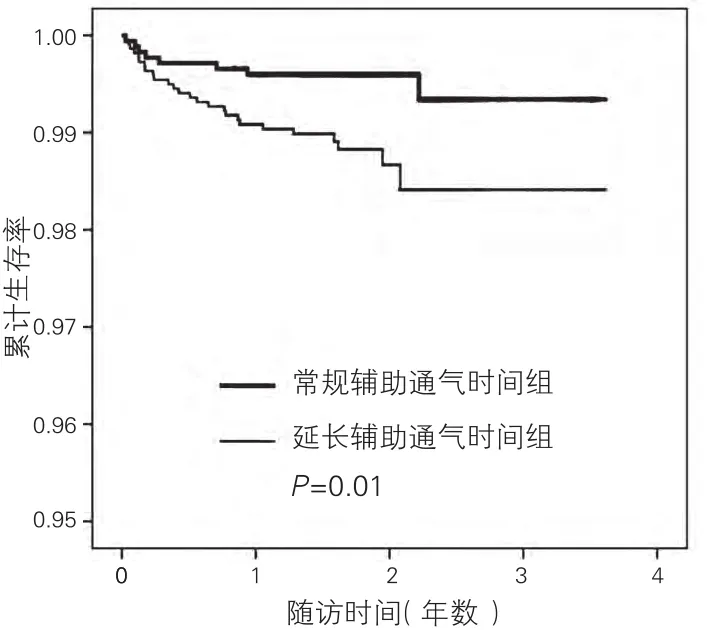
圖1 兩組患者心原性死亡的Kaplan-Meier生存曲線
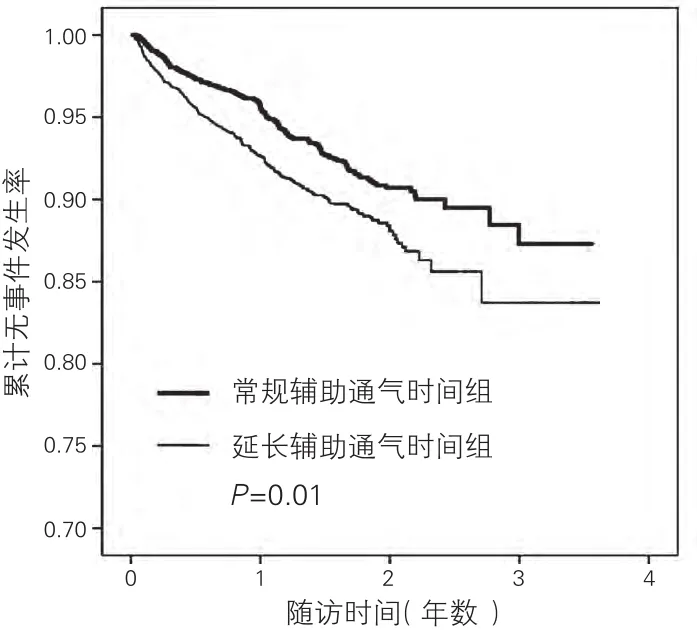
圖2 兩組患者因心臟病再次入院的Kaplan-Meier生存曲線
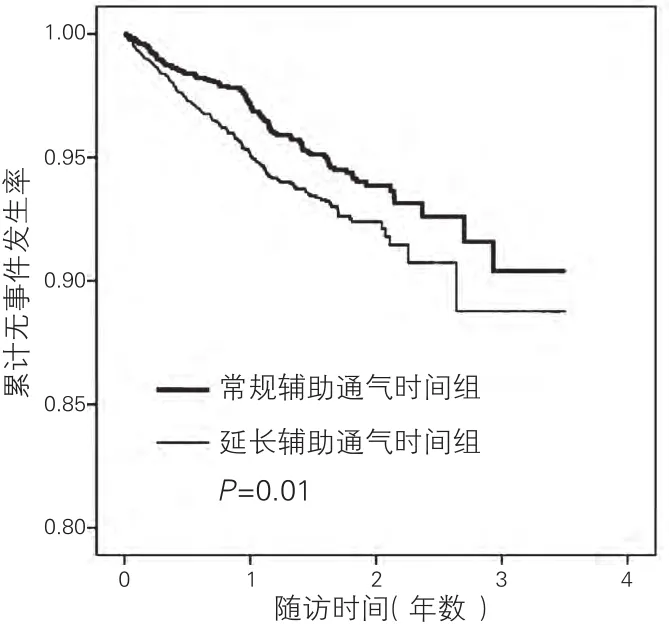
圖3 兩組患者心絞痛發作的Kaplan-Meier生存曲線
3 討論
這是我國目前對CABG術后PMV較大樣本量的回顧性研究。相對于常規輔助通氣的患者,PMV易發生于老年、低體重、有高血壓病史、頻繁心絞痛發作、心功能差、病變冠脈數量多、圍術期血制品、主動脈內氣囊反搏使用及術前靜脈硝酸酯類藥物使用的患者,其院內死亡及并發癥的發生率顯著增加[8]。同時,我們對近期死亡作死亡原因分析發現:30天死亡15例,其中10例為心原性死亡,180天死亡29例,其中19例為心原性死亡,從中我們可以發現30天及180天死亡主要原因為心原性死亡,高于遠期隨訪死亡中心原性死亡占全因死亡的比例50.75%,分析主要原因為少數患者術后出院時病情較重、心功能差。
PMV與遠期隨訪心原性死亡(HR=2.54)、因心臟病再次入院(HR=1.36)的風險顯著增加,而全因死亡(P=0.21)、MACCE事件(P=0.17)的風險無明顯差異,心絞痛發作(P=0.05)則邊緣相關。既往文獻較少對CABG術后PMV患者遠期生存狀態進行分析,Pappalardo等[2]對4 827例行心臟手術的患者按PMV時間≥7天分為延長和不延長輔助通氣組,隨訪(36±12)月,比較生存率并調查問卷隨訪生存質量,發現遠期生存率有顯著差異,隨著術后PMV時間的延長,其遠期生存率逐漸降低,生存質量亦顯著降低,Rajakaruna等[4]對7 553例行心臟手術的患者進行研究,輔助通氣時間>96 h定義為PMV,5年隨訪生存率顯著低下。
近十余年來,隨著術后輔助呼吸模式及鎮靜狀態的調整,患者輔助通氣時的不適已經明顯好轉,但疼痛、焦慮、恐懼無助仍是輔助通氣時的主要感受,這種生理、情感、心理的障礙不僅發生于ICU期間,也持續到出院后。Schou 等對CABG術后輔助通氣時間大于等于24 h并隨訪生存的患者,出院后2~5月訪談其于院內輔助通氣時的感受:不適、疼痛、無法溝通、失去控制及時間、地點定位、孤獨無助、恐懼、瀕死感等不同程度生理、情感、心理障礙,大多數患者隨著順利拔管轉出ICU逐漸恢復,部分患者仍存在頭暈、失眠、夢魘、焦慮、過度緊張、恐懼,尤其是延長輔助通氣的患者,部分甚至需要進行心理治療,并因過度焦慮緊張而增加再就醫率,這些均嚴重影響了患者術后的生活質量。雖然影響患者術后的遠期終點事件及生活質量的因素很多,但臨床實踐及既往研究我們可以看出它們與PMV的顯著相關性。不管是與院內及遠期終點事件的相關性角度,還是對患者術后長期生活質量的影響考慮,均提示我們CABG術后患者應盡快恢復自主呼吸,拔除氣管插管,終止機械輔助通氣。
本研究存在一定的局限: ① 非隨機雙盲的對照研究;② 單中心,但患者來自全國29個省市自治區,具有較為廣泛的代表性,也正是因為單中心的數據,故可大致消除對于手術適應癥的掌握、術前準備、手術技巧及術后治療等較多混雜因素的影響;③ 遠期死亡及并發癥發生率相對較低,也可能導致假陰性的結果,因此本研究定義五個終點事件進行分析,盡可能增加其指導意義。
[1]Higgins TL, Estafanous FG, Loop FD, et al. Stratification of morbidity and mortality outcome by preoperative risk factors in coronary artery bypass patients. JAMA , 1992, 267: 2344-2348.
[2]Pappalardo F, Franco A, Landoni G, et al. Long-term outcome and quality of life of patients requiring prolonged mechanical ventilation after cardiac surgery. Eur J Cardiothorac Surg, 2004, 25: 548-552.
[3]Perterson ED, Coombs LP, Ferguson TB, et al. Hospital variability in length of stay after coronary artery bypass surgery: results from the Society of Thoracic Surgeon’s National Cardiac Database. Ann Thorac Surg, 2002;74: 464-473.
[4]Rajakaruna C, Rogers CA, Angelini GD, et al. Risk factors for and economic implications of prolonged ventilation after cardiac surgery. J Thorac Cardiovasc Surg, 2005, 130: 1270-1277.
[5]Branca P, McGaw P, Light R. Factors associated with prolonged mechanical ventilation following coronary artery bypass surgery.Chest, 2001, 119: 537-546.
[6]Weissman C. Pulmonary complications after cardiac surgery. Semin Cardiothorac Vasc Anesth , 2004, 8: 185-211.
[7]Verrier ED, Wright IH, Cochran RP, et al. Changes in cardiovascular surgical approaches to achieve early extubation. J Cardiothorac Vasc Anesth, 1995, 9: 10-15.
[8]吳慧, 胡盛壽, 鄭哲, 等. 冠狀動脈旁路移植術后患者延長機械通氣時間的危險因素及近期臨床結果分析. 中國心血管雜志, 2012,17: 172-176.
[9]Légaré JF, Hirsch GM, Buth KJ, et al. Preoperative prediction of prolonged mechanical ventilation following coronary artery bypass grafting. Eur J Cardio thorac Surg, 2001, 20: 930-936.
[10]Biancari F, Kangasniemi OP, Aliasim Mahar M, et al. Changing risk of patients undergoing coronary artery bypass surgery. Interact CardioVasc Thorac Surg, 2009, 8: 40-44.
[11]Dunning J, Au J, Kalkat M, et al. A validated rule for predicting patients who require prolonged ventilation post cardiac surgery. Eur J Cardiothorac Surg, 2003, 24: 270-276.
[12]Reddy SL, Grayson AD, Griffiths EM, et al. Logistic risk model for prolonged ventilation after adult cardiac surgery. Ann Thorac Surg ,2007, 84: 528-536.
[13]Cislaghi F, Condemi AM, Corona A. Predictors of prolonged mechanical ventilation in a cohort of 3269 CABG patients. Minerva anestesiol , 2007, 73: 615-621.
Relationship Between Prolonged Mechanical Ventilation After Coronary Artery Bypass Grafting and Long-term Mortality of Cardiac Death
WU Hui, HU Sheng-shou, ZHENG Zhe, YUAN Xin, HOU Jian-feng, CHEN Zu-jun, YAO Yao.
Intensive Care Unit of Cardiovascular Surgery, Cardiovascular Institute and Fu Wai Hospital, CAMS and PUMC,Beijing (100037), China
HU Sheng-shou, Email: shengshouhu@yahoo.com
Objective: To analyze the relationship between prolonged mechanical ventilation (PMV) after coronary artery bypass grafting (CABG) and long-term mortality of cardiac death.
Methods: A total of 4022 consecutive patients undergoing isolated CABG in our hospital from 2006-01 to 2008-12 were retrospectively analyzed. The patients were divided into 2 groups, Conventional group, n=1764 patients with mechanical ventilation time ≤12 hours and PMV group, n=2205 patients with mechanical ventilation time >12hours.Multivariate Cox regression analysis was conducted to analyze the relationship between PMV and the long-term endpoint events including all-cause death, cardiac death, major adverse cardiac and cerebrovascular events (MACCE), angina and re-hospitalization rate.
Results: Compared with Conventional group, PMV group presented the higher rates of cardiac death (HR=2.54,95%CI 1.14-5.66) and re-hospitalization rate (HR=1.36, 95% CI 1.10-1.69) both P<0.05. PMV patients had the critical correlation to angina occurrence (HR=1.29, 95%CI 0.99-1.68), P=0.05, had no correlation to all-cause death (HR=1.38,95%CI 0.83-2.29) and MACCE (HR=1.20, 95%CI 0.93-1.55) both P>0.05.
Conclusion: PMV obviously increased the long-term cardiac death rate and re-hospitalization rate in patients with cardiovascular disease.
Coronary artery bypass grafting; Mechanical ventilation; Long-term follow-up; Mortality; Major adverse cardiac and cerebrovascular events
100037 北京市,中國醫學科學院 北京協和醫學院 心血管病研究所 阜外心血管病醫院 成人外科中心重癥監護病房
吳慧 主治醫師 博士 主要從事成人心血管外科圍術期治療 Email: wuhuifw@163.com 通訊作者:胡盛壽 Email:shengshouhu@yahoo.com
R541
A
1000-3614(2014)03-0216-04
10.3969/j.issn.1000-3614.2014.03.015
2013-10-08)
(助理編輯:曹洪紅)

