大蒜素的臭氧氧化合成以及在大蒜精油中的應用研究
, ,,,
(暨南大學理工學院食品科學與工程系,廣東廣州 510632)
大蒜素的臭氧氧化合成以及在大蒜精油中的應用研究
李文清,周華*,晏日安,黃雪松,歐仕益
(暨南大學理工學院食品科學與工程系,廣東廣州 510632)
為了提高大蒜素的產率和大蒜精油中大蒜素的含量,本文以二烯丙基二硫醚為原料,以臭氧為氧化劑化學合成大蒜素,研究反應溫度、反應時間、反應物濃度、臭氧流量對大蒜素產率的影響。結果表明:大蒜素產率隨著反應時間的增加而不斷上升,但在反應進行4h后,有副產物產生;大蒜素產率隨著反應溫度、二烯丙基二硫醚濃度、臭氧流量的增加呈現先上升后下降的趨勢。采用響應面分析法,得到了大蒜素的最優合成條件:反應時間為4.0h,反應溫度為8.06℃,臭氧通入量為0.28L/min,二烯丙基二硫醚濃度為0.18mmol/mL,大蒜素產率為59.53%。說明最優條件下,采用臭氧氧化大蒜精油,可以獲得富含大蒜素的大蒜精油,大蒜精油的品質得到了提升和改善。
大蒜素,臭氧,氧化,大蒜精油
大蒜素(別名:二烯丙基硫代亞磺酸酯;英文名:Allicin)是大蒜中最具代表性的一種含硫化合物,就其風味而言,大蒜素比大蒜中其他含硫化合物更接近新鮮大蒜的味道[1],其生物活性特別是抗氧化活性更是遠遠強于大蒜中的其他化學成分[2-4]。目前制備大蒜素的方法主要有兩種:一、從大蒜中直接提取,李瑜等報道用乙醇提取大蒜,可以得到大蒜素含量為75.03%的大蒜精油[5],但放置一段時間后,大蒜素因為分解而所剩無幾[6]。必須說明的是,目前工業生產中使用的大蒜精油,基本都采用水蒸氣提取法[7-8]。但是該方法得到的不是大蒜素,而是以二烯丙基二硫醚為主要成分的混合物。二、化學合成法,采用雙氧水[9]或對氯過氧苯甲酸[10]為氧化劑,以二烯丙基二硫醚為反應原料,經化學合成得到。這兩種方法各有利弊,直接提取法,優點在于純天然,缺點是成本較高;第二種方法優點在于合成效率高,但是產品非天然。但無論采用上述哪種方法,大蒜素均不能保存太長的時間。為了提高大蒜素的產率和大蒜精油中大蒜素的含量,本文以二烯丙基二硫醚為模型化合物(其為水蒸氣提取大蒜精油中的主要成分),采用臭氧(家庭一般具有消毒柜,里面包括臭氧發生器)氧化制備大蒜素,研究合成大蒜素的影響因素和最優工藝條件。并將此最優工藝條件應用于大蒜精油(由水蒸氣常壓蒸餾法提取得到)的臭氧氧化反應中,得到富含大蒜素的大蒜精油,從而提高其生物活性,保持新鮮大蒜的味道。該方法是提高大蒜精油品質的一種簡單有效方法。
1 材料與方法
1.1材料與儀器
二烯丙基二硫醚、L-半胱氨酸、DTNB、Tris-Base緩沖劑 購自阿拉丁試劑公司;氫氧化鈉、冰乙酸 購自廣州化學試劑廠;石油醚、乙酸乙酯、無水乙醇、硅膠、濃鹽酸、二氯甲烷 購自天津市大茂化學試劑廠;大蒜 購自于暨南大學興安超市。
TU-1900型雙光束紫外可見分光光度計 北京普析通用儀器有限公司;Acculab ALC210型電子分析天平 上海第二天平儀器廠;HJ-5多功能攪拌器 常州澳華儀器有限公司;101A-1 型電熱鼓風干燥箱 上海實驗儀器廠有限公司;WFH-203(ZF-I)型三用紫外分析儀 上海顧村電光儀器廠;臭氧發生器 上海實驗儀器廠有限公司;pH檢測儀 上海安亭科學儀器廠。
1.2實驗方法
1.2.1 大蒜素的臭氧氧化合成 稱取一定質量的二烯丙基二硫醚,將其移至干凈的三口燒瓶中,再加入5mL無水乙醇。將三口燒瓶置于水浴鍋中,保持一定溫度,打開臭氧發生器通入臭氧。反應開始后,用TLC法跟蹤反應進程,待反應結束后使用柱層析分離純化得到大蒜素。經核磁測定產物結構,其氫譜和碳譜數據為1HNMR(400MHz,CD3COOD):δ 3.72~3.92(m,4H),5.20~5.56(m,4H),5.88~5.99(m,2H)ppm;13CNMR(75MHz,CD3COOD):δ 35.02、59.90、119.10、124.00、125.80、132.90ppm。與文獻報道一致[10]。

在5mL的容量瓶中的依次加入1.0mmol/L半胱氨酸溶液0.5mL,稀釋后的大蒜素樣品液0.5mL,在26℃保溫15min。而后再加入1mL 1.0mmol/L DTNB溶液,50mmol/L pH7.5的Tris-HCl緩沖溶液定容,26℃下保溫15min,412nm波長測定其吸光值A。
大蒜素含量計算方法如下:
C大蒜素=ΔA412×d/(2×14150ml/mmol)
ΔA412=A0-A
式中:d為總稀釋倍數;在本實驗中稀釋倍數為10000。
1.2.3 大蒜精油的提取 選擇顆粒完整、無霉爛的大蒜200g,大小不限。切去大蒜的鱗莖盤,去掉大蒜干枯鱗片葉備用。用破碎機破碎,在30℃下酶解1h。將酶解后的大蒜,按固液比1∶2加入394.5mL蒸餾水中,上鍋蒸餾。電熱套功率保持在50~75W,時間1.5h,收集蒸出料液備用。用二氯甲烷提取分離大蒜油,經硅膠脫水和活性炭脫色精制,得到大蒜精油。
1.2.4 大蒜精油的臭氧氧化 將1.2.3提取的大蒜精油配成一定濃度的乙醇溶液,按1.2.1實驗步驟進行臭氧氧化。反應時間為4h,反應溫度為8℃,臭氧流量為0.28L/min,臭氧氧化大蒜精油。用TLC法監測反應體系中的二烯丙基二硫醚已經反應完全,而后過柱分離,得到大蒜素粗品,再按步驟1.2.2的分析方法,計算大蒜素產率,公式如下:
式中:m(大蒜素)為反應得到的大蒜素質量;m(二烯丙基二硫醚)為反應物中所含二烯丙基二硫醚質量。
1.2.5 單因素實驗
1.2.5.1 反應溫度的影響 控制反應時間為3h,二烯丙基二硫醚乙醇溶液濃度為 0.4mmol/mL,臭氧流量為0.15L/min的情況下,改變反應溫度,考察其對大蒜素產率的影響。每個實驗點做三次重復。
1.2.5.2 反應時間的影響 在反應溫度為20℃,二烯丙基二硫醚乙醇溶液濃度為0.4mmol/mL,臭氧流量為0.15L/min的條件下,考察反應時間對大蒜素產率的影響。每個實驗點做三次重復。
1.2.5.3 臭氧流量的影響 在反應溫度為20℃,二烯丙基二硫醚乙醇溶液濃度為0.4mmol/mL,反應時間為3h的條件下,考察臭氧流量對大蒜素產率的影響。每個實驗點做三次重復。
1.2.5.4 原料濃度的影響 在反應溫度為20℃,臭氧流量為0.15L/min,反應時間為3h的條件下,考察二烯丙基二硫醚乙醇溶液濃度對大蒜素產率的影響。每個實驗點做三次重復。
1.2.6 Box-Behnken設計實驗 應用Design Expert軟件,根據Box-Behnken中心組合設計原理,以大蒜素的產率為響應值,在單因素實驗結果的基礎上,對反應溫度、反應時間、臭氧濃度、原料濃度四個因素進行響應曲面實驗設計。因素水平見表1。每個實驗點做三次重復。

表1 響應面實驗設計因素水平表
1.2.7 數據處理 以SPSS軟件作統計學分析,實驗數據以平均數標準差表示。
2 結果與討論
2.1臭氧氧化合成大蒜素的影響因素探討
2.1.1 反應溫度對大蒜素合成產率的影響 由圖1可知,在保持其他條件不變的情況下,大蒜素的產率先是隨著反應溫度的升高而增加,在10℃時產率達到最大值(46.99%),隨后溫度繼續升高,產率下降,溫度升到30℃時產率僅為27.34%。故選取溫度0、10、20℃為響應面溫度的三水平。
2.1.2 反應時間對大蒜素產率的影響 從圖2可知,隨著反應時間的增加,大蒜素的產率不斷提高,反應至1h,大蒜素的產率為14.37%,反應進行到5h,產率達到40.12%。通過TLC法跟蹤反應進程,當反應進行到4h時,產物中伴隨有副產物的出現。故選取時間3、3.5、4h為響應面時間的三水平。

圖1 反應溫度對大蒜素產率的影響
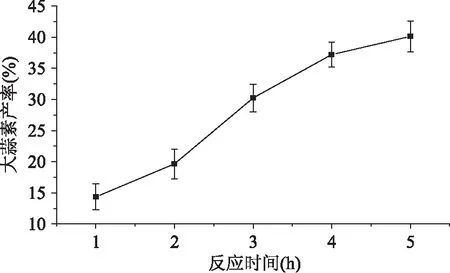
圖2 反應時間對大蒜素產率的影響
2.1.3 臭氧流量對大蒜素產率的影響 從圖3可以看出,隨著臭氧流量從0.10L/min增大到0.30L/min的過程中,大蒜素的產率呈現先上升后下降的趨勢,當臭氧流量為0.20L/min時,大蒜素的產率最高為38.63%,之后隨著臭氧流量的增大,大蒜素的產率反而下降。這可能是由于臭氧量增大到一定程度后,臭氧氧化了二烯丙基二硫醚中的兩個雙鍵,產生副產物。故選取臭氧流量0.15、0.20、0.25L/min為響應面臭氧流量的三水平。

圖3 臭氧流量對大蒜素產率影響
2.1.4 原料濃度對大蒜素產率的影響 從圖4可以看出,隨著二烯丙基二硫醚的濃度不斷增大,大蒜素的產率表現為先增加后減少,當二烯丙基二硫醚濃度為0.2mmol/mL時,大蒜素的產率最高,達到48.32%。隨后,大蒜素的產率不斷降低。故選取二烯丙基二硫醚濃度0.2、0.3、0.4mmol/mL為響應面二烯丙基二硫醚濃度的三水平。

圖4 反應物濃度對大蒜素產率的影響
2.2運用響應面法分析影響因素并確定最優條件
2.2.1 臭氧氧化合成大蒜素的實驗數據分析 以反應溫度、反應時間、臭氧流量、原料濃度為四個可控的工藝參數,以大蒜素產率為實驗指標,采用Box-Behnken設計方法來優化大蒜素合成工藝條件,實驗設計方案及結果見表2。
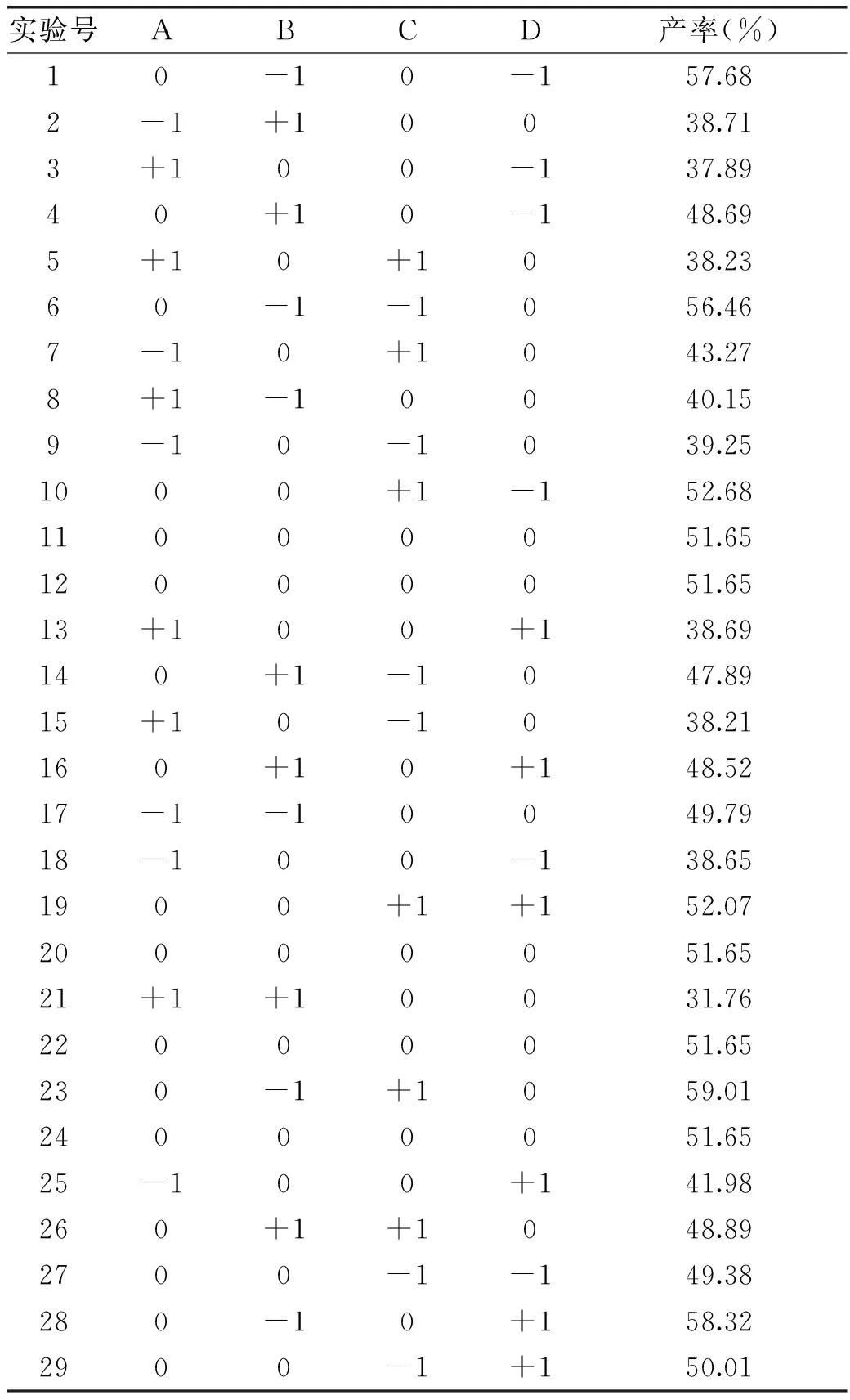
表2 Box-Behnken設計實驗的結果

表3 回歸模型方差分析
注:*:p<0.05,表示顯著;**:p<0.01,表示極顯著。 通過Design-Expert軟件,對表3實驗數據進行多元回歸擬合,獲得了大蒜素產率對編碼自變量反應溫度、反應時間、臭氧流量、原料濃度的二次多元回歸方程:Y(%)=30.38750+2.99725×A-98.03333×B+8.88167×C+91.23333×D+0.67250×A×B-0.20000A×C-1.26500×A×D-7.75000×B×C-40.50000×B×D-12.40000×C×D-0.12343×A2+131.79167×B2+0.011667×C2-38.33333×D2。該方程回歸顯著,R2=0.9803,說明回歸方程的擬合程度良好,失擬較小,可以用該方程代替真實實驗點進行分析。方程中A、B、C對吸光值的影響達顯著水平,方程中A2、B2對吸光值的影響也達極顯著水平。表明實驗因子對響應值不是簡單的線性關系。精密度>4.0是令人滿意的,而本模型的精密度為23.83,說明模型適當。
2.1.5 響應面分析及反應的最優條件 采用Design-Expert軟件分析了反應的最優化條件,得到臭氧氧化合成大蒜素的最佳條件為反應時間為4.0h,反應溫度為8.06℃,臭氧通入量為0.28L/min,二烯丙基二硫醚濃度為0.18mmol/mL。為檢驗響應曲面法所得結果的可靠性,采用上述優化條件下合成大蒜素,測得大蒜素產率為59.53%,與理論預測值59.77%相比,其相對誤差較小。因此,基于響應面分析法所得的臭氧氧化合成大蒜素的反應條件參數準確可靠,具有實用價值。
2.3大蒜精油的臭氧氧化
采用2.1.5提到的反應條件對大蒜精油進行臭氧氧化,大蒜素的綜合產率為63.61%。該值比理論預測值59.77%要略高一些,原因可能是:大蒜精油包含二烯丙基二硫醚、二烯丙基三硫醚、二烯丙基硫醚等混合物,這些化合物之間可以相互轉化,并存在一定的化學平衡,在二烯丙基二硫醚氧化生成大蒜素的過程中,使上述平衡發生移動,生成了比理論值更多的大蒜素。我們將氧化后的大蒜精油進行抗氧化活性研究,與氧化前的大蒜精油相比,其抗氧化性得到顯著提高,相關內容將另文發表。
3 結論
3.1 以單一的模型化合物二烯丙基二硫醚為反應原料,以臭氧為氧化劑,合成了大蒜素純品。研究反應溫度、反應時間、反應物濃度、臭氧流量對大蒜素產率的影響:大蒜素的產率隨著反應時間的增加而提高,但是在反應時間超過4h后,有副產物二烯丙基三硫醚等產生;大蒜素產率隨著反應溫度、二烯丙基二硫醚濃度、臭氧流量的增加產率表現為先上升而后下降。
3.2 針對單因素反應溫度、反應時間、反應物濃度、臭氧流量對大蒜素產率的影響,采用響應面法得到優化后的臭氧氧化合成大蒜素的反應條件:反應時間為4h,反應溫度約為8℃,臭氧通入量為0.25L/min,二烯丙基二硫醚乙醇溶液濃度為0.20mmol/mL。
3.3 采用最優條件下,用臭氧氧化大蒜精油,測定大蒜精油中大蒜素反應前后的含量,大蒜素產率達到63.96%,說明最優條件下,采用臭氧氧化大蒜精油,可以獲得富含大蒜素的大蒜精油,使大蒜精油的品質得到提升。
[1]孫君社,高孔榮. 大蒜和洋蔥風味物及其萃取[J]. 中國調味品,1995,10:9-13.
[2]Ilic D P,Nikolic V D,Nikolic L B,etal. Thermal degradation,antioxidant and antimicrobial activity of the synthesized allicin and allicin incorporated in gel[J]. Hem Ind,2010,64(2):85-91.
[3]Kubec R,Cody R B,Dane A J,etal. Applications of direct analysis in real time-mass spectrometry in allium chemistry.(Z)-butanethial S-oxide and 1-butenyl thiosulfinates and their S-(E)-1-butenyl cysteine S-oxide precursor from Allium siculum[J]. J Agric Food Chem,2010,58(2):1121-1128.
[4]Okada Y,Tanaka K,Sato E,etal. Antioxidant activity of the new thiosulfinate derivative,S-benzyl phenylmethanethiosulfinate,from Petiveria alliacea L[J]. Org Biomol Chem,2008,6(6):1097-1102.
[5]李瑜,許時嬰. 大蒜中硫代亞磺酸酯的提取工藝[J]. 無錫輕工大學學報,2004,23:76-81.
[6]Okada Y,Tanaka K,Sato E,etal. Antioxidant activity of the new thiosulfinate derivative,S-benzyl phenylmethane thiosulfinate,from Petiveria alliacea L[J]. Org Biomol Chem,2008,6(6):1097-1102.
[7]羅蘭,劉佳佳,何舒瀾. 不同提取方法的大蒜揮發油GC-MS比較分析[J]. 中成藥,2008,30(1):139-141.
[8]王搖風,孫蕓,熊曉輝,等. 大蒜油提取技術的研究進展[J]. 中國調味品,2010,35(3):31-33.
[9]Fillmore F,Huang B G.Garlic Chemistry nitric oxide oxidation of(2-propenyl)cysteine and S-(2-Propenyl)-Cystein Sulfoxide[J]. J Org Chem,1994,59:3227-3229.
[10]Vaidya V,Ungold K U,Pratt D A. Garlic:source of the ultimate antioxidants-sulfenic acids[J]. Angew Chem Int Ed,2009,48(1):157-160.
[11]Lawson L H,Han P A. spectrophoto metric method for quantitative determination of allicin and total garlic thiosulfinates[J]. Anal Biochem,1995,225(1):157-160.
Study on the synthesis of allicin by using ozone and the application of the method on garlic oil
LIWen-qing,ZHOUHua*,YANRi-an,HUANGXue-song,OUShi-yi
(Department of Food Science and Technology,Jinan University,Guangzhou 510632,China)
In order to attain the higher yield of allin and higher content of that in garlic oil,the key effect factors were investigated:as the reaction time was prolonged,the yield of allicin was increased,but the byproduct of reaction was presented after more than four hours. As the reaction temperature and reactant concentration and the ozone flow increased,the yield of allicin was first increasing and then decreasing. The respond surface methodology was used to optimize the synthesis condition of the reaction:the reaction time was 4h,and the reaction temperature was about 8.06℃,and the ozone flow was 0.28L/min,and reactant concentration was 0.18mmol/mL. In the above optimized synthesized condition,the ozone was used to oxidize the garlic oil,the yield of allicin was 59.53%. The garlic oil with high content of allicin could be obtained and the quality of garlic oil could be improved in the above-mentioned optimized condition.
allicin;ozone;oxidation;garlic oil
2013-06-28 *通訊聯系人
李文清(1987-),男,碩士研究生,研究方向:大蒜化學。
國家自然科學基金(31101323)資助。
TS234.3
:B
:1002-0306(2014)01-0202-05

