孕婦血清妊娠相關蛋白A魯米諾氧通道免疫測定方法的建立①
郝穎新 侯麗英 周宇捷 張月香 李會強
(天津醫科大學醫學檢驗學院臨床免疫學教研室,天津 300203)
妊娠相關蛋白A(Pregnancy associated plasm a protein A,PAPP-A)是一種由胎盤合體滋養層細胞和蛻膜產生的,與妊娠相關的大分子糖蛋白。孕早期在母體外周血中即可檢測到PAPP-A,且隨孕周增加,其水平會持續上升,孕足月時達到高峰[1,2]。目前,國際上普遍認為,PAPP-A是孕早期篩查唐氏綜合征的敏感指標[3],而且近年來,有研究發現,PAPP-A對許多妊娠并發癥也有一定的預測能力,包括妊娠期高血壓疾病、胎兒宮內生長受限、出生低體重兒及妊娠期糖尿病等[4-6]。因此,它是一個重要的產前篩查指標。
目前檢測PAPP-A的最常用方法是時間分辨熒光分析法(Time resolved fluoroimmunoassay,TRFIA),但其操作繁瑣,需反復洗板,耗時長。魯米諾氧通道免疫測定(Luminescent oxygen channeling immunoassay,LOCI)技術問世于上世紀90年代,具有均相、免清洗高檢測性能等優點,本實驗利用該方法建立了定量檢測血清PAPP-A的方法,并對檢測性能進行了初步評價。
1 材料與方法
1.1 血清標本 選自天津市中心婦產科醫院孕早期(孕9~13+6周)正常產檢孕婦血清標本50份及健康體檢男性混合血清。
1.2 主要試劑和儀器 受體微球和鏈霉親和素化的供體微球購自上海博陽生物科技有限公司;兔抗人PAPP-A多克隆抗體和鼠抗人PAPP-A單克隆抗體購自英國Abcam公司;長臂活化生物素(NHS-LCBiotin)購自美國Pierce公司;96孔發光微孔板和光激化學發光檢測儀購自上海博陽生物科技有限公司。
1.3 受體微球包被 取受體微球,按照參考文獻[7]的方法,用兔抗人PAPP-A多克隆抗體包被,調節受體微球濃度為1 mg/ml,避光保存于4℃備用。
1.4 生物素標記 參照產品說明書,將活化生物素溶于二甲基甲酰胺(DMF)中,按照生物素與鼠抗人PAPP-A單克隆抗體的摩爾比為20∶1的比例將生物素緩慢、逐滴加入抗體溶液中,室溫反應1 h;用0.01 mol/L PBS溶液于4℃透析24 h去除游離生物素,分裝,4℃保存備用。
1.5 標準品的配制 取PAPP-A純品,用含20%滅活小牛血清0.1 mol/L、pH7.8的Tris-HCl緩沖液配制成不同濃度的標準品溶液:0、40、160、800、3 200、8 000 mU/L,并利用質控血清進行校準,分裝后-20℃保存備用。
1.6 檢測步驟 向微孔板中依次加入50 μl生物素化抗體、10 μl待測樣品、50 μl受體微球,37℃ 孵育15 min,避光條件下再加入140 μl感光微粒,37℃孵育8 min后用化學發光檢測儀檢測光信號,以標準品濃度為橫坐標,光信號強度為縱坐標,用四參數擬合方式繪制PAPP-A濃度-光信號強度標準曲線,并獲得數學函數方程,根據光信號強度通過數學函數計算待測標本中PAPP-A的濃度。
1.7 檢測性能評價
1.7.1 靈敏度 以零參考值標準品當做樣品重復檢測20次,計算其均值及標準差。以其測定值的均值加上兩倍的標準差所得信號值,代入標準曲線方程計算得其分析靈敏度;將低值標本倍比稀釋后重復測定10次,當CV>20%時所對應的濃度值,即為該方法功能靈敏度。
1.7.2 精密度 取孕早期(孕9~13+6周)正常產檢孕婦的血清配制成高、中、低值的待測樣本,分裝后-20℃冷凍保存。每個濃度的標本分別連續測定10次計算各濃度批內的均值、標準差及變異系數(CV);每個濃度每天測定一次,連續測定10 d,計算各濃度日間的均值、標準差及CV。
1.7.3 添加回收試驗 將健康男性體檢者血清分為三份,分別向其中兩份加入等體積不同濃度的標準品,添加濃度分別是200、2 000 mU/L,另一份加入同體積但無PAPP-A的基質,用本試驗建立的方法檢測各樣品的濃度值,并按照下列公式計算回收率:回收率(%)=(分析樣品測定濃度-基礎樣品測定濃度)/加入濃度×100%。
1.7.4 干擾性檢測 主要通過干擾試驗評價,分別向100 μl低值血清和高值血清中加入濃度為210 μmol/L的膽紅素、5 g/L的血紅蛋白、15 mmol/L的甘油三酯各50 μl,對照樣本添加相同體積但無PAPP-A的基質,用本試驗建立的方法檢測各樣品的濃度值,并按照下列公式計算干擾率:干擾率(%)=(基礎樣品的測定濃度-分析樣品的測定濃度)/基礎樣品的測定濃度×100%。
1.7.5 Hook效應 用BASE稀釋液將PAPP-A標準品稀釋成 10 個濃度值,20、40、80、160、400、800、1 600、3 200、4 000、8 000(mU/L),每個濃度值重復測定4次,計算各濃度值均數。
1.7.6 方法學比較 分別用本實驗建立的方法和時間分辨熒光分析法檢測50例臨床標本的PAPP-A含量,以時間分辨熒光分析法測定值為橫坐標,以本實驗建立方法測定值為縱坐標,繪制散點圖,對兩種測定方法所得數據做相關分析。
2 結果
2.1 測定方法的建立 選用1∶100、1∶200、1∶300稀釋的受體微球(已包被)分別與1∶500、1∶1 000、1∶2 000稀釋的生物素化抗體進行組合,然后對最高標準品濃度和零值標準品濃度進行測定,通過棋盤滴定,結果顯示最高標準品光信號強度與零值標準品光信號強度比值(P/N)在5 μg/ml受體球與5.86 μg/ml稀釋度生物素化抗體組合達到最大值,本實驗最適合的生物素化抗體濃度為5.86 μg/ml(1∶500稀釋),最適的受體球濃度是5 μg/ml(1∶200稀釋)。標準品劑量-反應曲線如圖1,數學模型如下:y=(51 378.13-43.97)/[1+(x/6695.54)-0.986]+43.97。
2.2 方法學評價
2.2.1 靈敏度利用本實驗建立的方法檢測所得PAPP-A的分析靈敏度為2.8 mU/L,功能靈敏度為4.6 mU/L。
2.2.2 精密度 利用本實驗建立的方法檢測PAPP-A低、中、高值混合定值血清所得結果,顯示該方法的批內變異系數及批間變異系數均<10% 。測定結果見表1。
2.2.3 添加回收試驗 利用本實驗建立的方法檢測上述分析樣品的濃度200、5 000 mU/L,平均回收率分別為100.3%、96.7%。
2.2.4 干擾性檢測 利用本實驗建立的方法檢測上述分析樣品,血紅蛋白、總膽紅素和甘油三酯的干擾率見表2。
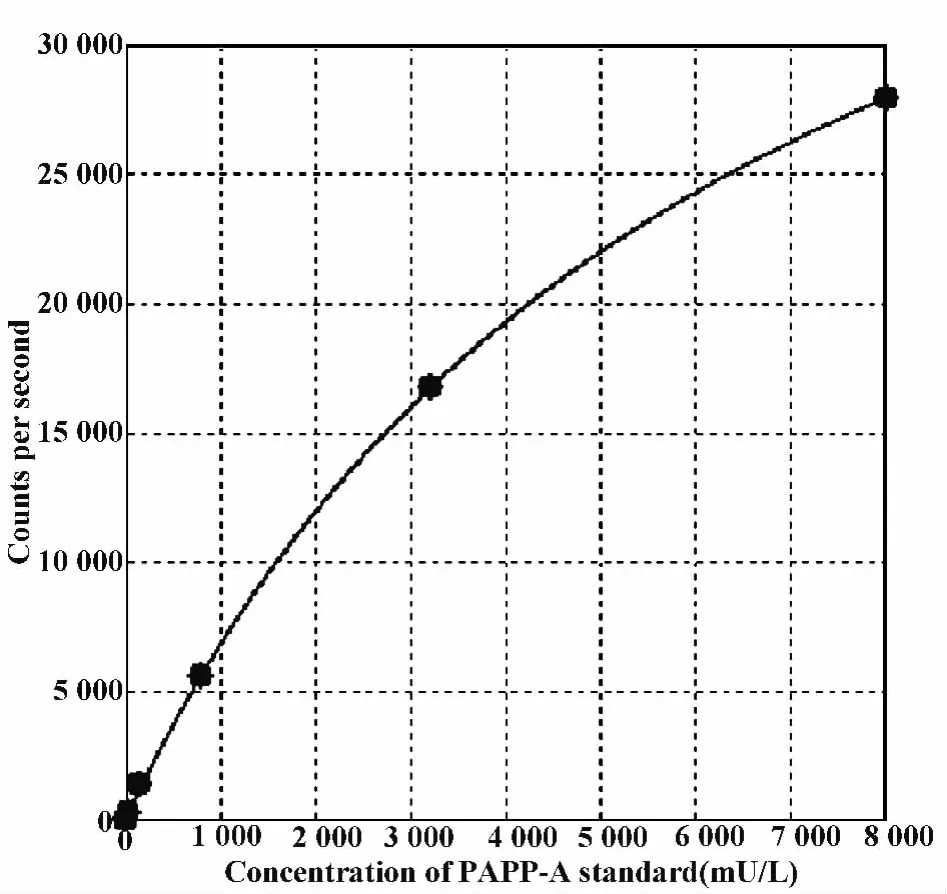
圖1 PAPP-A劑量-反應曲線Fig.1 Standard curve for PAPP-A

表1 精密度測定結果Tab.1 Precision of LOCI kit

表2 干擾率測定結果Tab.2 Specificity of LOCI kit
2.2.5 Hook效應 本檢測方法測定PAPP-A濃度在0~8 000 mU/L范圍內未見Hook效應,見圖2。
2.2.6 與時間分辨熒光分析法的比較 由線性回歸方程及相關系數顯示,本實驗建立的方法與時間分辨熒光分析法有較好的相關性,回歸方程為y=0.970x+71.85,r2=0.989,相關曲線見圖3。比較兩種方法的檢測性能(表3),可以看出兩者無顯著差別。時間分辨熒光分析法的檢測性能數據來自于PerkinElmer公司生產的PAPP-A試劑盒說明書。
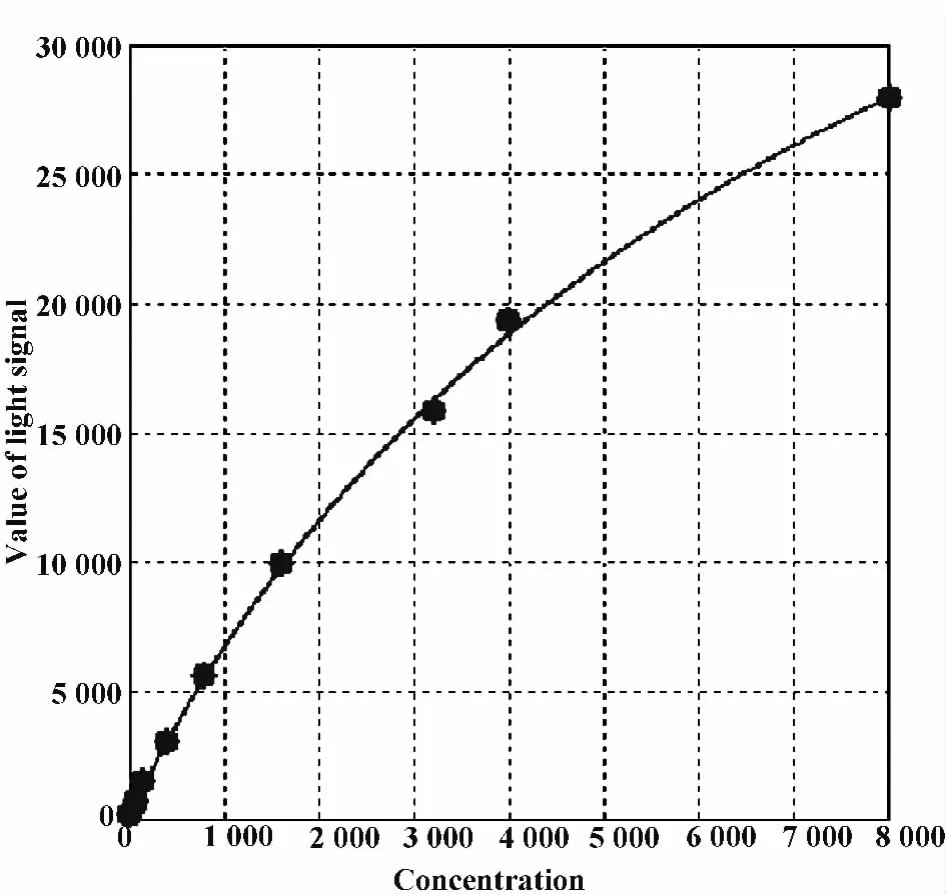
圖2 PAPP-A LOCI Hook實驗檢測信號值Fig.2 Hook experiment signal value of PAPP-A
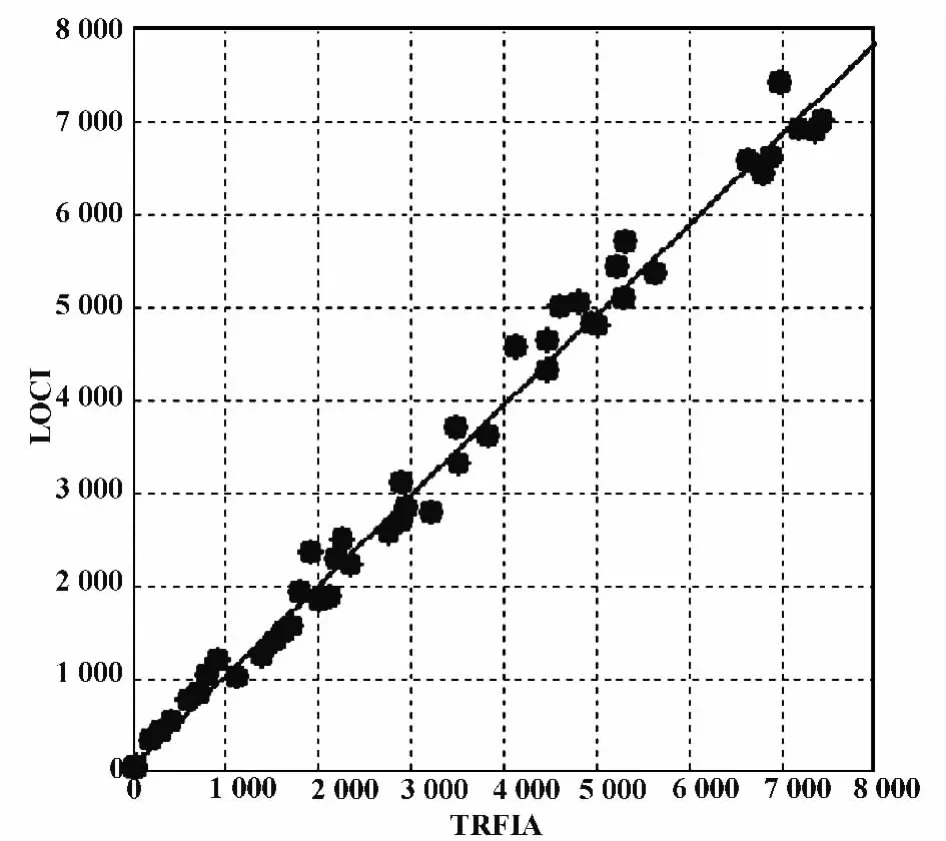
圖3 LOCI法與時間分辨熒光分析法的相關性Fig.3 Linear correlation between LOCI and TRFIA

表3 LOCI法與TRFIA法的性能比較Tab.3 Comparison of LOCI kit and TRFIA kit
3 討論
PAPP-A是與妊娠相關聯的一種大分子糖蛋白,測定孕婦血清PAPP-A含量變化在篩查異常胎兒方面得到國內外學者的證實和重視。當前檢測PAPP-A的方法主要有酶聯免疫測定法[8]和時間分辨熒光分析法[9],最常用的是時間分辨熒光分析法,此方法雖然準確性和特異性較高,但是孕婦血清PAPP-A含量高,標本均需要稀釋后檢測,增加了操作步驟,容易產生誤差,同時實驗需要兩次孵育及洗板過程,耗時2.5 h以上,產檢孕婦不能當天獲得篩查結果,給臨床帶來了不便,且利用該方法開發的進口試劑盒成本較高,不適合在基層醫療機構推廣使用。
魯米諾氧通道免疫測定(Luminescent oxygen channeling immunoassay,LOCI)技術是一種通過化學發光檢測微粒間的結合,進而檢測分析物含量的方法。最初是由 Ullman等[10]在 1994年報道,并由PerkinElmer公司完成商品化。該技術原理是感光微粒在680 nm的光照下激發產生單線態氧,單線態氧在極短距離內(<200 nm)擴散至發光微粒,與其中的發光物質反應,即可產生560~580 nm的化學發光,根據檢測到的光信號強度定量被檢測物的濃度。該技術以其獨特的檢測方法,實現了均相、免洗和高通量檢測,徹底避免了清洗和分離所帶來的誤差[11,12]。國內已有學者利用此項技術建立了促甲狀腺激素、胰島素、絨毛膜促性腺激素等多項微量物質的檢測方法[13-15]。
我們建立的血清PAPP-A的LOCI檢測方法,其分析靈敏度為2.8 mU/L,功能靈敏度為4.6 mU/L;回收實驗的回收率為96.7%~100.3%,符合臨床檢測回收率在90%~110%的要求;批內精密度與批間精密度分別為5.91%~7.94%和6.14%~9.69%,均小于10%,說明本法有較好的重復性;特異性分析中各干擾物的干擾率均<10%,說明本法有較強的抗溶血、黃疸及脂血的干擾;本實驗有較寬的線性范圍(2.8 mU/L~8 000 mU/L),當PAPP-A濃度高達8 000 mU/L時無Hook效應;本實驗結果與時間分辨熒光分析法的檢測結果有很好的相關性。
上述實驗結果表明本實驗初步建立的基于LOCI技術檢測PAPP-A的方法,具有較好的檢測性能,與其他試劑盒測定結果之間有較好相關性,且操作簡便,大大縮短實驗時間,有極大的臨床應用潛力,下一步可繼續進行大樣本量實驗,建立不同孕周PAPP-A的中位數,為不同孕周正常值參考范圍提供依據,有望替代同類進口PAPP-A檢測試劑盒。
[1]賈昭華.妊娠相關血清蛋白的臨床應用價值探討[J].中國醫藥指南,2011,9(22):253-254.
[2]熊 敏,楊曉華,周舒香.孕婦血清PAPP-A檢測在產前篩查中的應用[J].中國優生與遺傳雜志,2004,12(3):55-57.
[3]付小國,王素媚,王燕華.孕早期血清AFP、β-HCG、PAPP-A聯合檢測的產前篩查意義[J].中國優生優育,2009,15(2):108-110.
[4]Poon LC,Akolekar R,Lachmann R,et al.Hypertensive disorders in Pregnancy:screening by biophysical and biochemicalmarkers at 11-13 weeks[J].Ultrasound Obstet Gynecol,2010,35:662-670.
[5]Beneventi F,Simonetta M,Lovati E,et al.First trimester pregnancy-associated plasma protein-A in pregnancies complicated by subsequent gestational diabetes[J].Prenat Diagn,2011,31(6):523-528.
[6]Fox NS,Chasen ST.First trimester pregnancy-associated plasma protein-A as a marker for poor pregnancy outcome inpatients with early-onset fetal growth restriction[J].Prenat Diagn,2009,29:1244-1248.
[7]趙 爽,周宇捷,相 平.血清糖類抗原-125均相化學發光免疫檢測方法的初建[J].免疫學雜志,2013,29(5):434-437.
[8]李靈俊,陳淑蓮,李向東.妊娠相關血漿蛋白A定量測定方法的建立[J].天津醫藥,2010,38(5):356-359.
[9]Linskens IH,Levitus M,Frans A,et al.Performance of free betahuman chorionic gonadotrophin(free beta-hCG)and pregnancy assoiated plasma protein-A(PAPP-A)analysis between Delfia Xpress and AutoDelfia systems in The Netherlands[J].Clin Chem Lab Med,2009,47:222-226.
[10]Ullman EF,Kirakossian H,Switchenko AC,et al.Luminescent oxygen channeling assay(LOCITM):sensitive,broadly applicable homogeneous immunoassay method[J].Clin Chem,1996,42(9):1518-1526.
[11]Kricka LJ.Clinical applications of chemilumminescence[J].Anal Chim Acta,2003,500(1):279-286.
[12]Cauchon E,Liu S,Percival MD,et al.Development of a homogeneous immunoassay for the detection of angiotensinⅠin plasma using AlphaLISA acceptor beads technology[J].Anal Biochem,2009,388(1):134-139.
[13]金 磊,周 偉,高月求.光激化學發光免疫檢測法測定TSH功能靈敏度的評價[J].檢驗醫學,2011,26(6):379-382.
[14]鄒麗萍,賀 安,董志寧.胰島素光激化學發光免疫分析法的建立[J].免疫學雜志,2011,27(11):983-986.
[15]高云朝.光激化學發光技術研究進展及應用[J].中華檢驗醫學雜志,2009,32(4):474-476.

