菌克軟膏體外抗菌活性觀察
邵留英,瞿發林,陳 穎,倪玉佳,吳曉燕
菌克軟膏體外抗菌活性觀察
邵留英,瞿發林*,陳 穎,倪玉佳,吳曉燕
目的 觀察菌克軟膏的體外抗菌活性。方法 采用瓊脂擴散法進行藥敏試驗,測定菌克軟膏對4種6株標準致病細菌、9種23株標準致病真菌的抑菌圈直徑,并與林可霉素軟膏和硝酸咪康唑軟膏進行對比。結果 菌克軟膏對4種常見細菌都形成抑菌圈,且對金黃色葡萄球菌、大腸桿菌和枯草桿菌的抑菌圈直徑均大于林可霉素軟膏(P<0.01),對銅綠假單胞菌的抑菌圈直徑與林可霉素軟膏組比較差異無統計學意義(P>0.05)。菌克軟膏對9種常見真菌都形成抑菌圈,且對各種皮膚癬菌、念珠菌、裴氏著色真菌和糠秕馬拉色菌的抑菌圈直徑與硝酸咪康唑軟膏組比較差異無統計學意義(P>0.05)。結論 菌克軟膏體外抗細菌活性強于林可霉素軟膏,抗真菌活性強度與硝酸咪康唑軟膏相同。
菌克軟膏;抗菌活性;林可霉素軟膏;硝酸咪康唑軟膏
0 引言
菌克軟膏為我院自制制劑,批準文號:南制字(2011)F16001,其主藥為鹽酸林可霉素、硝酸咪康唑及醋酸地塞米松,臨床適用于手、足、體、股、頭癬及濕疹、脂溢性皮炎、過敏性皮炎、皮膚瘙癢等皮膚疾病[1-3]。該復方制劑目前尚無體外抗菌活性研究的報道。故本文通過對菌克軟膏和單一成分制劑林可霉素軟膏和硝酸咪康唑軟膏的體外抗菌活性進行對比研究,為菌克軟膏的臨床應用提供科學的實驗依據。
1 材料與試劑
1.1 儀器設備 生物安全柜(HFsafe1200型,上海力申科學儀器有限公司),凈化工作臺(SM-CJ-1FD型,蘇凈安泰),隔水式恒溫培養箱(303-6B型,南通科學儀器廠),霉菌培養箱(MJ-160型,上海躍進醫療器械廠),臺式滅菌器(TMQ.J-2540型,山東新華醫療器械股份有限公司),電熱恒溫鼓風干燥箱(DHG-9240型,上海一恒科技有限公司),紫外可見分光光度計(752N型,上海精科),往復水浴振蕩器(SHA-C型,金壇市晨陽電子儀器廠)。
1.2 培養基 營養瓊脂培養基(批號:140106,杭州天和微生物試劑有限公司),沙堡弱瓊脂培養基(批號:131216,杭州天和微生物試劑有限公司)。
1.3 試驗菌株 細菌:金黃色葡萄球菌3株(ATCC6538、ATCC43300、ATCC25923),大腸桿菌1株(ATCC8739),枯草桿菌1株(ATCC6633),銅綠假單胞菌1株(ATCC27853);真菌:白色念珠菌3株[CMCC(F)C1a、CMCC(F)C1b、CMCC(F)C1c],熱帶念珠菌3株[CMCC(F)C2a、CMCC(F)C2b、CMCC(F)C2c],紅色毛癬菌3株[CMCC(F)T1a、CMCC(F)T1g、CMCC(F)T1h],須癬毛癬菌3株[CMCC(F)T5a、CMCC(F)T5b、CMCC(F)T5c],斷發毛癬菌3株[CMCC(F)T4b、CMCC(F)T4c、CMCC(F)T4d],犬小孢子菌3株[CMCC(F)M3d、CMCC(F)M3e、CMCC(F)M3h],石膏樣小孢子菌3株[CMCC(F)M2b、CMCC(F)M2c、CMCC(F)M2d],裴氏著色真菌1株[CMCC(F)D6j],馬拉色菌1株[CMCC(F)G4h],均購自中國醫學科學院皮膚病研究所。
1.4 試驗藥物 菌克軟膏(規格:含鹽酸林可霉素15 mg/g,硝酸咪康唑15 mg/g,自制,批號:20140224);林可霉素軟膏(規格:含鹽酸林可霉素15 mg/g,自制,批號:20140225);硝酸咪康唑軟膏(規格:含硝酸咪康唑15 mg/g,自制,批號:20140226),陰性對照軟膏(自制,批號:20140227)。
2 方法
2.1 活化菌株 細菌用營養瓊脂培養基,37 ℃培養1~3 d。真菌用沙堡弱培養基,28 ℃培養5~7 d。
2.2 菌懸液制備 挑取一定量的菌落,溶于1 mL滅菌蒸餾水,充分混合均勻,在紫外分光光度計上用滅菌蒸餾水調節菌懸液濁度約為0.5 (OD600),相當于5×106CFU/mL。
2.3 含菌平板制備 取直徑9 cm培養皿,加入融化培養液20 mL,制作成培養基平板。將各菌懸液150 μL用玻璃涂布棒均勻涂布于培養基平板表面。
2.4 打孔加藥 使用直徑7 mm的打孔器在涂菌后的培養基上各打4個孔,將孔內瓊脂挑去后分別將新打開的菌克軟膏、林可霉素軟膏、硝酸咪康唑軟膏和陰性對照軟膏擠入孔內,使軟膏與孔邊緣平齊并充分接觸,勿使軟膏沾染孔外瓊脂平面[3]。
2.5 培養條件 細菌置隔水式恒溫培養箱37 ℃培養3 d,真菌置霉菌培養箱28 ℃培養7 d。
2.6 結果觀察 觀察各軟膏孔周圍抑菌圈大小并記錄其直徑(mm)。抑菌圈直徑取最大徑和最小徑的均數[4]。每株菌至少重復3次。
3 結果
3.1 抗細菌結果 4種軟膏對金黃色葡萄球菌、大腸桿菌、枯草桿菌和銅綠假單胞菌的抑菌效果比較見圖1、表1。
對金黃色葡萄球菌標準株抑菌圈直徑進行方差分析,得出F值為62.45 (P<0.01),說明4種軟膏形成的抑菌圈直徑比較差異有統計學意義。對4種軟膏的抑菌圈直徑均數用LSD法進行兩兩比較,結果表明,陰性對照軟膏分別與菌克軟膏、 林可霉素軟膏和硝酸咪康唑軟膏比較,差異均有統計學意義(P<0.01);菌克軟膏分別與林可霉素軟膏、硝酸咪康唑軟膏比較,差異有統計學意義(P<0.01)。由此可知,各軟膏的抑菌圈直徑大小順序:菌克軟膏>林可霉素軟膏>硝酸咪康唑軟膏>陰性對照軟膏。

圖1 細菌抑菌圈
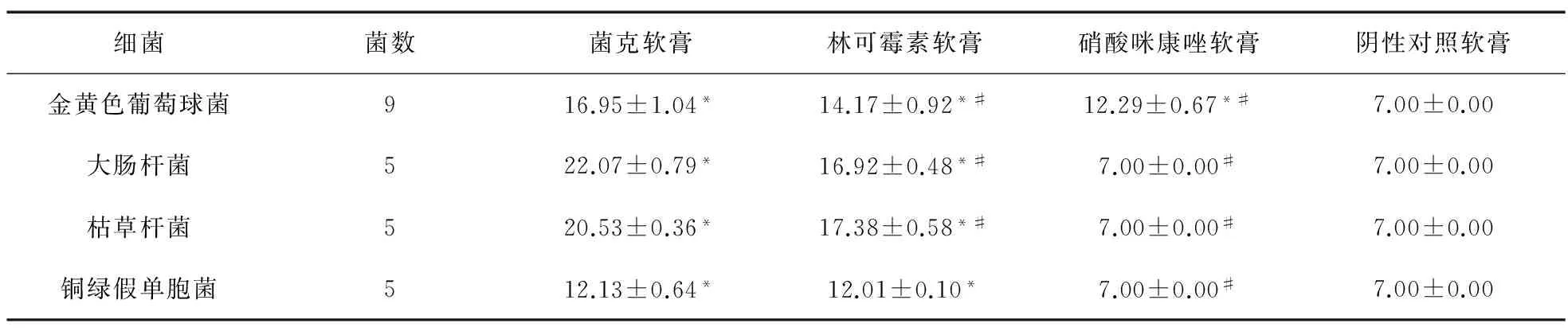
表1 四種軟膏對細菌的抑菌圈直徑比較(mm)
注:*與陰性對照軟膏比較,P<0.01;#與菌克軟膏比較,P<0.01
對大腸桿菌、枯草桿菌標準株抑菌圈直徑進行方差分析,得出F值分別為616.23 (P<0.01)、964.68 (P<0.01),表明4種軟膏形成的抑菌圈直徑比較差異有統計學意義。對4種軟膏的抑菌圈直徑均數分別用LSD法進行兩兩比較,結果表明,陰性對照軟膏分別與菌克軟膏、林可霉素軟膏比較,差異有統計學意義(P<0.01);菌克軟膏分別與林可霉素軟膏、硝酸咪康唑軟膏比較,差異有統計學意義(P<0.01)。由此可知,各軟膏的抑菌圈直徑大小順序:菌克軟膏>林可霉素軟膏>硝酸咪康唑軟膏=陰性對照軟膏。
對銅綠假單胞菌標準株抑菌圈直徑進行方差分析,得出F值為183.71 (P<0.01),說明4種軟膏形成的抑菌圈直徑比較差異有統計學意義。對4種軟膏的抑菌圈直徑均數用LSD法進行兩兩比較,結果表明,陰性對照軟膏組分別與菌克軟膏、林可霉素軟膏比較,差異有統計學意義(P<0.01);菌克軟膏與林可霉素軟膏比較差異無統計學意義(P>0.05);菌克軟膏與硝酸咪康唑軟膏比較差異有統計學意義(P<0.01)。由此可知,各軟膏的抑菌圈直徑大小順序:菌克軟膏=林可霉素軟膏>硝酸咪康唑軟膏=陰性對照軟膏。
硝酸咪康唑軟膏對大腸桿菌、枯草桿菌、銅綠假單胞菌的抑菌圈直徑為7 mm,陰性對照軟膏對4種細菌的抑菌圈直徑測量值為7 mm,與打孔器的直徑相同,實際上并無抑菌圈,說明硝酸咪康唑軟膏對大腸桿菌、枯草桿菌和銅綠假單胞菌均無抗菌活性,陰性對照軟膏對4種測試細菌也無抗菌活性。
3.2 抗真菌結果 4種軟膏對9種試驗真菌的抑菌效果比較見圖2、表2。
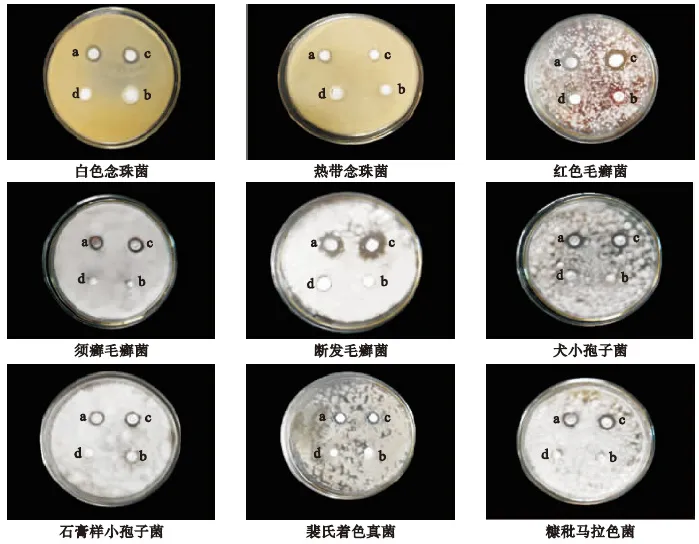
圖2 真菌抑菌圈
對各皮膚癬菌標準株抑菌圈直徑進行方差分析,得出F值為307.60 (P<0.01),表明4種軟膏形成的抑菌圈直徑比較差異有統計學意義。對4種軟膏的抑菌圈直徑均數用LSD法進行兩兩比較,結果表明,陰性對照軟膏組分別與菌克軟膏、硝酸咪康唑軟膏比較差異有統計學意義(P<0.01);菌克軟膏與林可霉素軟膏比較差異有統計學意義(P<0.01);菌克軟膏與硝酸咪康唑軟膏比較差異無統計學意義(P>0.05)。由此可知,各軟膏的抑菌圈直徑大小順序:菌克軟膏=硝酸咪康唑軟膏>林可霉素軟膏=陰性對照軟膏。
對各念珠菌標準株抑菌圈直徑進行方差分析,得出F值為299.03 (P<0.01),表明4種軟膏形成的抑菌圈直徑比較差異有統計學意義。對4種軟膏的抑菌圈直徑均數用LSD法進行兩兩比較,結果表明,陰性對照軟膏組分別與菌克軟膏、硝酸咪康唑軟膏比較差異均有統計學意義(P<0.01);菌克軟膏與林可霉素軟膏比較差異有統計學意義(P<0.01);菌克軟膏與硝酸咪康唑軟膏比較差異無統計學意義(P>0.05)。由此可知,各軟膏的抑菌圈直徑大小順序:菌克軟膏=硝酸咪康唑軟膏>林可霉素軟膏=陰性對照軟膏。
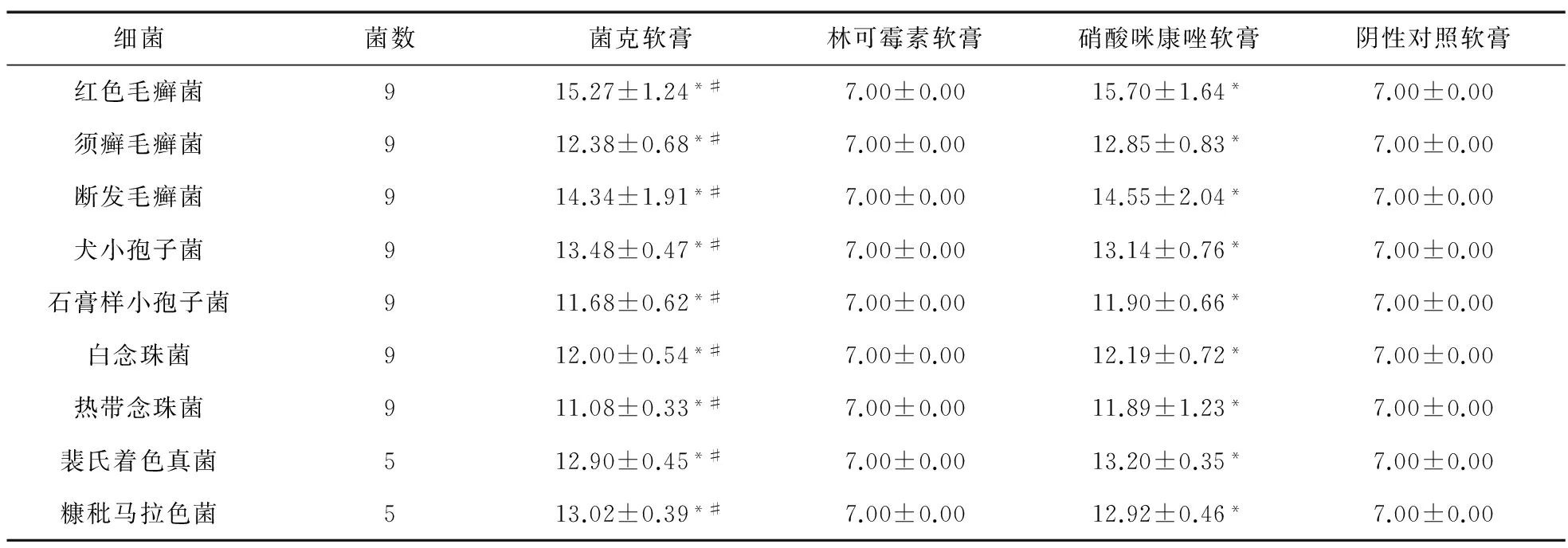
表2 四種軟膏對各皮膚癬菌的抑菌圈直徑比較(mm)
注:*與陰性對照軟膏比較,P<0.01;#與林可霉素軟膏比較,P<0.01
對裴氏著色真菌、糠秕馬拉色菌標準株抑菌圈直徑進行方差分析,得出F值分別為338.36 (P<0.01)、292.80 (P<0.01),說明4種軟膏形成的抑菌圈直徑比較差異有統計學意義。對4種軟膏的抑菌圈直徑均數分別用LSD法進行兩兩比較,結果表明,陰性對照軟膏分別與菌克軟膏、硝酸咪康唑軟膏比較,差異均有統計學意義(P<0.01);菌克軟膏與林可霉素軟膏比較差異有統計學意義(P<0.01);菌克軟膏與硝酸咪康唑軟膏比較差異無統計學意義(P>0.05)。由此可知,各軟膏的抑菌圈直徑大小順序:菌克軟膏=硝酸咪康唑軟膏>林可霉素軟膏=陰性對照軟膏。
林可霉素軟膏、陰性對照軟膏對9種真菌的抑菌圈直徑測量值為7 mm,與打孔器的直徑相同,實際上并無抑菌圈,說明林可霉素軟膏、陰性對照軟膏對9種測試真菌均無抗菌活性。
4 討論
菌克軟膏、林可霉素軟膏、硝酸咪康唑軟膏和陰性對照軟膏均采用水包油型乳劑型基質。菌克軟膏的主藥為鹽酸林可霉素、硝酸咪康唑及醋酸地塞米松。林可霉素的抗菌機制是與敏感菌核糖體的50s亞基結合,抑制肽酰基轉移酶的活性,使肽鏈延伸受阻而抑制細菌蛋白質合成[5]。咪康唑的抗菌機制是抑制真菌羊毛甾醇14α去甲基化酶(P45014DM),阻滯真菌細胞中羊毛甾醇14α位去甲基化反應,達到抑制真菌生長繁殖的目的[6-8]。地塞米松為長效糖皮質激素,具有抗炎、抗病毒、抗過敏、免疫抑制等藥理作用[9]。三藥合用有利于拓寬抗菌譜,增強抗菌活性和降低耐藥風險,并可減少單一用藥的劑量,降低毒副作用和提高臨床療效[10]。
本試驗觀察了菌克軟膏對4種細菌共6株標準菌株的體外抗菌活性,并與單一制劑林可霉素軟膏、硝酸咪康唑軟膏和陰性對照軟膏進行平行對照,觀察到在抗細菌方面,菌克軟膏的抗菌活性等于或者大于林可霉素軟膏。尤其在抗金黃色葡萄球菌、大腸桿菌及枯草桿菌時,菌克軟膏抗菌活性極大于林可霉素軟膏,其原因可能是硝酸咪康唑對金黃色葡萄球菌有殺菌性,對大腸桿菌、枯草桿菌有較強的抑菌性(但無殺菌性),因此鹽酸林可霉素與硝酸咪康唑合用有協同作用。而硝酸咪康唑對銅綠假單胞菌無抑菌性,因此鹽酸林可霉素與硝酸咪康唑合用無協同作用。
本試驗觀察了菌克軟膏對9種真菌共23株標準菌株的體外抗菌活性,并與單一制劑林可霉素軟膏、硝酸咪康唑軟膏和陰性對照軟膏進行平行對照,觀察到在抗真菌方面,菌克軟膏的抗菌活性等于硝酸咪康唑軟膏,其對常見皮膚癬菌、念珠菌、裴氏著色真菌、糠秕馬拉色菌均有抗菌作用,說明其抗菌譜廣,但形成的抑菌圈都很小,說明其對上述真菌的殺菌活性相對較弱。這一試驗結果與臨床研究結果一致[11-12]。
綜合考慮燈樁建設周期(通常1年)、總投資、勘察設計時間及成本等因素,結合燈樁建設選址位置,根據不同的地質條件,選擇幾個代表性的地質類型進行勘察,同類型燈樁勘察設計互相借鑒,以此類推,編制燈樁標準化勘察報告。
綜上所述,抗細菌藥物、抗真菌藥物與糖皮質激素聯合制成的菌克軟膏主要針對伴有常見細菌感染或者明顯炎癥反應的濕疹、皮炎、足癬等疾病。本試驗觀察菌克軟膏對常見致病細菌、真菌的體外抗菌活性,是治療皮膚疾病的關鍵。直接用軟膏避免了用原料藥所得藥敏結果與臨床實際用藥效果之間的差距。故菌克軟膏可以作為伴有常見細菌感染或者明顯炎癥反應的濕疹、皮炎、足癬等疾病的治療藥物。
[1]瞿發林,陸健,章杰兵.菌克軟膏質控標準的研究[J].中國現代應用藥學雜志,2005,12(22):505-506.
[2]瞿發林,陸健,章杰兵.菌克軟膏的制備及質量控制[J].中國藥師,2005,8(1):37-38.
[3]張瑞峰,冉玉平,王鵬,等.1%萘替芬-0.25%酮康唑乳膏與2%酮康唑乳膏和1%特比萘芬乳膏的體外抗真菌譜及抗真菌活性對比研究[J].中國循證醫學雜志,2011,11(5):508-514.
[4]尹斌,冉玉平,莊凱文,等.布替萘芬莫米松乳膏體外抗真菌譜及抗真菌活性研究[J].皮膚病與性病,2012,34(6):311-316.
[5]李春英.克林霉素的臨床副作用和用藥安全[J].泰山衛生,2008,32:25-26.
[6]曹安民,施暢,廖明陽.唑類抗真菌藥物的藥理學和毒理學研究進展[J].毒理學雜志,2006,20(2):128-130.
[7]袁敏,劉忠漢,黃欣,等.抗真菌藥物研究的新進展[J].中國真菌學雜志,2006,1(4):253-256.
[8]王愛平,李若瑜.系統抗真菌藥物概述[J].中國藥物評價,2012,29(1):10-13.
[9]王偉東.淺談糖皮質激素類藥物[J].航空航天醫藥,2010,21(3):429-430.
[10]張正華,劉維達.抗真菌藥物的協同作用[J].國外醫學:皮膚性病學分冊,2001,27(4):195-198.
[11]Schopf R,Hettler O,Brautigam M,et al.Efficacy and tolerability of terbinafine 1% topical solution used for 1 week compared with 4 weeks clotrimazole 1% topical solution in the treatment of interdigital tineapedis:a randomized,double-blind,multi-centre,8-week clinical trial[J].Mycoses,1999,42(5-6):415-420.
[12]Smith EB.Topical antifungal drugs in the treatment of tineapedis,tineacruris,and tineacorporis[J].J Am Acad Dermatol,1993,28:S24-S28.
Observation of antimicrobial activity of Junke creaminvitro
SHAO Liu-ying,QU Fa-lin*,CHEN Ying,NI Yu-jia,WU Xiao-yan
(The No.102 Hospital of PLA,Changzhou 213003,China)
Objective To observe the antimicrobial activity of Junke creaminvitro.Methods The drug susceptibility was detected by agar diffusion method.The inhibition zone diameters of Junke cream against 6 isolates of pathogenic bacteria from 4 species,and 23 isolates of pathogenic fungi from 9 species were determined,and the diameters of Junke cream were compared with those of lincomycin cream and miconazole nitrate cream.Results The inhibition zones of Junke cream against common pathogenic bacteria from 4 species were observed.The inhibition zones diameters of Junke cream againststaphylococcusaureus,escherichiacoli.andbacillussubtiliswere both larger than those of lincomycin cream (P<0.01),while no significant difference was found in the diameters of the creams againstpseudomonasaeruginosa(P>0.05).The inhibition zones of Junke cream against common pathogenic fungi from 9 species were observed.There was no significant difference in the inhibition zones diameters of Junke cream and miconazole nitrate cream against thedermatophyte,candidaspp,fonsecaeapedrosoiandmalasseziafurfur(P>0.05).Conclusion The antibacterial activity of Junke cream was greater than lincomycin cream,and the antifungi activity was similar as miconazole nitrate creaminvitro.
Junke cream; Antimicrobial activity; Lincomycin cream; Miconazole nitrate cream
2014-01-30
中國人民解放軍第102醫院制劑中心,江蘇 常州 213003
*通信作者
10.14053/j.cnki.ppcr.201507016

