烯基亞砜類化合物合成研究綜述
丁憲才,王建強
(浙江工業大學藥學院,浙江 杭州 310032)
0 前言
烯基亞砜類化合物是有機合成中一類非常重要的醫藥化工中間體[1],特別是手性的亞砜基團,有很強的手性誘導作用,被廣泛地用于不對稱合成中。它可以有效作為Michael 加成重要受體[2],親二烯體[3]和親偶極子[4]。此外,它也可作為Claisen 重排[5]和一些過渡金屬催化反應如:Heck反應[6]、Pauson/Khand 反應[7]的一類重要底物。因此合成各種有潛在用途的多取代烯基亞砜類化合物在有機合成中尤其是不對稱合成領域具有一定的應用價值。
1 烯基亞砜類化合物合成研究綜述
查閱相關文獻我們發現烯基亞砜類化合物的合成報道并不多,例如一些經典有機反應:Horner-Witting 反應[8]、Knoevenagel 反應[9]、Andersen 反應[10]等。另外,炔基亞砜和有機金屬試劑(如:Cu[11],Zr[12-14]等)加成反應也是合成取代烯基亞砜類化合物一種有效的方法。此外,烯基硫化合物的氧化[17]和炔基亞砜的還原[18]也可得到相應的烯基亞砜。最近,一些關于金屬Pd[15-16]參與的催化偶聯反應合成烯基砜類化合物也有報道。最后,其它的一些合成方法[19-21]我們也做了總結。
1.1 成烯反應方法
1.1.1 Horner-witting 反應
Van der Gen 等[8]報道了用Horner-witting 反應合成烯基亞砜類化合物,該反應在低溫-70 ℃~20 ℃下,和不同的醛類反應能夠生成以E 為主要構型的烯基亞砜,收率為41%~91%。該篇文獻還報道了在堿正丁基鋰基礎添加等量的叔丁醇鉀可以提高反應產物的選擇性。不足之處在于反應條件需要低溫,不利于工業化生產,此外,Horner-witting反應很難合成相對單一構型的產物(Scheme 1-1)。
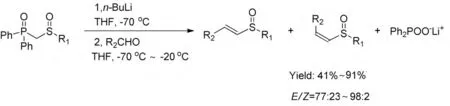
(Scheme 1-1)
1.1.2 Knoevenagel 反應
Hayashi 等[9]報道了另一種通過亞砜的碳負離子和不同羰基化合物縮合生成烯基亞砜類化合物。該方法通過甲基取代亞砜和不同的醛在堿LDA 下發生親核加成生成β 位取代羥基的亞砜化合物,然后在堿作用下形成甲磺酸酯再發生消去反應,生成對應的烯基亞砜類化合物,收率53%~72%。該反應也無法克服反應選擇性問題,生成了是正反式混合構型的烯基亞砜類產物(Scheme 1-2)。
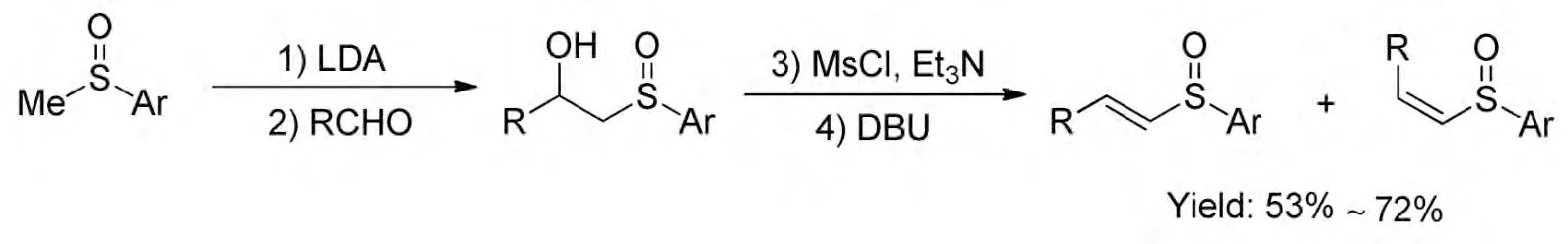
(Scheme 1-2)
1.1.3 Andersen 反應
Posner 等[10]在1978 年就報道了另外一種有效經典的合成烯基亞砜類化合物的方法,該方法能夠有效的選擇性合成單一構型的產物。首先,不同的端炔烴通過特定還原劑還原溴化選擇性生成反式E 構型的溴取代烯烴,然后再與金屬鎂在THF 下生成格式試劑,最后于不同的亞磺酸酯類化合物反應選擇性生成對應的E 型烯基亞砜類化合物,產率51%~75%。該反應選擇性控制關鍵是在于單一構型溴代烯烴的選擇(Scheme 1-3)。
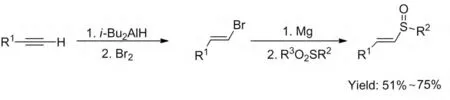
Scheme 1-3
1.2 炔烴的加成反應方法
1.2.1 有機銅試劑參與加成反應
炔烴的碳金屬化反應一直是合成多取代烯烴的良好方法,碳銅化反應是其中很重要的一類反應。Huang 等[11]首先研究報道了炔基亞砜與二烷基銅試劑或者單烷基銅試劑在低溫下的二組分反應,發現二烷基銅試劑的反應沒有得到目標加成產物,而單烷基銅試劑的反應則可以有效的得到目標加成產物。因此,將炔基亞砜與單烷基銅試劑的順式碳銅化反應擴展到含有多種取代基的烯基亞砜的合成中非常有效,產率39%-99%。此外,共扼烯炔是許多天然化合物中的結構單元,合成亞砜基取代的共扼烯炔具有一定的應用價值。該文還報道了中間體2 與碘的反應幾乎可以定量得到碘代產物,并繼續研究了α 位碘代烯基亞砜與端炔的Sonogashira 偶聯反應制備亞砜基取代的共扼烯炔化合物,收率中等到良好(Scheme 1-4)。
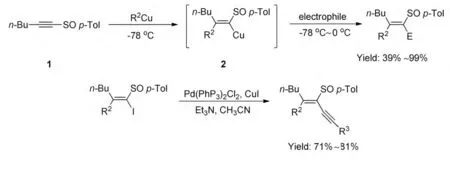
Scheme 1-4
1.2.2 有機鋯試劑參與加成反應
炔烴的碳金屬化反應一直以來都是廣大化學工作者研究的熱點,不同的有機金屬試劑都被運用開發出來,如有名的金屬鋯Schwartz 試劑[Cp2Zr(H)Cl][12],這種試劑能夠有效的和炔基砜或炔基亞砜反應生成Z 構型的烯基鋯螯合的有機化合物,這種化合物可被水淬滅,也可以和一些親電試劑反應生成一些不同取代基團的烯。Huang 等[13]就報道了炔基亞砜和鋯試劑在THF 溶劑中室溫下就能生成Z 構型的烯基鋯螯合的有機化合物,在水的處理下就得到烯基亞砜,但收率只有23%。另外,在NBS 的處理下也得到β 位溴取代的烯基亞砜(Scheme 1-5)。
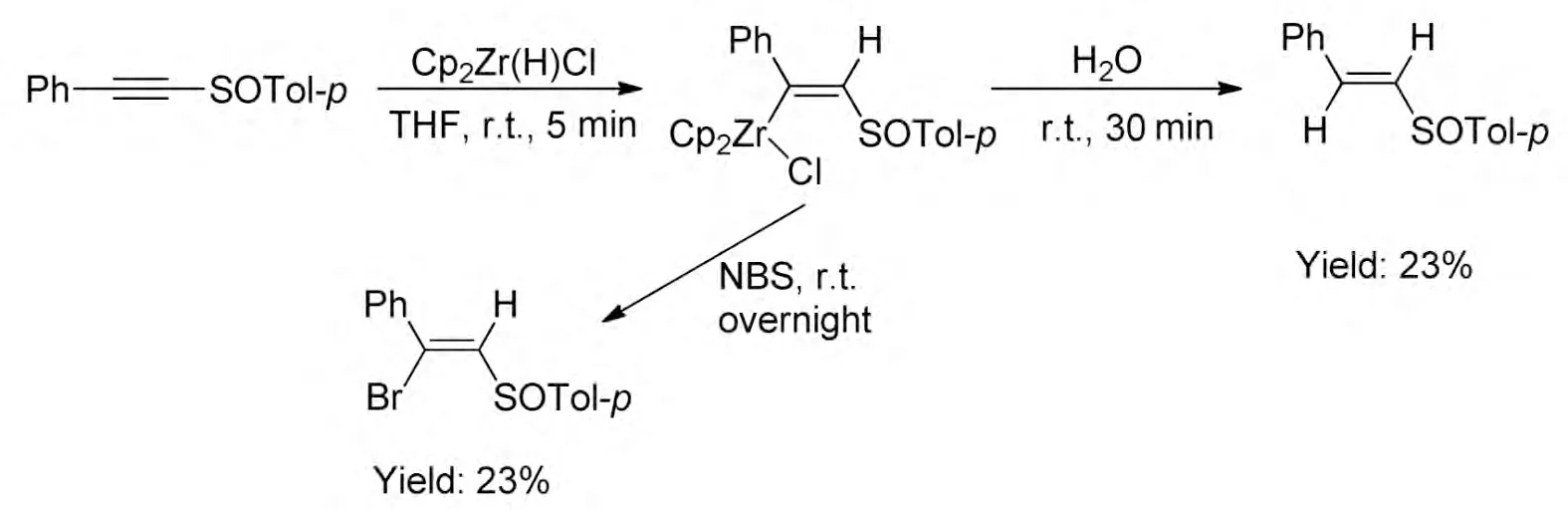
Scheme 1-5
此外,2000 年Huang 等[14]還報道了先用不同取代基的端炔和金屬鋯Schwartz 試劑[Cp2Zr(H)Cl]反應能夠有效生成Z 構型的烯基鋯螯合的有機化合物,然后再與不同亞磺酰氯反應生成對應烯基亞砜類化合物,產率74%~86%。(Scheme 1-6)。
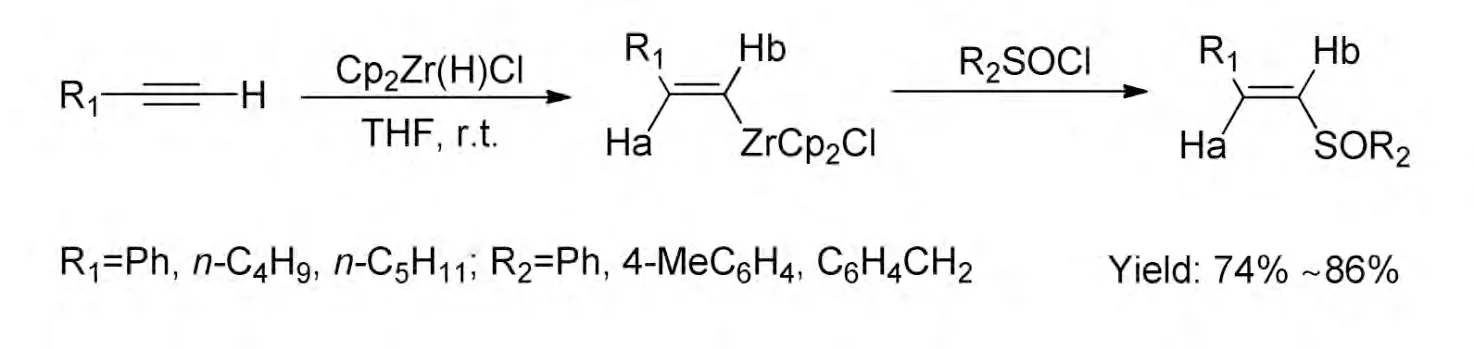
Scheme 1-6
1.3 金屬Pd 參與催化偶聯反應方法
1.3.1 Heck 反應
Heck 反應是指鹵代烴與活化不飽和烴在鈀催化下,生成反式烯烴產物的反應。Carretero 等[15]在2001 年報道了通過金屬鈀參與的Heck 反應合成了不同的β,β’ 二取代烯基亞砜類化合物。該文報道了通過不同的含有鄰二甲基氨苯基烯基亞砜類底物和不同的芳香碘化合物在金屬鈀等催化劑下發生偶聯反應,選擇性合成了以E 構型為主要構型的β,β’ 二取代烯基亞砜類化合物,產率66%~75%。底物中二甲氨基在鈀催化循環中起了一定的配位作用,有效地促進了偶聯反應的進行(Scheme 1-7)。
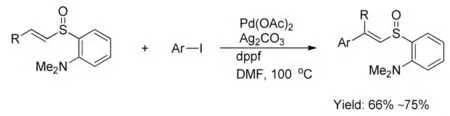
Scheme 1-7
1.3.2 Suzuki 反應
此外,Mercedes Medio-Simó 等[16]在2010 年報道了通過金屬鈀參與的Suzuki 反應合成了不同的烯基亞砜類化合物,產率23%~90%。本文通過1 位鹵代的烯基亞砜和不同芳基或烯基硼酸酯合成對應的不同取代的烯基亞砜,該反應收率高,具有一般的底物普適性和官能團容忍性。此外,本文中鈀催化劑Pd(PPh3)4和Pd(OAc)2/DABCO都有很好的活性,一般來講一些含氮的化合物如DABCO 能夠很好促進一些金屬鈀試劑的活性,但本文中Pd(PPh3)4表現更好(Scheme 1-8)。
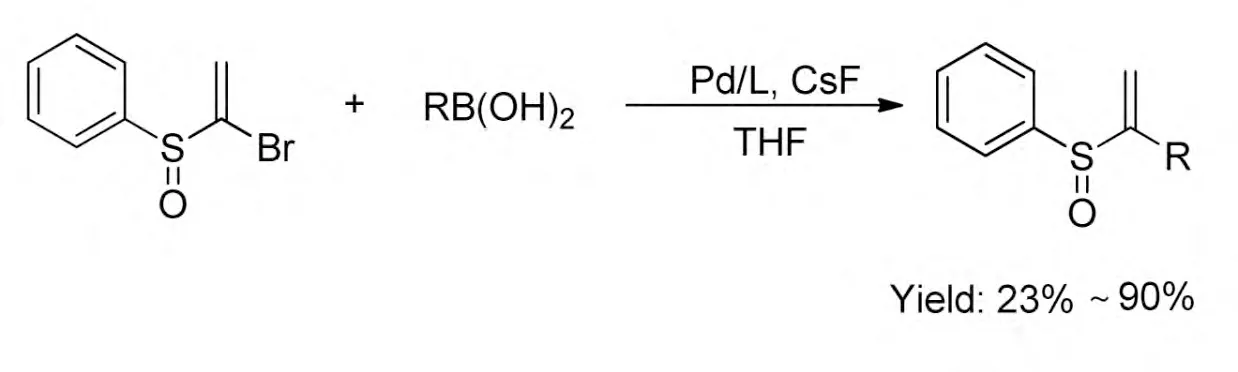
Scheme 1-8
1.4 烯基硫化合物氧化反應方法
Zhu 等[17]在2012 年報道了一種相對綠色,收率高和具有一定選擇性的合成烯基亞砜類化合物的方法。本文研究不同的端炔和不同芳基硫酚在溫和的條件下一鍋法可以合成烯基亞砜類化合物,產率71%~98%,且產物主要是E 構型為主要構型的混合產物。但本方法也仍有一定的不足之處,如不同的炔試劑價格昂貴,不利于工業化生產,此外,本文只報道了芳基類烯基亞砜的合成,該反應對底物的普適性可能有一定的限制(Scheme 1-9)。

Scheme 1-9
1.5 炔基亞砜還原反應方法
炔基亞砜還原是合成烯基亞砜類化合的一類重要方法,該種方法能夠很好控制反應產物構型的優點。Akira Takahashi 等[18]在1987 年報道了這方面的研究,首先,通過不同的炔格式試劑和亞磺酸酯在甲苯中能夠高效反應生成不同炔基亞砜類化合物。在還原劑LAH 或者DIBAH,溫度-90 ℃,THF 溶劑下,可以選擇性合成E 構型的烯基亞砜類化合物,產率81%~84%。另外在Wilkinson 催化劑RhCl(PPh3)3下,加氫可以選擇性生成Z 構型的烯基亞砜類化合物,產率65%~97%(Scheme 1-10)。
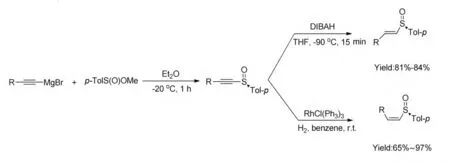
Scheme 1-10
1.6 其他反應方法
1.6.1 磷葉立德參與的反應
磷葉立德是一類化合物,由三級膦與鹵代烴反應,經強堿(如苯基鋰)處理而得。一般均不經離析而直接用于后續合成反應。由于有相反電荷共存于共價鍵分子內,使之表現出若干獨特性質,負碳離子易發生一系列親核反應,是制備烯烴的重要方法。Cristau 等[19]報道了用磷葉立德試劑合成烯基亞砜類化合物的一種方法。本文研究了磷葉立德試劑和亞磺酸酯反應生成α 位亞磺基的磷葉立德,然后和不同的醛類在甲苯中回流生成不同E 構型的烯基亞砜類化合物,產率50%~88%,反應具有一定的選擇性(Scheme 1-11)。
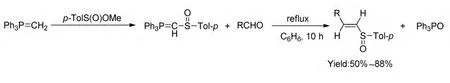
Scheme 1-11
1.6.2 環氧化合物參與的反應
另外,環氧化合物也是合成烯基砜類的一種原料,在1991 年報道[20]了以正丙硫醇和環氧乙烷為原料,經開環加成,脫水和氧化反應合成丙基乙烯基亞砜,產率65%。本合成方法適合于一些低碳烷基或苯基乙烯基亞砜的合成,實驗中,在丙硫酚與環氧乙烷的加成反應中,添加少量NaOH 能加速反應,并能提高反應收率。此外,在氧化反應中,添加少量十二烷基苯磺酸鈉能使過氧化氫水溶液和丙基乙烯基硫醚呈均相體系,有利于氧化反應進行(Scheme 1-12)。
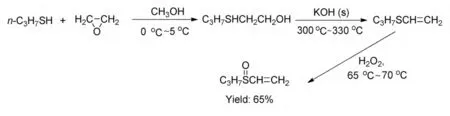
Scheme 1-12
1.6.3 聯烯參與的反應
Liu 等[21]在2009 年報道了亞磺酰氯和不同聯烯反應生成了烯基亞砜的方法。當烷氧基取代的聯烯在0 ℃下和亞磺酰氯反應,生成了不同烷氧取代的烯基亞砜,產率47%~77%,當烷氧聯烯上有不同烷基取代基團時,和亞磺酰氯反應生成α位酮代的烯基亞砜類化合物,產率65%~82%。該反應其特點在于反應條件溫和,但聯烯價格昂貴(Scheme 1-13)。
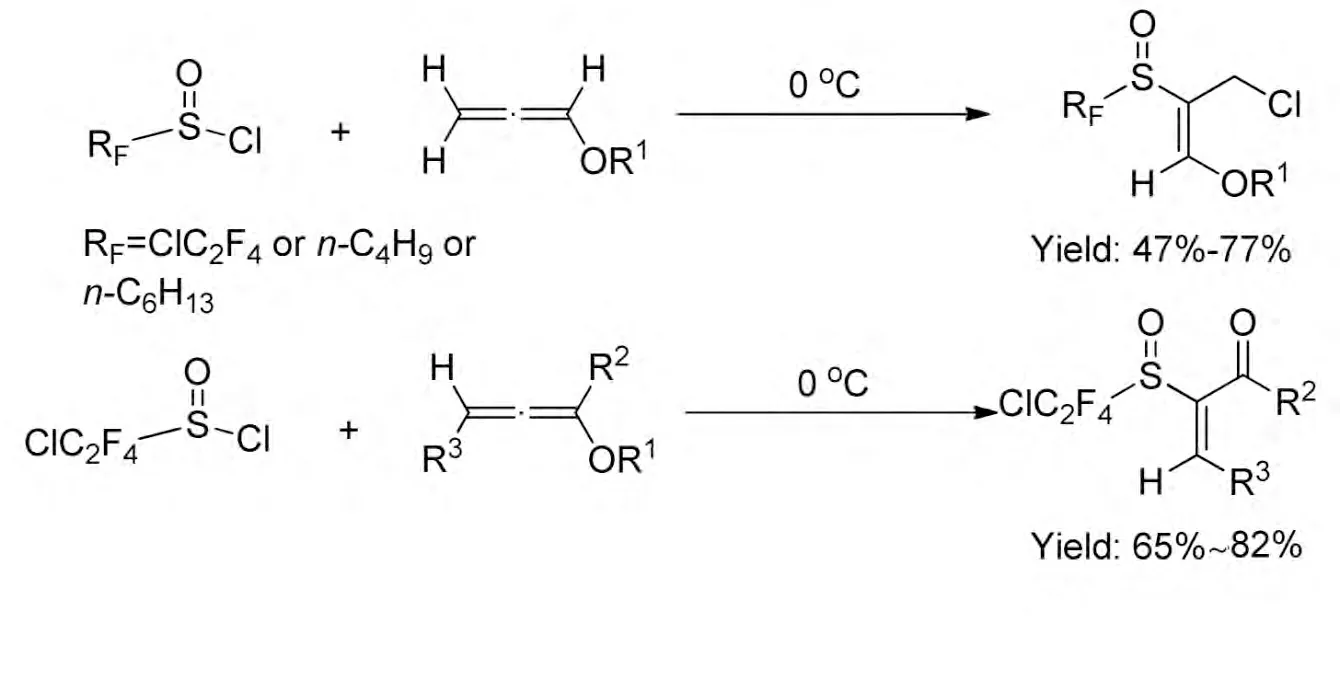
Scheme 1-13
2 結束語
綜上所述,大量的化學工作者以對烯基亞砜類化合物的合成及研究做出巨大的貢獻,但仍然存在著一些不足,如反應產物的選擇性不高[8-9,15-17],反應條件苛刻[8,11,18]和一些昂貴試劑[12,15-16,18]的使用,此外,一些過渡金屬元素,如Cu[11],Zr[12-14],Li[8,18]和Pd[15-16]等的使用,不可避免地對環境造成了污染。因此,研究發現一些其它合成烯基亞砜類化合物的方法,在有機合成中仍具有重要意義。
[1](a) Viso A,Fernandez R,Urena M,et al.Highly diastereoselective addition of lithio vinyl sulfoxides to N-sulfinimines:an entry to enantiopure 3-sulfinyl-2,5-cis-dihydropyrroles [J].Org.Lett.,2008,10 (21):4775-4778;(b)Mori K,Ohmori K,Suzuki K.Stereochemical relay via axially chiral styrenes:asymmetric synthesis of the antibiotic TAN-1085[J].Angew.Chem.Int.Ed.,2009,48:5633-5637.
[2]Wedel T,Gehring T,Podlech J,et al.Nucleophilic additions to alkylidene bis(sulfoxides)-stereoelectronic effects in vinyl sulfoxides[J].Chem.Eur.J.,2008,14(15):4631-4639.
[3]Fernándezdela Pradilla R,Baile R,Tortosa M.Sulfoxidedirected thermal intramolecular [4+2]cycloadditions between 2-sulfinyl butadienes and unactivated alkynes[J].Chem.Commun.,2003,(19):2476-2477.
[4]Garcia J L,Fraile A,Martin et al.Pyrrolo [2,1-b]thiazole derivatives by asymmetric 1,3-dipolar reactions of thiazoli um azomethine ylides to activated vinyl sulfoxides[J].J.Org.Chem.,2008,73(21):8484-8490.
[5]Fernándezdela Pradilla R,Montero C,Tortosa M.Sulfinylmediated chirality transfer in diastereoselective claisen rearrangements[J].Org.Lett.,2002,4(14):?2373-2376.
[6]Díaz N,Carretero J C.Sulfinyl group as a novel chiral auxiliary in asymmetric heck reactions[J].J.Am.Chem.Soc.,1998,120(28):7129-7130.
[7]Rodríguez Rivero M,Alonso I,Carretero J C.Vinyl sulfoxides as stereochemical controllers in intermolecular Pauson-Khand reactions:applications to the enantioselective synthesis of natural cyclopentanoids[J].Chem.Eur.J.,2004,10(21):5443-5459.
[8]Van Steenis J H,Van Es J J G S,Van der Gen A.Stereoselective synthesis of(e)-vinyl sulfoxides by the hornerwitting reaction[J].Eur.J.Org.Chem.,2000,2787-2793.
[9]Tsuboi K K S,Hayashi M S.Selective synthesis of cis-α,β-unsaturated sulfoxides and sulfides by the Horner-Witting reaction with bis(2,2,2-trifluoroethyl)phosphono sulfoxides and aromatic aldehydes[J].Synthesis,1996,(5):637-640.
[10]Posner G H,Tang P W.Stereocontrolled preparation of chiral(e)-1-alkenyl sulfoxides.Efficient reduction of alkenyl sulfoxides to the corresponding alkenyl sulfides[J].J.Org.Chem.,1978,43(21):4131-4133.
[11]Xu Q,Huang X.cis-Carbocuperation of acetylenic sulfoxides and corresponding applications in the regio-and stereoselective synthesis of polysubstituted vinyl sulfoxides[J].Tetrahedron Lett.,2004,45:5657-5660.
[12]Hart D W,Schwartz J.Organic synthesis via organozirconium intermediates.Synthesis and rearrangement of alkylzirconium(IV)complexes and their reaction with electrophiles[J].J.Am.Chem.Soc.,1974,96:8115-8116.
[13]Huang X,Duan D H,Zheng W X.Studies on hydrozirconation of 1-alkynyl sulfoxides or sulfones and the application for the synthesis of stereodefined vinyl sulfoxides or sulfones[J].J.Org.Chem.,2003,68:1958-1963.
[14]Zhong P,Guo M P,Huang X.Simple and stereoselective synthetic route to(E)-1-alkenyl sulfoxides via terminal alkynes[J].J.Chem.Research.,2000,588-589.
[15]Alonso I,Carretero J C.Highly stereoselective synthesis of trisubstituted α,β-unsaturated sulfoxides by heck reaction[J].J.Org.Chem.,2001,66:4453-4456.
[16]Ana B G M,Rodríguez C N,Medio-Simón M,et al.Efficient synthesis of racemic and chiral alkenyl sulfoxides by palladium-catalyzed Suzuki coupling[J].Tetrahedron,2010,66:6901-6905.
[17]Xue Q C,Mao Z J,Zhu C J.Metal-free,one-pot highly selective synthesis of(E)-vinyl sulfones and sulfoxides via addition-oxidation of thiols with alkynes[J].Tetrahedron Lett.,2012,53:1851-1854.
[18]Kosugi H,Kitaoka M,Tagami K,et al.Simple and stereocontrolled preparation of optically pure(E)-and-1-alkenyl p-tolyl sulfoxides via 1-alkynyl p-tolyl sulfoxides[J].J.Org.Chem.,1987,52(6):1079.
[19]Miko覥ajczyk M,Perlikowska W.Stereoselective synthesis of racemic and optically active e-vinyl and e-dienyl sulfoxides via wittig reaction of α-sulfinyl phosphonium ylides[J].J.Org.Chem.,1998,63:9716-9722.
[20]龔張水,張一烽,沈之荃.丙基乙烯基亞硯的合成[J].浙江大學學報,1991,2(6):726-727.
[21]Chen L J,Liu J T.The addition of perfluoroalkanesulfinyl chlorides to alkoxyallenes[J].Journal of Fluorine Chemistry,2009,130:329–331.

