高甲氧基果膠對酸性大豆蛋白體系的穩(wěn)定機(jī)理
李新新,劉志勝,鄔 娟,李保國,*,謝曼曼
(1.上海理工大學(xué)醫(yī)療器械與食品學(xué)院,上海 20 0093;2.豐益全球研發(fā)中心,上海 200137)
?
高甲氧基果膠對酸性大豆蛋白體系的穩(wěn)定機(jī)理
李新新1,劉志勝2,鄔 娟2,李保國1,*,謝曼曼1
(1.上海理工大學(xué)醫(yī)療器械與食品學(xué)院,上海 20 0093;2.豐益全球研發(fā)中心,上海 200137)
摘 要:為揭示高甲氧基果膠對酸性豆乳體系穩(wěn)定的作用機(jī)理,通過添加不同質(zhì)量濃度果膠,研究在pH值由7.0~3.0降低過程中大豆蛋白的粒徑、ζ-電位以及微觀結(jié)構(gòu)變化。結(jié)果表明:當(dāng)體系pH<6.0時,果膠通過靜電作用吸附在大豆蛋白膠粒上,阻止了大豆蛋白顆粒在酸性狀態(tài)的聚集。果膠質(zhì)量濃度≤0.2 g/100 mL,質(zhì)量濃度1.5 g/100 mL的大豆蛋白聚集,體系失穩(wěn);果膠質(zhì)量濃度≥0.4 g/100 mL,質(zhì)量濃度1.5 g/100 mL的大豆蛋白體系在一定pH值內(nèi)穩(wěn)定,果膠質(zhì)量濃度越大,穩(wěn)定性越好。酸性大豆蛋白體系的 穩(wěn)定性與大豆蛋白和果膠之間的靜電吸附作用以及果膠質(zhì)量濃度有關(guān)。
關(guān)鍵詞:大豆蛋白;果膠;pH值;粒徑;ζ-電位
隨著人們對大豆蛋白保健作用認(rèn)識的提高,大豆蛋白的需求也在不斷的增大。但大豆蛋白在其等電點pH 4.5附近溶解性差,限制了它在酸性食品中的應(yīng)用[1-3],而加入陰離子多糖果膠可改善大豆蛋白在酸性條件下的穩(wěn)定性[4-7]。
果膠是酸性蛋白飲料中應(yīng)用廣泛的穩(wěn)定劑,不僅能提高產(chǎn)品的穩(wěn)定性,還可改善產(chǎn)品風(fēng)味和質(zhì)構(gòu)特性[5]。果膠的主鏈?zhǔn)怯蒁-半乳糖醛酸通過α-1,4-糖苷鍵鍵合在一起組成的D-半乳糖醛酸聚合體,支鏈為中性小分子糖。根據(jù)酯化度(degree of esterification,DE)分為高甲氧基果膠(high-methyl pection,HMP,DE>50%)和低甲氧基果膠(low-methyl pectin,LMP,DE<50%)。低甲氧基果膠因帶有大量的負(fù)電荷,在蛋白表面吸附一定量后會與體系中的果膠發(fā)生靜電排斥作用,阻礙果膠的進(jìn)一步吸附,而高甲氧基果膠因電荷少而在蛋白表面吸附較多,提供空間位阻作用維持酸性體系的穩(wěn)定,Liu Jinru[8]、Lam[9]等研究表明高甲氧基果膠比低甲氧基果膠更有利于酸性乳飲料的穩(wěn)定。
果膠與酪蛋白形成復(fù)合物,其相互作用機(jī)理已有大量的研究[10-13],研究表明pH<5.0時陰離 子多糖果膠和酪蛋白表面的正電荷通過 靜電吸引力結(jié)合,并通過靜電斥力和空間位阻作用維持體系的穩(wěn)定。但果膠與大豆蛋白之間的相互作用機(jī)理研究較少。Lam等[14]研究了pH 3.8和pH 7.2時果膠與大豆蛋白的相互結(jié)合,表明高甲氧基果膠和大豆蛋白在酸性條件下能夠結(jié)合形成復(fù)合物,并且大豆蛋白體系能夠在pH 3.8條件下維持穩(wěn)定。Jaramillo等[15]研究了pH值對高甲氧基果膠和大豆分離蛋白混合物的影響。研究表明果膠與大豆蛋白在酸性體系下也能夠形成復(fù)合物,維持酸性大豆蛋白體系的穩(wěn)定。
本實驗通過考察大豆蛋白和果膠在酸化過程中聚合物的粒徑、ζ-電位的變化和酸性狀態(tài)下的微觀結(jié)構(gòu),研究不同的pH值、不同質(zhì)量濃度的高甲氧基果膠與大豆蛋白相互作用,從而進(jìn)一步揭示果膠對酸性大豆蛋白體系穩(wěn)定機(jī)理,為酸性豆乳生產(chǎn)工藝提供理論參考。
1 材料與方法
1.1材料與試劑
大豆分離蛋白(蛋白質(zhì)含量90%) 益海嘉里秦皇島食品有限公司;果膠(食品級) 美國CP Kelco公司;檸檬酸(分析純) 國藥集團(tuán)(上海)化學(xué)試劑有限公司。
1.2儀器與設(shè)備
BSA2202S型電子天平 德國Sartorius公司;FA25型高剪切分散乳化機(jī) 德國Fluko公司;RCT BS25型磁力攪拌器 德國IKA公司;S20 SevenEasypH型酸度計瑞士Mettler Toledo公司;ZetasizerNano ZS90型納米粒度儀 英國Malvern公司;BX41型顯微鏡 日本Olympus公司;Milli-Q超純水制造系統(tǒng) 美國Millipore公司。
1.3方法
1.3.1 樣品的制備
將質(zhì)量濃度1.5 g/100 mL大豆分離蛋白在40 ℃的超純水中800 r/min攪拌分散不同的時間,冷卻至室溫后用高速剪切機(jī)10 000 r/min剪切1 min使大豆蛋白充分水合,用超純水稀釋100 倍,測定不同分散時間的粒徑。納米粒度儀的參數(shù)設(shè)定為:散射角度90 o,激光波長63 3 nm;溫度25 ℃;顆粒折射率1.470,顆粒吸收率0.001;分散劑為水,分散劑折射率1.330[13]。每個樣品重復(fù)3 次,取平均值。
1.3.2 粒徑和ζ-電位的測定
將質(zhì)量濃度1.5 g/100 mL大豆分離蛋白在40 ℃的超純水中800 r/min攪拌分散3 h,冷卻至室 溫,用高速剪切機(jī)10 000 r/min剪切1 min。將質(zhì)量濃度1 g/100 mL的果膠在75 ℃熱水中溶解至少30 min,冷卻備用。將大豆分離蛋白和果膠混合后用超純水稀釋100 倍,得到1.5 個蛋白分別對應(yīng)0.2、0.4、0.6、0.8 個果膠的混合液,通過動態(tài)光散射法測定pH值下降過程中大豆蛋白和果膠混合液中膠粒的粒徑和ζ-電位。參數(shù)設(shè)定同1.3.1節(jié)。
1.3.3 酸性大豆蛋白飲料的制備和微觀結(jié)構(gòu)觀察
配制質(zhì)量濃度為3 g/100 mL的大豆蛋白溶液和2 g/100 mL的果膠溶液,將兩種液體按不同比例混合均勻,得到蛋白質(zhì)量濃度為1.5 g/100 mL,果膠質(zhì)量濃度分別為0.2、0.4 g/100 mL和0.6 g/100 mL的混合液。將混合液酸調(diào)至pH 4.2,混勻后200 bar均質(zhì)后100 ℃水浴殺菌10 min,冷卻至室溫得到酸性大豆蛋白飲料。400 倍顯微鏡下觀察混合液的狀態(tài)。
2 結(jié)果與分析
2.1攪拌時間對大豆蛋白膠粒粒徑的影響
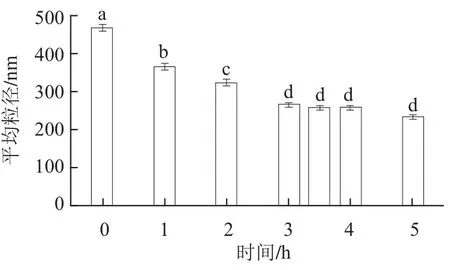
圖1 攪拌時間對大豆蛋白平均粒徑的影響Fig.1 Influence of mixing time of soybean protein on average particle size
由圖1可知,隨著攪拌時間的延長,大豆蛋白的平均粒徑不斷減小,攪拌溶解3 h后,大豆蛋白在水中已充分水合分散,平均粒徑達(dá)到一個較為穩(wěn)定的值(252.30±13.17) nm。
2.2果膠對大豆蛋白酸化過程中粒徑的影響
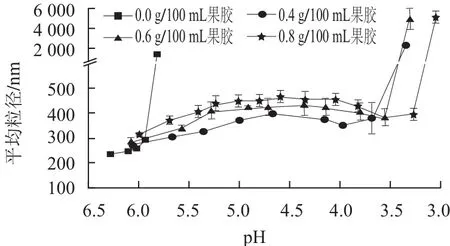
圖2 果膠質(zhì)量濃度對大豆蛋白酸化過程中膠粒平均粒徑變化的影響Fig.2 Influence of pectin concentration on the average particle size of colloidal particles during acidification
由圖2可知,因果膠為酸性陰離子多糖,添加果膠后,體系的pH值有所降低,平均粒徑增大,果膠質(zhì)量濃度越大,pH值越低,平均粒徑越大,表明果膠吸附在了大豆蛋白表面。預(yù)備實驗表明,當(dāng)1.5 g/100 mL大豆蛋白體系中含有0.2 g/100 mL的果膠時,混合液中會出現(xiàn)明顯的絮凝,這是由于果膠質(zhì)量濃度低,單個聚合物分子連接兩個或多個蛋白分子引起“架橋絮凝”的結(jié)果[16]。
由圖2可知,隨著pH值的減小,不含果膠的對照組大豆蛋白平均粒徑不斷增大,聚集點的pH值為5.8,與Ringgenberg等[17]用葡萄糖酸內(nèi)酯(gluconolactone,GDL)酸化豆?jié){凝膠,Roesch等[18]將酪蛋白與大豆蛋白混合,蛋白質(zhì)的聚集pH值從5.3上升到了5.8相類似。果膠質(zhì)量濃度從0.4 g/100 mL增加到0.8 g/100 mL時,大豆蛋白平均粒徑的變化趨勢相同,呈現(xiàn)先增加后平穩(wěn)再略微下降,然后顆粒聚集粒徑大于1 μm,聚集點的pH值分別降到3.9、3.5和3.0,并且果膠的質(zhì)量濃度越大,大豆蛋白膠粒的平均粒徑越大,聚集點的pH值越低。當(dāng)pH值為4.2時,添加不同質(zhì)量濃度果膠大豆蛋白膠粒的粒徑分如圖3所示,顆粒大小呈正態(tài)分布,而且隨著果膠質(zhì)量濃度的增大,粒徑分布峰值右移,果膠質(zhì)量濃度為0.6 g/100 mL 和0.8 g/100 mL時的粒徑分布相似,只是峰值不同。實驗結(jié)果表明,在酸化過程中,果膠通過靜電作用吸附在大豆蛋白顆粒的表面而使顆粒的粒徑變大,可能是由于當(dāng)大豆蛋白表面吸附力與質(zhì)子化作用平衡時,大豆蛋白表面吸附的果膠和吸附層的塌陷量相同,大豆蛋白粒徑保持不變,隨著H+增多,質(zhì)子化作用加大,吸附層塌陷粒徑減小,當(dāng)吸附層不足以提供足夠的空間位阻作用時,顆粒聚集,體系失穩(wěn)[19-20]。果膠質(zhì)量濃度越大,果膠吸附層的厚度和空間阻力越大,聚集點pH值降低,體系可以在低酸性條件下穩(wěn)定。果膠吸附層的厚度是維持體系酸性狀態(tài)穩(wěn)定的重要因素之一。
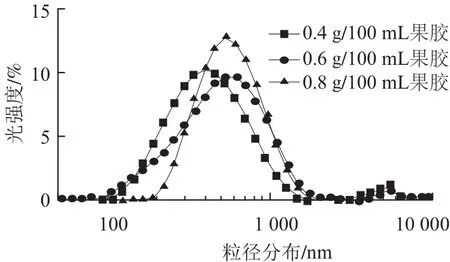
圖3 大豆蛋白和果膠混合液在pH 4.2的粒徑分布Fig.3 Particle size distribution of soy protein isolate-pectin mixture at pH 4.2
2.3果膠質(zhì)量濃度對大豆蛋白酸化過程中ζ-電位的影響
由圖4可知,添加果膠后,因果膠為酸性陰離子多糖,體系的pH值降低,少量果膠吸附到大豆蛋白表面,膠粒ζ-電位絕對值略微地增大,酸性狀態(tài)下ζ-電位絕對值始終大于對照組,表明聚陰離子多糖果膠分子在靜電作用下吸附到大豆蛋白分子的表面。膠粒ζ-電位的絕對值越大,顆粒間的靜電排斥作用越強,阻止粒子間相互聚集[21],有利于維持體系的穩(wěn)定。
在pH 6.0~4.0范圍內(nèi),當(dāng)果膠質(zhì)量濃度從0.4 g/100 mL增加到0.8 g/100 mL,與對照的ζ-電位絕對值線性減小相比,ζ-電位絕對值先略微增大后減小并始終大于對照組,果膠質(zhì)量濃度對ζ-電位的絕對值沒有影響,pH<4.0時,果膠質(zhì)量濃度為0.4、0.6 g/100 mL和0.8 g/100 mL的ζ-電位絕對值顯著變化點分別為pH 3.9、3.5和3.0,與粒徑結(jié)果一致。實驗結(jié)果表明酸化過程中果膠通過靜電作用吸附在大豆蛋白表面,大豆蛋白顆粒表面的負(fù)電荷與體系中帶有負(fù)電荷的陰離子多糖果膠間的靜電排斥作用阻止聚合電解質(zhì)的進(jìn)一步吸附而使體系的ζ-電位絕對值減小[22]。果膠質(zhì)量濃度越大,吸附量越大,大豆蛋白的ζ-電位越負(fù),靜電斥力越強,體系失穩(wěn)的pH值點越低。因此酸性狀態(tài)下果膠吸附層的靜電斥力也是酸性豆乳體系穩(wěn)定的因素之一。
2.4果膠質(zhì)量濃度對大豆蛋白微觀結(jié)構(gòu)的影響

圖5 果膠質(zhì)量濃度對pH 4.2膠粒微觀結(jié)構(gòu)的影響(400×)Fig.5 Effect of pectin concentration on the microstructure of colloidal particles at pH 4.2 (400 ×)
由圖5可知,對照組和添加0.2 g/100 mL果膠的體系中均有聚集顆粒,而且添加0.2 g/100 mL果膠的顆粒粒徑明顯大于對照組中大豆蛋白顆粒的粒徑,可能由于大豆蛋白顆粒未被果膠全部覆蓋,從而聚合物架橋連接兩個或者多個大豆蛋白的“架橋絮凝”所致[23]。添加0.4 g/100 mL和0.6 g/100 mL果膠后則呈現(xiàn)均勻細(xì)小的分散顆粒,添加0.6 g/100 mL果膠大豆蛋白顆粒分散性優(yōu)于添加0.4 g/100 mL果膠。因此,酸性狀態(tài)大豆蛋白膠體顆粒的穩(wěn)定性與果膠的質(zhì)量濃度相關(guān)。
3 結(jié) 論
在大豆蛋白中加入0.4~0.8 g/100 mL的果膠,酸化過程中大豆蛋白的平均粒徑在一定pH值內(nèi)保持穩(wěn)定,聚集點從pH 5.8降低到pH 3.9、3.5和3.0,果膠質(zhì)量濃度越大,大豆蛋白的平均粒徑越大,吸附層越厚,空間位阻作用越強,聚集點越低,酸性豆乳體系穩(wěn)定的pH值越低。酸化過程中的大豆蛋白和果膠混合體系的ζ-電位絕對值始終大于大豆蛋白體系,ζ-電位絕對值在各個質(zhì)量濃度的聚集點時減小速率加快,靜電排斥作用減弱,體系失穩(wěn)。高甲氧基果膠對大豆蛋白酸性狀態(tài)的穩(wěn)定性具有顯著效果,可為酸性豆乳的生產(chǎn)提供理論依據(jù)。
參考文獻(xiàn):
[1]MALHOTRA A, COUPLAN J N. The effect of surfactants on the solubility, zeta potential, and viscosity of soy protein isolates[J]. Food Hydrocolloids, 2004, 18(1): 101-108.
[2]NISHNARI K, FANG Y, GUO S, et al. Soy proteins: a review on composition, aggregation and emulsification[J]. Food Hydrocolloids, 2014, 39: 301-318.
[3]CAMPBELL J L, GU X, DEWAR J S, et al. Effects of heat treatment and glucono-σ-lactone-induced acidification on characteristics of soy protein isolate[J]. Food Hydrocolloids, 2011, 44(9): 1952-1957.
[4]LAURENHT M A, BOULENGUER P. Stabilization mechanism of acid dairy drinks (ADD) induced by pectin[J]. Food Hydrocolloids, 2003, 17(4): 445-454.
[5]TROMP R H, de KRUIF C G, van EIJK M, et al. On the mechanism of stabilisation of acidified milk drinks by pectin[J]. Food Hydrocolloids, 2004, 18(4): 565-572.
[6]NAKAMURA A, YOSHIDA R, MAEDA H, et al. The stabilizing behaviour of soybean soluble polysaccharide and pectin in acidified milk beverages[J]. International Dairy Journal, 2006, 16(4): 361-369.
[7]JENSEN S, ROLIN C, IPSEN R. Stabilisation of acidified skimmed milk with HM pectin[J]. Food Hydrocolloids, 2010, 24(4): 291-299.
[8]LIU Jinru, NAKAMURA A, CORREDIG M. Addition of pectin and soy soluble polysaccharide affects the particle size distribution of casein suspensions prepared from acidified skim milk[J]. Journal of Agricultural and Food Chemistry, 2006, 54(17): 6241-6246.
[9]LAM M, SHEN R, PAULSEN P, et al. Pectin stabilization of soy protein isolates at low pH[J]. Food Research International, 2007, 40(1): 101-110.
[10]TUINIER R, ROLIN C, de KRUIF C G. Electrosorption of pectin onto casein micelles[J]. Biomacromolecules, 2002, 3(3): 632-638.
[11]YE Aiqian. Complexation between milk proteins and polysaccharides via electrostatic interaction: principles and applications: a review[J]. International Journal of Food Science & Technology, 2008, 43(3): 406-415.
[12]KAZMIERSKI M, WICKER L, CORREDIG M. Interactions of β-lactoglobulin and high-methoxyl pectins in acidified systems[J]. Journal of Food Science, 2003, 68(5): 1673-1679.
[13]BEDIE G K, TURGEON S L, MAKHLOUF J. Formation of native whey protein isolate-low methoxyl pectin complexes as a matrix for hydro-soluble food ingredient entrapment in acidic foods[J]. Food Hydrocolloids, 2008, 22(5): 836-844.
[14]LAM M, PAULSEN P, CORREDIG M. Interactions of soy protein fractions with high-methoxylpectin[J]. Journal of Agricultural and Food Chemistry, 2008, 56(12): 4726-4735.
[15]JARAMILLO D P, ROBERTS R F, COUPLAND J N. Effect of pH on the properties of soy protein-pectin complexes[J]. Food Research International, 2011, 44(4): 911-916.
[16]MAROZIENE A, de KRUIF C G. Interaction of pectin and casein micelles[J]. Food Hydrocolloids, 2000, 14(4): 391-394.
[17]RINGGENBERG E, ALEXANDER M, CORREDIG M. Effect of concentration and incubation temperature on the acid induced aggregation of soymilk[J]. Food Hydrocolloids, 2013, 30(1): 463-469.
[18]ROESCH R, JUNEJA M, MONAGLE C, et al. Aggregation of soy/milk mixes during acidification[J]. Food Research International, 2004, 37(3): 209-215.
[19]PEREYRA R, SCHMIDT K A, WICKER L. Interaction and stabilization of acid casein dispersions with low and high methoxyl pectins[J]. Journal of Agricultural and Food Chemistry, 1997, 45: 3448-3451.
[20]WU Juan, LIU Junliang, DAI Qiaoyu, et al. The stabilisation of acidified whole milk drinks by carboxymethylcellulose[J]. International Dairy Journal, 2013, 28: 40-42.
[21]MORRISON I D, ROSS S. Colloidal dispersions: suspensions, emulsions, and foams[M]. New York: Wiley-Interscience, 2002: 333-354.
[22]DU Baiqiao, LI Jing, ZHANG Hongbin, et al. The stabilization mechanism of acidified milk drinks induced by carboxymethylcellulose[J]. Le Lait, 2007, 87(4/5): 287-300.
[23]SYRBE A, BAUER W J, KLOSTERMEYER H. Polymer science concepts in dairy systems: an overview of milk protein and food hydrocolloid interaction[J]. International Dairy Journal, 1998, 8(3): 179-193.
Mechanism of Stabilization of Acidic Soy Protein System by High Methoxyl Pectin
LI Xinxin1, LIU Zhisheng2, WU Juan2, LI Baoguo1,*, XIE Manman1
(1. School of Medical Instrument and Food Engineering, University of Shanghai for Science and Technology, Shanghai 200093, China; 2. Wilmar Global Research and Development Center, Shanghai 200137, China)
Abstract:The interactions of soy protein isolate with high methoxyl pectin (HMP) at various concentrations were studied over a pH range of 7.0–3.0 to understand the stabilization mechanism of acidic soymilk system. The particle diameter, ζ-potential and microstructure of the system during the acidification of soy protein in the presence of HMP demonstrated that the electrostatical adsorption of HMP could take place below pH 6.0 and prevent the formation of aggregates. The acidic soy protein system had flocculation and instability at 0.2 g/100 mL or less pectin concentration. It was stable within a certain pH range at 0.4 g/100 mL or more pectin concentration. More pectin could result in better stability. The stability of the colloid particles at acidic condition depended on both the electrostatical interaction of the protein with pectin and HMP concentration.
Key words:soy protein; pectin; pH; particle size; ζ-potential
doi:10.7506/spkx1002-6630-201507008
中圖分類號:TS252.1
文獻(xiàn)標(biāo)志碼:A
文章編號:1002-6630(2015)07-0041-04
*通信作者:李保國(1961—),男,教授,博士,研究方向為食品科學(xué)與工程。E-mail:lbaoguo@126.com
作者簡介:李新新(1989—),女,碩士研究生,研究方向為多糖與大豆蛋白的結(jié)合。E-mail:lixinxin_19891110@163.com
基金項目:上海市教委科研創(chuàng)新項目(14ZZ133);上海市科促會聯(lián)盟計劃項目(LM201337);上海理工大學(xué)研究生創(chuàng)新基金項目
收稿日期:2014-06-15

