HPLC法測定甲硫酸新斯的明注射液的含量
孫 莉
(安徽省蕪湖市食品藥品檢驗所,安徽蕪湖 241001)
甲硫酸新斯的明是一種抗膽堿酯酶藥,常用于重癥肌無力、手術后功能性腸脹氣及尿潴留等病的治療,也能發揮改善眼睛調節功能,減輕眼結膜充血的作用。對于其制劑甲硫酸新斯的明注射液的含量測定,《中國藥典》則采用半微量定氮法[1],該方法取樣量,操作繁瑣,結果誤差大。經過系統的試驗,筆者采用HPLC法測定甲硫酸新斯的明注射液中甲硫酸新斯的明的含量,方法簡便、準確、專屬性強,獲得了滿意的結果。
1 儀器與試藥
Agilent 1260型高效液相色譜儀;紫外檢測器(美國安捷倫公司);梅特勒-托利多AB265-S電子分析天平(德國梅特勒-托利多公司);UV-3900紫外可見分光光度計(日本日立公司)。甲硫酸新斯的明對照品(批號:100550-200401,中國藥品生物制品檢定所);甲硫酸新斯的明注射液4批(上海信誼金朱藥業有限公司,批號120412;上海信誼金朱藥業有限公司,批號120706;河南潤弘制藥股份有限公司,批號1208171;河南潤弘制藥股份有限公司,批號1302011);乙腈為色譜純,其他試劑均為分析純,水為二次去離子水。
2 方法與結果
2.1 色譜條件及系統適用性試驗 色譜柱:Agilent ZORAX Eclipse XDB C18(250 mm ×4.6 mm,5 μm);流動相:0.05 moL·L-1磷酸二氫鉀溶液(用磷酸調節 pH 為 3.0)—乙腈(90∶10),流速為 1.0 mL·min-1,檢測波長為215 nm,進樣量:10 μL,柱溫:室溫。理論塔板數按甲硫酸新斯的明峰計算應不小于2 000,甲硫酸新斯的明與相鄰雜質峰的分離度應符合要求,2.2項下溶液的色譜圖見圖1(a~b)。
2.2 溶液的制備
2.2.1 對照品溶液的制備 精密稱取甲硫酸新斯的明對照品10.20 mg,置20 mL量瓶中,加水使溶解并稀釋至刻度,搖勻,作為對照品溶液。
2.2.2 供試品溶液的制備 取本品,用水稀釋制成每1 mL中含甲硫酸新斯的明0.5 mg的溶液,作為供試品溶液。
2.3 線性關系考察 精密稱取甲硫酸新斯的明對照品51.00 mg,置50 mL量瓶中,加水使溶解并稀釋至刻度,搖勻,作為對照品儲備液。精密量取對照品儲備液1.0、2.0、4.0、6.0、8.0、10.0 mL 分別置10 mL量瓶中,加水稀釋至刻度,搖勻,按擬定的色譜條件進行檢測,記錄色譜圖,以甲硫酸新斯的明濃度(g·L-1)為橫坐標,峰面積為縱坐標作線性回歸,得回歸方程 Y=171.75+18 694X,r=0.999 9。表明甲硫酸新斯的明在0.102 ~1.02 g·L-1濃度范圍內與峰面積線性關系良好。
2.4 精密度、重復性及穩定性試驗 分別取同一種對照品溶液(0.51 g·L-1),在上述色譜條件下,重復測定6次,每次10μL,甲硫酸新斯的明峰面積的RSD為0.049%(n=6),表明精密度良好。
分別取同一批甲硫酸新斯的明注射液(批號:120706)共6份,在上述色譜條件下進樣,記錄色譜圖,甲硫酸新斯的明含量測定的RSD為0.046%,表明本法重復性好。
分別取同一種對照品溶液(0.51 g·L-1),在室溫下放置,分別于 0、2、4、6、8 h 進樣,記錄色譜圖。甲硫酸新斯的明峰面積的RSD為0.17%,表明溶液的穩定性良好。
2.5 回收率試驗 取已知含量的供試品溶液(120706)2 mL各9份,置10 mL容量瓶中,分別加入對照品溶液(1.02 g·L-1)0.8、1.0、1.2 mL 各 3份,用水稀釋至刻度,搖勻,按2.1項下色譜條件,分別進樣。記錄色譜圖與峰面積,本方法的平均回收率為99.57%,RSD為0.95%符合要求。
2.6 專屬性試驗
2.6.1 酸降解溶液的配制 精密量取甲硫酸新斯的明注射液(批號:120706)1 mL,置10 mL量瓶中,加5 mol·L-1鹽酸溶液 100 μL,放置 30 min,加 5 mol·L-1氫氧化鈉溶液100μL,加水稀釋至刻度,搖勻。
第三,企業所得稅。抵債資產的公允數據以及繳納的其他稅收金額是企業所得稅的計稅基礎。重組債權的計稅成本是貸款資產以及表內所需收取的利息,另外還需要對收到的抵債資產的公允價值與計稅成本之間的差異,明確當期的利潤或損失,并對所需繳納得稅款進行計算。抵債資產在持有環節獲取的收益(如抵債資產用于租賃所發生的其他業務收入扣除其他業務支出后的差額)需按照規定申報繳納企業所得稅;商業銀行抵債資產處置收入,應當按照抵債資產在處置環節的收入和支出申報繳納企業所得稅。
2.6.2 堿降解溶液的配制 精密量取甲硫酸新斯的明注射液(批號:120706)1 mL,置10 mL量瓶中,加5 mol·L-1氫氧化鈉溶液 100 μL,放置 30 min,加5 mol·L-1鹽酸溶液100μL,加水稀釋至刻度,搖勻。
2.6.3 光降解溶液的配制 將甲硫酸新斯的明注射液(批號:120706),置太陽光下放置24 h后,即得。
2.6.4 熱降解溶液的配制 將甲硫酸新斯的明注射液(批號:120706),置100℃水浴中加熱3 h后,即得。
按上述色譜條件進樣,記錄色譜圖(圖1 c~f)。結果顯示,本品在強酸和強堿破壞條件下,在保留時間為3.5 min附近降解物峰面積增大明顯,雜質個數無明顯增加,而在加熱和光照條件下,樣品降解不明顯,在此色譜條件下,主峰的分離度約為8.5,表明該方法專屬性良好。
2.7 檢測限和定量限 取對照品溶液(0.102 g·L-1)用水稀釋若干倍,在上述色譜條件下測定,以信噪比S/N=3計算檢測限,甲硫酸新斯的明檢測限約為1.0 ng。以信噪比S/N=10估算定量下限,約為4.0 ng。實配4.0 ng稀溶液,經檢測通過。
2.8 樣品含量測定 精密量取本品適量,加水稀釋制成每1 mL中約含0.5 mg的溶液,作為供試品溶液。精密量取10μL注入液相色譜儀,記錄色譜圖。另取甲硫酸新斯的明對照品,同法操作,按外標法以峰面積計算,即得,結果見表1。
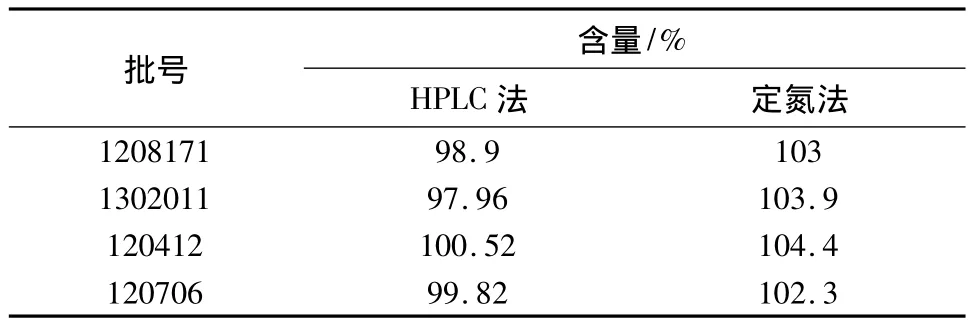
表1 樣品含量測定結果
3 討論
參照《中國藥典》有關物質檢查項下,筆者將流動相0.05 moL·L-1磷酸二氫鉀溶液(用磷酸調節pH 為 3.0)—乙腈(90∶10)和 0.05 moL·L-1磷酸二氫鉀溶液(用磷酸調節 pH為 3.0)—乙腈(90∶10)(含0.001 5 moL·L-1庚烷磺酸鈉)進行了比較,發現0.001 5 moL·L-1庚烷磺酸鈉對主峰的峰形及塔板無明顯改善,故選擇了相對簡單的前者作為流動相。
從表1數據可以看出,藥典采用的半微量定氮法所測得結果相對于液相方法均高出3% ~6%,可見藥典方法的誤差因素較多,而本文所采用的HPLC法檢測甲硫酸新斯的明的含量結果可靠,可用于甲硫酸新斯的明注射液的質量控制。
[1] 國家藥典委員會.中國藥典(二部)[S].北京:中國醫藥科技出版社,2010:附錄Ⅵ,159.
[2] 王希東,郝少君,李文俊,等.HPLC法測定益復康口服液中阿魏酸的含量[J].河南中醫,2014,34(1):154 -155.
[3] 馬若群,丁蘇蘇,徐興亞,等.HPLC法測定雙唑乳膏中克霉唑與硝酸益康唑的含量[J].天津藥學,2013,25(6):6 -8.
[4] 陳秀琳.HPLC法測定鹽酸二甲雙胍緩釋片的含量[J].海峽藥學,2013,25(12):108 -109.
[5] 羅 文,譚群友,熊華蓉,等.紫外分光光度法測定新斯的明片中新斯的明的含量[J].中國藥房,2011,22(16):1505 -1506.
[6] 夏苗芬,李士敏,袁京群.HPLC測定復方新斯的明眼用凝膠中甲硫酸新斯的明含量[J].中國藥師,2010,13(5):703 -704.
[7] 邢懷陽,趙 仁,沈蔡月,等.高效液相色譜法測定復方鹽酸氨基葡糖硫酸軟骨素片中硫酸軟骨素的含量[J].安徽醫藥,2013,17(12):2037 -2038.
[8] 李 萌,劉 斐,孫 松,等.高效液相色譜法測定多索茶堿注射液有關物質與含量[J].安徽醫藥,2013,17(12):2046 -2049.
[9] 謝子立.HPLC法測定維生素B2片的含量及有關物質[J].安徽醫藥,2013,17(2):204 -206.

