硫酸頭孢喹肟乳房(干乳期)注入劑在奶牛乳汁中的殘留消除研究
魏占勇,劉欣,魏麗娟,耿智霞?,張櫻,宋婷婷,賈興,連麗娟,夏曦
(1.河北遠(yuǎn)征藥業(yè)有限公司,石家莊050041;2.中國(guó)農(nóng)業(yè)大學(xué),北京100083)
硫酸頭孢喹肟乳房(干乳期)注入劑在奶牛乳汁中的殘留消除研究
魏占勇1,劉欣1,魏麗娟1,耿智霞1?,張櫻1,宋婷婷1,賈興1,連麗娟1,夏曦2
(1.河北遠(yuǎn)征藥業(yè)有限公司,石家莊050041;2.中國(guó)農(nóng)業(yè)大學(xué),北京100083)
建立了牛奶中硫酸頭孢喹肟殘留超高效液相色譜-串聯(lián)質(zhì)譜檢測(cè)方法(UPLC-MS/MS)。選取18頭剛進(jìn)入干乳期的健康奶牛,隨機(jī)分為6個(gè)組,分別于預(yù)產(chǎn)期前的42、35、28、21、14和7 d進(jìn)行乳房注入硫酸頭孢喹肟乳房注入劑(3 g∶150 mg/支),只用藥一次,產(chǎn)犢后采集奶樣。結(jié)果表明:預(yù)產(chǎn)期前7 d給藥,奶牛產(chǎn)犢72 h后采集的奶樣中頭孢喹肟殘留量降至MRL(20 μg/kg)附近;預(yù)產(chǎn)期前14 d和21 d給藥,奶牛產(chǎn)犢12 h后采集的奶樣中頭孢喹肟殘留量降至MRL以下,均低于檢測(cè)限;預(yù)產(chǎn)期前28、35和42 d給藥,所有采集奶樣的頭孢喹肟殘留量均低于檢測(cè)限。建議在預(yù)產(chǎn)期前7、14和21 d給藥硫酸頭孢喹肟乳房注入劑的棄奶期分別為產(chǎn)犢后5、1和0 d。
頭孢喹肟;牛奶;殘留;超高效液相色譜-串聯(lián)質(zhì)譜法
頭孢喹肟(Cefquinome)是目前第四代頭孢菌素中唯一的動(dòng)物專用藥,具有抗菌譜廣、抗菌活性強(qiáng)、動(dòng)力學(xué)特點(diǎn)優(yōu)良的特點(diǎn),對(duì)革蘭氏陽(yáng)性菌和革蘭氏陰性菌均顯示良好的抗菌活性[1-3]。目前國(guó)內(nèi)關(guān)于頭孢喹肟乳房注入劑的研究越來(lái)越多[4-6],因此加強(qiáng)頭孢喹肟在奶牛乳汁中的殘留消除研究顯得尤為重要。本試驗(yàn)在建立的奶牛乳汁中頭孢喹肟的超高效液相色譜-串聯(lián)質(zhì)譜檢測(cè)方法(UPLCMS/MS)的基礎(chǔ)上,進(jìn)行了奶牛給藥硫酸頭孢喹肟乳房(干乳期)注入劑后在乳汁中的殘留消除研究,旨在為制定硫酸頭孢喹肟乳房(干乳期)注入劑的休藥期和臨床合理使用提供理論依據(jù)。
1 材料與方法
1.1 材料
1.1.1 藥品與試劑 頭孢喹肟對(duì)照品:含量≥80.1%,批號(hào)K0320906,購(gòu)自中國(guó)獸醫(yī)藥品監(jiān)察所;硫酸頭孢喹肟乳房(干乳期)注入劑(3 g∶150 mg/支),批號(hào):111021,由河北遠(yuǎn)征藥業(yè)有限公司提供;乙腈、甲醇、正己烷與甲酸均為色譜純;氯化鈉為分析純。
1.1.2 儀器與設(shè)備 液相色譜-串聯(lián)質(zhì)譜儀(Micromass Quattro LC,配電噴霧離子源);分析天平(Sartorius CPA225D,賽多利斯科學(xué)儀器(北京)有限公司);天平(JJ500,常熟市雙杰測(cè)試儀器廠);組織勻漿機(jī)(AM-2,日本Nissei公司);高速冷凍離心機(jī)(5804R,德國(guó)Eppendorf公司);渦旋混合器(HQ-60-II,北方同正生物技術(shù)發(fā)展有限公司);超聲清洗儀(KQ2200型,昆山市超聲儀器有限公司);固相萃取裝置(美國(guó)Waters公司);氮吹儀(N-Evap 112,美國(guó)Organomation Associates公司);Oasis HLB固相萃取柱(美國(guó)Waters公司)。
1.1.3 主要溶液配制 精密稱取頭孢喹肟對(duì)照品約12.48 mg,于10 mL容量瓶中,用乙腈溶解并定容,配制成濃度為1 mg/mL的頭孢喹肟標(biāo)準(zhǔn)貯備液。準(zhǔn)確量取1 mg/mL頭孢喹肟標(biāo)準(zhǔn)貯備液1 mL和0.1 mL,于10 mL容量瓶中,用乙腈稀釋并定容,配制成濃度為100 μg/mL和10 μg/mL的標(biāo)準(zhǔn)工作液。
1.1.4 實(shí)驗(yàn)動(dòng)物 18頭剛進(jìn)入干乳期的健康奶牛,由四川涼山州科華奶牛繁育有限公司奶牛場(chǎng)提供。給予正常飼料,自由飲水,飼料和飲水中不含頭孢類等抗菌藥物。
1.2 方法
1.2.1 給藥及采樣 將試驗(yàn)?zāi)膛kS機(jī)分為6個(gè)組(I、II、III、IV、V、VI組,每組3頭),根據(jù)每頭奶牛的配種記錄計(jì)算預(yù)產(chǎn)期。I、II、III、IV、V、VI組每頭奶牛的4個(gè)乳區(qū)分別在預(yù)產(chǎn)期前42、35、28、21、14、7 d進(jìn)行給藥,灌注硫酸頭孢喹肟乳房(干乳期)注入劑,給藥劑量為1支/乳區(qū),僅給藥一次。各試驗(yàn)?zāi)膛T诋a(chǎn)犢后第0、12、24、36、48、60、72 h采集奶樣,-20℃低溫保存,備用。
1.2.2 樣品前處理
1.2.2.1 提取 取解凍的空白或供試牛奶試料(5.00±0.02)g,于50 mL離心管中,加水8 mL、NaCl 3 g,渦動(dòng)2 min,超聲20 min,10000 r/min 0℃離心10 min。上清液轉(zhuǎn)移至另一50 mL離心管中,加正己烷10 mL,渦動(dòng)30 s,10000 r/min 0℃離心10 min。棄上層正己烷,下層水相備用。
1.2.2.2 凈化 依次用甲醇2 mL和水2 mL活化Oasis HLB固相萃取柱,取備用液過柱,再用水2 mL淋洗,用甲醇-水溶液(60∶40,V/V)2 mL洗脫。洗脫液30℃水浴氮?dú)獯抵列∮?00 μL,加入含0.1%甲酸的水溶液定容至1 mL,渦動(dòng)1 min復(fù)溶,14000 r/min離心10 min,過濾膜后供UPLC-MS/MS測(cè)定。
1.2.3 色譜條件
1.2.3.1 液相色譜條件 色譜柱:BEH C18(1.7 μm,50 mm×2.1 mm);流動(dòng)相:A相為0.1%甲酸水溶液;B相為0.1%甲酸乙腈溶液;梯度洗脫:0、0.5、1.5、2.0、2.1、3.5 min時(shí),B相分別為10%、10%、90%、90%、10%、10%;流速:0.3 mL/min;柱溫:30℃;進(jìn)樣量:10 μL。
1.2.3.2 質(zhì)譜條件 離子源:電噴霧離子源;掃描方式:正離子掃描;檢測(cè)方式:多反應(yīng)監(jiān)測(cè);電離電壓:3.0 kV;源溫:100℃;霧化溫度:350℃;錐孔氣流速:30 L/h;霧化氣流速:600 L/h;測(cè)試藥物定性、定量離子對(duì)及對(duì)應(yīng)的錐孔電壓、碰撞能量見表1。

表1 頭孢喹肟的定性、定量離子及錐孔電壓、碰撞能量
2 試驗(yàn)結(jié)果
2.1 方法學(xué)驗(yàn)證
2.1.1 線性范圍 制備基質(zhì)匹配標(biāo)準(zhǔn)曲線,濃度分別為0、50、250、500、2500、5000、10000、15000 μg/L,以測(cè)得特征離子峰面積為縱坐標(biāo),對(duì)應(yīng)的標(biāo)準(zhǔn)溶液濃度為橫坐標(biāo),繪制標(biāo)準(zhǔn)曲線,得回歸方程為:y=25.027x+78.4327,相關(guān)系數(shù)r為0.9998,表明藥物在50~15000 μg/L的濃度范圍內(nèi),峰面積與濃度線性關(guān)系良好。
2.1.2 特異性 處理不同來(lái)源空白樣品,目標(biāo)化合物的保留時(shí)間附近沒有雜質(zhì)干擾,空白樣品、空白牛奶添加樣品、基質(zhì)標(biāo)準(zhǔn)溶液的特征離子質(zhì)量色譜圖見圖1-圖3。

圖1 空白牛奶樣品特征離子質(zhì)量色譜圖
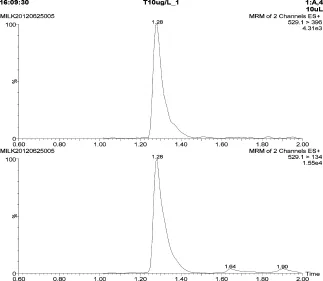
圖2 空白牛奶添加樣品特征離子質(zhì)量色譜圖(10 μg/kg)

圖3 基質(zhì)標(biāo)準(zhǔn)溶液特征離子質(zhì)量色譜圖(50 μg/L)
2.1.3 準(zhǔn)確度和精密度 進(jìn)行添加回收試驗(yàn),選擇1/2MRL(10 μg/kg)、MRL(20 μg/kg)、2MRL(40 μg/kg)三個(gè)濃度,各濃度制備6個(gè)平行樣品,重復(fù)3批次。表2結(jié)果表明,藥物在10、20、40 μg/kg添加濃度水平上的回收率為80%~110%之間,批內(nèi)變異系數(shù)≤7.4%,批間變異系數(shù)≤6.3%。
2.1.4 靈敏度 添加適量標(biāo)準(zhǔn)工作液于5 g空白樣品,經(jīng)提取凈化后測(cè)定。以3倍信噪比為方法的檢測(cè)限,測(cè)得牛奶中頭孢喹肟的檢測(cè)限為2 μg/kg,以10倍信噪比為方法的定量限,測(cè)得牛奶中頭孢喹肟的定量限為10 μg/kg。
2.2 試驗(yàn)牛產(chǎn)犢后乳汁中頭孢喹肟的殘留消除情況 由表3數(shù)據(jù)可看出,預(yù)產(chǎn)期前7 d給藥(VI組),奶牛產(chǎn)犢后0 h采集奶樣的頭孢喹肟殘留量最高,約為3000 μg/kg,產(chǎn)犢后12 h采集奶樣的頭孢喹肟殘留量迅速降為257.6~627.8 μg/kg,之后消除趨于緩慢,產(chǎn)犢后72 h采集奶樣的頭孢喹肟殘留量降至MRL(20 μg/kg)附近,濃度為17.1~31.3 μg/kg。預(yù)產(chǎn)期前14 d給藥(V組),奶牛產(chǎn)犢后0 h采集奶樣的頭孢喹肟殘留量為243.2~809.7 μg/kg,產(chǎn)犢后12 h采集奶樣的頭孢喹肟殘留量迅速降至MRL以下,均低于檢測(cè)限。預(yù)產(chǎn)期前21 d給藥(IV組),奶牛產(chǎn)犢后0 h采集奶樣的頭孢喹肟殘留量為37.3~83.1 μg/kg,產(chǎn)犢后12 h采集奶樣的頭孢喹肟殘留量均低于檢測(cè)限。預(yù)產(chǎn)期前28 d給藥(III組),奶牛產(chǎn)犢后所有采集奶樣的頭孢喹肟殘留量均低于檢測(cè)限。

表2 牛奶中頭孢喹肟添加回收試驗(yàn)結(jié)果

表3 單次使用(150 mg/乳區(qū))硫酸頭孢喹肟乳房(干乳期)注入劑奶牛產(chǎn)犢后各時(shí)間點(diǎn)采集奶樣的頭孢喹肟殘留量檢測(cè)結(jié)果
2.3 休藥期計(jì)算 根據(jù)上述試驗(yàn)所得的殘留消除數(shù)據(jù),根據(jù)我國(guó)牛奶中頭孢喹肟MRL(20 μg/kg)規(guī)定和歐盟關(guān)于休藥期計(jì)算的要求,以雙單側(cè)95%置信區(qū)間計(jì)算,按推薦用法和用量[干乳期乳房?jī)?nèi)注入,1支(150 mg)/乳區(qū),只用藥一次]給奶牛使用硫酸頭孢喹肟乳房(干乳期)注入劑,在預(yù)產(chǎn)期7 d前給藥,建議棄奶期為產(chǎn)犢后5 d;在奶牛預(yù)產(chǎn)期14 d前給藥,建議棄奶期為產(chǎn)犢后1 d;在奶牛預(yù)產(chǎn)期21 d前給藥,建議棄奶期為產(chǎn)犢后1 d;在奶牛預(yù)產(chǎn)期28 d前給藥,產(chǎn)犢后分泌乳汁已檢測(cè)不到頭孢喹肟殘留,建議棄奶期為產(chǎn)犢后0 d。
3 討論
目前,檢測(cè)頭孢喹肟在可食性組織和牛奶中的殘留方法主要有微生物法[7]、酶聯(lián)免疫法[8]、HPLC法[9-11]以及HPLC-MS/MS[12-13],其中以HPLC法和HPLC-MS/MS應(yīng)用最多。本試驗(yàn)采用HPLCMS/MS方法檢測(cè)牛奶乳汁中頭孢喹肟殘留,專屬性好,峰形良好,靈敏度高,測(cè)定牛奶中頭孢喹肟的檢測(cè)限為2 μg/kg,定量限為10 μg/kg,歐盟制定頭孢喹肟在牛奶中的最大殘留量(MRLs)為20 μg/kg,因此能夠滿足頭孢喹肟在乳中殘留檢測(cè)的要求。
國(guó)內(nèi)外關(guān)于頭孢喹肟的殘留研究結(jié)果均表明按合理的給藥方案,經(jīng)過休藥期后,各種組織器官的殘留量均低于規(guī)定的限度[14]。頭孢喹肟在動(dòng)物可食性組織和乳中殘留消除速度較快[14]。乳房灌注頭孢喹肟后在泌乳牛中的殘留消除研究結(jié)果顯示[9],僅能在治療后24 h的腎臟檢出頭孢喹肟,且含量低于200 μg/kg,而在用藥后第一次的擠奶中殘留最高,在第10次泌乳期后,所有批次的牛奶樣品的殘留濃度均低于20 μg/kg。Ehinger等[4]研究了奶牛干乳期應(yīng)用頭孢喹肟后在可食性組織和乳汁中殘留,藥物未進(jìn)入體循環(huán),產(chǎn)后乳汁和所有可食性組織中頭孢喹肟的殘留濃度均低于最大殘留限量。從本實(shí)驗(yàn)的結(jié)果來(lái)看,在干乳期給藥硫酸頭孢喹肟乳房注入劑后,藥物在奶牛乳汁中代謝較快,硫酸頭孢喹肟殘留量可很快降至MRL(20 μg/kg)以下。
[1] CVMP(Committee for Veterinary Medicial Products).Cefquinome Summary Report[R].London:European Agency for the Evaluation of Medicinal Products,1995.
[2] CVMP(Committee for Veterinary Medical Products).Cefquinome Summary Report-1[R].London:European Agency for the Evaluation of Medicinal Products,1999.
[3] CVMP(Committee for Veterinary Medical Products).Cefquinome Summary Report-2[R].London:European Agency for the Evaluation of Medicinal Products,2003.
[4] Ehinger A M,Allan M J,Hartmann M,et al.Deletion of residues in edible tissues and milk following treatment with a new cefquinome dry cow formulation[R].Quebec:Intervet Innovation GmbH,2004.
[5] 魏占勇,劉欣,魏麗娟,等.硫酸頭孢喹肟乳房注入劑在牛奶中的藥代動(dòng)力學(xué)研究[J].中國(guó)獸藥雜志,2014,48(12):22-26.
[6] 閆星,劉義明,路永強(qiáng),等.硫酸頭孢喹肟乳房注入劑對(duì)泌乳期奶牛的安全性研究[J].中國(guó)畜牧獸醫(yī),2014,41(11):278-282.
[7] Errecalde C A,Clin MV E C,Prieto G F,et al.Cefquinome pharmacokinetics in calves by intramuscular administration[J].Rev Col Pec Vol,2002,15(3):281-285.
[8] Zhang X1,Li J,Jiang H,et al.Residue depletion of cefquinome in swine tissues after intramuscular administration[J].J Agric Food Chem,2007,55(25):10493-10498.
[9] 高金興.頭孢喹肟在牛奶中殘留的HPLC檢測(cè)及消除規(guī)律研究[D].揚(yáng)州:揚(yáng)州大學(xué),2009.
[10]徐向明,楊海峰,金禮琴,等.頭孢喹肟注射液在豬組織中的殘留消除研究[J].江蘇農(nóng)業(yè)科學(xué),2008,(6):193-195.
[11]劉利鋒,覃少華,趙杰,等.豬組織中硫酸頭孢喹肟含量測(cè)定和肌注給藥殘留研究[J].甘肅農(nóng)業(yè)大學(xué)學(xué)報(bào),2008,43(2):1-7.
[12]王林,束建花,趙寧,等.牛奶和牛血漿中頭孢喹肟HPLCMS/MS檢測(cè)方法的建立[J].畜牧與獸醫(yī),2012,44(11):55-59.
[13]嚴(yán)鳳,李丹妮,顧欣,等.超高效液相色譜-串聯(lián)質(zhì)譜檢測(cè)動(dòng)物源性食品中頭孢喹肟殘留[J].中國(guó)獸藥雜志,2012,46(7):23-25.
[14]王付民,陳杖榴.頭孢喹肟的研究進(jìn)展[J].動(dòng)物醫(yī)學(xué)進(jìn)展,2004,25(4):50-53.
(編輯:李文平)
Residual Study of Cefquinome Sulfate Intramammary Infusion(Dry Period)in Milk
WEI Zhan-yong1,LIU Xin1,WEI Li-juan1,GENG Zhi-xia1?,ZHANG Ying1,SONG Ting-ting1,JIA Xing1,LIAN Li-juan1,XIA Xi2
((1.HeBei Yuanzheng Pharmaceutical Co.,Ltd.Shijiazhuang 050041,China;2.China Agriculturial University,Beijing 100083,China)
The high performance liquid chromatography and tandem mass spectrometry method(UPLC-MS/MS)was established for the residual study of cefquinome sulfate in milk.18 healthy cows that just entering the dry period were selected and were randomly divided into 6 groups.The 6 groups of cow were respectably administrated cefquinome sulfate intramammary infusion(dry period)once in mammary region at the dose of 3 g for each region and their milk were collected after calving.The results demonstrated that:administrated 7 days before preterm birth,concentration of cefquinome in milk collected 72h after calving decreased to about MRL;administrated 14 and 21 days before preterm birth,concentration of cefquinome in milk collected 12h after calving dropped below MRL,all below the detection limit;administrated 28、35 and 42 days before preterm birth,concentration of cefquinome in all the milk were below the detection limit.It is suggested that the milk withholding period were respectably 5,1 and 0 days that administrated cefquinome sulfate intramammary infusion7,14 and 21 days before preterm birth.
cefquinome;milk;residue;UPLC-MS/MS
2015-02-05
A
1002-1280(2015)05-0049-05
S859.84
魏占勇,高級(jí)工程師,從事藥物制劑研究方面的研究。
耿智霞。E-mail:gengzhixia2011@aliyun.com

