麥羥硅鈉石對水中Zn2+的吸附性能研究
戈明亮,王雁武,陳 萌 (華南理工大學,聚合物成型加工工程教育部重點實驗室,聚合物新型成型裝備國家工程研究中心,廣東 廣州 510640)
麥羥硅鈉石對水中Zn2+的吸附性能研究
戈明亮*,王雁武,陳萌 (華南理工大學,聚合物成型加工工程教育部重點實驗室,聚合物新型成型裝備國家工程研究中心,廣東 廣州 510640)
以沉淀白炭黑、NaOH、Na2CO3和水為原料,制備了單一晶相麥羥硅鈉石(magadiite),并用BET、X射線衍射、紅外以及SEM對其進行表征,并考察了magadiite對Zn2+離子的吸附行為.結果表明:magadiite是一種比表面積為19.38m2/g的非孔型材料,在25℃、Zn2+初始濃度20mg/L、pH值為6、吸附平衡時間為60min時,magadiite的飽和吸附量為42.55mg/g. Magadiite對Zn2+的吸附動力學符合準二級動力學方程,吸附等溫線符合Langmuir方程.結合BET、X射線衍射、紅外、SEM分析推斷magadiite對Zn2+的吸附是物理吸附和化學吸附共存,但以化學吸附為主.
麥羥硅鈉石;吸附;Zn2+;動力學;吸附等溫線
工業的高速發展使得重金屬離子廢水污染日益嚴重,Zn2+是工業廢水中典型的污染物,主要來源于電鍍、冶金、化工等行業,是一種累積性毒物,廢水中的Zn2+可直接進入水生生物體內,最重要的是Zn2+可以通過食物鏈網,進入人體,在人體內累積,造成發育不良、頭痛、高熱、頭暈、干咳、全身無力等癥狀[1-2],故需要嚴格加以控制以防其污染環境,危害人類健康.
目前,吸附法是重金屬離子廢水處理方法中常見的一種,用于吸附的吸附劑種類很多,目前常用的吸附劑是活性炭[3],但活性炭價格貴、使用壽命短、難再生、操作費用高,因此尋求簡單易得、高效吸附、成本較低的吸附劑材料迫在眉睫.麥羥硅鈉石(magadiite)是一種天然二維層狀硅酸鹽礦物,最初是 Eugster等[4]在肯尼亞的 magadi堿湖中發現的.根據目前的研究,magadiite可以用國內資源豐富的硅藻土合成[5],也可以由價格較低的沉淀白炭黑合成[6].與傳統黏土礦物膨潤土、蒙脫石等相比具有以下優點:一是通過控制合成工藝,能夠得到高純度的產物;二是magadiite內外表面有很多硅羥基(Si—OH),層板帶有負電荷,并可通過層間的Na+和H+等陽離子來平衡電荷;三是層板具有優異的膨化性能,層間陽離子交換量遠大于膨潤土,水合 Na+還可以被質子、其他陽離子或大的季銨鹽陽離子取代[7-8],能夠保證層板插層剝離的順利進行;四是magadiite單個片層較厚,結構穩定性好;五是magadiite層板僅有硅氧四面體[SiO4]組成,組成單一,不含容易水解的鋁,因而具有較好的耐酸性和熱穩定性,同時具有良好的生物相容性,在生物酶固定、生物傳感以及藥物緩釋等方面具有潛在的應用價值[7].目前,國內外對magadiite的合成工藝研究趨于成熟,對其改性和應用方面的研究相對較少[4-8],其在吸附性能方面僅限于對砷離子和幾種有機物的吸附研究[9-13],其中未改性的magadiite對水中 Zn2+的吸附能力的探究至今鮮見報道.筆者以沉淀白炭黑、Na2CO3、NaOH等為原料,采用水熱合成法合成magadiite[6],在靜態條件下,考察了pH值對其吸附活性的影響,接著研究了magadiite對Zn2+的吸附動力學及吸附熱力學特性并結合X射線衍射、紅外以及SEM對吸附機理進行初步探討.
收稿日期:2014-12-02
基金項目:中國博士后科學基金資助項目(20100470911)
* 責任作者,副教授,gml@scut.edu.cn
1 材料與方法
1.1試劑與儀器
沉淀白炭黑(93%SiO2,7%H2O),上海振江化工有限公司;NaOH,分析純,南京化學試劑有限公司;Na2CO3,分析純,廣州化學試劑廠;水為去離子水;硝酸鋅(天津市科密歐化學試劑有限公司).
ASAP2020型比表面與孔隙率分析儀(美國麥克公司);Z-2000型原子吸收分光光度計(日本日歷公司);WHY-2S旋轉水浴恒溫振蕩器(江蘇常州中捷實驗儀器制造有限公司);FA系列電子天平(上海方瑞儀器有限公司);pHS-3C型精密酸度計(上海雷磁儀器廠);LD4-2A離心機(北京雷勃爾離心機有限公司);Nova Nano SEM 430型掃描電子顯微鏡(美國 FEI公司);NEXUS 670型Fourier變換紅外光譜儀(美國 Nicolet公司);D8ADVANCE型X射線衍射儀(德國Bruker公司).
1.2Magadiite的制備及表征
1.2.1Magadiite的制備按文獻[6]的方法制備magadiite.將其用水洗至pH=7~8后,在80℃下干燥12h后研磨、篩分,取300目篩分后的顆粒,置于干燥器中備用.其結構見圖1[14].
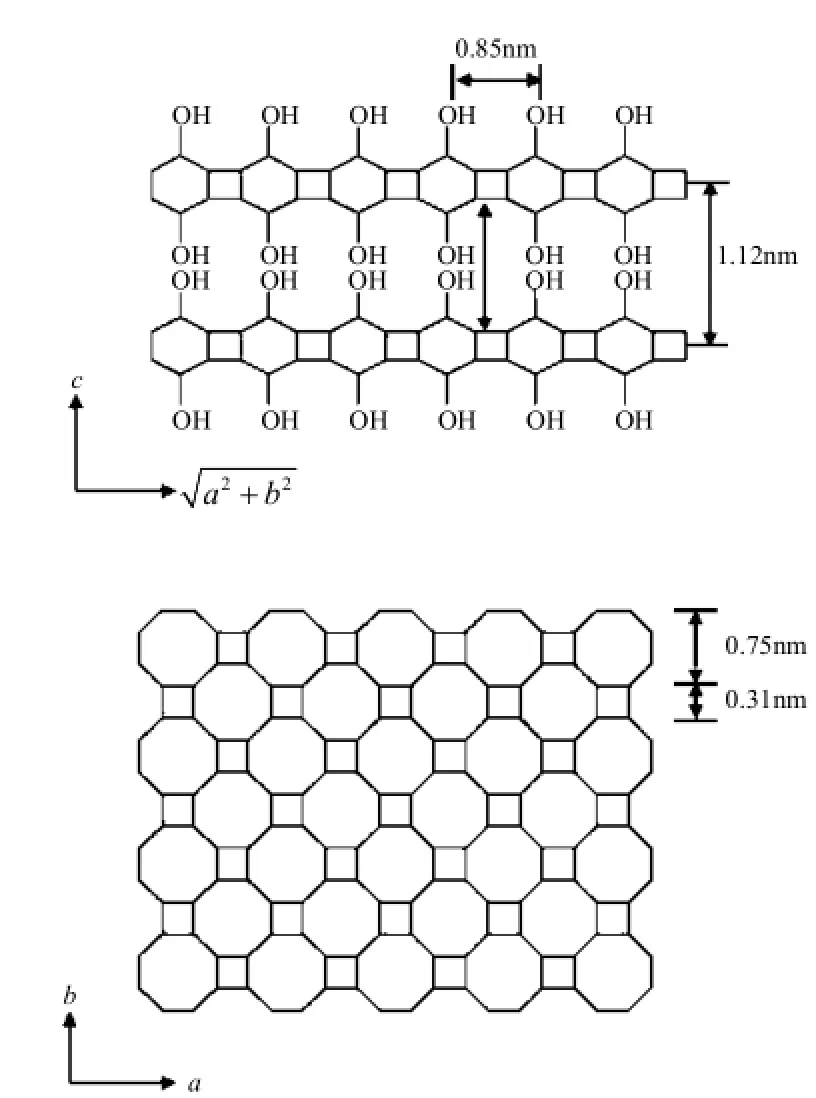
圖1 Magadiite層板結構示意[14]Fig.1 Structure schematic of magadiite[14]
1.2.2Magadiite的表征用BET測定比表面積,用X射線衍射儀分析樣品的物相,用掃描電鏡觀察了其表面形態,用 KBr壓片法測定了樣品在400~4000cm-1波數下的紅外光譜.
1.3靜態吸附實驗
配制濃度為1000mg/L的Zn2+溶液作為儲備液,用時稀釋到相應濃度.
1.3.1pH值對 Zn2+吸附的影響配制一系列pH值為 2~6.5,體積為 50mL,Zn2+初始濃度為20mg/L的溶液,各加入0.05g magadiite,在25℃的恒溫振蕩器上振蕩(60r/min)60min,取出后離心(3500r/min,10min)分離,取定量上清液測定其中Zn2+含量,平行實驗 3次取平均值,根據公式計算吸附量和去除率.即:
吸附量(Qt):
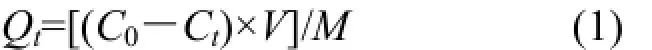
去除率(η):
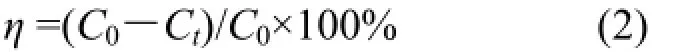
式中:t為反應時間,min;C0為 Zn2+的初始濃度,mg/L;Ct為反應t時刻溶液中Zn2+的濃度,mg/L;V為溶液的體積,L;M為加入magadiite的質量,g. 1.3.2吸附動力學的測定室溫下向 50mL濃度為 20mg/L的 Zn2+溶液中加入 0.050g的magadiite,調節pH=6,在25℃的恒溫振蕩器上振蕩(60r/min)60min,取出后離心分離(3500r/min,10min),取定量上清液測定其中Zn2+含量,平行實驗3次取平均值計算吸附量和去除率.
1.3.3吸附等溫線的測定室溫下分別向50mL不同初始濃度的 Zn2+溶液中加入 0.050g 的magadiite,調節pH=6,在25℃的恒溫振蕩器上振蕩(60r/min)60min,取出后離心分離(3500r/min,10min),取定量上清液測定其中Zn2+含量,平行實驗3次取平均值計算吸附量和去除率.
2 結果與討論
2.1吸附劑物化性質表征
通過BET比表面積測定、X射線衍射、紅外以及SEM對吸附機理進行初步探討.
2.1.1BET表征圖 2為實驗中測定的magadiite的氮氣吸附-脫附等溫線,從實驗中測定的氮氣吸附數據,利用BET方程可以計算其表面積,利用脫附等溫線 BJH模型計算孔結構.magadiite的比表面積為 19.38m2/g,平均孔徑為 18.62nm,平均孔容為 0.08759cm3/g.樣品的吸附等溫線呈現出典型的Ⅱ型等溫線,說明magadiite是非孔性的材料,或孔徑很大可近似看作是非孔性的[15-16].
2.1.2X射線衍射分析圖3為magadiite吸附前后的 XRD圖,將該圖譜吸附前的曲線與已知的magadiite譜圖進行對比,整個譜圖與magadiite的特征衍射峰相吻合,從圖中可以看出,通過水熱處理合成的產物均具有良好的衍射峰型,樣品均在 2θ角為 5.809°(1.52nm),11.36° (0.78nm)和17.11°(0.52nm)處分別出現了(001)(002)和(003)特征晶面衍射峰(對照JCPDS #42-1350),在2θ角24.76°~28.60°處的五指峰為magadiite的特征峰,這與文獻報道的magadiite的衍射峰一致[7,17],確定該晶相為magadiite.
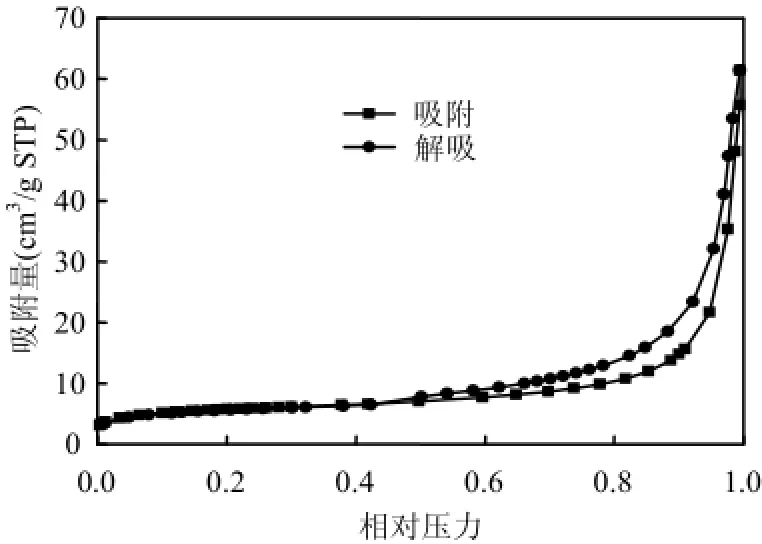
圖2 Magadiite的氮氣吸附-脫附等溫線Fig.2 Nitrogen adsorption-desorption isothermsos of magadiite
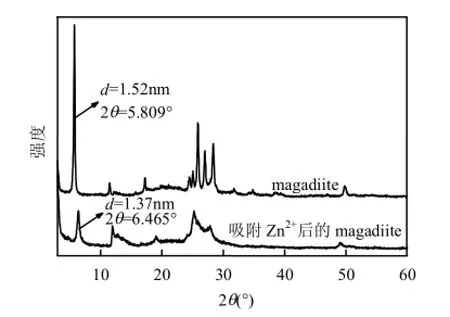
圖3 Magadiite吸附前后的XRD圖Fig.3 XRD patterns of magadiite and resulting products after adsorption
平衡吸附后的 magadiite的衍射峰向大角度方向偏移,層間距由 1.52nm減小到 1.37nm,這是由于當 magadiite加入到 Zn2+溶液中時,Zn2+與 Na+發生離子交換,Na+的離子半徑(0.102nm)較 Zn2+的離子半徑(0.074nm)大,而且在離子交換時要兩個Na+置換一個Zn2+才能保持magadiite層間電荷平衡,因此Zn2+通過離子交換作用進入到magadiite,magadiite通過離子交換吸附了Zn2+.
2.1.3紅外分析圖4為吸附前后的magadiite的紅外光譜圖.由圖可知,當magadiite吸附Zn2+后,magadiite在3418cm-1處締合Si—OH鍵的伸縮振動吸收峰藍移至3447cm-1;在1627cm-1處的—OH的彎曲振動吸收峰藍移至 1638cm-1.波數移動的原因是 Zn2+與—OH形成絡合物后,部分破環了 magadiite分子間或分子內原有的氫鍵,使吸收向高波數移動[18].這表明了magadiite表面的—OH中的O原子與Zn2+形成配位絡合,從而實現對Zn2+的吸附.
表面絡合作用模型可用來描述magadiite表面的吸附Zn2+的行為.在magadiite片層表面上的Si—OH中的O原子可提供孤對電子,與Zn2+外層4s和4p的sp3雜化軌道形成配位數為4的配合物[18].根據 magadiite和Zn2+結構特點[19-21],結合吸附前后的紅外圖譜,推測 magadiite和 Zn2+之間最有可能形成的2種配位方式,如圖5所示.
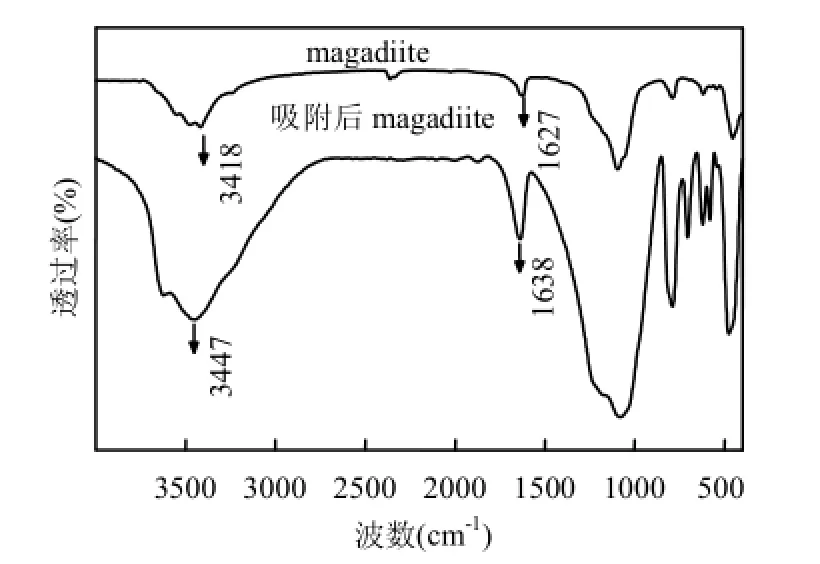
圖4 Magadiite吸附前后的紅外光譜圖Fig.4 IR spectra of magadiite and resulting products after adsorption
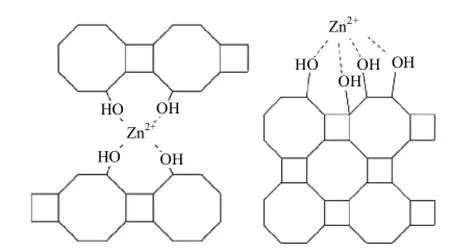
圖5 Magadiite-Zn2+配合物的結構示意Fig.5 Structure schematic of magadiite-Zn2+complex
2.1.4掃描電鏡(SEM)分析通過對圖 6的分析,可以看出未吸附的magadiite其形貌為玫瑰花形,這與之前的文獻報道[22]是一致的,吸附后的magadiite表面變粗糙,層狀結構變模糊,這可能是由于吸附 Zn2+后,magadiite表面官能團(硅羥基Si—OH)與Zn2+發生反應所引起的.

圖6 magadiite吸附前(左)后(右)的SEM圖Fig.6 SEM of magadiite (left) and resulting products after adsorption (right)
2.2pH值的影響
由圖7可以看出,當pH值小于3時,Zn2+的去除率非常低,只有百分之幾,隨著 pH值的增加,Zn2+的去除率迅速增加.這是因為在 pH值較低時,溶液中存在大量的H+,而H+的離子半徑比Zn2+小,更容易進入到magadiite層間將Na+置換出來,同時由于H+與 magadiite層間表面的活性Si—OH結合,降低了Zn2+與Si—OH的表面絡合作用,進而降低了去除率,在堿性條件下,Zn2+會生成Zn(OH)2沉淀.故本實驗選擇最佳吸附pH值為6.
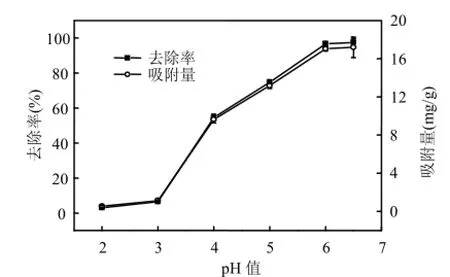
圖7 pH值對吸附效果的影響Fig.7 Effect of pH on the adsorption capacity
2.3吸附動力學和吸附等溫線
2.3.1吸附動力學研究由圖8可知,magadiite因具有大量的活性位點(Si—OH),在剛開始5min時與Zn2+的吸附過程非常迅速,5min時已大于平衡吸附量的80%,當吸附時間達到20min時接近平衡點時,吸附速度減慢,30min時吸附量增至平衡吸附量的 90%以上;隨后,吸附量趨于穩定,達到吸附-解吸平衡.初期吸附速度較快而后期吸附速度較慢有兩個方面的原因:一方面,magadiite片層表面有大量活性位點,隨著吸附進行,活性位點逐漸被 Zn2+占據,Zn2+緩慢擴散到層狀結構內部,使吸附速度降低;另一方面,隨著反應的進行,magadiite片層內的 Na+濃度逐漸減小,Zn2+濃度逐漸增加,因此,濃度差推動的離子擴散速度降低導致了后期吸附速率下降.為保證吸附達到充分平衡,吸附平衡時間定為60min.
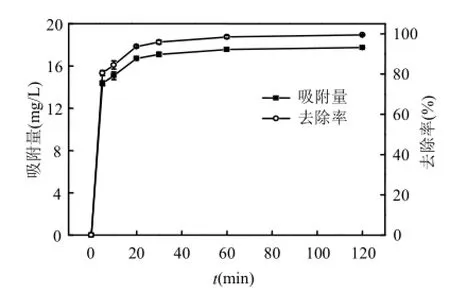
圖8 時間對吸附效果的影響Fig.8 Effect of time on the adsorption capacity
吸附動力學主要用于描述吸附劑吸附溶質速率的快慢,通過動力學方程擬合,從而探討其吸附機理.
準一級動力學方程采用基于固體吸附量Lagergren方程計算吸附速率[23]:
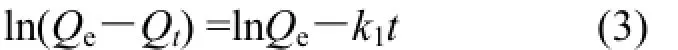
準二級動力學方程是建立在吸附速率受化學吸附機理的控制的二級力學模型[24]:
式中:k1,k2分別為準一級、準二級速率常數g/(mg·min);Qe,Qt分別為平衡吸附量、t時刻吸附量 mg/g; t為吸附時間,min.
將magadiite吸附Zn2+數據經計算并分別用準一級動力學方程和準二級動力學方程進行擬合,結果如圖9和10,擬合參數見表1.
由擬合結果和擬合曲線的相關系數(R2)來看,準二級動力學模型的相關系數(R2>0.999)大于準一級動力學模型的相關系數,具有更好的線性相關性,這說明magadiite對Zn2+的吸附動力學過程能很好的符合準二級動力學模型,對準一級動力學方程的符合程度較差.由此表明Zn2+在magadiite上的吸附主要體現出化學吸附行為.

表1 Magadiite吸附Zn2+的動力學參數Table 1 Kinetic parameters of Zn2+adsorption by magadiite
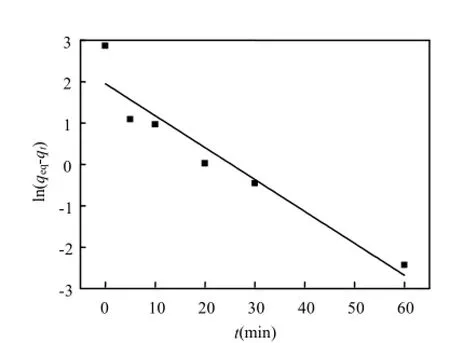
圖9 Magadiite吸附Zn2+準一級動力學方程模擬Fig.9 The pseudo-first-order kinetic plot of theadsorption of Zn2+by magadiite
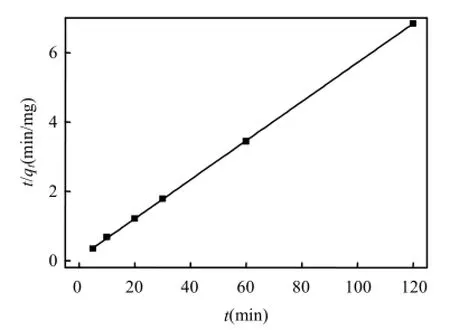
圖10 Magadiite吸附Zn2+準二級動力學模擬Fig.10 The pseudo-secont-order kinetic plot of the adsorption of Zn2+by magadiite adsorbent
2.3.2吸附等溫線由圖 11可見,隨著溶液中Zn2+濃度的增加,magadiite對其去除率降低,吸附量卻呈上升趨勢.這主要是因為在 Zn2+濃度較小時,magadiite的用量是過量的,Zn2+基本被吸附,去除率比較高并保持不變,單位magadiite的吸附量很低,隨著 Zn2+濃度的增加,在magadiite用量不變的情況下Zn2+過量,magadiite表面的吸附活性位點逐漸達到飽和吸附,同時magadiite內用于離子交換的 Na+逐漸減少,過量的 Zn2+在溶液中處于游離狀態,所以去除率也降低,單位magadiite的吸附量逐漸升高并直至吸附達到飽和狀態趨于穩定,magadiite對Zn2+的飽和吸附量為42.55mg/g.
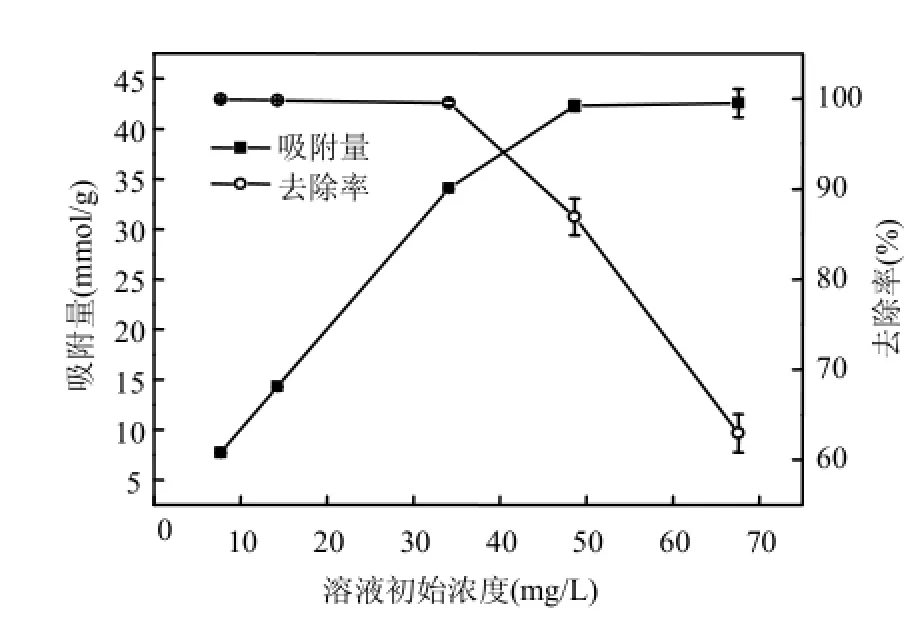
圖11 magadiite的吸附等溫線Fig.11 Adsorption isotherm curve of magadiite
將magadiite吸附Zn2+數據經計算并分別用Langmuir方程和Freundlich方程進行擬合,結果如圖12和13,擬合參數見表2.
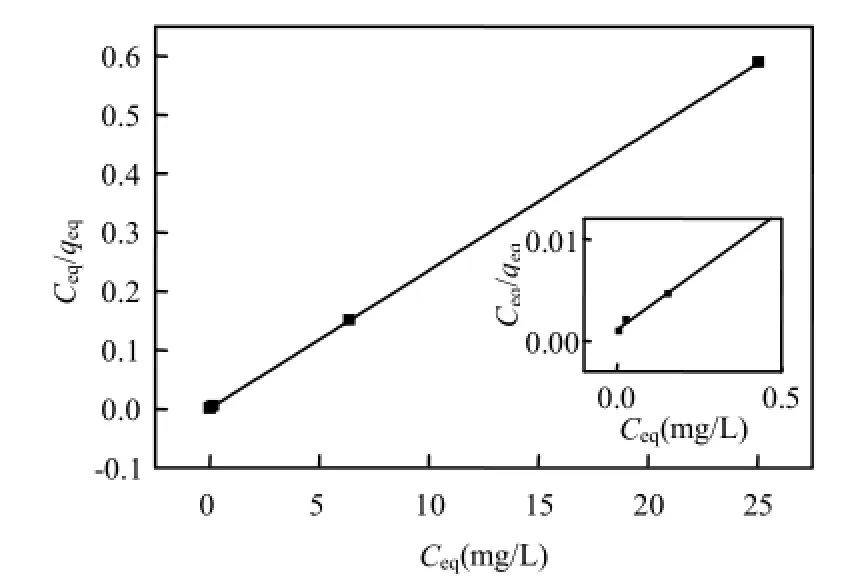
圖12 Magadiite等溫吸附的Langumir模型擬合Fig.12 Simulated plot of Langmuir isotherm equation for magadiite
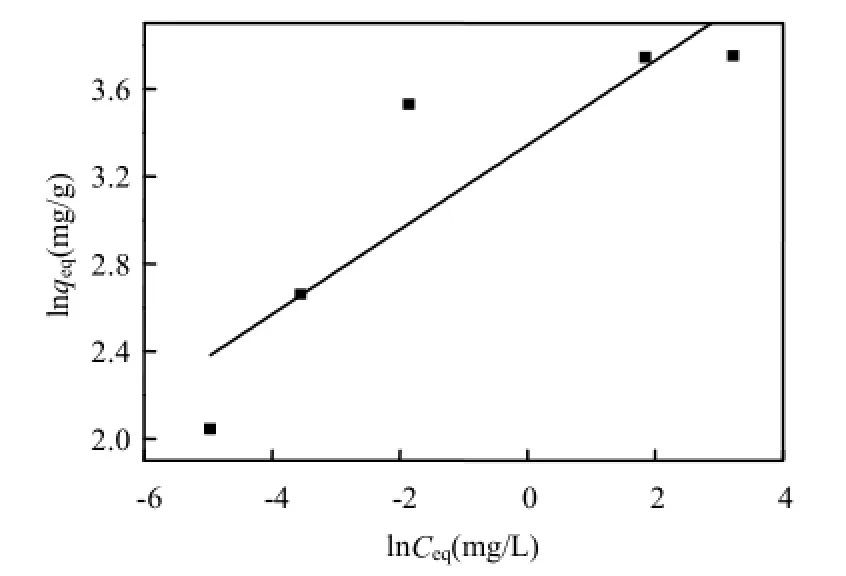
圖13 Magadiite等溫吸附的Freundlich模型擬合Fig.13 Simulated plot of Frciicllich isotherm equation for magadiite
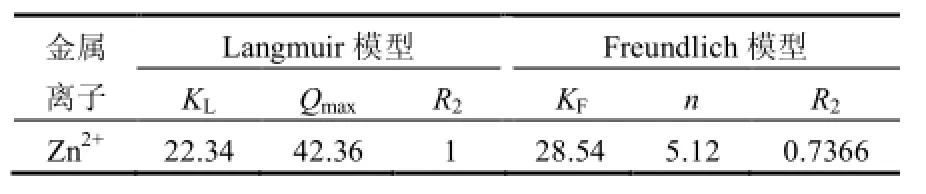
表2 Magadiite吸附Zn2+的等溫吸附模型參數Table 2 Parameters of isotherm models of Zn2+adsorption by magadiite
Langmuir吸附等溫式是從動力學角度出發,通過一系列假設條件而推導出來的單分子層吸附公式,該吸附等溫模型中有最大吸附量 Qmax(飽和吸附容量);Fruendlich吸附等溫模型則是一種經驗模型,能粗略地反映吸附劑的吸附能力和親和力.由擬合結果和擬合曲線的相關系數來看,Langmuir方程的擬合效果更好,表明 Langmuir模型更適合描述 magadiite對 Zn2+的吸附過程,由于物理吸附往往發生多分子層吸附,而化學吸附則生成單分子層,因此magadiite的吸附是以化學吸附為主[25-26].結合X射線衍射、紅外分、SEM和動力學分析對其機理進行探討,推斷magadiite 對Zn2+的吸附不是單純的物理吸附或者化學吸附,但以化學吸附(離子交換和表面絡合反應)為主.使用Langmuir等溫吸附模型擬合,計算得出Qmax為42.36mg/g,與實測值有較好的一致性,該結果高于鈉基膨潤土、電氣石粉、活性炭和改性梨渣對 Zn2+的吸附容量(分別為 2.33[27]、15.41[28]、28.42[29]、28.90mg/g[30]).
3 結論
3.1通過X射線衍射圖譜、紅外分析圖譜和SEM圖對其機理進行探討,推斷magadiite對Zn2+的吸附存在離子交換吸附和表面絡合作用吸附.
3.2pH<3時,Zn2+的去除率非常低,隨著pH值的增加,Zn2+的去除率迅速增加,最佳pH值為6,吸附平衡時間為60min,飽和吸附量為42.55mg/g.
3.3Magadiite對Zn2+的吸附動力學符合準二階動力學方程,吸附等溫線符合 Langmuir方程,結合 BET、X射線衍射、紅外、SEM分析推斷magadiite對 Zn2+的吸附不是單純的物理吸附或者化學吸附,但以化學吸附(離子交換和表面絡合反應)為主.
[1] Aldegs Y,Khraishen M,Tutunji M F. Adsorption of lead ions on diatomite and manganese oxides modified diatomite [J]. Wat. Res.,2000,35(15):3724-3728.
[2] 李仲謹,楊威,劉艷,等.β-環糊精聚合物微球對 Zn2+的吸附行為及機理 [J]. 食品科學,2011,32(1):35-38.
[3] 劉有才,鐘宏,劉洪萍.重金屬廢水處理技術研究現狀與發展趨勢 [J]. 廣東化工,2005,4:36-39.
[4] Eugster H P. Hydrous sodium silicate from Lake Magadi,Kenya,precursors of bedded chert [J]. Science,1967,157:1177-1179.
[5] Wang Y,Shang Y S,Zhu J. Synthesis of magadiite using a natural diatomite material [J]. J. Chem. Technol. Biotechnol.,2009,84: 1894-1898.
[6] 戈明亮,陳萌.麥羥硅鈉石的制備與表征 [J]. 硅酸鹽學報,2013,42(12):1704-1708.
[7] 張叢.新型多孔magadiite基異質結構的合成、表征及應用研究 [D]. 北京:北京化工大學,2012:27-28.
[8] Kooli F,Li M,Alshahateet S F,et al. Characterization and thermal stability properties of intercalated Na-magadiite with cetyltrimethylammonium (C16TMA) surfactants [J]. J. Phys. Chem. Solids.,2006,67:926-931.
[9] Guerra D L,Pintoa A A,Souzab A J. Kinetic and thermodynamic uranyl (II) adsorption process into modified Na-Magadiite and Na-Kanemite [J]. J. Hazardous Materials,2009,166:1550-1555.
[10] Fujita I,Kuroda K,Ogawa M. Synthesis of Interlamellar Silylated Derivatives of Magadiite and the Adsorption Behavior for Aliphatic Alcohols [J]. Chem. Mater.,2003,15:3134-3141.
[11] Guerra D L,Pinto A A,Viana R R. Modification of magadiite surface by organofunctionalization for application in removing As(V) from aqueous media: Kineticand thermodynamic [J]. Applied Surface Science,2009,256:702-709.
[12] Guerra D L,Pinto A A,Airoldi C. Adsorption of arsenic (III) into modified lamellar Na-magadiite in aqueous medium-Thermodynamic of adsorption process [J]. Journal of Solid State Chemistry,2008,181:3374-3379.
[13] Nunes A R,Moura A O,Prado A G S. Calorimetric aspects of adsorption of pesticides 2,4-D,diuronand atrazine on a magadiite surface [J]. J. Therm. Anal. Calorim.,2011,106:445-452.
[14] Peng S,Gao Q,Wang Q,et al. Layered structural heme protein magadiite nanocomposites with high enzyme-like peroxidase activity [J]. Chem. Mater.,2004,16:2675-2684.
[15] 王瑜.magadiite的合成及其轉晶制備沸石分子篩研究 [D].大連:大連理工大學,2010:46-47.
[16] 蔡子達.大分子在層狀硅酸鹽中的模板效應研究 [D]. 大連:大連理工大學,2012:17-18.
[17] Eypert B C,Sauzeat E,Pelletier M. Hydration mechanisms and swelling behavior of Na-magadiite [J]. Chem.Mater.,2001,13:1480-1486.
[18] 李寧,梅征.新型環糊精聚合物對 Zn2+的吸附研究 [J]. 中國環境科學,2012,32(7):1210-1215.
[19] Peng S,Gao Q,Wang Q,et al. Layered structural heme protein magadiite nanocomposites with high enzyme-like peroxidase activity [J]. Chem. Mater. 2004,16:2675-2684.
[20] Peng S,Gao Q,Wang Q,et al. Precursors of TAA-magadiite nanocomposites [J]. Applied Clay Science,2006,31:229-237.
[21] Ko Y,Kim M H,Kim S J,et al. Synthesis of Co-Silicalite-1from a Layered Silicate [J]. Korean J. Chem. Eng,2001,18(3):392-395.
[22] Wang Y R,Wang S F,Chang L C. Hydrothermal synthesis of magadiite [J]. Appl. Clay Sci.,2006,33(1):73-77.
[23] HO Y S,McKAY G. A comparison of chemisorptions kinetic models applied to pollutant removal on various sorbents [J]. Process Safety and Environmental Protection,1998,76:332-340.
[24] Bekta N,Ag?m B A,Kara S. Kinetic and equilibrium studies in removing lead ions form aqueous solutions by natural sepiolite [J]. J. Hazard. Mater.,2004,112(1/2):115-122.
[25] 張繼義,梁麗萍,蒲麗君,等.小麥秸稈對 Cr(Ⅵ)的吸附特性及動
力學、熱力學分析 [J]. 環境科學研究,2010,23(12):1546-1552.
[26] 楊軍,張玉龍,楊丹,等.稻秸對 Pb2+的吸附特性 [J]. 環境科學研究,2012,25(7):815-819.
[27] 楊秀敏,胡振琪,李寧,等.鈉基膨潤土對重金屬離子 Cu2+,Zn2+,Cd2+的吸附實驗 [J]. 煤炭學報,2009,34(6):819-822.
[28] 祝愛俠,劉海英,謝中國,等.超細電氣石粉吸附水體中的Cu(Ⅱ)、Pb(Ⅱ)和Zn(Ⅱ) [J]. 硅酸鹽學報,2011,39(10):1585-1591.
[29] 周蘭娟,荊國華,周作明.超聲場中活性炭上Zn2+的吸附/脫附 [J].中國環境科學,2011,31(5):755-760.
[30] 高貴珍,徐禮生,劉巧鳳.磷酸酯化改性梨渣吸附污染水體中鋅離子的研究 [J]. 光譜實驗室,2011,28(2):681-684.
Adsorption characteristics of Zn2+onto magadiite.
GE Ming-liang*,WANG Yan-wu,CHEN Meng (National Engineering Research Center of Novel Equipment for Polymer Processing,Key Laboratory of Polymer Processing Engineering of Ministry of Education,South China university of Technology,Guangzhou 510640,China).
China Environmental Science,2015,35(7):2065~2071
The magadiite as a single phase was prepared by a hydrothermal synthesis method in SiO2-NaOH-Na2CO3-H2O system and characterized by Brunauer-Emmett-Teller (BET) method,X-ray diffraction,FT-IR spectroscopy and scanning electron microscope and then the adsorption of Zn2+onto magadiite from water was examined. The results showed that,magadiite was nonporous material that has surface areas of 19.38 square metres per gram. The best adsorption conditions at 25℃ were obtained: the initial concentration of Zn2+was 20mg /L,pH = 6,the adsorption of magadiite reached equilibrium at 60min and the adsorption capacity of Zn2+was 42.55mg/g. In addition,the adsorption kinetics of the magadiite was best described by pseudo-second-order kinetic equation and the adsorption isotherms of the magadiite were fitted with the Langmuir adsorption model. The chemical and physical adsorption processes (mainly chemical process) in metal ions adsorption occur concurrently.
magadiite;adsorption;Zn2+;kinetics;adsorption isotherms
X703.1
A
1000-6923(2015)07-2065-07
戈明亮(1970-),男,安徽省和縣人,副教授,博士,主要從事高分子材料的改性及功能化、納米復合材料及功能高分子等的研究.發表論文60余篇.

