蛋制品中沙門氏菌的PCR及實時熒光PCR檢測方法
陳筱婷
(1,華南理工大學輕工與食品學院,廣東 廣州 510640;2,福建省產品質量檢驗研究院國家加工食品質量監督檢驗中心(福州), 福建 福州 350000)
蛋制品中沙門氏菌的PCR及實時熒光PCR檢測方法
陳筱婷1,2
(1,華南理工大學輕工與食品學院,廣東 廣州 510640;2,福建省產品質量檢驗研究院國家加工食品質量監督檢驗中心(福州), 福建 福州 350000)
研究針對蛋制品中沙門氏菌的檢測開發了一種快速靈敏的PCR檢測方法。研究方法采用煮沸法提取樣品DNA,運用PCR方法篩查樣品中的沙門氏菌基因成分。根據沙門氏菌基因組中的保守序列設計特異性引物與探針,PCR擴增結果表明,陽性樣品擴增獲得的序列與Genebank中沙門氏菌的基因序列完全匹配。采用實時PCR檢測方法可檢出濃度低至1.57×10-5μg . μL-1的沙門氏菌DNA,檢測時間少于24 h,對比常規的微生物培養方法,該方法顯著地提高了檢測速度。研究方法具有特異性強、靈敏度高等優點,可以廣泛應用于蛋制品及相關食品中沙門氏菌的高通量篩查檢測。
蛋制品;沙門氏菌;食品;PCR;實時PCR
沙門氏菌(Salmonella)是一群寄生于人和動物腸道內的無芽孢革蘭氏陰性直桿菌,其菌型繁多,分布廣泛,是一種重要的引起食源感染性腹瀉的致病微生物[1~6]。食品中沙門氏菌快速有效的檢測體系對于食品安全至關重要。蛋制品是一類重要的食品,在我國具有廣泛的消費市場,蛋制品在加工過程中容易遭受沙門氏菌的污染,從而帶來了一定的食品安全風險。從食品安全角度考慮,建立一種快速、靈敏、高效的蛋制品中沙門氏菌的檢測方法具有重大意義。
在我國,目前對沙門氏菌的檢測主要還依賴于傳統的微生物學檢測方法,該方法步驟繁瑣、費時費力,檢測過程一般需要3d的時間。為了適應食品安全快速檢測趨勢與要求,急需開發一種快速篩查食品中沙門氏菌的檢測方法。
PCR是聚合酶鏈式反應的簡稱,是分子生物學中廣泛運用的一種技術,主要原理是通過熱循環,達到目的基因片段的大量擴增。目前這項技術越來越廣泛地運用于食品中致病菌的篩查檢測。目前在國際上已有較多PCR技術應用于沙門氏菌檢測的研究報導[7~20],相關研究表明,采用PCR方法進行樣品中沙門氏菌的檢測分析,具有高特異性、高靈敏度等特點。
為了節約檢測時間,提高檢測效率,該研究開發了蛋制品中沙門氏菌的PCR以及實時熒光PCR檢測方法。通過試驗比較,方法選用煮沸法提取樣品DNA,采用PCR技術檢測沙門氏菌。方法主要步驟包括使用培養基溶液預增菌,采用煮沸法提取DNA,運用PCR技術特異性地檢測沙門氏菌。
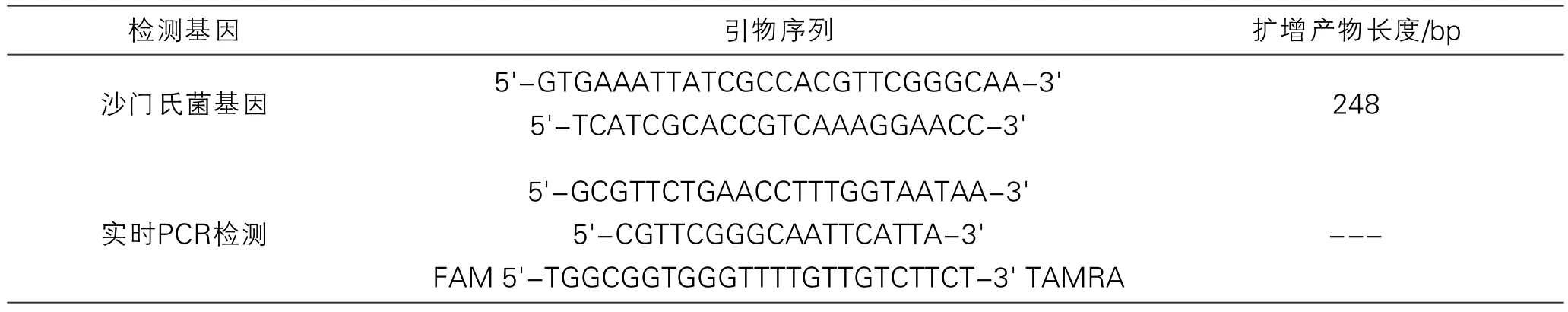
表1 引物信息以及擴增產物長度
實驗結果表明,應用該研究方法可快速、準確、靈敏地檢測出蛋制品中的沙門氏菌。
1 材料與方法
1.1 材料
1.1.1 菌株沙門氏菌(Salmonella)與陰性對照菌株大腸桿菌(Escherichia coli)等由福建省產品質量檢驗研究院食品所微生物實驗室保藏。
1.1.2 蛋制品,部分購于市場,部分經微生物方法檢測結果為陽性,于4 ℃冰箱中保存。
1.1.3 試劑:LB培養基,每升含有胰蛋白胨10g、酵母提取物5g、氯化鈉10g,pH 7.0);TaKaRa rTaq(5 U.μL-1)、MgCl2(25 mmol . L-1)、dNTPs(10 mmol . L-1)、DL2000 DNA Marker、加樣緩沖液(TaKaRa,大連寶生物工程有限公司)、溴化乙淀、瓊脂糖、Qiagen Generation Capture Column Kit。
1.1.4 主要儀器:MJPCR基因擴增儀(PTC-200 DNA擴增儀),Bio-Rad電泳儀,Bio-Rad UV凝膠成像系統,Bio-Rad生物光學紫外分光光度計,Applied Biosystems 7300定量PCR檢測系統。
1.2 方法
1.2.1 預增菌:純菌培養所用試驗菌株接種于10 mL液體LB培養基中,37℃震蕩培養10 h (220 r.p.m . min-1)。蛋制品取1~3 g,加入液體LB培養基中,渦旋震蕩60 s,37℃培養10 h(220 r.p.m. min-1)。
預增菌后,分別取兩管3 mL菌液用于DNA提取。為了比較不同DNA提取方法應用于沙門氏菌的提取效果,我們收集的一管菌液采用煮沸法提取DNA,另一管菌液采用Qiagen試劑盒進行提取。
1.2.2 PCR模板的制備方法
煮沸法提取DNA:取細菌培養液3.0 mL,置于小離心管中,8 000 r.p.m. min-1離心5 min。棄上清,沉淀用300 μL TE緩沖液懸浮,于95~98 ℃隔水煮沸15 min,10 000 r.p.m. min-1離心10 min。取上清,即為DNA模板溶液。
試劑盒法提取DNA:按照Qiagen試劑盒操作說明書進行DNA提取。
1.2.3 引物的合成
根據沙門氏菌基因組保守序列設計特異性引物,引物信息見表1,引物合成于Invitrogen公司。
1.2.4 PCR反應體系
常規PCR擴增采用Taq DNA聚合酶,反應體系為25 μL體系,其中10×PCR buffer 2.5 μL、MgCl2 2.5 μL、dNTPs 1.0 μL、上、下游引物各0.5 μL、Taq酶0.3 μL,模板溶液2.0 μL、滅菌雙蒸水補足體積至25 μL。
常規PCR儀器反應條件為94℃預變性5 min后,按94℃30 s、55℃1 min、72℃1 min,共進行35個循環,最后72℃ 延伸10 min,PCR產物于4℃保存。
實時PCR反應體系:在25 μL反應體系中,10×PCR buffer 2.5 μL、MgCl2 2.5 μL、dNTPs 1.0 μL、上、下游引物各0.5 μL、Taq酶0.3 μL,探針0.3 μL,模板溶液2.0 μL,滅菌雙蒸水補足體積至25 μL。
實時PCR反應條件:94℃預變性3 min;94℃變性45 s,53℃退火60 s。72 ℃延伸60 s。經5個循環;94℃變性45 s,58 ℃退火60 s,72℃延伸60 s,經35個循環;循環結束后,72℃,10min。
1.2.5 靈敏度試驗
LB增菌培養液DNA提取用菌落平板記數法定量的菌液,加入5 mL液體LB培養基。于37℃、220 r.p.m. min-1的搖床中增菌培養10 h。吸取增菌液1 mL,用煮沸法制備PCR模板。
實時PCR檢測沙門氏菌的敏感性試驗用煮沸法提取沙門氏菌的基因組DNA作為模板溶液,測定基因組DNA濃度,將其梯度稀釋后進行實時PCR反應,繪制各自的擴增曲線。
2 結果與分析
2.1 蛋制品樣品中沙門氏菌的檢測結果
用合成的引物及PCR方法對20份蛋制品中的沙門氏菌進行PCR檢測分析。電泳結果如圖1所示,20份蛋制品中有12份蛋制品檢測出248 bp的沙門氏菌特異性基因片段,與預期基因片段長度相符。對于PCR檢測結果為陽性的樣品,采用國家標準方法驗證試驗結果,具體比對試驗結果見2.2。作為陰性對照的大腸桿菌樣品DNA未擴增出目標基因片段。試驗結果說明,引物的靈敏度及特異性較好,適合進行蛋制品中沙門氏菌的檢測。
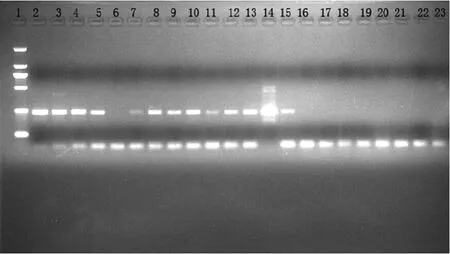
圖1 蛋制品中沙門氏菌的檢測結果
2.2 PCR檢測方法與國家標準方法比對結果
對20份蛋制品中的沙門氏菌進行PCR檢測分析。電泳結果如圖1所示,20份蛋制品中有12份蛋制品檢測出248 bp的沙門氏菌特異性基因片段,與預期基因片段長度相符。對于PCR檢測結果為陽性的樣品,采用國家標準方法驗證試驗結果。作為陰性對照的大腸桿菌樣品DNA未擴增出目標基因片段。試驗結果說明,引物的靈敏度及特異性較好,適合進行蛋制品中沙門氏菌的檢測。

表2
2.3 方法靈敏度試驗
將純菌培養的沙門氏菌菌液按照煮沸法提取DNA,使用核酸蛋白測定儀測定核酸濃度,梯度倍比稀釋,使用實時熒光PCR儀進行檢測,確定沙門氏菌的檢測靈敏度,檢測結果如圖2所示,結果顯示當基因組DNA含量為1.57×10-5μg/μL時,仍可被檢測出,說明實時PCR技術檢測沙門氏菌的靈敏度極高,且擴增曲線與模板DNA含量呈明顯相關性。
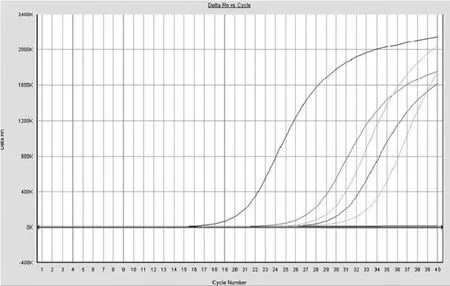
圖2 倍比稀釋的沙門氏菌菌液DNA的擴增曲線
3 討論
蛋制品是人民普遍喜愛的食品,它具有豐富的營養。蛋制品如果加工處理措施不當,容易帶入細菌,這對蛋制品的質量安全檢測提出了更高的要求。蛋制品及相關食品中微生物的檢測一直是食品安全檢測重點,其中沙門氏菌由于具有較強的危害性,引起人們較多的關注。研究旨在建立一種能快速篩查檢測蛋制品中沙門氏菌的方法。
為了建立一種快速、靈敏、高效的蛋制品等食品中沙門氏菌的PCR檢測方法,模板DNA的制備是關鍵的一步。為此,我們對蛋制品中沙門氏菌模板DNA的制備方法進行了比較研究。分別采用煮沸法與試劑盒法制備沙門氏菌的DNA模板,上述兩種方法提取的沙門氏菌DNA經PCR擴增后均能擴增出248 bp大小的特異性基因片段,說明煮沸法與試劑盒法均適用于蛋制品中沙門氏菌的檢測分析。試劑盒法由于使用成本較高,不適合于大量樣品中沙門氏菌的篩查與檢測分析。比較而言,煮沸法最為快捷、簡便易行,節省試劑消耗,且在試驗中可減少菌液和蛋制品中顆粒物質對PCR的干擾。核酸擴增檢測以及DNA電泳結果均表明煮沸法提取得到的DNA濃度以及純度可以滿足檢測需求。考慮到提取效率與提取時間,研究采用煮沸法提取蛋制品預增菌液中的DNA模板。
文章選擇沙門氏菌組氨酸轉運操作子基因上的一段特異性序列合成引物與探針,擴增片段大小為248 bp,檢測結果顯示,引物與探針具有良好的靈敏性與特異性。通過優化了的引物濃度、PCR反應體系、退火溫度等條件,保證沙門氏菌PCR檢測結果的穩定性和可重復性。
文章將PCR與實時PCR技術相結合,應用于蛋制品中沙門氏菌的檢測中。實時PCR技術檢測沙門氏菌的全過程在PCR管中得以完成,實現了檢測的定量和實時,省略了常規PCR的電泳步驟,同時避免了因電泳帶來的誤差。試驗中,定量PCR擴增曲線對于不同劑量的DNA模板,在1.57×10-1~1.57×10-5μg . μL-1范圍內具有良好的線性關系,即使樣品中模板濃度僅為1.57×10-5μg. μL-1依然可以被檢出。結果表明,實時PCR法對致病菌的實時定量檢測具有較好的應用前景。當然,由于實時PCR需要特殊熒光染料試劑和昂貴的定量PCR儀器,給一些基層單位的檢測工作帶來困難。
研究建立的PCR方法只需經過簡單的增菌即可以用煮沸法提取DNA進行檢測,簡便快捷,能在24小時之內獲得擴增結果,大大縮短了沙門氏菌的檢測時間,特別適用于大量樣品中沙門氏菌的快速篩查檢測。文章將常規PCR與實時PCR技術相結合,應用于蛋制品中沙門氏菌的檢測中,建立了一整套從樣品預增菌到DNA提取到PCR檢測的方法,方法可推廣應用于蛋制品及相關食品中沙門氏菌的快速高通量檢測中,具有較高的實用和推廣價值。
[1]CDC (2009) Multistate outbreak of Salmonella infections associated with peanut butter and peanut butter-containing products United States, 2008-2009. MMWR Morb Mortal Wkly Rep 58, 85-90.
[2]Brenner, F.W., Villar, R.G., Angulo, F.J., Tauxe, R. and Swaminathan,B. (2000) Salmonella nomenclature. J Clin Microbiol38, 2465-2467.
[3]Mahajan, R.K., Khan, S.A., Chandel, D.S., Kumar, N., Hans,C. and Chaudhry, R. (2003) Fatal case of Salmonella enterica subsp. arizonae gastroenteritis in an infant with microcephaly. J Clin Microbiol 41, 5830-5832.
[4]Tatavarthy, A., Peak, K., Veguilla, W., Cutting, T., Harwood,V.J., Roberts, J., Amuso, P., Cattani, J. et al. (2009) An accelerated method for isolation of Salmonella enterica serotype Typhimurium from artificially contaminated foods, using a short preenrichment, immunomagnetic separation, and xylose-lysine-desoxycholate agar (6IX method). J Food Prot 72, 583-590.
[5]Nastasi, A., Mammina, C. and Salsa, L. (1999) Outbreak of Salmonella enteritis bongori 48:z35:- in Sicily. Euro Surveill 4, 97-98.
[6]Khoo, C.H., Cheah, Y.K., Lee, L.H., Sim, J.H., Salleh, N.A.,Sidik, S.M., Radu, S. and Sukardi, S. (2009) Virulotyping of Salmonella enterica subsp. enterica isolated from indigenous vegetables and poultry meat in Malaysia using multiplex-PCR. Antonie Van Leeuwenhoek 96, 441-457.
[7]Warren B R, Yuk H G, Schneider K R. Detection of Salmonella by flow through immunocapture real-time PCR in selected foods within 8 hours[J].J Food Prot.,2007,70(4):1 002-1 006.
[8]石曉路,扈慶華,張佳峰,等. 多重實時PCR快速同時檢測沙門菌和志賀菌[J]. 中華流行病學雜志,2006,27(12):1 053-1 056.
[9]Samantha Hu Liming,Arvind A Bhagwat.Application of a molecular beacon real-time PCR technology to detect Salmonella species contaminating fruits and vegetables[J].International Journal of Food Microbiology,2004,(95):177-187.
[10]黃金林,焦新安,等. 應用聚合酶鏈式反應快速檢測沙門氏菌[J]. 揚州大學學報,2002,23(3):5-7.
[11]Hatta M, Smits H L Detection of Salmonella typhi by nested polymerase chain reaction in Mood, urine and stool samples[J].Am J Trop Med Hyg,2007,76(1):139-143.
[12]Trkov M.Avgustin G.An improved 16S rRNA based PCR method for the specific detection of Salmonella enteric[J].International Journal of Food Microbiology,2003,80(1):67-75.
[13]Baumler, A.J., Heffron, F. and Reissbrodt, R. (1997) Rapid detection of Salmonella enterica with primers specific for iroB. J Clin Microbiol 35, 1224-1230.
[14]Cheng, C.M., Lin, W., Van, K.T., Phan, L., Tran, N.N. and Farmer, D. (2008) Rapid detection of Salmonella in foods using real-time PCR. J Food Prot 71, 2436-2441.
[15]Csordas, A.T., Barak, J.D. and Delwiche, M.J. (2004) Comparison of primers for the detection of Salmonella enterica serovars using real-time PCR. Lett Appl Microbiol 39,187-193.
[16]Gallegos-Robles, M.A., Morales-Loredo, A., Alvarez-Ojeda, G.,Osuna-Garcia, J.A., Martinez, I.O., Morales-Ramos,L.H.and Fratamico, P. (2009) PCR detection and microbiological isolation of Salmonella spp. from fresh beef and cantaloupes.J Food Sci 74, M37-M40.
[17]Kwang, J., Littledike, E.T. and Keen, J.E. (1996) Use of the polymerase chain reaction for Salmonella detection. Lett Appl Microbiol 22, 46-51.
[18]Moore, M.M. and Feist, M.D. (2007) Real-time PCR method for Salmonella spp. targeting the stn gene. J Appl Microbiol 102, 516-530.
[19]Rodriguez-Lazaro, D., Hernandez, M., Esteve, T., Hoorfar, J.and Pla, M. (2003) A rapid and direct real time PCR-based method for identification of Salmonella spp. J Microbiol Methods 54, 381-390.
[20]Ziemer, C.J. and Steadham, S.R. (2003) Evaluation of the specificity of Salmonella PCR primers using various intestinal bacterial species. Lett Appl Microbiol 37, 463-469.
10.3969/j.issn.1007-550X.2015-07-001
TS253.7
A
1007-550X(2015)07-0025-05
2015-06-15
陳筱婷,女,工程師,主要從事食品安全方面的研究。

