應(yīng)用高內(nèi)涵分析技術(shù)進(jìn)行藥物肝毒性風(fēng)險(xiǎn)評估的研究
高 陽,胡宇馳,左澤平,王志斌,金家金,王立娜,程 源
(1.中藥成分分析與生物評價(jià)北京市重點(diǎn)實(shí)驗(yàn)室,北京市保健食品化妝品檢驗(yàn)中心,北京市藥品檢驗(yàn)所,北京 100035;2.北京中醫(yī)藥大學(xué),北京 100102)
·實(shí)驗(yàn)研究·
應(yīng)用高內(nèi)涵分析技術(shù)進(jìn)行藥物肝毒性風(fēng)險(xiǎn)評估的研究
高陽1,胡宇馳1,左澤平1,王志斌1,金家金2,王立娜2,程源2
(1.中藥成分分析與生物評價(jià)北京市重點(diǎn)實(shí)驗(yàn)室,北京市保健食品化妝品檢驗(yàn)中心,北京市藥品檢驗(yàn)所,北京100035;2.北京中醫(yī)藥大學(xué),北京100102)
目的研究嘗試應(yīng)用高內(nèi)涵分析技術(shù)建立藥物肝毒性高內(nèi)涵毒性評價(jià)指數(shù)測定的標(biāo)準(zhǔn)方法。方法采用ToxInsight藥物肝毒性檢測試劑盒,利用對多靶點(diǎn)的特異性染色,結(jié)合高內(nèi)涵活細(xì)胞成像分析平臺考察4種藥物對人源性肝癌細(xì)胞HepG2的細(xì)胞毒性作用,包括對該細(xì)胞的細(xì)胞數(shù)、核DNA含量、細(xì)胞質(zhì)內(nèi)谷胱甘肽降低水平、活性氧水平、線粒體膜電位的改變等5個指標(biāo)進(jìn)行綜合分析,擬對受試樣品的肝毒性進(jìn)行評估。結(jié)果氟西汀和羅格列酮的肝毒性評估結(jié)果為陰性;甲芬那酸和噻氯匹定的肝毒性評估結(jié)果為陽性,提示具有肝毒性風(fēng)險(xiǎn),且甲芬那酸的肝毒性風(fēng)險(xiǎn)比噻氯匹定的高。結(jié)論應(yīng)用高內(nèi)涵分析技術(shù)評估藥物肝毒性的方法基于活細(xì)胞、多參數(shù)、實(shí)時(shí)、高通量,能夠?qū)崿F(xiàn)藥物多種生物活性、毒性的早期、快速檢測,并且靈敏穩(wěn)定,簡便可行,可嘗試用于對藥物進(jìn)行體外肝毒性的安全風(fēng)險(xiǎn)評估。
高內(nèi)涵分析;藥物肝毒性;毒性評估
高內(nèi)涵分析技術(shù)(High content analysis,HCA)是一種基于細(xì)胞表型分析的高效篩選技術(shù),能夠在保持細(xì)胞結(jié)構(gòu)和功能完整的前提下,同時(shí)檢測待測樣品對細(xì)胞形態(tài)、生長、周期、遷移、凋亡、代謝途徑及信號傳導(dǎo)等方面的影響,從單一試驗(yàn)中獲取大量有關(guān)信息,從而確定化合物的生物活性以及潛在毒性[1,2]。
藥物肝毒性的評價(jià)在新藥研發(fā)及藥物安全風(fēng)險(xiǎn)評估中占重要地位。目前HCA能夠?qū)崟r(shí)監(jiān)測體外肝細(xì)胞與毒性機(jī)制相關(guān)的多個重要標(biāo)志分子,包括細(xì)胞核的形態(tài)和數(shù)量、線粒體膜電位以及氧化應(yīng)激狀態(tài)、凋亡與早期DNA損傷的變化等,是體外評價(jià)化合物潛在肝毒性和從機(jī)制上預(yù)測候選藥物安全性的高效手段。該方法能夠彌補(bǔ)動物實(shí)驗(yàn)靈敏度低、周期長、不能量化的缺點(diǎn),因此,HCA已成為藥品質(zhì)量風(fēng)險(xiǎn)與安全風(fēng)險(xiǎn)評估的新技術(shù)趨勢[3~5]。
本試驗(yàn)采用 ToxInsight藥物肝毒性試劑盒,利用對多靶點(diǎn)的特異性染色,結(jié)合高內(nèi)涵活細(xì)胞成像分析平臺考察4種藥物對人源性肝癌細(xì)胞HepG2的細(xì)胞毒性作用,包括對該細(xì)胞的細(xì)胞數(shù)、核DNA含量、細(xì)胞質(zhì)內(nèi)谷胱甘肽(GSH)降低水平、細(xì)胞內(nèi)活性氧(ROS)水平、線粒體膜電位(MMP)的改變等5個指標(biāo)進(jìn)行綜合分析,擬對受試樣品的肝毒性進(jìn)行評估。嘗試建立藥物肝毒性高內(nèi)涵毒性評價(jià)指數(shù)測定的標(biāo)準(zhǔn)方法,以期實(shí)現(xiàn)利用HCA對藥物進(jìn)行體外肝毒性的安全風(fēng)險(xiǎn)評估。
1 材料與方法
1.1細(xì)胞人肝癌細(xì)胞系HepG2細(xì)胞,購自中國細(xì)胞庫(上海),本實(shí)驗(yàn)室細(xì)胞庫保存;細(xì)胞用DMEM完全培養(yǎng)基[含15%的胎牛血清(FBS,V/ V),100 U·mL-1的青鏈霉素]培養(yǎng)。培養(yǎng)條件為37℃,5%CO2。
1.2藥物和對照品氟西汀(批號:WXBB5990V)、羅格列酮(批號:034M4736V)、噻氯匹定(批號:101296953)、甲芬那酸(批號:MKBR7799V)均購于Sigma公司。陰性對照品阿司匹林(批號:00209,德國Dr.Ehrenstorfer公司)。
1.3主要儀器與試劑體外毒性分析平臺(美國Thermo Scientific Cellomics),該系統(tǒng)主要組成部分是:熒光顯微系統(tǒng)、自動化熒光圖像獲取系統(tǒng)、檢測儀器、圖像處理分析軟件、結(jié)果分析和數(shù)據(jù)管理系統(tǒng)等;Vortex Genie-2型渦流振蕩器;超凈工作臺;倒置顯微鏡;臺式離心機(jī);電子天平;Napco Model 5410型CO2培養(yǎng)箱;全自動細(xì)胞計(jì)數(shù)儀。
高內(nèi)涵肝毒性試劑盒(批號:0k192906,Thermo Scientific Cellomics);Ⅰ型膠原蛋白包被的96孔細(xì)胞培養(yǎng)板(批號:354407,BD公司);DMEM培養(yǎng)基(批號:1294154,Gibco公司);標(biāo)準(zhǔn)胎牛血清(批號:20130726,天津市灝洋生物制品科技有限公司);青鏈霉素(批號:1308300,Gibco公司);胰蛋白酶(批號:2035B358-0458,Amresco公司);PBS(NaCl 8 g·L-1,KCl 0.2g·L-1,Na2HPO4·12H2O 3.4g·L-1,KH2PO40.2g·L-1,pH 7.2);二甲基亞砜(DMSO)(批號:2035B358-0231,Amresco公司)等。
1.4HepG2細(xì)胞準(zhǔn)備HepG2細(xì)胞復(fù)蘇傳代生長至70%~90%后,棄去培養(yǎng)瓶內(nèi)培養(yǎng)基,PBS清洗2 ~3次,0.25%胰蛋白酶覆蓋細(xì)胞約30 s后吸去胰酶,37℃放置2~3 min,加入含15%FBS的 DMEM完全培養(yǎng)基終止消化并吹打細(xì)胞,制備細(xì)胞混懸液并計(jì)數(shù)。完全培養(yǎng)基調(diào)整細(xì)胞濃度至2.0× 105·mL-1。將調(diào)整好密度的細(xì)胞液接種到Collagen-Ⅰ包被的96孔細(xì)胞培養(yǎng)板中,每孔100 μL(即20 000個/孔)。將培養(yǎng)板置37℃,5%CO2培養(yǎng)箱中培養(yǎng)16~24 h。
1.5樣品配制無菌條件下配制。陰性對照品和各樣品均以200×Cmax(最大血藥濃度)為最高劑量,在無菌EP管內(nèi)用無血清DMEM培養(yǎng)基依次向下倍比稀釋7個濃度,振蕩混勻備用。終濃度分別為200、100、50、25、12.5、6.25、3.13、1.6Cmax。陰性對照品阿司匹林的Cmax為0.995 μg·mL-1;各樣品Cmax分別為:氟西汀0.015 μg·mL-1、羅格列酮0.373 μg·mL-1、噻氯匹定2.13μg·mL-1、甲芬那酸6.5μg·mL-1(藥物肝毒性試劑盒說明書提供)。
1.6加樣操作無菌條件下操作,依次將各樣品和陰性對照品加入培養(yǎng)板孔內(nèi),每個濃度重復(fù)3孔,每塊培養(yǎng)板設(shè)溶媒對照(即無血清培養(yǎng)基)24孔,每孔100 μL。將加樣后培養(yǎng)板置37℃,5%CO2培養(yǎng)箱中繼續(xù)培養(yǎng)24 h。
1.7染色測試當(dāng)天,按藥物肝毒性試劑盒說明書配制Monochlorobimane(mBCl)染色液、ROS染色液、Hoechst 33342及Mito染色液。小心吸去培養(yǎng)板內(nèi)的液體,加入配制好的染液,每孔100 μL。培養(yǎng)板置37℃,5%CO2培養(yǎng)箱中孵育45 min。將板孔內(nèi)液體小心吸去,用放置至室溫的PBS溶液清洗1遍,再在每孔中加入100 μL PBS,待測。
1.8肝毒性檢測采用高內(nèi)涵分析平臺的DILIAcqonly模塊采集圖像。采集條件如下:第一通道波長為360 nm/460 nm檢測Hoechst 33342標(biāo)記的細(xì)胞核DNA并記錄細(xì)胞數(shù),第二通道波長為380 nm/ 461 nm檢測mBCl標(biāo)記的GSH,第三通道波長為504 nm/529 nm檢測 ROS Dye標(biāo)記的ROS,第四通道波長為584 nm/606 nm檢測Mito Dye標(biāo)記的線粒體膜電位;選擇20倍物鏡,每孔采集9個視野的圖像,存儲信息用于圖像分析。
1.9肝毒性分析采用DILI-HepG2-HELLY分析軟件對細(xì)胞核數(shù)量、核面積、核DNA、谷胱甘肽(GSH)、過氧化物(ROS)、線粒體膜電位(MMP)進(jìn)行定位和定量分析,并以細(xì)胞數(shù)量、核DNA含量、GSH水平、ROS水平和MMP改變參數(shù)形式表示。最終數(shù)據(jù)在Excel工作表的DILI模塊中計(jì)算匯總,以統(tǒng)計(jì)學(xué)方式將多個單參數(shù)結(jié)果匯總成稱為“毒性指標(biāo)”的多參數(shù)計(jì)算值,比較不同樣品之間和不同劑量之間的毒性風(fēng)險(xiǎn)。
2 結(jié)果
2.1對HepG2細(xì)胞凋亡的影響試驗(yàn)結(jié)果顯示,不同濃度的4種藥物與HepG2細(xì)胞分別作用24 h后,甲芬那酸和噻氯匹定對細(xì)胞存活有明顯的抑制作用,能明顯抑制HepG2細(xì)胞的增值。而氟西汀和羅格列酮與陰性對照(阿司匹林)相比,細(xì)胞數(shù)量無顯著差異。Hoechst 33342染色結(jié)果表明,陰性對照的細(xì)胞核呈均勻的熒光(E),而甲芬那酸和噻氯匹定分別作用24 h后,隨藥物濃度的增加,出現(xiàn)不同程度的細(xì)胞核皺縮,染色質(zhì)凝集,細(xì)胞數(shù)量明顯減少,顯示細(xì)胞凋亡的特征。如圖1所示。
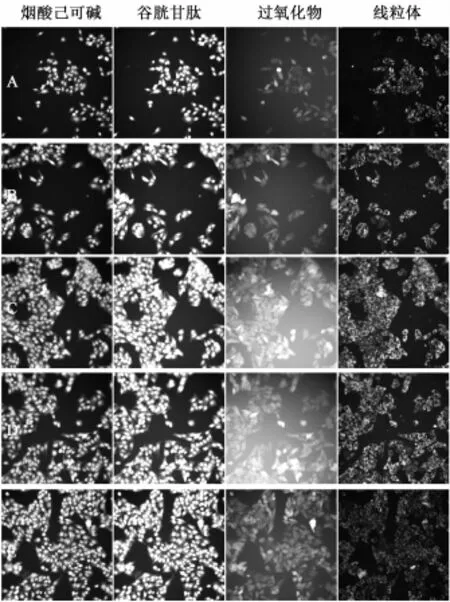
圖1 4種藥物對HepG2細(xì)胞的細(xì)胞狀態(tài)和熒光強(qiáng)度的比較結(jié)果(200×Cmax)
2.2對HepG2細(xì)胞GSH和ROS的影響如圖2所示,甲芬那酸隨劑量的增加,GSH水平基本呈現(xiàn)下降趨勢,同時(shí),ROS水平則呈上升趨勢。200× Cmax濃度時(shí),GSH水平降至陰性對照的閾值以下,顯示出毒性預(yù)警。而氟西汀各劑量組的GSH和ROS均在陰性對照的安全閾值以內(nèi),提示無毒性風(fēng)險(xiǎn)。
2.3對HepG2細(xì)胞線粒體膜電位的影響高內(nèi)涵熒光成像系統(tǒng)結(jié)果顯示,陰性對照的細(xì)胞膜電位最高,呈現(xiàn)紫紅色熒光,熒光強(qiáng)度較強(qiáng)。甲芬那酸和噻氯匹定細(xì)胞紅色熒光逐漸減弱。隨濃度的增加,對應(yīng)的紅色熒光強(qiáng)度的細(xì)胞群比例有所下降,且熒光強(qiáng)度降低。甲芬那酸隨濃度的增加,線粒體膜電位的水平顯著降低,超出陰性對照的安全閾值的下限范圍,提示具有毒性風(fēng)險(xiǎn)。如圖2、3所示。
2.4肝毒性風(fēng)險(xiǎn)評估DILI-HepG2-HELLY分析軟件對細(xì)胞數(shù)量、核DNA含量、GSH水平、ROS水平和MMP改變5項(xiàng)參數(shù)匯總,以統(tǒng)計(jì)學(xué)方式將多個單參數(shù)結(jié)果匯總成“毒性指標(biāo)”的多參數(shù)總結(jié)果,氟西汀和羅格列酮5項(xiàng)檢測指標(biāo)均為陰性,提示無肝毒性風(fēng)險(xiǎn)。噻氯匹定細(xì)胞數(shù)量、GSH水平和MMP改變3項(xiàng)檢測指標(biāo)為陽性,甲芬那酸5項(xiàng)檢測指標(biāo)也均為陽性,提示噻氯匹定和甲芬那酸具有肝毒性風(fēng)險(xiǎn),且甲芬那酸的毒性風(fēng)險(xiǎn)比噻氯匹定的高,具有更高的毒性預(yù)警,結(jié)果見表1。
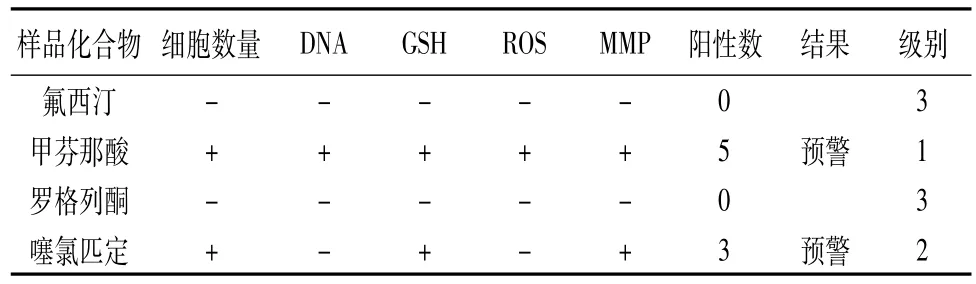
表1 4種目標(biāo)藥物肝毒性分析結(jié)果(DILI分析模塊)
3 討論
以陰性對照(阿司匹林)確定毒性閾值(細(xì)胞增值不認(rèn)為是一種毒性反應(yīng),不設(shè)上限;低水平的ROS不認(rèn)為是一種毒性反應(yīng),不設(shè)下限),分析各個靶點(diǎn)上的毒性反應(yīng),運(yùn)用多個參數(shù)進(jìn)行肝毒性預(yù)測及等級排序。藥物的毒性反應(yīng)是根據(jù)所有濃度下各個靶點(diǎn)的毒性結(jié)果的綜合評價(jià)。通過對5個測量靶點(diǎn)的觀察,若有一個靶點(diǎn)的任何一個濃度反應(yīng)超過毒性閾值,則確定該藥物有毒性,從而解決沒有直接量效曲線的問題。本試驗(yàn)中,氟西汀和羅格列酮結(jié)果為陰性,提示在試驗(yàn)劑量下無肝毒性風(fēng)險(xiǎn)。高劑量的甲芬那酸和噻氯匹定能顯著抑制HepG2細(xì)胞的增值,誘導(dǎo)其凋亡,檢測結(jié)果為陽性,表現(xiàn)出一定的肝毒性風(fēng)險(xiǎn),且甲芬那酸的毒性風(fēng)險(xiǎn)比噻氯匹定的高。試驗(yàn)結(jié)果與美國Thermo公司提供的國外試驗(yàn)數(shù)據(jù)結(jié)果基本一致。該方法基于活細(xì)胞、多參數(shù)、實(shí)時(shí)、高通量,能夠?qū)崿F(xiàn)藥物多種生物活性、毒性的早期、快速檢測,并且靈敏穩(wěn)定,簡便可行,可嘗試用于對藥物進(jìn)行體外肝毒性的安全風(fēng)險(xiǎn)評估[6]。
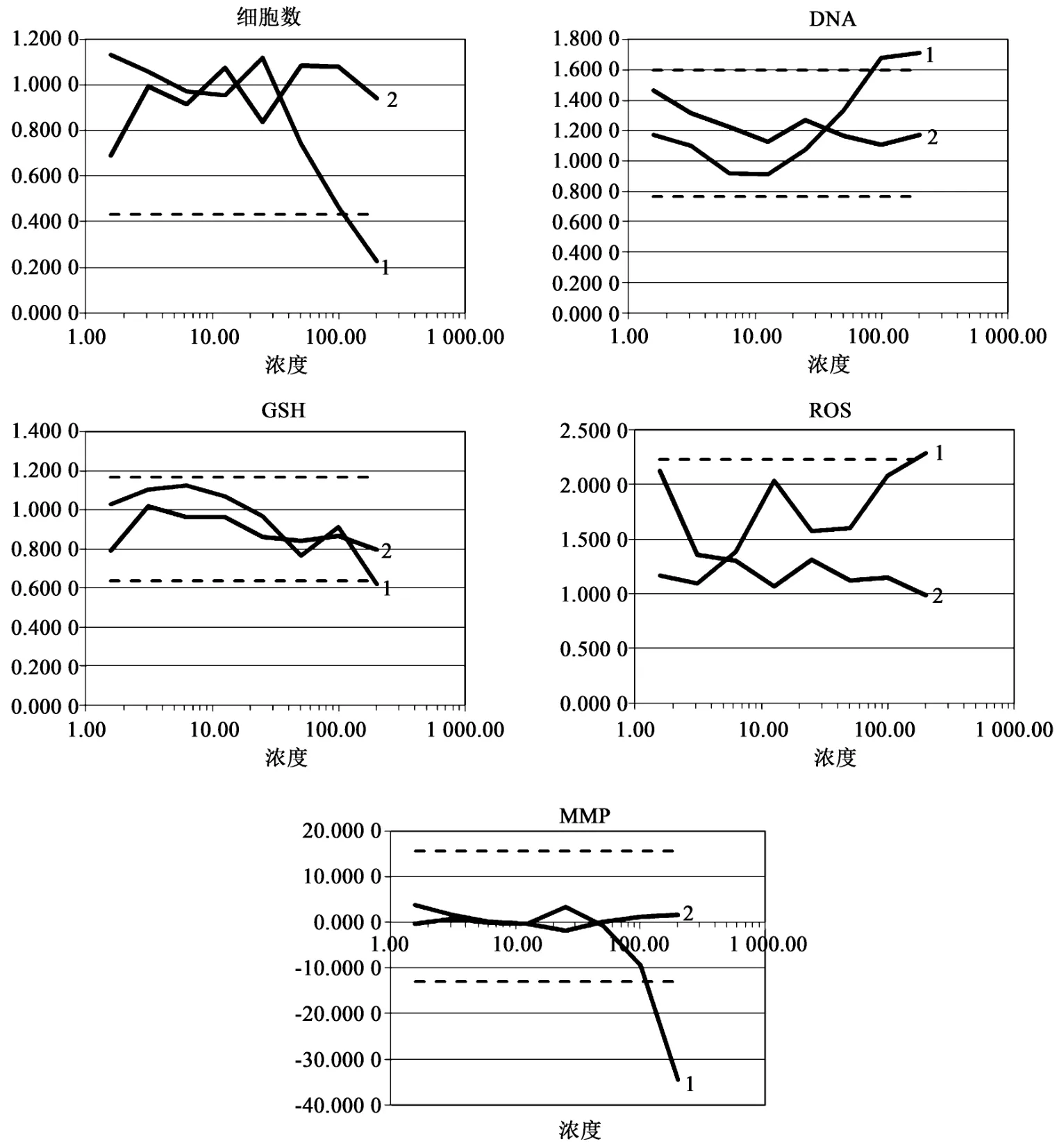
圖2 甲芬那酸(1)和氟西汀(2)抑制HepG2細(xì)胞增殖,對HepG2細(xì)胞數(shù)、DNA損傷、GSH水平、ROS水平和MMP變化的影響(量效曲線)
試驗(yàn)表明,藥物HCA不但可以闡明被篩樣品與藥靶之間的相互作用關(guān)系,而且還能同時(shí)了解細(xì)胞的其它生物學(xué)改變,通過觀察細(xì)胞形態(tài)來預(yù)測化合物的毒性以及進(jìn)行相關(guān)代謝途徑的研究,彌補(bǔ)了現(xiàn)有毒理學(xué)篩選方法在通量、毒性機(jī)制檢測、潛在毒性揭示等方面的不足,是毒理學(xué)新興和最具效率的技術(shù)[7,8]。常規(guī)的細(xì)胞毒性檢測內(nèi)容包括膜完整性的喪失或細(xì)胞溶解、凋亡、關(guān)鍵大分子損耗、代謝抑制效應(yīng)和增殖抑制效應(yīng)等。這些檢測可以初步觀察化合物毒性特點(diǎn)。然而,不同的方法分開進(jìn)行,既耗時(shí)且難以獲得一致的試驗(yàn)數(shù)據(jù)。HCA用于細(xì)胞毒性測定,在一次試驗(yàn)中平行監(jiān)測與毒性機(jī)制相關(guān)的多個參數(shù)甚至是信號轉(zhuǎn)導(dǎo)分子,更能全面準(zhǔn)確地反映化合物誘導(dǎo)的毒性特征及潛在機(jī)制[9,10]。
[1]Zock JM.Applications of high content screening in life science research[J].Comb Chem High Throughput Screen,2009,12(9):870-876.
[2]Taylor DL,Haskins JR,Giuliano KA.Methods in Molecular Biology:Vol.356.High Content Screening:A Powerful Approach to Systems Cell Biology and Drug Discovery [M].Totowa:Humana,2007:83-94.
[3]Dragunow M.High-content analysis in neuroscience [J].Nat Rev Neurosci,2008,9(10):779-788.
[4]Edwards BS,Oprea T,Prossnitz ER,et al.Flow cytometry for high-throughput,high-content screening[J].Curr Opin Chem Biol,2004,8(4):392-398.
[5]趙金伴,喻希.化學(xué)技術(shù)的前沿——高內(nèi)涵篩選技術(shù)的研究及應(yīng)用[J].化工技術(shù)與開發(fā),2008,37(8):19-22.
[6]O′Brien PJ,Irwin W,Diaz D,et al.High concordance of drug-induced human hepatotoxicity with in vitro cytotoxicity measured in a novel cell-based model using high content screening[J].Arch Toxicol,2006,80(9):580-604.
[7]Lang P,Yeow K,Nicholsa A,et al.Cellular imaging in drug discovery[J].Nat Rev Drug Discov,2006,5(4):343-356.
[8]Freeley M,Bakos G,Davies A,et al.A high-content analysis toolbox permits dissection of diverse signaling pathways for T lymphocyte polarization[J].J Biomol Screen,2010,15(5):541-555.
[9]胡經(jīng)陽,嚴(yán)春琳,朱彥,等.高內(nèi)涵篩選應(yīng)用于中藥現(xiàn)代化的前景展望[J].天津中醫(yī)藥大學(xué)學(xué)報(bào),2013,32(2):120-124.
[10]劉利波,王莉莉.高內(nèi)涵分析在新藥發(fā)現(xiàn)毒理學(xué)中的應(yīng)用進(jìn)展[J].中國藥理學(xué)與毒理學(xué)雜志,2012,26(6):893-896.
Study on the risk assessment of drug hepatoxicty by high content analysis
GAO Yang1,HU Yu-chi1,ZUO Ze-ping1,WANG Zhi-bin1,JIN Jia-jin2,WANG Li-na2,CHENG Yuan2(1.Beijing Key Laboratory of Analysis and Biological Evaluation of Traditional Chinese Medicine
Composition,Beijing Center for Health Food and Cosmetics Control,Beijing Institute for Drug Control,Beijing 100035,China;2.Beijing University of Chinese Medicine,Beijing 100102,China)
Objective To study a standard method for the determination of drug hepatoxicty evaluation index using high content analysis.Methods To investigate the cytotoxic effect of four drugs on HepG2cells in human hepatocellular carcinoma cells by using ToxInsight Drug Induced Liver Injury Assay Cartridge and combining high content live cell imaging analysis platform.Through the comprehensive analysis of 5 indexes,the number of cells,DNA content,GSH level,ROS level and mitochondrial membrane potential,the liver toxicity of the tested samples were evaluated.Results The results of fluoxetine and rosiglitazone were negative.The results of mefenamic acid and ticlopidine were positive,which indicated that the risk of liver toxicity was high,and the risk of liver toxicity of mefenamic acid was higher than that of ticlopidine.Conclusion HCA was based on living cells,multi parameters,real-time and high content,can achieve a variety of biological activity,drug toxicity of the early and rapid detection.It was sensitive,stable,simple and feasible.HCA can be used to evaluate the risk of drug hepatoxicty in vitro.
High content analysis;Drug induced liver injury;Assessment of toxicity
R965
A
2095-5375(2015)12-0688-005
2013年北京市科技計(jì)劃項(xiàng)目(No.Z131100005613032)
高陽,女,研究方向:藥物藥理學(xué)與毒理學(xué)研究,E-mail:gaoyang527@yeah.net
胡宇馳,男,主管藥師,研究方向:藥物藥理學(xué)與毒理學(xué)研究,Tel:010-83229474,E-mail:yuchihu@bidc.org.cn

